Химических элементов Д. И. Менделеева. Закономерности изменения свойств элементов малых периодов и главных подгрупп в зависимости от атомного (порядкового) номера
| Вид материала | Закон |
Содержание24. Строение атома: ядро, электронная оболочка. Химический элемент. Схемы строения атомов на примере химических элементов третье |
- Тема №1 «Общая химия», 73.57kb.
- Материалы для подготовки к экзамену по химии, 462.84kb.
- Билеты для переводной аттестации по химии, 8 класс Билет, 100.43kb.
- Характеристика химических элементов малых периодов по их положению в периодической, 97.2kb.
- Урок повторение и обобщение по темам, 121.04kb.
- Урок тема: Металлы главных подгрупп, 62.33kb.
- Задачи урока: Обучающая: Создать условия для исследования учащимися физических и химических, 64.17kb.
- Химических элементов Д. И. Менделеева, 32.78kb.
- Контрольная работа по темам: «Общие свойства металлов», 69.86kb.
- Задачи: Обучающая: Познакомить учащихся со свойствами щелочных металлов, Щелочно-земельных, 51.5kb.
24. Строение атома: ядро, электронная оболочка. Химический элемент. Схемы строения атомов на примере химических элементов третьего периода.
В результате экспериментов, посвященных изучению строения атома, было установлено, что атом состоит из положительно заряженного ядра и электронной оболочки.
Ядро образовано протонами и нейтронами.
Протон — это частица, имеющая положительный заряд (+1).
Нейтрон — это нейтральная частица, заряд ее равен 0.
Из определений следует, что величина заряда ядра атома равна числу протонов и имеет положительное значение.
Электронная оболочка образована электронами, заряд у которых отрицательный. Число электронов равно числу протонов, поэтому заряд атома в целом равен 0 (т. е. атом электронейтральная частица).
Число протонов, а следовательно, заряд ядра и число электронов численно равны порядковому номеру химического элемента.
Далее следует отметить, что практически вся масса атома сосредоточена в ядре. Это связано с тем, что масса электрона настолько меньше массы протона или нейтрона, что ею пренебрегают (не учитывают).
Электроны двигаются вокруг ядра атома, не беспорядочно, а в зависимости от энергии, которой они обладают, образуя так называемый электронный слой.
На каждом электронном слое может располагаться определенное число электронов: на первом — не больше двух, на втором — не больше восьми, на третьем — не больше восемнадцати.
Число электронных слоев определяется по номеру периода, в котором расположен химический элемент.
Число электронов на последнем (внешнем) слое определяется по номеру группы рассматриваемого элемента.
Так, например, кислород расположен во втором периоде VI группы. Из этого следует, что у него два электронных слоя и на внешнем (втором) расположено шесть электронов.
Электронные слои заполняются у атомов постепенно, по мере увеличения общего числа электронов, которое соответствует порядковому номеру химического элемента. В сумме на первых двух электронных слоях может располагаться не более 10 электронов, т. е. элементом, завершающим второй период, является неон (Ne).
У атомов третьего периода в атоме находится три электронных слоя. Первый и второй электронные слои заполнены электронами до предела. Для первого представителя элементов третьего периода натрия схема расположения электронов в атоме выглядит так:

Из схемы видно, что атом натрия имеет заряд ядра +11. Электронную оболочку атома составляют 11 электронов. На первом электронном слое находится два электрона, на втором — восемь, а на третьем — один электрон. У магния, как элемента II группы этого периода, на внешнем электронном слое находится уже два электрона:
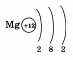
Для остальных элементов периода изменение строения атома происходит аналогично. У каждого последующего элемента, в отличие от предыдущего, заряд ядра больше на одну единицу и на внешнем электронном слое расположено на один электрон больше. Число электронов, располагающихся на внешнем электронном слое, равно номеру группы.
Завершает период аргон. Заряд его ядра +18. Это элемент VIII группы, поэтому на внешнем электронном слое его атома находится восемь электронов:
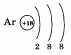
Далее можно сделать выводы и об изменении свойств элементов в периоде.
Любой период (кроме первого) начинается типичным металлом. В третьем периоде это натрий Na. Далее следует магний Mg, также обладающий ярко выраженными металлическими свойствами. Следующий элемент в периоде — алюминий А1. Это амфотерный элемент, проявляющий двойственные свойства (и металлов и неметаллов). Остальные элементы в периоде — неметаллы: кремний Si, фосфор Р, хлор С1. И заканчивается период инертным газом аргоном Аг.
Таким образом, в периоде происходит постепенное ослабление металлических свойств и возрастание свойств неметаллов. Такое изменение свойств объясняется увеличением числа электронов на внешнем электронном слое: от 1 — 2, характерных для металлов, и заканчивая 5 — 8 электронами, соответствующими элементам-неметаллам.
25. Натрий, его положение в периодической системе химических элементов Д. И. Менделеева, строение атома. Физические и химические свойства; взаимодействие с неметаллами, водой.
В периодической таблице химических элементов натрий Na расположен в третьем периоде I группы главной подгруппы.
Рассказывая о строении атома натрия, учащийся должен изобразить распределение электронов по электронным слоям:
Однако по желанию учащийся может расширить свой ответ информацией о составе атома графической схемой и электронной формулой:
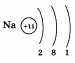
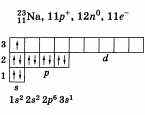
Натрий — металл. Основная степень окисления +1. Натрий образует оксид Na2O и гидроксид NaOH, которые проявляют основные свойства.
При освещении вопроса о нахождении натрия и его соединений в природе необходимо отметить, что как простое вещество натрий в природе не встречается из-за высокой химической активности. Получают натрий из расплава хлорида или гидроксида натрия при прохождении через него электрического тока.
Натрий — серебристо-белый металл, с небольшой плотностью, легкоплавкий, легко окисляется на воздухе.
При характеристике химических свойств необходимо отметить, что натрий, как и другие щелочные металлы, чрезвычайно активный металл. Это происходит потому, что он легко отдает единственный электрон, находящийся на внешнем электронном слое.
Далее можно рассмотреть его взаимодействие: а) с простыми веществами; б) со сложными веществами.
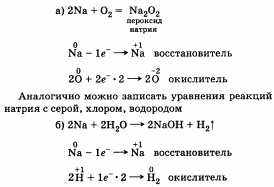
При записи уравнений реакций со сложными веществами необходимо помнить, что в растворах кислот натрий сначала реагирует с водой (см. реакцию выше), а потом уже идет реакция между щелочью и кислотой:
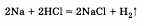
Закончить ответ можно рассказом о применении натрия.
Применение натрия как металла связано с его восстановительными свойствами; он используется в качестве катализатора в органической химии, газа-наполнителя в светильниках, в виде сплава с калием — как хладагент в ядерных реакторах-размножителях на быстрых нейтронах. Мировое ежегодное потребление натрия и его соединений превосходит 100 млн т.
Наиболее важные соединения натрия, применяемые в быту и на производстве, — бикарбонат натрия NaHCO3, карбонат натрия Na2CO3, гидроксид натрия NaOH, раствор силиката натрия Na2SiO3 (жидкое стекло) — силикатный клей.
