«Загальні відомості про неметали та їх сполуки»
| Вид материала | Урок |
СодержаниеДодатковий матеріал Завдання 2 команди Завдання 3 команди 4 етап – Завдання – змагання 4 етап – Завдання – змагання По вертикалі |
- Загальні висновки І рекомендації 8 Список використаної літератури 9 Додатки, 569.55kb.
- План загальні історичні відомості про розвиток малярства на склі, зокрема на Гуцульщині., 207.25kb.
- І. Загальні відомості про хвору дитину (praefatio), 518.46kb.
- Предмет: Органічна хімія Мета, 369.43kb.
- Муровомокуриловецький р-н, Вінницька обл, 2723.63kb.
- Про суспільно-політичну ситуацію у лютому 2012 року, 119.31kb.
- Програма вступного іспиту з фаху на напрям 100101"Енергетика та електротехнічні системи, 43.34kb.
- Лекція 1 хф (лекція) Тема Загальні властивості неметалів, 1201.72kb.
- Зміст навчальної програми з вищої математики для студентів 1 курсу фармацевтичного, 32.69kb.
- 1. Загальні відомості про суб'єкта господарювання*, 78.9kb.
ПОВІДОМЛЕННЯ
Повідомлення 1 команди:
Історія силіцію – дуже цікава. У епоху палеоліту, тобто 800-1000 тисячоліть тому, силіцій допоміг людині в боротьбі за життя. Цей твердий камінь, від якого легко відбити шматок з гострими краями, послужив матеріалом для першої зброї (наконечником копій і стріл) і перших знарядь праці (сокир, ножів і так далі). Пізніше, коли на зміну каменю пришли мідь, бронза, залізо, кремінь знайшов використання у вигляді кресала. При ударі твердого кремнію об залізо від нього відриваються дрібні осколки, нагріті до високої температури, унаслідок швидкого переходу механічної енергії удару в теплову. А розжарене залізо легко спалахує на повітрі і запалює трут. До винаходу сірників такий спосіб добування вогню був широко поширений. За цим же принципом влаштована старовинна зброя - кременевий пістолет, тільки в нім замість труту запалав порох.
Повідомлення 2 команди:
У неорганічній природі силіцій, мабуть, грає таку ж важливу роль, як карбон в живій. По поширеності в земній корі силіцій – другий (після кисню) элемент.12% маси земної кори складає кремнезем і більш75% - складніші кисневі з'єднання силіцію (глини, сланці, польові шпати, слюда і так далі) Потрапляючи в тканині рослин і відкладаючись в них, з'єднання силіцію підвищують їх жорсткість, і здатність рости вгору. Не випадково особливо багато кремнію в рослинах “ високого зростання” - в бамбуку хвощах; зола одного з хвощів містить до 20% SіO2. Багато силіцію і в стеблах жорсткої осоки (пригадайте, як неприємно – точно вістрям бритви – порізатися осокою)
Повідомлення 3 команди.
Карбон – один з не багатьох елементів, ім'я першовідкривача якого невідоме. Алмаз, графіт, не кажучи вже про вугілля, знайомі людству з якнайдавніших часів.
Атом карбону має два стійкі ізотопи: 12С і 13С. Дуже важливий радіоактивний ізотоп карбону 14С, що випускає α - частинки і період напіврозпаду, що має 5570 років.
Відкриття цього ізотопу мало надзвичайно важливі наслідки для археології, геології, палеонтології і історії! За допомогою цього ізотопу учені змогли досить точно визначати вік карбонвмістних порід, стоянок стародавньої людини, його починання, останків тварин і рослин, давно зниклих з лиця землі. Визначаючи радіоактивність неживої органічної речовини, і порівнюючи її з радіоактивністю такої ж кількості органічної речовини живої рослини, можна розрахувати час, протягом якого відбувався розпад 14С. Іншими словами – дізнатися вік знахідки.
Недаремно говорять, що всі науки зв'язані між собою і залежать одна від одної.
Додатковий матеріал
2 етап - Домашнє завдання
-
- Завдання 1 команди: Складіть рівняння реакцій,, які відбуваються з утворенням оксиду карбону(IV) в побуті, в промисловості, в лабораторії.
- Завдання 2 команди: Свіча, яка горить(лучина), гасне в нітрогені і в оксиді карбону(IV) Чому? Як ці гази можна відрізнити один від одного?
Завдання 3 команди: Чому в вогнегасниках використовують натрій гідрокарбонат , а не натрій карбонат?
- Завдання 1 команди: Складіть рівняння реакцій,, які відбуваються з утворенням оксиду карбону(IV) в побуті, в промисловості, в лабораторії.
4 етап – Завдання – змагання
| 1 команда  |
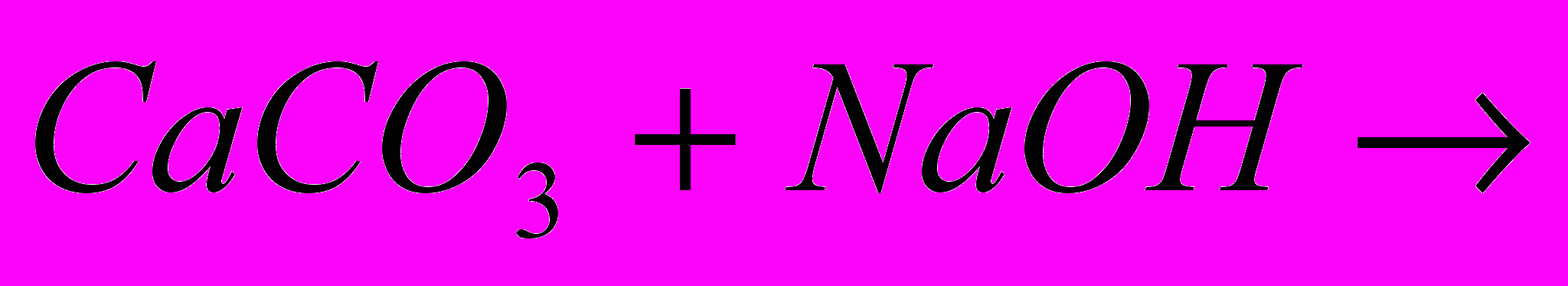 |
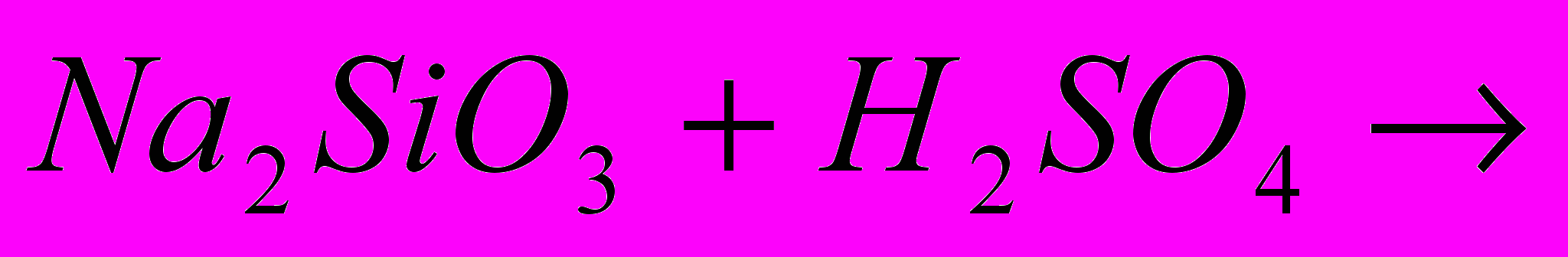 |
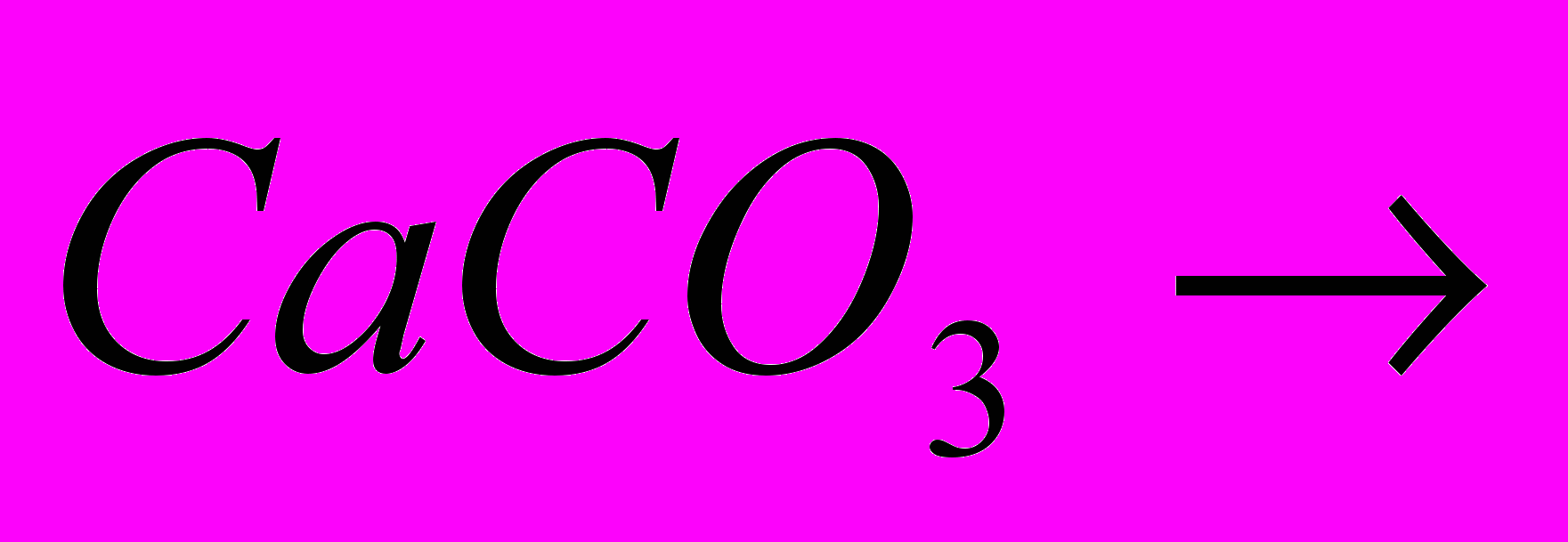 |
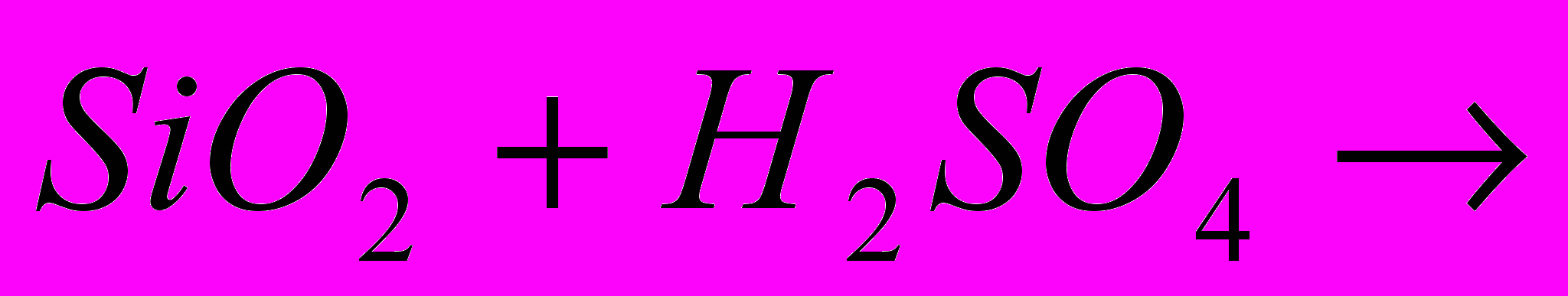 |
| Задача: При відновленні оксида заліза (ІІІ) карбоном, було отримано 10,08 г заліза, що склало 90% від теоретично можливого виходу. Яка маса оксида заліза (ІІІ))? |
4 етап – Завдання – змагання
| 2 команда  | |
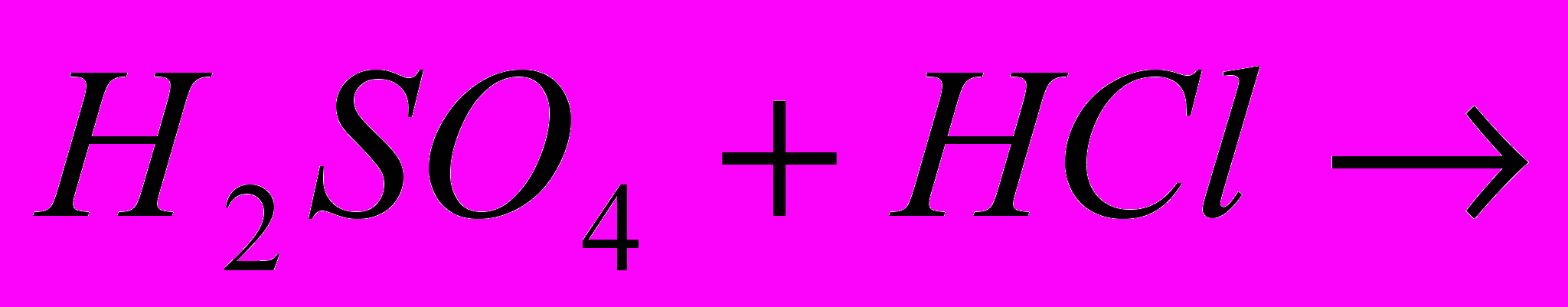 | |
 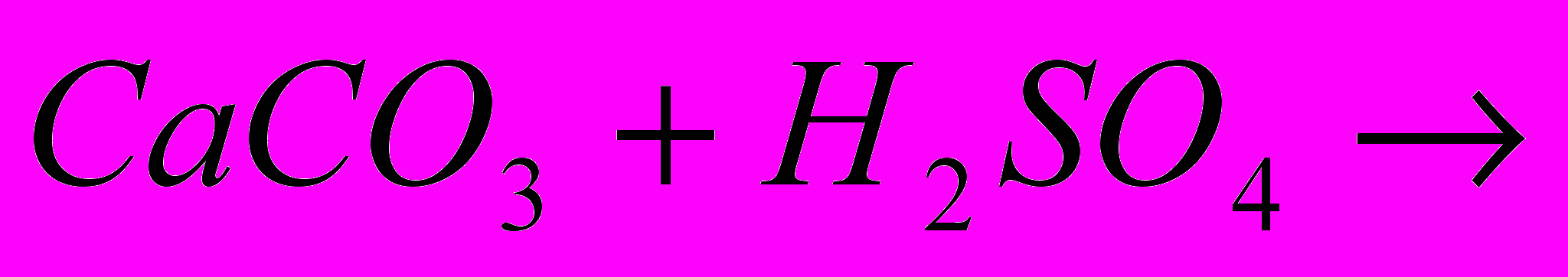 | |
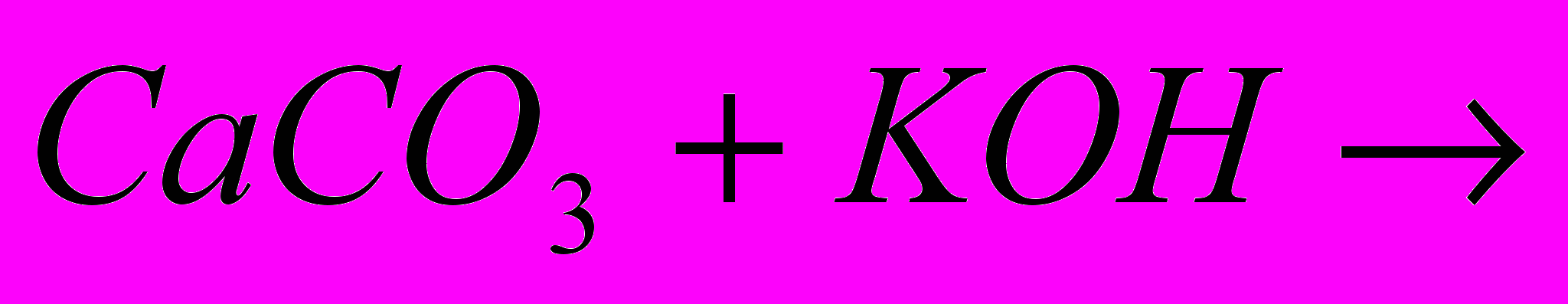 | |
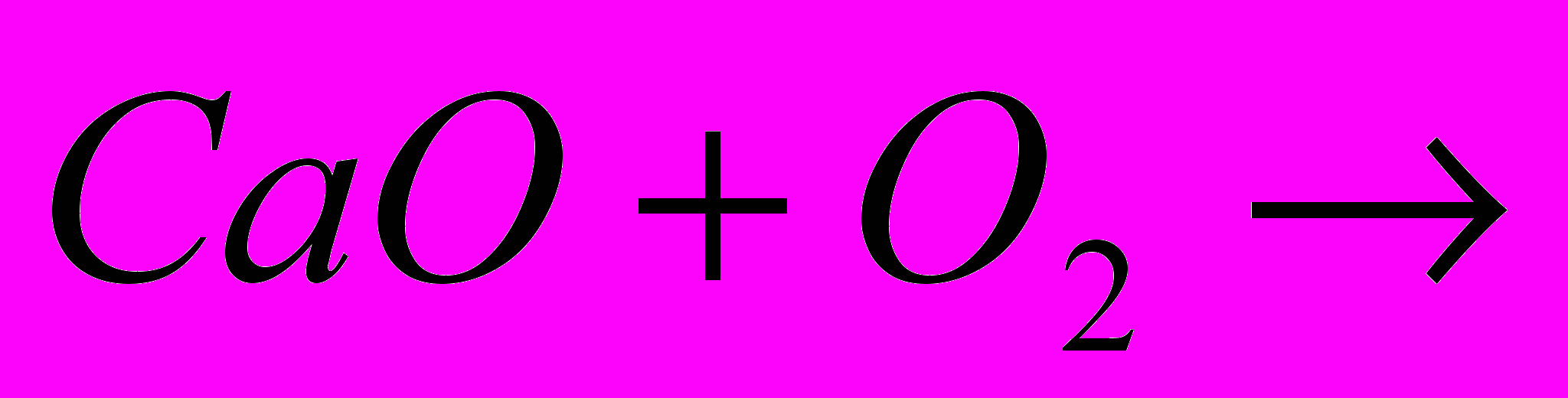 | |
| Задача: Скільки силікату натрію отримаємо при сплавленні оксида силіція (IV) з 64,2 кг соди, в якій міститься 5% домішок |
4 етап – Завдання – змагання
| 3 команда  |
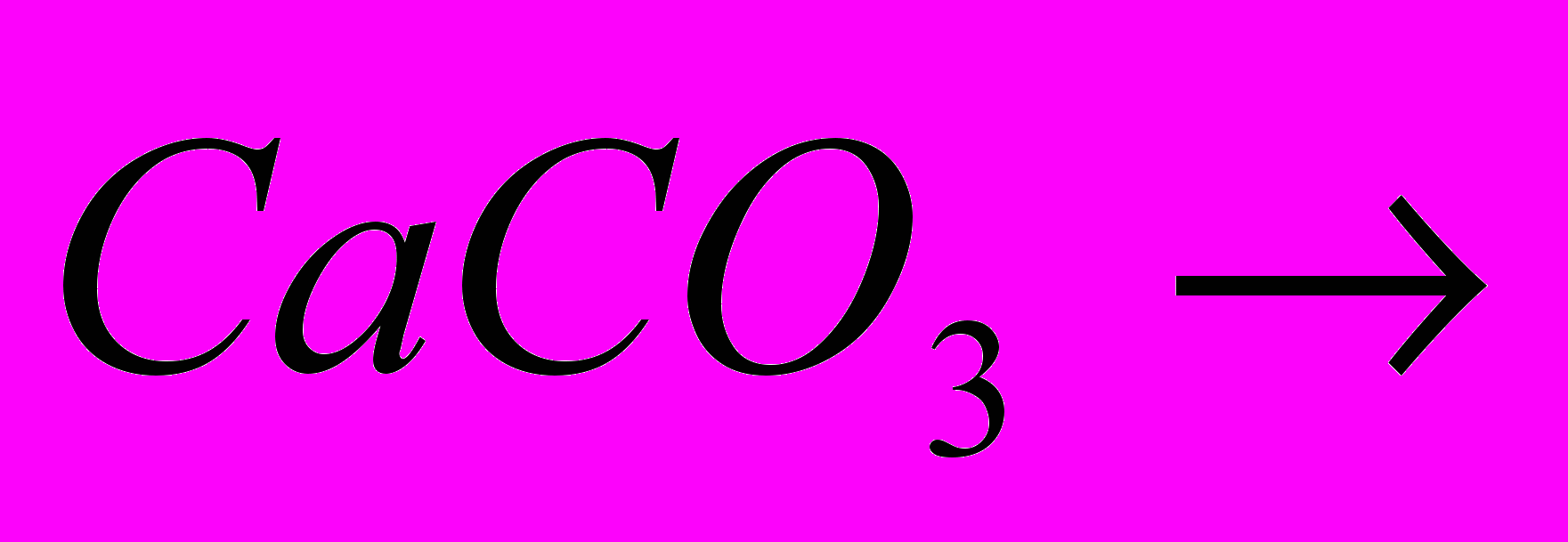 |
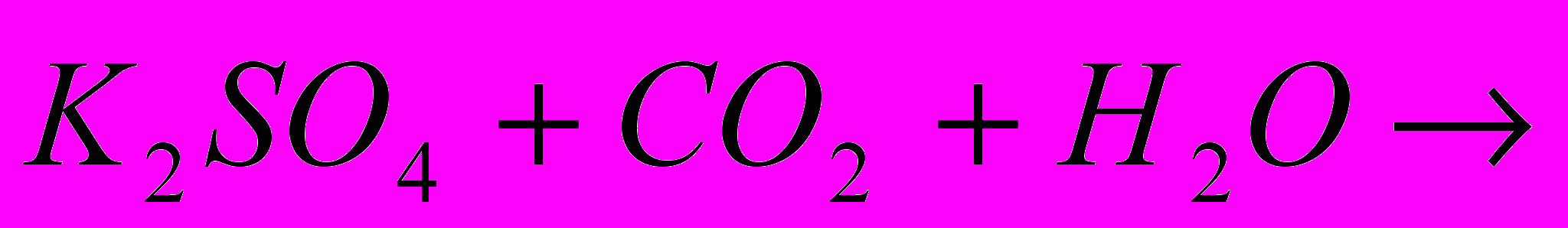 |
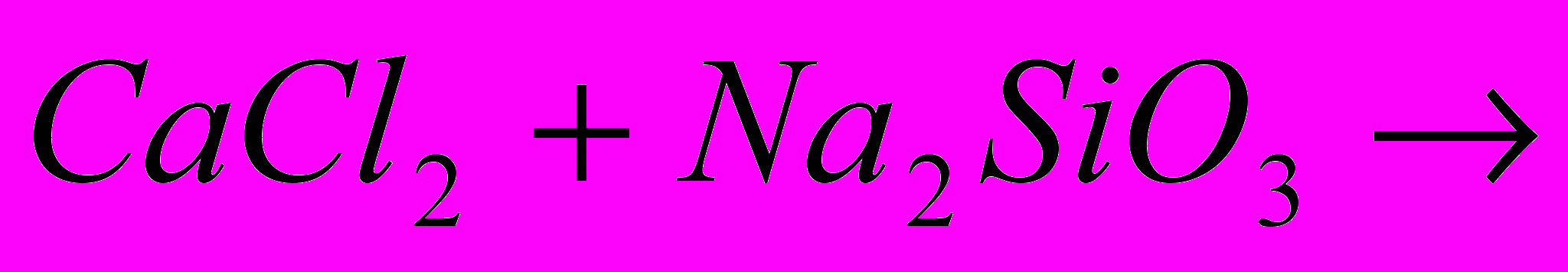 |
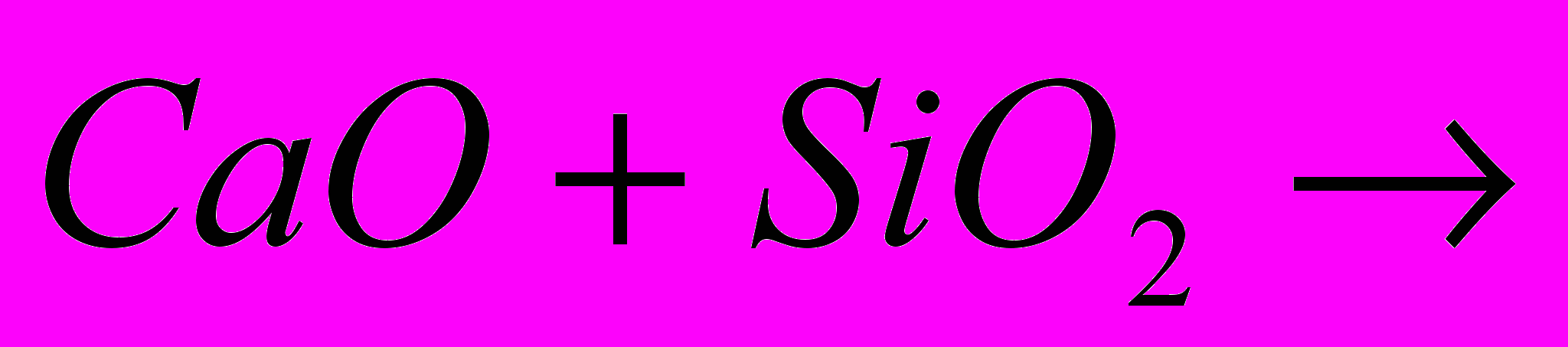 |
| Задача: При дії хлоридної кислоти на 50 г карбонату кальцію отримали 20 г оксиду карбону (IV). Який вихід оксиду карбону (IV) ( в %) від теоретично можливого? |
Кросворд.
По вертикалі:
1. Сіль карбонової кислоти.
По горизонталі:
1.Має формулу SiO2. Зустрічається в природі в вигляді піску.
При накалюванні суміші піску з вуглем отримують карборунд, який використовують для вигнотовлення точильних каменів.
2.Формула CaCO3 входить до складу вапнякових порід. Прозорий різновид – ісландський шпат, використовують для виготовлення призм в оптичних приладах.
3.Сама розповсюджена гірська порода. Складається з кварцу, польового шпату і слюди. Містить до 70% кремнезему. Гарний будівельний матеріал
4.3MgO*2H2O*2SiO3-природний силікат магнію, відрізняється вогнестійкістю. Використовується в якості тепло - і електроізоляційного матеріалу.
5.
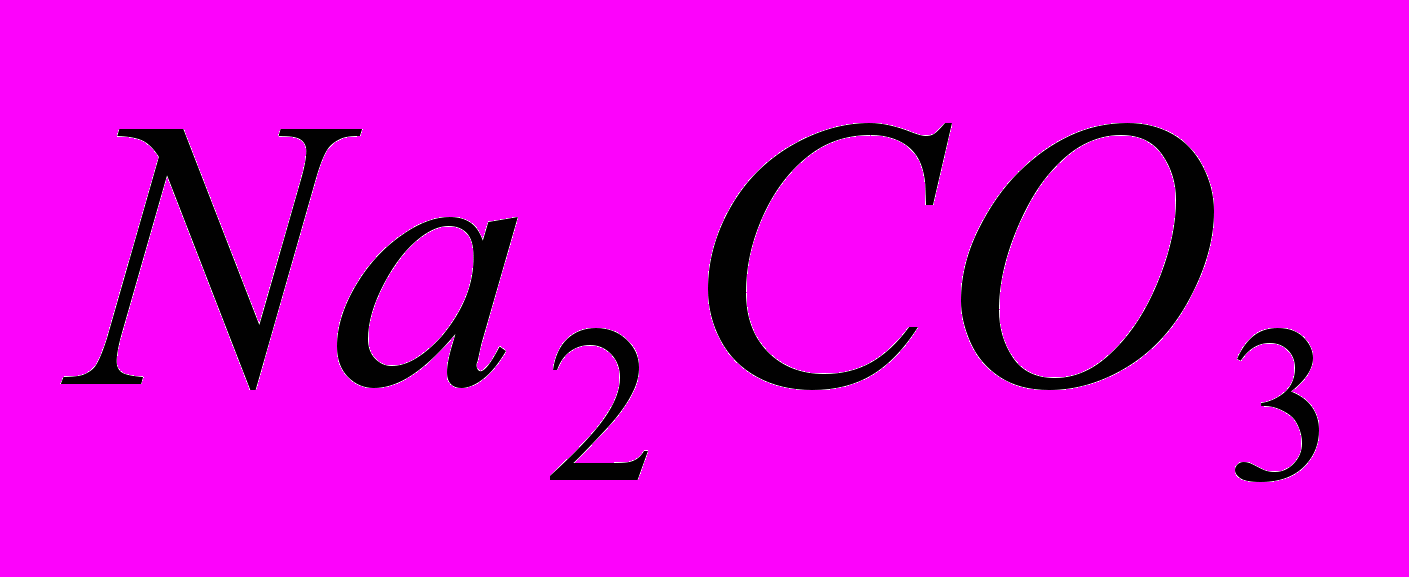 .безбарвна кристалічна речовина. Належить до найважливіших хімічних продуктів. У дуже великій кількості застосовується в ссылка скрыта, ссылка скрыта, ссылка скрыта і ссылка скрыта, а також у паросиловому господарстві для пом’якшення води і в домашньому побуті.
.безбарвна кристалічна речовина. Належить до найважливіших хімічних продуктів. У дуже великій кількості застосовується в ссылка скрыта, ссылка скрыта, ссылка скрыта і ссылка скрыта, а також у паросиловому господарстві для пом’якшення води і в домашньому побуті.6.Al2 O3*2SiO2*2H2O. Слугує основною сировиною в керамічній промисловості, в якій виготовляють фарфор и фаянс.
7.(CuOH)2CO3. Свою назву цей мінерал зеленого кольору отримав від грецького слова отримав «малхе», що значить «трава».В древності печатки з цього мінералу відрізнялися чіткістю відтисків.
8.3MgO*H2O*4SiO2-природний магнія силікат. Використовується в паперовій, парфумерній промисловості, в медицині.
| | 1 | | | | | | | ||
|---|---|---|---|---|---|---|---|---|---|
| | | 2 | | | | | | | |
| 3 | | | | | | | | ||
| 4 | | | | | | | | ||
| | 5 | | | | | | |||
| 6 | | | | | | | |||
| | 7 | | | | | | | | |
| | 8 | | | | | | | ||
