«Загальні відомості про неметали та їх сполуки»
| Вид материала | Урок |
- Загальні висновки І рекомендації 8 Список використаної літератури 9 Додатки, 569.55kb.
- План загальні історичні відомості про розвиток малярства на склі, зокрема на Гуцульщині., 207.25kb.
- І. Загальні відомості про хвору дитину (praefatio), 518.46kb.
- Предмет: Органічна хімія Мета, 369.43kb.
- Муровомокуриловецький р-н, Вінницька обл, 2723.63kb.
- Про суспільно-політичну ситуацію у лютому 2012 року, 119.31kb.
- Програма вступного іспиту з фаху на напрям 100101"Енергетика та електротехнічні системи, 43.34kb.
- Лекція 1 хф (лекція) Тема Загальні властивості неметалів, 1201.72kb.
- Зміст навчальної програми з вищої математики для студентів 1 курсу фармацевтичного, 32.69kb.
- 1. Загальні відомості про суб'єкта господарювання*, 78.9kb.
Головне управління освіти і науки
Харківської обласної державної адміністрації
Харківський обласний методичний центр професійно – технічної підготовки
Вище професійно – технічне училище будівництва
Розділ І. «Загальні відомості про неметали та їхні сполуки»
(27 год)
Тема3 «Карбон і силіцій»(9 годин)
Урок № 27-35
Тематична контрольна робота: урок №35
Викладач: ЖакунВМ
Розділ 1
Тема «Загальні відомості про неметали та їх сполуки»
(9 годин)
| Урок № 27. | Карбон і Силіцій, їх місце в періодичній системі, будова атомів. Алотропні модифікації Карбону. |
| Урок № 28 | Хімічні властивості карбону і силіцію: взаємодія з киснем, воднем, відновні властивості. |
| Урок № 29 | Оксиди карбону (II) і карбону (ІУ), Оксид силіцію (IV). їхні властивості, застосування. Поняття про парниковий ефект. |
| Урок № 30 | Карбонатна кислота і карбонати. Якісна реакція на карбонат-іони. Перетворення карбонатів. Поняття про кислі солі. Поняття про твердість води |
| Урок № 31 | Практична робота. Добування оксиду карбону (IV). Взаємоперетворення карбонатів і гідрокарбонатів |
| Урок № 32 | Кругообіг Карбону в природі |
| Урок № 33 | Силікатна кислота і силікати .Будівельні матеріали |
| Урок № 34 | Поширення Карбону і Силіцію в природі, їхнє значення в живій і не живій природі |
| Урок № 35 | Контрольна робота |
Зміст тематичної папки
- Перелік питань, які будуть відпрацьовані при вивчені теми: «Карбон і Силіцій»
- Плани уроків з конспектами до уроків і прикладами дидактичного матеріалу.
- Завдання для оцінювання знань учнів.
- Характеристика теми.
- Методичні рекомендації
Питання, які будуть відпрацьовані при вивчені теми: «Карбон і Силіцій»
1. Характеристика Карбону і Силіцію за положенням у ПСХЕ. Будова атома. Можливі ступені окиснення.
2. Поширення Карбону і силіцію в природі
3. Алотропні модифікації Карбону.
4. Адсорбція
5. Хімічні властивості карбону і його отримання.
6.Хімічні властивості силіцію і його отримання.
7 Оксиди карбону і силіцію (будова молекул, фізичні властивості, хімічні властивості, отримання.)
8.Якісна реакція для виявлення вуглекислого газу.
9. Карбонатна кислота та її властивості
10. Якісна реакція на карбонат іони.
11Твердість води ( постійна і непостійна).
12. Методи усунення твердості води.
13.Дослідження впливу засобів побутової хімії
14 Кругообіг карбону в природі.
15.Силікатна кислота, її властивості
16. Будівельні матеріали.
№ уроку 27
Тема: Загальні відомості про неметали та їх сполуки
Тема уроку: Карбон. Будова атома. Алотропні модифікації Карбону. Адсорбція.
Мета: познайомити учнів з представниками четвертої групи головної підгрупи – Карбоном і силіцієм; розглянути будову атома, валентні можливості атома Карбону і сіліцію; вивчити алотропні модифікації цієї речовини, їх властивості, застосування; вивчити явище адсорбції; вдосконалювати вміння складати опорний конспект, а також уміння аналізувати, порівнювати, узагальнювати різні факти.
Обладнання і матеріали: Періодична система хімічних елементів Д.І.Менделєєва, дидактичний роздатковий матеріал.
Тип уроку: вивчення нового матеріалу.
Хід уроку.
- Організаційний етап
- Перевірка облікового складу учнів
- Перевірка готовності групи до уроку
- Запис дати, теми, плану уроку.
2. Підготовка до основного етапу занять (мотивація)
Відгадайте загадку:
Зовут меня на букву «С»
Всё видно на моём лице,
Валентность у меня четыре,
Бывает иногда и два.
По атомной 12 массе
Встречаюсь я везде, всегда.
В свободном виде – крайне редко
Алмазом крепким я лежу.
А вот графитом – очень часто,
Везде и всюду я пишу.
Но это только в чистом виде,
А если посмотреть вокруг –
В живых и мёртвых организмах,
В угле, и торфе, и оксидах,
В солях, кислотах, даже в меле –
Везде и всюду я живу.
Сьогодні ми відвідаємо країну Карбону – елемента життя. Карбон відкриває головну підгрупу четвертої групи.

3. Вивчення нового матеріалу.
рацію знебарвлення розчину лакмусу таблетками активованого вугілля. Користуючись параграфом підручника дають відповідь на питання 113 на с.86 |
Карбон – хімічний елемент IV групи головної підгрупи Періодичної системи Д.І.Менделєєва, належить до макроелементів.
| C | 6 |
| 12,0107 | |
| 2s22p2 | |
| карбон | |
У природі існує у вигляді простих речовин алмазу та графіту, а також у вигляді сполук. Карбон входить до складу 112 мінералів і гірських порід, горючих корисних копалин, зокрема, антрацит містить 96% карбону, нафта – 85%, кам’яне вугілля – 80%, деревина – 50%. Карбон є складовою горючих сланців, природного, попутного й нафтових газів. У вигляді сполук присутній в атмосфері, гідросфері, в рослинах, тваринах та в організмі людини.
Карбон поширений у космосі. Метан (СН4) та вуглекислий газ (СО2) знайдено в складі майже всіх планет Сонячної системи та Сонця. Сполуки Карбону присутні в зірках, кометах, туманностях та метеоритах. Доведено, до виникнення Карбону в зіркових речовинах – результат термоядерних реакцій.
Карбон у вигляді вуглекислого газу входить до складу атмосфери та складає за об’ємом 0,03%. У гідросфері цього газу майже в 60 разів більше, ніж в атмосфері.
У живих організмах частка Карбону може становити майже 18% за масою. Рослини на світлі поглинають вуглекислий газ і синтезують вуглеводні – сполуки Карбону. Цей процес називається фотосинтезом.
У той же час вуглекислий газ безперервно наповнює атмосферу за рахунок життєдіяльності тварин, рослин, людини, вулканічної діяльності, тобто відбувається постійний кругообіг Карбону в природі.
Важко уявити існування життя на планеті Земля без Карбону. Карбон – життєво важливий елемент організму людини, оскільки є скелетною основою всіх органічних сполук. Вміст Карбону в організмі людини масою 70 кг становить 14,7 кг (21%). Карбон входить до складу білків, нуклеїнових кислот, жирів, вуглеводів, ферментів, вітамінів, гормонів та мінеральних солей.
Вміст Карбону в білках становить 50 – 55%, у глюкозі – 40%, у глікогені – 44,44%. Вітамін Е містить 80,93% Карбону, вітамін Д – 92,09%. Один з гормонів – адреналін – на 59% складається з цього елемента.
Потрапляє Карбон в організм людини разом з питною водою (у вигляді іонів НСО32-) та з продуктами харчування. Продукти рослинного і тваринного походження містять білки, жири, вуглеводи, вітаміни, мінеральні солі, з яких організм будує свої органи, здійснює життєві процеси.
Антропогенними джерелами надходження Карбону в довкілля є аерозолі, що крім сажі містять СО та СО2, промислові підприємства автомобільного транспорту й побутові опалювальні системи.
Через органи дихання сажа потрапляє в організм людини, де спричиняє антракози, бронхіти, які згодом провокують виникнення туберкульозу та онкологічні хвороби людей. Найчастіше такі хвороби виникають у шахтарів, робітників коксохімічних печей, цукрорафінадних заводів та робітників, зайнятих на виробництві й використанні технічного вуглецю. Дрібні часточки сажі, потрапляючи в око, призводять до різних захворювань очей. У разі постійного контактування шкіри робітників із сажею можливий розвиток шкірних хвороб у вигляді дерматитів і дерматозів. Потрапляючи в ротову порожнину, сажа руйнує зуби.
Алотропні модифікації Карбону.
XVII ст.: Аксель де-Бут, а потім Ньютон висловили припущення про те, що алмаз повинен горіти.
1694 р: флорентійські академіки провели дослід спалювання алмазу у фокусі вигнутого дзеркала. Алмаз спочатку тлів, як вугілля, а потім повністю згорів.
1772 р: Лавуазьє остаточно довів, що при спалюванні алмазу, як і при спалюванні вугілля, виходить лише вуглекислий газ.
1779 р: Шееле довів, що графіт та вугілля – видозміни одного й того самого елемента.
1797 р: Теннант після багатьох дослідів дійшов висновку: алмаз – чистісінький Карбон.
1841 р: Берцеліус вперше дав характеристику сажі, алмазу та графіту як видозмінення того самого елемента і ввів у хімію поняття „алотропія”.
1968 р: в лабораторії російського вченого Сладкова синтезували ще одну алотропну модифікацію Карбону – карбін, що має лінійну структуру.
1985 р: вчені США одержали нову алотропну модифікацію – букибол С60, який має сферичну структуру (форма футбольного м’яча)
|
4. Закріплення знань
Учні разом з вчителем розбирають тести.
5. Домашнє завдання. Робота з конспектом, знайти матеріал про:
- вуглецевий годинник,
- історію відкриття адсорбції
6. Підведення підсумків уроку.
1. Самооцінювання учнів
2. Оцінювання учителем роботи класу та окремих учнів
3. Аргументація виставлених оцінок
Головне управління освіти і науки
Харківської обласної державної адміністрації
Харківський обласний методичний центр професійно – технічної підготовки
Вище професійно – технічне училище будівництва
м. Харків
Самостійна робота з теми
«Карбон і Силіцій»
Тема уроку:«Карбон. Будова атома. Алотропні модифікації Карбону. Адсорбція.»
Назва самостійної роботи: «Характеристика елемента за положенням у Періодичній системі хімічних елементів Д.І. Менделєєва»
Урок № 27
Урок №27
Самостійна робота
«Характеристика елемента за положенням у Періодичній системі хімічних елементів Д.І. Менделєєва»
| C | 6 |
| 12,0107 | |
| 2s22p2 | |
| Карбон | |
План характеристики:
- Назва елементу
- Порядковий номер елемента (заряд ядра).
- Період, в якому знаходиться елемент (кількість енергетичних рівней).
- Група, в якій знаходиться елемент (кількість електронів на зовнішньому енергетичному рівні.)
- Визначити за положенням в періодичній системі Д.І. Менделєєва до металів, або неметалів відноситься елемент.
- Атомна маса елементу.
- Написати формулу найвищого оксиду.

Головне управління освіти і науки
Харківської обласної державної адміністрації
Харківський обласний методичний центр професійно – технічної підготовки
Вище професійно – технічне училище будівництва
м. Харків
Самостійна робота з теми
«Карбон і Силіцій»
Тема уроку:«Карбон. Будова атома. Алотропні модифікації Карбону. Адсорбція.»
Назва самостійної роботи: «Карбон. Поширення у природі»
Урок № 27
Урок №27
Самостійна робота
«Карбон. Поширення у природі»
Завдання:
Зробити опорний конспект.
План
1 Поширення у природі у вигляді простих речовин
2.Поширення у космосі.
3.Знаходження карбону в складі атмосфери і гідросфери
4. Знаходження карбону в живих організмах.
У природі існує у вигляді простих речовин алмазу та графіту, а також у вигляді сполук. Карбон входить до складу 112 мінералів і гірських порід, горючих корисних копалин, зокрема, антрацит містить 96% карбону, нафта – 85%, кам’яне вугілля – 80%, деревина – 50%. Карбон є складовою горючих сланців, природного, попутного й нафтових газів. У вигляді сполук присутній в атмосфері, гідросфері, в рослинах, тваринах та в організмі людини.
Карбон поширений у космосі. Метан (СН4) та вуглекислий газ (СО2) знайдено в складі майже всіх планет Сонячної системи та Сонця. Сполуки Карбону присутні в зірках, кометах, туманностях та метеоритах. Доведено, до виникнення Карбону в зіркових речовинах – результат термоядерних реакцій.
Карбон у вигляді вуглекислого газу входить до складу атмосфери та складає за об’ємом 0,03%. У гідросфері цього газу майже в 60 разів більше, ніж в атмосфері.
У живих організмах частка Карбону може становити майже 18% за масою. Рослини на світлі поглинають вуглекислий газ і синтезують вуглеводні – сполуки Карбону. Цей процес називається фотосинтезом.
У той же час вуглекислий газ безперервно наповнює атмосферу за рахунок життєдіяльності тварин, рослин, людини, вулканічної діяльності, тобто відбувається постійний кругообіг Карбону в природі.
Важко уявити існування життя на планеті Земля без Карбону. Карбон – життєво важливий елемент організму людини, оскільки є скелетною основою всіх органічних сполук.
Вміст Карбону в організмі людини масою 70 кг становить 14,7 кг (21%). Карбон входить до складу білків, нуклеїнових кислот, жирів, вуглеводів, ферментів, вітамінів, гормонів та мінеральних солей.
Вміст Карбону в білках становить 50 – 55%, у глюкозі – 40%, у глікогені – 44,44%. Вітамін Е містить 80,93% Карбону, вітамін Д – 92,09%. Один з гормонів – адреналін – на 59% складається з цього елемента.
Потрапляє Карбон в організм людини разом з питною водою (у вигляді іонів НСО3-) та з продуктами харчування. Продукти рослинного і тваринного походження містять білки, жири, вуглеводи, вітаміни, мінеральні солі, з яких організм будує свої органи, здійснює життєві процеси.
Антропогенними джерелами надходження Карбону в довкілля є аерозолі, що крім сажі містять СО та СО2, промислові підприємства автомобільного транспорту й побутові опалювальні системи.
Через органи дихання сажа потрапляє в організм людини, де спричиняє антракози, бронхіти, які згодом провокують виникнення туберкульозу та онкологічні хвороби людей. Найчастіше такі хвороби виникають у шахтарів, робітників коксохімічних печей, цукрорафінадних заводів та робітників, зайнятих на виробництві й використанні технічного вуглецю.
Дрібні часточки сажі, потрапляючи в око, призводять до різних захворювань очей. У разі постійного контактування шкіри робітників із сажею можливий розвиток шкірних хвороб у вигляді дерматитів і дерматозів. Потрапляючи в ротову порожнину, сажа руйнує зуби.
Головне управління освіти і науки
Харківської обласної державної адміністрації
Харківський обласний методичний центр професійно – технічної підготовки
Вище професійно – технічне училище будівництва
м. Харків
Самостійна робота з теми
«Карбон і Силіцій»
Тема уроку:«Карбон. Будова атома. Алотропні модифікації Карбону. Адсорбція.»
Назва самостійної роботи: «Алотропні модифікації карбону»
Урок № 27
Урок №27
Самостійна робота
Алотропні модифікації карбону
XVII ст.: Аксель де-Бут, а потім Ньютон висловили припущення про те, що алмаз повинен горіти.
1694 р: флорентійські академіки провели дослід спалювання алмазу у фокусі вигнутого дзеркала. Алмаз спочатку тлів, як вугілля, а потім повністю згорів.
1772 р: Лавуазьє остаточно довів, що при спалюванні алмазу, як і при спалюванні вугілля, виходить лише вуглекислий газ.
1779 р: Шееле довів, що графіт та вугілля – видозміни одного й того самого елемента.
1797 р: Теннант після багатьох дослідів дійшов висновку: алмаз – чистісінький Карбон.
1841 р: Берцеліус вперше дав характеристику сажі, алмазу та графіту як видозмінення того самого елемента і ввів у хімію поняття „алотропія”.
1968 р: в лабораторії російського вченого Сладкова синтезували ще одну алотропну модифікацію Карбону – карбін, що має лінійну структуру.
1985 р: вчені США одержали нову алотропну модифікацію – букибол С60, який має сферичну структуру (форма футбольного м’яча)
Має чотири алотропні модифікації: алмаз, графіт, карбін і фулерен. :
Алмаз

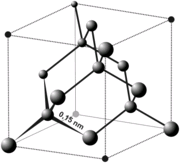  |  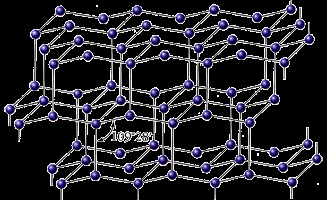 |
| Алмаз кубічний | Алмаз гексагональний |
Карбін
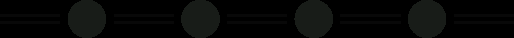
поліін
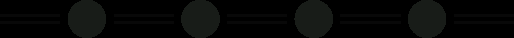
кумулен
Графіт.

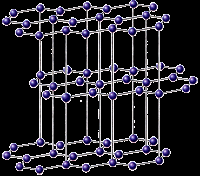
Фулерен.

Існує ще аморфний карбон – сажа, склоуглерод.
Заповнити таблицю:
| Властивості | Алмаз | Графіт |
| Тип кристалічної решітки | | |
| Твердість | | |
| Колір | | |
| Блиск | | |
| Електропровідність | | |
| Галузі застосування | | |
№ уроку28
Тема: Загальні відомості про неметали та їх сполуки
Тема уроку: Хімічні властивості вуглецю і силіцію: взаємодія з киснем, воднем, відновні властивості
Мета: розглянути хімічні властивості простих речовин утворених карбоном і силіцієм; дати уявлення про відновні властивості карбону і силіцію; повторити поняття окисник і відновник.
Тип уроку:. комбінований
Обладнання і матеріали: Періодична система хімічних елементів Д.І.Менделєєва, зразки мінералів: .колекція: «Мінеральні та гірські породи», «Вапняки»
Епіграф розумне вже передумане, треба тільки спробувати
передумати це ще один раз".
___________________
Базові поняття і терміни: відновні властивості, карбіди, силіциди, силани, активність і інертність елементів
Структура уроку:
1Організаційний етап.
2.Підготовка до основного етапу занять (мотивація).
3.Актуалізація опорних знань.
4.Вивчення нового матеріалу
5.Закріплення знань .
6.Домашнє завдання.
7.Підведення підсумків уроку
Хід уроку
1.Організаційний етап
- Перевірка облікового складу учнів
- Перевірка готовності групи до уроку
- Запис дати, теми, плану уроку.
2.Підготовка до основного етапу занять (мотивація).
На кожному уроці ми з вами проходимо маленьку сходинку в набуванні знань з хімії, а це є знаннями нашого життя, Скажіть, а чи потрібно нам знати як ведуть ті чи інші речовини в оточуючому нас середовищі. Можливо ці знання нам зовсім не потрібні?
Проблемне запитання:
Які сполуки карбону і силіцію на ваш погляд віджіграють в нашому житті важливу роль? Чому?
3.Актуалізація опорних знань:
Двоє учнів роблять доповіді по темам:
- вуглецевий годинник,
- історію відкриття адсорбції
Опитування:
- Де в періодичній системі знаходиться карбон?
- Де в періодичній системі знаходяться силіцій?
- Це метали чи неметали?
- З якими речовинами реагують неметали?
- Яку валентність і ступень окислення вони виявляють у сполуках?
4.Вивчення нового матеріалу
