«Федеральный центр сердца, крови и эндокринологии им. В. А. Алмазова Федерального агентства по оказанию высокотехнологичной медицинской помощи»
| Вид материала | Автореферат |
- Редукция полости левого предсердия при хирургической коррекции порока митрального клапана, 235.93kb.
- Особенности структурно-функциональных изменений миокарда и нарушения сердечного ритма, 287.4kb.
- Работа выполнена в Военно-медицинской академии им., 699.27kb.
- Ишемического инсульта, 630.79kb.
- «Уральский научно-исследовательский институт травматологии и ортопедии им. В. Д. Чаклина, 485.31kb.
- «Нижегородский научно-исследовательский институт травматологии и ортопедии Федерального, 434.13kb.
- Актуальные вопросы аритмологии, 88.42kb.
- Организация специализированной ортопедической помощи больным остеоартрозами тазобедренного, 840.56kb.
- «Военно-медицинская академия им. С. М. Кирова», 845.84kb.
- Гусаева ханум замрутдиновна современные аспекты патогенеза, диагностики и лечения сочетанных, 556.52kb.
2.11. Исследование пирогенности
Сумма повышения температуры у трех кроликов составила 0,6°C, что, в соответствии с требованиями ГФ XI, вып. 2, свидетельствует об отсутствии пирогенности у препарата «Аноцептин».
2.12. Результаты фармакокинетического исследования
2.12.1. Результаты исследования фармакокинетики препарата «Аноцептин» на животных
При внутривенном введении аноцептина собакам фармакокинетика препарата в плазме крови описывается 3-компартментной зависимостью. Первая фаза распределения протекает стремительно. За первые 10 минут из плазмы крови уходит около 95% препарата. Следующая фаза длится с 10 минуты и до начала 2-го часа. Среднее время присутствия препарата в организме – показатель MRT – составляет 5,5–6,0 часов. Высокие значения таких показателей, как клиренс (450-500 мл/кг/ч) и стационарный объем распределения (2,5 л/кг) свидетельствуют о том, что препарат очень активно распределяется из системного кровотока. Отсюда следует, что большая часть препарата, вероятно, не выводится, а подвергается метаболизму и утилизируется в самом организме. Учитывая химическую природу коменовой кислоты (наличие в ее структуре гидроксильной и карбоксильной групп), возможными ее метаболитами могут быть комплексные соединения с катионами металлов.
2.12.2. Результаты исследования фармакокинетики препарата «Аноцептин» у здоровых добровольцев
При внутривенном введении аноцептина здоровым людям изменение концентрации действующего вещества – коменовой кислоты – в плазме крови на основном участке описывается 2-х или 3-х частевой зависимостью (рис.1 и рис.2). Фаза распределения протекает быстро. В течение первых 10 минут концентрация снижается примерно в 4–5 раз, а в течение первого часа – в 200 раз. После 1-го часа, по-видимому, наступает фаза истинной элиминации с периодом полувыведения порядка 2.0–2.5 ч. MRT – лежит в диапазоне от 0,5 до 1,0 час. Клиренс – около 1000 мл/кг/ч. Основная часть препарата, не выводится, а матаболизируется и утилизируется в самом организме. Возможными метаболитами могут быть комплексные соединения с катионами металлов. Характер полученных кинетических кривых заставляет предположить, что фармакокинетика аноцептина определяется сочетанием кинетических и метаболических процессов. При высоких концентрациях основную роль играют распределение и выведение, а при низких – метаболизм. Следует отметить высокий уровень индивидуального разброса, особенно на участке, на котором можно предполагать доминирующую роль метаболических процессов. Возможно, именно эти процессы определяют судьбу препарата в организме в долгосрочном плане.
При изучении безопасности обнаружено, что препарат «Аноцептин» в исследуемых дозах (10, 20, 60мг/в сутки) при рекомендованном курсе лечения (10 дней) безопасен. Аноцептин не обладает раздражающим действием в местах инъекций, аллергических реакций в ходе исследования не выявлено. Препарат не оказывает негативного действия на нервную, пищеварительную, дыхательную, сердечно-сосудистую, выделительную, репродуктивную системы (Поляков Ю.И. и др., 2007; Polyakov Yu. I., et al., 2008).
Особое внимание было уделено клинической оценке возможных проявлений развития физической и психической зависимости. При структурированной беседе и клиническом обследовании ни у одного добровольца признаков психофизической зависимости, наблюдаемых при приеме наркотических аналгетиков, выявлено не было. Результаты исследования подтвердили данные доклинического исследования об отсутствии у препарата наркогенного потенциала (Поляков Ю.И. и др., 2007; Polyakov Yu. I., et al., 2008).
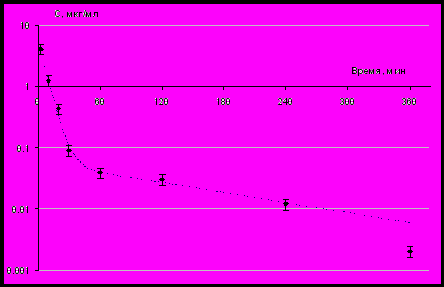
Рис. 1. Испытуемый № 3
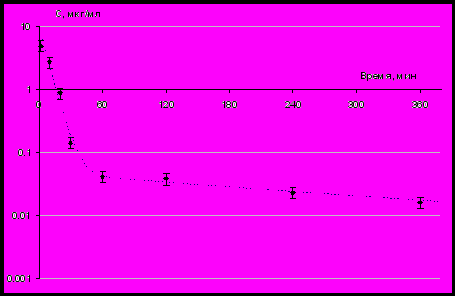
Рис. 2. Испытуемый № 7
ЗАКЛЮЧЕНИЕ
Проведенные исследования позволили теоретически и экспериментально обосновать новое перспективное направление – создание аналгетических средств, механизм действия которых основан на фармакологической модуляции сигнальной функции Na+,K+-АТФазы нейронов ЦНС. Тест-системой для исследований в экспериментах in vitro, осуществляемых с помощью patch-clamp метода, стал ансамбль, состоящий из 3-х (Крылов Б.В. и др., 1999) или 2-х звеньев. В первом случае ноцицептивные сигналы при прохождении через систему, включающую в себя опиоидоподобный рецептор – Na+,K+-АТФазу (трансдуктор) – Nav1.8-канал (эффекторное звено) можно регулировать рецептор-опоредованно при помощи коменовой кислоты. Во втором случае ансамбль составляют два звена – Na+,K+-АТФаза и Nav1.8-канал. Оуабаин в концентрациях, сопоставимых с эндогенными, регулирует ноцицептивные сигналы трансдуктор-опосредованно. Впервые на сенсорных нейронах ЦНС млекопитающих удалось получить доказательства того, что Na+,K+-АТФаза одновременно может выполнять функции рецептора к сердечным гликозидам и трансдуктора ноцицептивных сигналов, функционируя в ансамбле с Nav1.8-каналом. Участие Na+,K+-АТФазы в модуляции ноцицептивных сигналов нашло свое подтверждение в условиях формалинового теста. Анализ полученных данных показал, что физиологическая роль эндогенного оуабаина заключается в трансдуктор-опосредованной регуляции ноцицептивной информации на разных этапах онтогенеза, при стрессе и развитии воспалительного процесса.
Исследование участия Na+,K+-АТФазы в регуляции роста и развития клеток разных тканей в эмбриональный период онтогенеза подтвердило, что сигнальную функцию фермента также можно модулировать двумя путями. В первом случае фармакологическими агентами были оуабаин, строфантин К, дигоксин. Сочетание теоретических квантовохимических расчетов и метода органотипической культуры ткани позволило доказать, что наличие в молекуле оуабаина рамнозильного остатка определяет тканеспецифичность сердечного гликозида, повышает аффинность Na+,K+-АТФазы к этому стероиду и увеличивает вероятность модуляции сигнальной функции фермента. Во втором случае сигнальную функцию фермента рецептор-опосредованно модулировала производная гамма-пирона коменовая кислота. Наибольшую тропность исследуемые вещества проявили в отношении регуляции роста и пролиферации клеток тканей нейронального происхождения. Результаты экспериментов свидетельствуют о том, что α3-изоформа α-субъединицы Na+,K+-АТФазы оказывает тонкое регуляторное действие на рост и пролиферацию клеток возбудимых тканей в эмбриональный период онтогенеза, выполняя функцию трансдуктора сигнала.
Благодаря проведенным исследованиям разработан оригинальный лекарственный препарат с аналгетической активностью, механизм действия которого связан с рецептор-опосредованной модуляцией сигнальной функции фермента. Доказана его безопасность и эффективность. Взаимодействие лиганда (хелатного комплекса натриевой соли коменовой кислоты) с рецептором мембраны ноцицептивных нейронов спинальных ганглиев служит сигналом для активации ансамбля: опиоидоподобный рецептор – Na+,K+-АТФаза (трансдуктор) – Nav1.8-канал (эффекторное звено). Аноцептин проникает через гематоэнцефалический барьер, аналгетический эффект наступает через 4 минуты после попадания препарата в кровоток и сохраняется до 6 часов. Обнаружены противовоспалительный и трофотропный эффекты препарата. Эти эффекты отставлены во времени и развиваются постепенно после курса инъекций аноцептина. Доказано, что применение препарата «Аноцептин» не вызывает активации системы положительного подкрепления латерального гипоталамуса. При длительном парентеральном введении аноцептина не отмечается развитие лекарственной зависимости, наркогенный потенциал у препарата отсутствует. На модели экспериментального туберкулезного хориоретинита показано, что препарат «Аноцептин» достоверно повышает эффективность стандартной терапии, хорошо сочетается с антибиотиками и позволяет сохранить клетки пигментного эпителия сетчатки в зоне параспецифического воспаления.
Аналгетические свойства аноцептина реализуются за счет снижения потенциалочувствительности активационного воротного устройства Nav1.8-канала. Проведенные исследования позволили теоретически и экспериментально обосновать новое перспективное направление – создание аналгетических средств, обладающих противовоспалительными свойствами, механизм действия которых основан на фармакологической модуляции сигнальной функции Na+,K+-АТФазы.
ВЫВОДЫ
1. Оуабаин в концентрациях, сопоставимых с эндогенными, модулирует сигнальную функцию Na+,K+-АТФазы. Наличие рамнозильного остатка в молекуле гликозида определяет его тканеспецифичность и повышает аффинность Na+,K+-АТФазы мембраны клеток разных типов к оуабаину.
2. При трансдуктор-опосредованной модуляции оубаином Na+,K+-АТФазы происходит снижение потенциалочувствительности активационного воротного устройства Nav1.8 каналов мембраны ноцицептивных нейронов спинальных ганглиев, что свидетельствует о способности гликозида регулировать ноцицептивные сигналы.
3. Сигнальная функция Na+,K+-АТФазы заключается в обеспечении модуляции процесса кодирования ноцицептивных сигналов ансамблем: опиоидоподобный рецептор – Na+,K+-АТФаза – Nav1.8-канал (либо Na+,K+-АТФаза – Nav1.8-канал) мембраны ноцицептивных нейронов спинальных ганглиев и регуляции тканевого моделирования на различных этапах онтогенеза.
4. При регуляции процессов роста и пролиферации кардиомиоцитов и клеток ткани сетчатки и роста нейритов сенсорных нейронов в эмбриональный период онтогенеза оуабаин в эндогенных концентрациях по эффективности превосходит строфантин К, дигоксин, оуабагенин и сопоставим с коменовой кислотой.
5. По своему действию на потенциалочувствительность активационного воротного устройства медленных натриевых каналов мембраны ноцицептивных нейронов коменовая кислота близка к влиянию сердечного гликозида оуабаина.
6. На основе производной гамма-пирона коменовой кислоты создан препарат «Аноцептин». Инъекция аноцептина мышам в тесте «горячая пластина» и крысам в формалиновом тесте оказывает выраженное болеутоляющее действие. Аналгетический эффект препарата проявляется через 4-6 минут после парентерального введения и сохраняется до 6 часов. В дозах, оказывающих аналгетическое действие, аноцептин угнетает реакцию самостимуляции латерального гипоталамуса крысы, что свидетельствует об отсутствии у животных лекарственной зависимости от препарата. Терапевтический индекс аноцептина в экспериментах на крысах соответствует 64. У препарата отсутствуют канцерогенные и тератогенные свойства. Аноцептин апирогенен.
7. После парабульбарного введения аноцептина в течение 10 дней проявляется противовоспалительный эффект препарата. В опытах in vitro аноцептин не обнаружил антимикробной активности в отношении микобактерий туберкулеза. Использование аноцептина при комплексной химиотерапии экспериментального туберкулезного хориоретинита сопровождается повышением эффективности лечения за счет уменьшения воспалительных явлений в очаге поражения. Аноцептин, оказывая активирующее влияние на трофические процессы в сетчатке, на фоне комплексной противотуберкулезной терапии экспериментальных туберкулезных хориоретинитов способствует сохранению клеток пигментного эпителия как в зоне параспецифического воспаления (в 90%), так и в области очага (в 33%).
8. Безопасность действия аноцептина в терапевтических дозах подтверждена в клиническом исследовании. Препарат в дозах, вызывающих аналгетическое действие, у здоровых людей не оказывает побочного влияния на нервную, пищеварительную, дыхательную, сердечно-сосудистую, выделительную системы, не обладает раздражающим действием в местах инъекций. Отсутствует психофизическая зависимость при длительном приема препарата.
9. Распределение препарата при внутривенном введении у здоровых добровольцев описывается 2-х или 3-х компартментной зависимостью. Аноцептин быстро исчезает из системного кровотока, в течение первых 10 минут концентрация препарата снижается в 4–5 раз. Среднее время присутствия препарата в организме лежит в диапазоне от 0,5 до 1,0 час. Клиренс - около 1000 мл/кг/ч. Основная часть препарата, не выводится, а матаболизируется и утилизируется в самом организме.
10. На основе изучения влияния соединений, изменяющих активность Na+,K+-АТФазы, разработана новая методология поиска и изучения обезболивающих препаратов, механизм действия которых основан на модуляции сигнальной функции этого фермента.
РАБОТЫ, ОПУБЛИКОВАННЫЕ ПО ТЕМЕ ДИССЕРТАЦИИ
ПАТЕНТЫ
1. Крылов Б.В., Лопатина Е.В. «Синтетическое анальгетическое средство и способ лечения на основе этого средства» патент РФ № 2322977 приоритет от 01.08. 2006 МПК А61К031/351А61Р029/02 дата публикации 27.04.2008. Бюллетень изобретений. № 12- 2008. - С. 1-30.
2. Крылов Б.В., Лопатина Е.В «Анальгетическое средство и способ лечения болевого синдрома различной этиологии с помощью этого средства» патент РФ № 2367432 приоритет от 27.09.2007 МПК А61КА61Р дата публикации 20.09.2009. Бюллетень изобретений. - 2009. № 26 - С.1-25.
3. Лопатина Е.В., Карецкий А.В., Крылов Б.В. «Регенерирующее противовоспалительное средство и способы лечения с помощью этого средства» патент РФ № 2362554 приоритет от 27.09.2007 МПК А61КА61Р дата публикации 27.07.2009. Бюллетень изобретений. № 21 - 2009. - С. 1-27.
СТАТЬИ В ЖУРНАЛАХ, РЕКОМЕНДОВАННЫХ ВАК
- Лопатина Е.В., Пеннияйнен В.А., Зайка А.А. Исследования участия Na+,K+-АТФазы в регуляции роста эксплантатов ткани сердца в органотипической культуре. Бюллетень экспериментальной биологии и медицины. 2005. Т. 140. № 8. С. 150-153.
- Пеннияйнен В.А., Лопатина Е.В. Исследование роли Na+,K+-АТФазы в регуляции роста нейритов сенсорных нейронов. Бюллетень экспериментальной биологии и медицины. 2005. Т. 139, № 2. С. 147-160.
- Лопатина Е.В., Пеннияйнен В.А., Цырлин В.А. Сравнительный анализ действия сердечных гликозидов на роста эксплантатов ткани сердца. Российский Физиологический журнал им. И.М. Сеченова. 2005. Т. 91. № 11. С.1299-1304.
- Пеннияйнен В.А., Лопатина Е.В., Цырлин В.А., Крылов Б.В. Влияние ингибиторов натриевого насоса на рост нейритов сенсорных ганглиев. Российский Физиологический журнал им. И.М. Сеченова. 2008. Т.94. №3. С. 326-330.
- Лопатина Е.В., Пеннияйнен В.А., Рогачевский И.В., Крылов Б.В. Фармакологическая модуляция трансдукторной функции Na+,K+-АТФазы
Бюллетень экспериментальной биологии и медицины. 2008. Т.146. №10. С. 416-418.
- Лопатина Е.В., Карецкий А.В., Пеннияйнен В.А., Виноградова Т.В. Участие сердечных гликозидов в регуляции роста эксплантатов ткани сетчатки. Бюллетень экспериментальной биологии и медицины. 2008. Т.146. №12. С. 651-653.
- Рогачевский И.В., Лопатина Е.В., Пеннияйнен В.А., Крылов Б.В. Неэмпирический конформационный анализ хелатных комплексов молекулы оуабаина с Са2+ и возможный механизм модуляции трансдукторной функции Na+, K+-АТФазы. Журнал общей химии. 2008. Т.78. Вып. 10. С. 1673-1683.
- Penniyainen V. A., Lopatina E. V.,. Tsyrlin V. A, Krylov B. V.The effects of sodium pump inhibitors on sensory ganglion neurite growth //Neurosci. and Behav. Physiol. 2009. Vol.39. N. 3. - P. 301-304.
- Кипенко А.В., Пеннияйнен В.А., Лопатина Е.В., Рогачевский И.В., Цырлин В.А., Крылов Б.В. Роль оуабаина в регуляции роста тканей разных типов. Российский Физиологический журнал им. И.М. Сеченова. 2009. Т.95. №2. С. 137-142.
ОСНОВНЫЕ ПУБЛИКАЦИИ
- Лопатина Е.В., Пеннияйнен В.А., Шевцова Е.С. Роль Na+,K+-АТФазы, как регулятора процессов роста в клетках разных типов. Конгресс ассоциации кардиологов стран СНГ «Фундаментальные исследования и прогресс в кардиологии», СПб. 2003 г. Научно-практический ж. Кардиология СНГ Т.1. С. 173.
- Крылов Б.В., Щеголев Б.Ф., Лопатина Е.В., Буткевич И.П., Отеллин В.А. Новый метод купирования опиатного абстинентного синдрома. Роль медленных натриевых каналов. Фундаментальные науки – медицине. Москва (10-11 декабря) 2003. С.39-40.
- Лопатина Е.В., Пеннияйнен В.А., Зайка А.А. Исследование роли сердечных гликозидов в регуляции роста кардиомиоцитов. III Всероссийская с международным участием Школа-конференция по физиологии кровообращения, Москва. 2004. С.55-56.
- Лопатина Е.В., Пеннияйнен В.А. Участие сердечных гликозидов в регуляции роста кардиомиоцитов. XIX съезд физиологического общества им. И.П. Павлова. Российский Физиологический журнал им. И.М. Сеченова. 2004. Т. 90. № 8. С. 442-443.
- Пеннияйнен В.А., Лопатина Е.В. Исследование участия Na+, K+-АТФазы в регуляции роста клеток разных типов в органотипической культуре ткани. Сборник статей Международная конференция, посвященная юбилею И.П. Павлова, Минск. 2004. С. 298-299.
- Пеннияйнен В.А., Лопатина Е.В., Карецкий А.В., Хокканен В.М., Крылов Б.В. Влияние оуабаина и норадреналина на рост клеток сетчатки в органотипической культуре ткани. Сборник статей конференции, посвященной 60-летию Института глазных болезней им. Гельмгольца, Москва. 2004. С.25-26.
- Пеннияйнен В.А., Лопатина Е.В., Карецкий А.В., Хокканен В.М., Крылов Б.В. 3 изоформа Na/K-АТФазы модулирует процессы роста клеток сетчатки. XIX съезд физиологического общества им. И.П. Павлова. Российский Физиологический журнал им. И.М. Сеченова. 2004. Т. 90. № 8. С. 331-332.
- Карецкий А.В., Пеннияйнен В.А., Лопатина Е.В., Хокканен В.М., Крылов Б.В. Перспективы лечения осложнений хориоретинитов, в том числе туберкулезного характера. “Современные возможности диагностики и лечения витреоретинальной патологии”, Москва 27 мая 2004 года. Сб. науч. Статей по материалам науч.-пр. конф. - М.: "Экономика", 2004. С. 49-50.
- Карецкий А.В., Лопатина Е.В., Крылов Б.В., Пеннияйнен В.А., Хокканен В.М. Влияние Q-134 на рост клеток сетчатки в органотипической культуре ткани // Клеточные технологии в офтальмологии: регенеративная медицина и трансплантация тканей в офтальмологии: материалы международ. конф. – М., 2005. – С. 26-27.
- Karetsky A.V., Lopatina E.V., Penniyaynen V.A. α3-izoform of Na+, K+-ATPase modulates process of cells growth in the chicken retina. Humboldt-Kolleg Conference "Technologies of the 21st century: biological, physical, informational and social aspects", Saint-Petersburg. 2005. P.30.
- Lopatina E.V., Tsyrlin A.V. The influence of cardiac glycoside on the growth of explantat of cardiac tissue Humboldt-Kolleg Conference "Technologies of the 21st century: biological, physical, informational and social aspects" Saint-Petersburg. 2005. P.54-55.
- Рогачевский И.В., Плахова В.Б., Лопатина Е.В., Буткевич И.П., Крылов Б.В. Принципы создания новых лекарственных препаратов: от молекулряной физиологии до клинического эффекта // Исследование, разработка и применение высоких технологий в промышленности: Сб. трудов 2-й междунар. науч.-практ. конф. /Под ред. А.П.Кудинова и др.– Т.6. Высокие технологии, фундаментальные и прикладные исследования, образование. СПб.: Изд-во Политехн . Ун-та, 2006. С. 169-183.
- Лопатина Е.В., Карецкий А.В., Пенниянен В.А., Хокканен В.М., Крылов Б.В. Моделирование процесса пролиферации клеток сетчатки теплокровных. Морфология. 2006. Т .129. №2. С .55.
- Лопатина Е.В., Пеннияйнен В.А., Крылов Б.В., Цырлин В.А. Na/Ka - АТФаза модулирует синтетические процессы в тканях разных типов. Физиологическое общество им И.П.Павлова. Съезд XX, Москва. 4-8 июня, 2007.– М.: Издат. дом «Русский врач», 2007. С.311-312.
- Лопатина Е.В., Пеннияйнен В.А., Виноградова Т.В. Участие Na+, K+-АТФазы в регуляции роста ткани сетчатки в органотипической культуре. Всероссийская конференция студентов, аспирантов и молодых ученых «Наука и инновации в технических университета», Санкт-Петербург. 10-12 октября, 2007. С. 189.
- Лопатина Е.В., Пеннияйнен В.А.Физиологическая роль эндогенного оуабаина.// Гормональные механизмы адаптации: Программа и тезисы Всероссийского симпозиума с международным участием «Гормональные механизмы адаптации» (Посвящается памяти проф. А.А. Филаретова), Санкт-Петербург, 3-5 октября, 2007.- СПб.: Ин-т физиологии им. И.П. Павлова, 2007. С.49-50.
- Карецкий А.В., Хокканен В.А., Лопатина Е.В. Использование метода органотипической культуры ткани в экспериментальной офтальмологии // Новейшие достижения в лечении и диагностике глазных заболеваний. – М., 2007. – С.45-46.
- Рогачевский И.В., Плахова В.Б., Лопатина Е.В., Крылов Б.В. Технология создания новых лекарственных препаратов на основе производных гамма-пирона // Новые технологии и их применение. 2007. N 3. С. 46-53.
- Поляков Ю.И., Лопатина Е.В., Коротков А.Д. Механизм действия и специфическая фармакологическая активность нового синтетического ненаркотического анальгетического средства – препарата “Аноцептин”. Конференция «Фундаментальные науки медицине» – Москва, 3-4 декабря 2007 г.
- Лопатина Е.В., Карецкий А.В., Пеннияйнен В.А., Крылов Б.В. Новые подходы к лечению дистрофических заболеваний сетчатки глаза.// Нейрохимические механизмы формирования адаптивных и патологических состояний мозга. Санкт-Петербург, 10-12 сентября, 2008.- СПб.-Колтуши: Ин-т физиологии им. И.П. Павлова, 2008. С. 82.
- Lopatina E.V., Penniyaynen V.A., Plakhova V.B., Butkevich I.P., Tsyrlin V.A. Endogenous ouabain controls analgesic function of sodium pump.// The 2nd St.-Petersburg Humboldt-Kolleg Conference «Technologies of the 21st Century: Biological, Physical, Informational and Social Aspects». Saint-Petersburg. October 7–9, 2008. P. 21-22.
- Лопатина Е.В., Пеннияйнен В.А., Плахова В.Б., Подзорова С.А., Кипенко А.В., Крылов Б.В., Цырлин В.А. Физиологическая роль сигнальной функции Na,K-АТФазы // ссылка скрыта.
- Кипенко А.В., Пеннияйнен В.А., Лопатина Е.В. О возможности образования хелатного комплекса оуабаин-Са2+.// Второй всероссийский форум студентов, аспирантов и молодых ученых «Наука и инновации в технических университетах». Санкт-Петербург. 28-31 октября, 2008. С. 172-173.
- Лопатина Е.В., Карецкий А.В., Крылов Б.В. Синтетический ненаркотический анальгетик «Аноцептин» Симпозиум «Результаты фундаментальных и прикладных исследований для создания новых лекарственных средств». Фундаментальные науки новым лекарствам. ОАО «Московская типография № 6». Москва, 9-11 июня 2008. С.117-118.
- Пеннияйнен В.А., Лопатина Е.В., Панова Т.И., Крылов Б.В. Новый механизм модуляции роста нейритов: роль коменовой кислоты. Питання експериментальної та клінічної медицини збірник статей, 2008, Випуск 12, Том 1 С. 120-125.
- Кипенко А.В., Пеннияйнен В.А., Лопатина Е.В. Исследование действия коменовой кислоты на состояние сердечно-сосудистой системы теплокровных животных // Материалы конференций политехнического симпозиума «Молодые ученые – промышленности северо-западного региона». – Санкт-Петербург, 22 мая, 2009. – С. 166-167.
- Лопатина Е.В., Плахова В.Б., Шелых Т.Н., Рогачевский И.В., Пеннияйнен В.А., Подзорова С.А., Крылов Б.В. Ионные механизмы кодирования ноцицептивных сигналов. Биологические мембраны. 2009. Т. 26. № 4. С. 319.
- Лопатина Е.В Рецептор-опосредованная фармакологическая модуляция сигнальной функции Na+,K+-АТФазы. Механизмы функционирования висцеральных систем. VII Всероссийская конференция с международным участием, посвященная 160-летию со дня рождения И.П.Павлова. – 2009. – 29 сентября-02 октября. Санкт-Петербург. Издательство ООО «Турусел». Россия. С.249.
- Лопатина Е.В., Пеннияйнен В.А., Кипенко А.В., Цырлин В.А. Физиологическое значение рамнозильного остатка в молекулах сердечных гликозидов. VII Всероссийская конференция с международным участием, посвященная 160-летию со дня рождения И.П.Павлова. – 2009. – 29 сентября-02 октября. Санкт-Петербург. Издательство ООО «Турусел». Россия. С.250-251.
- Рогачевский И.В., Лопатина Е.В., Пеннияйнен В.А., Крылов Б.В. Квантовохимические механизмы лиганд-рецепторного связывания молекулы уабаина с Na+,K+-АТФазой возбудимых клеток. VII Всероссийская конференция с международным участием, посвященная 160-летию со дня рождения И.П.Павлова. – 2009. – 29 сентября-02 октября. Санкт-Петербург. Издательство ООО «Турусел». Россия. С. 370-371.
