Под общей редакцией проф. Малого В. П., проф. Кратенко И. С. Харьков 2008
| Вид материала | Диплом |
СодержаниеПроблема лекарственной устойчивости микроорганизмов. От эмпиризма к методологии точной науки Жалко-Титаренко В.П. |
- Учебник под редакцией, 9200.03kb.
- Під загальною редакцією проф. Малого В. П. проф. Кратенко I. С. Харків 2006, 5907.56kb.
- Р. А. Хальфин 08. 12. 2006 г. N 6530-рх методические рекомендации, 1062.91kb.
- Программа студенческой олимпиады мгмсу по стоматологии 30. 10., 33.94kb.
- Оао «Сильвинит» "ахиллес" соль древнего пермского моря пермь Соликамск. 2001 ббк. 65., 502.69kb.
- Удк 37 ббк 74. 05, 475.58kb.
- М. А. Рыбалко (отв редактор), проф, 973.68kb.
- Матер І а л и науково-практичної конференції з міжнародною участю 1-2 березня 2007, 7242.75kb.
- Реферат циклу підручників «Україна в світовій політиці», 148.74kb.
- Колективу авторів у складі: проф. Гаращенко Ф. Г., проф. Закусило О. К., проф. Зайченко, 259.94kb.
Проблема лекарственной устойчивости микроорганизмов. От эмпиризма к методологии точной науки
Жалко-Титаренко В.П.
Институт эпидемиологии и инфекционных болезней им. акад. Л.В.Громашевского, АМН Украины
Более половины столетия лекарственная устойчивость микроорганизмов остаётся животрепещущей проблемой медицины. За этот внушительный отрезок времени были сделаны многие важные общебиологические открытия. Была установлена связь резистентности с хромосомными и внехромосомными факторами. Глубокому исследованию подверглись биохимия, молекулярная биология и генетические структуры микроорганизмов. Современные представления о жизнедеятельности клетки многим обязаны использованию маркеров бактериальной резистентности. Биотехнология обогатилась целой системой химиотерапевтических препаратов, способных оказать мощный лечебный эффект практически против любого возбудителя.
К сожалению, проблема осталась нерешенной, и предупредить либо избежать возникновения лекарственной устойчивости в клинической практике более чем сложно. Причина лежит в самой природе резистентности как микроэволюционного явления. Тем не менее, многое зависит от научного подхода к проблеме. Лекарственная устойчивость, как правило, изучалась и оценивалась по отношению к бактериальной клетке, бактериальному клону, чистой культуре, донорам и реципиентам внехромосомных факторов резистентности. Однако в реальных условиях больного организма жизнь резистентной и чувствительной популяции встречается с вызовами, сильно отличающимися от лабораторных тестов. Судьба любой – резистентной и чувствительной популяции – зависит от стартовой дозы, от наличия или отсутствия латентной фазы, от скорости размножения и скорости отмирания в условиях химиотерапии, от взаимного популяционного давления, от частоты возникновения резистентности и реверсии. Огромное значение имеет селективное воздействие организма, особенно иммунной системы на микробную популяцию. Причём весь этот массив факторов является лишь первым приближением, в котором не учитывается многообразие форм и структур патологического очага, особенностей биологии микробов, воздействия сторонней микрофлоры и многое другое.
К сожалению, реальная жизнь и развитие резистентных и чувствительных популяций в условиях организма далеко не познана в силу практической недоступности объекта исследования. По этой причине в проблеме резистентности доминирует скорее бытовая логика типа «выделили резистентные микроорганизмы – ищем препараты на замену» чем научная: «резистентность – процесс, которым нужно научиться управлять». Бытовую логику легко удовлетворить анализом микрофлоры на устойчивость к антибиотикам. Для научного подхода этого совершенно недостаточно, так как уже следующий законный вопрос – «а на сколько патогенна устойчивая часть популяции?» - остаётся без ответа. Но и вопрос о патогенности далеко не однозначен.
Понятие патогенности на много шире представления о болезнетворности. Патогенным действием обладают не только облигатно-патогенные возбудители, но и микробы, у которых нет биологической необходимости вызывать инфекцию (оппортунистическая микрофлора). Есть и такие, которые вообще ведут сапрофитический образ жизни, а болезнь вызывается их экзотоксинами. Первые вызывают эпидемии, вторые и третьи могут обусловливать инфекционные состояния, которые, однако, не способны обусловить самоподдерживающийся эпидемический процесс. Сомнительно чтобы лекарственная устойчивость первых, вторых и третьих имела одинаковые медико-биологические последствия. Особенно если учесть, что прямым болезнетворным действием обладает всё что угодно, даже дистиллированная вода. Вопрос лишь в том – сколько и куда введен соответствующий агент.
Научный подход призван решить главную проблему - как управлять возникновением лекарственной устойчивости в процессе лечения? Найти полное решение этой задачи, ограничиваясь эмпирическими методами в принципе невозможно. Ведь резистентность возникает на перекрестьи динамик роста чувствительной и резистентной популяции, их взаимной конкуренции за место обитания, частот мутаций, реверсий и передачи факторов резистентности, динамики иммунного пресса. Даже если бы имелась возможность на любом этапе инфекционного процесса оценивать состояние паразитирующей популяции, сочетание нескольких динамических процессов всё равно делает задачу невыполнимой. К счастью современные естественные науки располагают хорошо отработанным подходом к решению подобных проблем. Он состоит в построении теоретических, в том числе компьютерных, моделей с последующей перепроверкой после насыщения их необходимой экспериментальной и медико-биологической информацией. Эффективность этого подхода доказывает тот факт, что нынешняя наука о материи и вселенной, вместе с современной цивилизацией созданы с помощью именно такой методологии.
Попыток создать теоретическую модель развития инфекции и записать её в математической форме литература ХХ столетия содержит немало [N.Bailey-1967, М.Ханин и Л.Элькин-1976,О.В.Бароян и Л.Г.Рвачёв-1979 и др.]. Но им присущ общий недостаток – отсутствие «системной однородности», благодаря чему биологические процессы нередко интерпретировались по аналогии с физическими явлениями либо вообще произвольно. В противоположность этому мы приняли самоочевидное положение, что инфекционное состояние в своей биологической основе является ростом, развитием и последующим отмиранием популяции возбудителя. Этот подход не имел бы никакой цены, если бы нам не удалось разработать методы, обеспечивающие насыщение параметров модели адекватной экспериментальной медико-биологической информацией, полученной в частности на фрагментах постоперационных органах человека. Такое комплексное решение проблемы привело к разработке следующей системы уравнений:

Первое уравнение моделирует рост чувствительной патогенной популяции, второе – резистентной. Первые два члена первого и вторые два члена второго уравнения отражают этап возникновения и роста популяции соответственно чувствительных
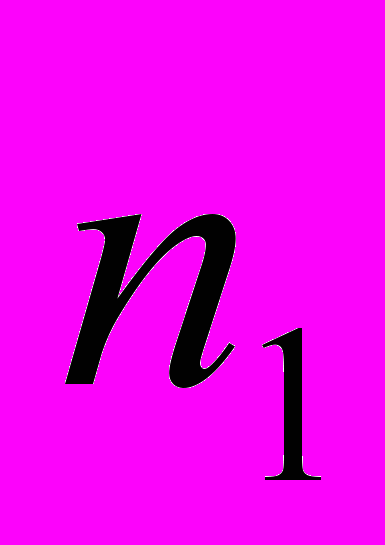 и резистентных
и резистентных 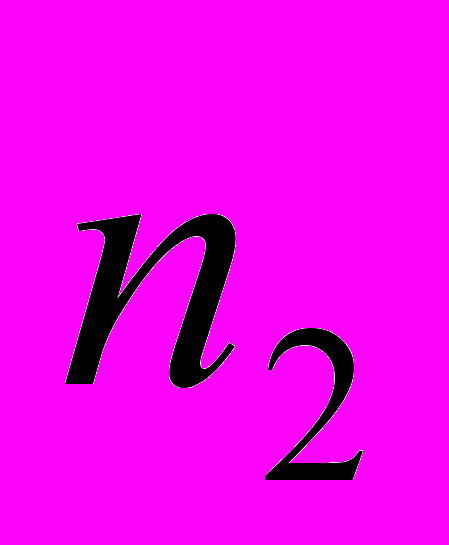 до достижения ими максимальной численности
до достижения ими максимальной численности  . Третий из первого уравнения, четвёртый из второго моделируют отмирание популяции под действием иммунитета. Четвёртый член из первого уравнения отражает отмирание чувствительной части популяции под действием антибиотика. Пятый член второго уравнения моделирует популяционные взаимоотношения чувствительного и резистентного клона. Первый член второго уравнения показывает число возникающих резистентных в зависимости от частоты мутаций и ассимиляции факторов внехромосомной лекарственной устойчивости
. Третий из первого уравнения, четвёртый из второго моделируют отмирание популяции под действием иммунитета. Четвёртый член из первого уравнения отражает отмирание чувствительной части популяции под действием антибиотика. Пятый член второго уравнения моделирует популяционные взаимоотношения чувствительного и резистентного клона. Первый член второго уравнения показывает число возникающих резистентных в зависимости от частоты мутаций и ассимиляции факторов внехромосомной лекарственной устойчивости  . Время генерации
. Время генерации 

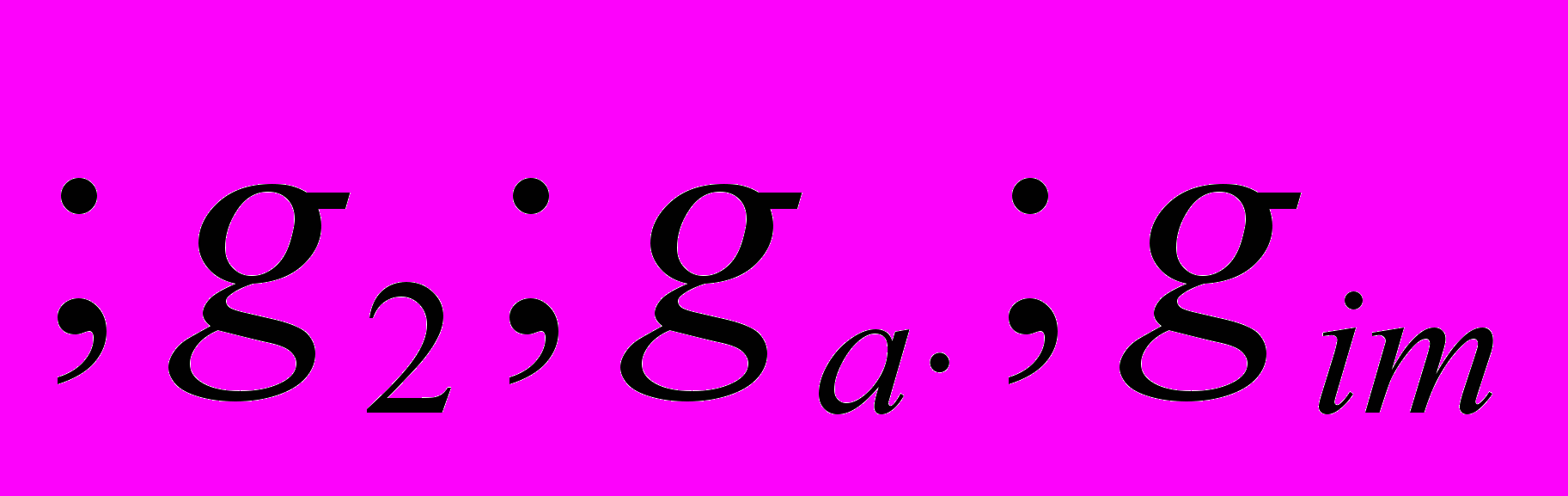 - соответственно: чувствительной, резистентной популяции, обратной генерации под действием антибиотика и под действием иммунитета. Интервал времени до начала антибиотикотерапии и до начала действия иммунного ответа задаются соответственно функциями Хевисайда
- соответственно: чувствительной, резистентной популяции, обратной генерации под действием антибиотика и под действием иммунитета. Интервал времени до начала антибиотикотерапии и до начала действия иммунного ответа задаются соответственно функциями Хевисайда  .
.Моделирование инфекционного процесса на основе системы уравнений (1-2) было успешным, и полученные результаты соответствовали общим клиническим наблюдениям. На компьютерной модели хорошо воспроизводится возникновение резистентности при запаздывании начала химиотерапии и снижение вероятности формирования резистентности при раннем назначении лечения. Воспроизводится успешность комбинированного применения и последовательного замещения антибиотических препаратов. Моделируется эффективность иммунного ответа.
Достигнутый результат доказывает факт создания канонической модели развития популяции возбудителя в организме и воздействия на неё химиотерапии. Модель показывает, как может быть найден режим применения химиотерапевтических средств, который способен затормозить развитие лекарственной устойчивости. Создание канонической модели является основополагающим этапом формирования нового научного направления – компьютерного сопровождения химиотерапевтического процесса.
