Эндоскопические аспекты ранней диагностики и лечения больных с острым билиарным панкреатитом (клинико-морфологическое исследование) 14. 00. 27 хирургия 03. 00. 25 гистология, цитология, клеточная биология
| Вид материала | Исследование |
| 1.2. Морфологическое исследование 1.3. Статистический анализ II. РЕЗУЛЬТАТЫ КЛИНИЧЕСКОГО ИССЛЕДОВАНИЯ 2.1. Эндоскопическая диагностика и лечение острого билиарного панкреатита |
- Оптимизация хирургического лечения больных билиарным отечным панкреатитом в сочетании, 285.74kb.
- Экспериментальное обоснование применения нейропептидов в комплексной терапии острого, 259.86kb.
- Ультраструктурная и цитохимическая характеристика макрофагов, инфицированных рнк-содержащими, 636.4kb.
- Закономерности дегенерации и адаптации сетчатки глаз при экспериментальных ретинопатиях,, 745.16kb.
- Влияние биологически активных клеточных компонентов растений на структурные изменения, 324.85kb.
- Цитологические особенности вторичных миелодисплазий при лимфомах 03. 00. 25 гистология,, 526.98kb.
- Структурно-функциональная организация палеоамигдалы: фундаментальные закономерности, 2391.63kb.
- Морфофункциональная характеристика пульпы зуба и оценка иммунного статуса при кариесе,, 552.48kb.
- Лимфоидные органы и миокард в системе мать-плод при вибрации, воздействии кадмием, 640.36kb.
- Молекулярные механизмы апоптоза при окислительном стрессе 14. 00. 16 патологическая, 606.37kb.
1.2. Морфологическое исследование
Для морфологических исследований у 15 пациентов из каждой группы эндоскопически брали биоптаты слизистой оболочки в зоне большого дуоденального сосочка до операции, через 3 и 5 суток послеоперационного периода. Биоптаты фиксировали погружением в смесь 4% раствора параформальдегида на среде Хенкса в течение 2 часов при температуре +4оС. После этого материал рассекали на пластины толщиной 1 мм, которые дофиксировали в аналогичном растворе фиксатора в течение 12-24 часов при +4оС. Затем биоптаты помещали в 1% раствор четырехокиси осмия на 2 часа, обезвоживали в спиртах восходящей концентрации и заключали в смесь эпона и аралдита. Для электронной микроскопии использовали ультратонкие (70-100 нм) срезы, которые готовили на ультрамикротоме “Ultracut-E” (фирма Reichert-Jung), помещали на сетки без подложки и контрастировали уранилацетатом и цитратом свинца. Просмотр и фотографирование ультратонких срезов производили на электронном микроскопе “Hitachi-600H”. При электронномикроскопическом исследовании проводили качественную и количественную оценку всех структурных компонентов слизистой оболочки ДПК. Для светооптического и морфометрического исследования использовали полутонкие срезы ( 1 мкм), окрашенные гематоксилин-эозином и азур – эозином (Семченко В.В. и соавт., 2006).
1.3. Статистический анализ
Статистическую обработку полученного материала осуществляли с помощью пакета прикладных программ STATISTICA 6.0 (Боровиков В., 2001), согласно современным требованиям к проведению анализа медицинских данных (Гланц С., 1998; Реброва О.Ю., 2001). Предпочтение было отдано менее чувствительной, но и менее ограниченной условиями применения непараметрической ранговой статистике. Различия между независимыми выборками определяли с помощью двухвыборочного критерия Колмогорова-Смирнова, зависимыми выборками – W-критерий Вилкоксона парных сравнений. Использовали также ранговый дисперсионный анализ Фридмана и Краскела-Уоллиса. Для категориальных переменных применяли критерий 2 или точный критерий Фишера. Степень стохастической связи между двумя переменными устанавливали с помощью корреляции Спирмена (r). Нулевая гипотеза отвергалась, а альтернативная принималась при -ошибке = 0,05 и -ошибке = 0,25. При этом мощность исследования была на уровне 0,7-0,9 (Реброва О.Ю., 2001; Гланц С., 1998).
Для оценки эффективности лечения применяли таблицу сопряженности, на основании которой определяли абсолютный и относительный риск развития того или иного события, снижение или повышение относительного риска, а также показатель эффективности лечения. Определение статистической значимости различий по приведенным выше параметрам проводили с помощью построения доверительных интервалов (Реброва О.Ю., 2002).
Все клинические исследования выполнены на базе МУЗ ГК БСМП №1 г.Омска, морфологические – на базе Омской государственной медицинской академии (кафедра гистологии, цитологии и эмбриологии) и частично (электронная микроскопия) в лаборатории ультраструктуры и патоморфологии института молекулярной биологии научного центра «Вектор» МЗ РФ (зав. лабораторией доктор биол. наук Е.И.Рябчикова) с участием врачей Р.А.Арестовича и канд. мед. наук Е.В.Сосновской. Статистический анализ и обработка данных морфологического исследования осуществлены при консультативной помощи доктора медицинских наук С.С.Степанова и профессора В.В.Семченко.
II. РЕЗУЛЬТАТЫ КЛИНИЧЕСКОГО ИССЛЕДОВАНИЯ
2.1. Эндоскопическая диагностика и лечение острого билиарного панкреатита
При исследовании верхних отделов желудочно-кишечного тракта (ЖКТ) у пациентов с острым билиарным панкреатитом (ОБП) выявлялись признаки реактивного гастродуоденита (100%), снижения гастродуоденальной моторики (94%), дуодено-гастрального рефлюкса (90%), недостаточности пилорического и кардиального сфинктеров (80%), лимфангиоэктазии (55%), острых гастродуоденальных изъязвлений (36%).
Основным эндоскопическим признаком ОБП было наличие острой обтурации БДС желчными камнями с полным отсутствием поступления желчи и панкреатического сока в просвет ДПК. При этом БДС был резко увеличен в размерах и напряжен, поверхность его была гладкая и блестящая. При выраженном выбухании БДС занимал до 2/3 просвета ДПК. Эластичность покрывающей БДС слизистой была снижена. По данным эндопальпации, сосочек имел плотную консистенцию и при давлении на него практически не смещался. Продольная складка, являющаяся контуром интрадуоденальной части холедоха, была утолщена и напряжена. В ряде случаев через устье БДС пролабировал конкремент или сгусток фибрина. При длительной фиксации камня появлялись признаки некроза слизистой оболочки в области устья БДС, возникала и нарастала имбибиция слизистой парапапиллярной зоны панкреатическим соком. Предрасполагающим фактором развития обтурации БДС конкрементом или «сладжем» было наличие парапапиллярного дивертикула.
ОБП развивался на фоне полной обтурации ампулы и устья БДС большими (около 5 мм) желчными камнями, миграции и вклинении нескольких камней в ампулу БДС, протяженной обтурации на фоне рубцового папиллостеноза или опухолевого поражения БДС, а также при сочетании причин.
По нашим данным, при ОБП в 100% случаев выявлялась обтурация БДС конкрементами, в 76% – рубцовый папиллостеноз, в 64% – признаки гипертензии интрамуральной части холедоха, в 22% – имбибиция парапапиллярной зоны, 6% – парапапиллярный дивертикул, 4% – аденома БДС, в 3% – состояние после резекции желудка по Бильрот-II.
После выявления обтурации БДС конкрементом проводили комбинированную эндоскопическую папиллосфинктеротомию (ЭПСТ). Вначале рассечение производилось с помощью игольчатого или торцевого электрода на 11-12 часах по крыше БДС в направлении продольной складки до вскрытия ампулярной полости. Ткани над конкрементом рассекались полностью. При этом в подавляющем большинстве случаев наблюдалось отхождение вколоченного в ампулу БДС конкремента. При выраженном рубцовом папиллостенозе причиной обтурацити БДС была группа микролитов, «замазка» или плотный сгусток желчи. Ампулярная полость представляла либо резко суженную фистулу, либо решетчатую фиброзную структуру в виде «сот» заполненную микролитами, так называемым «билиарным гравием» или «сладжем».
У всех пациентов производили адекватный осмотр и вмешательство на БДС. При таком типе операции использовали ретроградный осмотр сосочка, поэтому исследование проводилось удлиненным аппаратом с торцевой оптикой (GIF-1T20). Достаточно было продвижения эндоскопа на 30-40 см за гастроэнтероанастомоз в приводящую кишку, чтобы достичь культи ДПК. Однако непривычное положение конца эндоскопа у фатерова сосочка диктовало некоторые технические особенности при проведение ЭПСТ и литоэкстракции. Эти особенности были связаны с «обратным» расположением продольной складки ДПК в поле зрения эндоскопа, а также с теми анатомическими изменениями, которые образуются в брюшной полости после хирургической операции. Для проведения ЭПСТ применялся игольчатый электрод или папиллотом типа Soma.
При ликвидации обтурации отмечалось поступление в просвет кишки мутной с нитями фибрина или гнойной желчи и панкреатического сока. Количество и активность поступления измененной желчи и гноя из ОЖП при холангите были от 2-5 мл до 50-100 мл, вплоть до полного заполнения просвета ДПК. Характер воспалительных изменений желчи и её количество зависели от продолжительности обтурации. Небольшое количество выделений из холедоха указывало на возможное наличие препятствия (конкременты, стриктура, экстраорганное сдавление) в отделах расположенных проксимальнее ампулярного. При большом поступлении гнойного содержимого производилась его эвакуация через инструментальный канал из просвета кишки с помощью электроотсоса.
Вторым этапом лечения было проведение селективной эндоскопической ретроградной холангиографии (ЭРХГ) при которой выявлялось состояние желчевыводящей системы. Для контрастирования протоковой системы применялись водорастворимые контрастные вещества (омнипак, урографин, ультравист, вазотраст). В просвет холедоха через папиллотомный разрез проводилась канюля с рентгенконтрастными метками. Во всех случаях при контрастировании отмечалось расширение внепеченочных желчных протоков. Размеры увеличения диаметра общего желчного протока были от 7 мм до 35 мм.
При ЭРХГ выявлялись вколоченные конкременты ампулярного отдела (100%), дилятация желчевыводящих протоков (100%), конкременты общего желчного протока (33%), единичные камни холедоха (22%), множественный холедохолитиаз (11%), лигатурный холедохолитиаз (2%), синдром Миризи (1%), холецистолитиаз (10%), стеноз дистального отдела холедоха (14%), признаки холангита (84%), культя пузырного протока в виде «слепого мешка» (3%).
Обнаруженные мелкие конкременты диаметром до 5-7 мм удалялись через имеющийся папиллотомный разрез. Единичные камни захватывались корзиной Дормиа и низводились в просвет ДПК. При наличии расположенных цепочкой мелких конкрементов корзиной захватывался проксимально расположенный конкремент. Далее производилась экстракция, при которой под давлением, сверху подтягиваемым камнем, дистально расположенные конкременты удалялись из общего желчного протока.
При наличии крупных конкрементов в просвете холедоха выполнялось дополнительное рассечение сфинктера с применением метода канюляционной струнной папиллосфинктеротомии. В обязательном порядке полностью рассекался сосочек и разрез продолжался по продольной складке в пределах её выраженного контурирования (в среднем на расстояние до 10 мм). Рассекался сфинктер Одди и дистальный отрезок сфинктера Бойдена. Длина папиллотомного разреза колебалась от 15 до 30 мм. При ЭПСТ благодаря рассечению самого сосочка и выше лежащей интрамуральной сфинктерной части холедоха создавалось широкое соустье между общим желчным протоком и ДПК.
При выполнении ЭПСТ канюляционным методом после введения папиллотома контролировали его положение в холедохе рентгенологически или по поступлению содержимого в катетер при аспирации через папиллотом. Невыполнение этих мероприятий могло привести к нежелательной травме панкреатического протока и ткани поджелудочной железы.
После проведения широкой ЭПСТ и при отсутствии стриктуры терминального отдела холедоха появлялась возможность удаления более крупных конкрементов (до 10-15 мм в диаметре). Главным условием было соответствие диаметров папиллотомного соустья и терминального отдела холедоха диаметру извлекаемого конкремента. Извлечение конкремента производилось корзиной. Конкремент захватывался и выводился в ДПК. При множественном холедохолитиазе процедура экстракции осуществлялась повторно. Если конкременты были расположены друг за другом, а диаметр полностью раскрытой корзины позволял захватить 2-3 конкремента, проводили одномоментное удаление группы конкрементов. Захваченные петлей Дормиа и выведенные в просвет ДПК конкременты оставляли в кишке или извлекали вместе с эндоскопом.
Следует помнить, что проведение насильственной экстракции при несоответствии размеров конкремента и нижележащих отделов ОЖП чреваты возникновением осложнений (перфорация ОЖП, кровотечение, заклинивание корзины с камнем), которые могут повлечь за собой необходимость срочной лапаротомии.
Когда размеры камня не соответствовал диаметру образованного после ЭПСТ устья холедоха или его интрапанкреатической части, или конкремент находился выше стриктуры холедоха, камень извлекали после предварительного дробления. Применялся наиболее безопасный, дешевый и одновременно эффективный метод ретроградной внутрипротоковой механической литотрипсии. Под рентгенологическим контролем литотриптер проводили по инструментальному каналу эндоскопа через папиллотомное соустье в холедох и захватывали камень, который затем разрушался в результате механического сдавления. После разрушения камня выполняли холангиоскопию. В случае наличия крупных фрагментов этим же литотриптором производили разрушение отломков до размеров, позволяющих удалить эти фрагменты. Фрагменты конкремента извлекали захватами (петля, корзина). При наличии большого количества мелких фрагментов, замазки, «билиарной грязи» их удаление производили баллонным экстрактором.
Таким образом, приведенные выше эндоскопические технологии позволяют эффективно диагностировать и лечить пациентов на раннем этапе развития ОБП. При этом высокая эффективность лечения сочетается с малой травматичностью эндоскопической операции, а дополнительная холангиоскопия позволяет выявить остатки конкрементов и сразу же удалить их. На основании полученных результатов мы создали алгоритм диагностики и лечения острого билиарного панкреатита, представленный ниже.
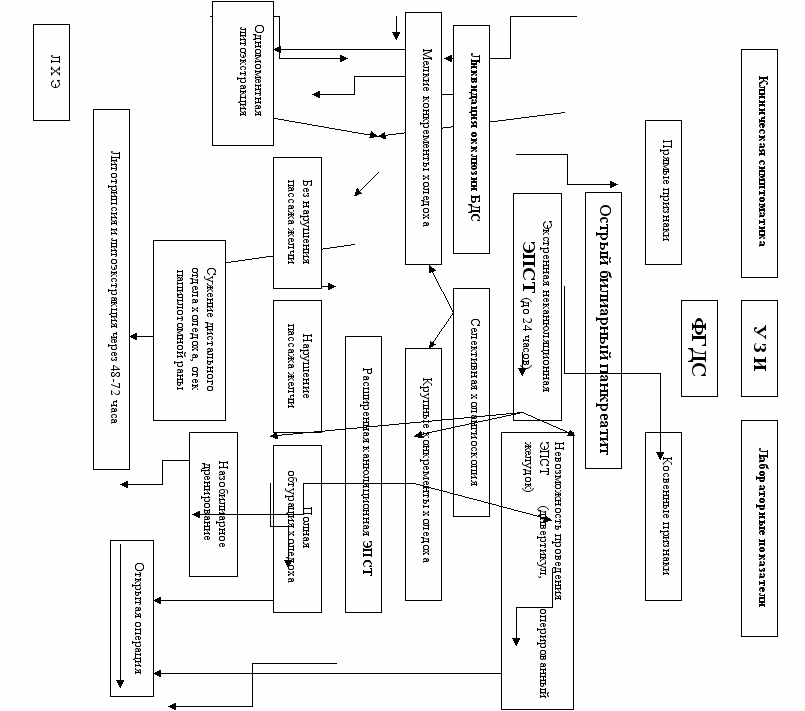 Алгоритм эндоскопической диагностики и лечения острого билиарного панкреатита, вызванного обтурацией большого дуоденального сосочка и общего желчного протока.
Алгоритм эндоскопической диагностики и лечения острого билиарного панкреатита, вызванного обтурацией большого дуоденального сосочка и общего желчного протока.