Учебное пособие для модульно-рейтинговой технологии обучения Бийск
| Вид материала | Учебное пособие |
- Методические рекомендации по организации учебного процесса с использованием модульно-рейтинговой, 554.48kb.
- Я. В. Вакула Нефтегазовые технологии Учебное пособие, 2652.31kb.
- Учебное пособие «управление персоналом» для студентов заочного обучения специальности, 1516.37kb.
- М. Н. Машкин Информационные технологии Учебное пособие, 2701.91kb.
- Учебное пособие Уфа 2005 удк 338 (075. 8) Ббк, 1087.66kb.
- Учебный план как средство реализации принципов модульно-рейтинговой технологии обучения, 68.67kb.
- О. Д. Картавцева интенсивный курс обучения изобразительной грамоте учебное пособие, 780.71kb.
- Менеджмента качества положение о модульно-рейтинговой системе квалиметрии учебной деятельности, 1381.23kb.
- Учебное пособие 28365942 Москва 2008 ббк 66., 2986.28kb.
- Формирование профессиональной компетентности будущих специалистов в области вычислительной, 372.85kb.
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
«Алтайский государственный технический университет
имени И.И. Ползунова»

Т.И. Макрушина
ХИМИЯ
Модуль 2
РАСТВОРЫ. ДИСПЕРСНЫЕ СИСТЕМЫ
Учебное пособие
для модульно-рейтинговой технологии обучения
Бийск
2007
УДК 546 (075.5)
Макрушина, Т.И. ХИМИЯ. Модуль 2. Растворы. Дисперсные системы: учебное пособие для модульно-рейтинговой технологии обучения / Т.И. Макрушина.
Алт. гос. техн. ун-т БТИ. – Бийск.
Изд-во Алт. гос. техн. ун-та, 2007. – 148 с.
В данном учебном пособии представлена система методической документации для модульно-рейтинговой технологии изучения раздела «Растворы. Дисперсные системы» курса «Химия», а также для изучения дисциплин, рабочие программы которых предусматривают изучение разделов, рассмотренных в данном пособии.
Учебное пособие разработано в соответствии с Государственным образовательным стандартом УМО высшего профессионального образования по направлениям подготовки дипломированных специалистов специальностей 151001, 160302, 190603, 080401, 170104, 230201, 080502, 260204, 240901, 240701, 240702, 240706, 260601, 200106 всех форм обучения.
Учебное пособие предназначено для преподавателей и студентов технических и химико-технологических вузов.
Рассмотрено и одобрено на заседании
кафедры общей химии и экспертизы товаров.
Протокол № 45 от 16.12.06 г.
Рецензент: доктор химических наук В.М. Аксененко
© Макрушина Т. И., 2007
© БТИ Алт ГТУ, 2007
СОДЕРЖАНИЕ
| ВВЕДЕНИЕ | 5 |
| МОДУЛЬ 2. РАСТВОРЫ. ДИСПЕРСНЫЕ СИСТЕМЫ | 8 |
| 1 Общие положения | 8 |
| 1.1 Цели обучения | 9 |
| 1.2 Программа модуля | 9 |
| 1.3 Тематический план модуля | 11 |
| 1.4 Перечень необходимых средств для выполнения программы модуля | 11 |
| 1.5 План-график изучения модуля | 11 |
| 1.6 Планы лабораторных занятий | 13 |
| 1.7 Индивидуальное расчетное задание | 15 |
| 1.8 Самостоятельная работа студентов | 18 |
| 1.9 Модульный экзамен | 18 |
| 2 Растворы | 20 |
| 2.1 Цели изучения раздела | 20 |
| 2.2 Методические рекомендации по изучению материала | 20 |
| 2.3 Химические системы | 21 |
| 2.4 Классификация растворов | 29 |
| 2.5 Растворимость | 31 |
| 2.6 Общие свойства растворов | 37 |
| 2.7 Теория электролитической диссоциации | 47 |
| 2.8 Теории кислот и оснований | 50 |
| 2.9 Слабые электролиты | 56 |
| 2.10 Растворы сильных электролитов | 66 |
| 2.11 Произведение растворимости | 69 |
| 2.12 Гидролиз солей | 72 |
| 2.13 Ионный обмен | 79 |
| 3 Дисперсные системы | 83 |
| 3.1 Цели изучения раздела | 83 |
| 3.2 Методические рекомендации по изучению материала | 83 |
| 3.3 Общие понятия о дисперсных системах | 84 |
| 3.4 Коллоидные растворы | 86 |
| 3.5 Поверхностные явления | 88 |
| 3.6 Строение мицеллы | 91 |
| 3.7 Методы получения коллоидных растворов | 93 |
| 3.8 Оптические свойства коллоидных растворов | 96 |
| 3.9 Кинетические свойства коллоидных растворов | 97 |
| 3.10 Электрические свойства коллоидных растворов | 98 |
| 3.11 Агрегативная устойчивость коллоидных растворов | 100 |
| 3.12 Коллоидные растворы в природе и технике | 103 |
| 3.13 Грубодисперсные системы | 104 |
| Заключение по модулю 2 «Растворы. Дисперсные системы» | 109 |
| Литература | 111 |
| ПРИЛОЖЕНИЕ А. Основные термины и определения | 112 |
| ПРИЛОЖЕНИЕ Б. Тестовые задания | 118 |
| ПРИЛОЖЕНИЕ В. Примерный перечень вопросов к экзамену | 141 |
| ПРИЛОЖЕНИЕ Г. Растворимость солей, кислот, оснований в воде | 143 |
| ПРИЛОЖЕНИЕ Д. Степени диссоциации электролитов | 144 |
| ПРИЛОЖЕНИЕ Е. Средние коэффициенты активности ионов при различной ионной силе раствора | 145 |
| ПРИЛОЖЕНИЕ Ж. Константы диссоциации некоторых слабых электролитов | 146 |
| ПРИЛОЖЕНИЕ И. Произведения растворимости | 147 |
ВВЕДЕНИЕ
Очень многие химические реакции, в том числе технические и жизненно важные, протекают в жидкой фазе.
Природная вода является раствором, и многие вещества в ней находятся в коллоидном состоянии. Жизнь на Земле не могла бы возникнуть без растворов и различных дисперсных систем. Растворами и коллоидными системами являются физиологические жидкости: плазма крови, лимфа, желудочный сок и др. Растворы и дисперсные системы широко применяются в различных сферах деятельности человека. Многие медицинские препараты являются растворами различных химических веществ в воде или в спирте.
В различных производственных и биологических процессах большую роль играют растворы электролитов. Свойства этих растворов объясняет теория электролитической диссоциации. Знание теории электролитической диссоциации и свойств коллоидных растворов является основой для изучения свойств неорганических и органических соединений и глубокого понимания механизмов химических реакций в различных дисперсных системах.
Изучение второго модуля курса «Химия» строится на базе интеграции принципа процессного подхода и модульно-рейтинговой технологии обучения, основанной на образовательном стандарте высшего профессионального образования АлтГТУ им. И.И. Ползунова: «Положение о модульно-рейтинговой системе квалиметрии учебной деятельности студентов. СМК ОПД 01-19-2005» (рисунок 1).
В качестве основного методического материала при изучении модуля «Растворы. Дисперсные системы» рекомендуется использовать приведенные далее структурно-логические схемы, отвечающие системному анализу раздела. Структурно-логические схемы курса, разделов отражают не только внешние и внутренние связи, но и дают четкое представление о последовательности работы с учебным материалом. Структурно-логические схемы также фиксируют внимание студентов на наиболее важных положениях и понятиях каждого раздела курса, то есть они помогают формированию стержневых идей курса и опорных знаний.
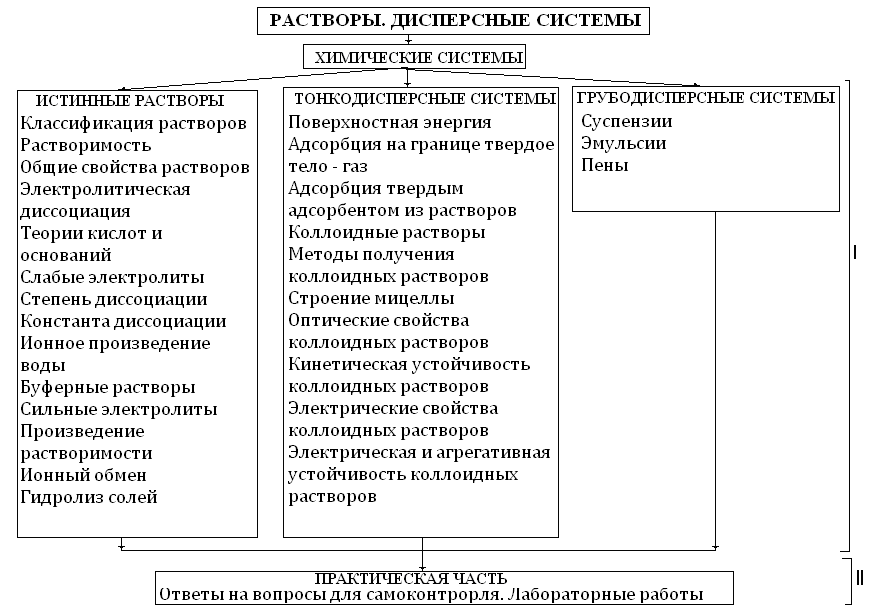
Рисунок 1 – Структура второго модуля курса «Химия»
Решающей стадией и итогом любого обучения является самообучение как самоосознание собственного умения делать или понимать (знать) что-либо. В настоящее время становится важным обучение умению самостоятельно добывать нужную информацию, определять проблемы и искать пути их рационального решения, уметь критически анализировать получаемые знания и применять их для решения все новых задач. Индивидуальная творческая работа позволяет достичь стратегической цели системы образования в современном обществе: интеллектуальное и нравственное развитие человека.
Изучение модуля завершается выполнением индивидуального расчетного задания (ИРЗ). Умение мобилизовать все накопленные знания и опыт для решения конкретной задачи, тщательно обосновывать любое решение, критически относиться к полученным результатам, постоянно искать оптимальное, «лучшее» решение – это то, что нужно и необходимо всегда, в любых ситуациях, это то, что в себе надо всегда и постоянно тренировать. И это то, что нужно и необходимо для успешного выполнения ИРЗ.
План-график изучения модуля составлен исходя из того, что студент еженедельно 4−5 часов самостоятельно выполняет задания, предусмотренные этим планом. Содержательная и методическая сторона учебных заданий предполагает, что самостоятельная работа должна протекать по ряду параллельных направлений, отличных друг от друга по своим образовательным и формирующим целям: работа с учебной и научной литературой, выполнение лабораторных работ, тестовых заданий, решение типовых задач, выполнение индивидуальных заданий, написание докладов, сообщений, рефератов, подготовка к промежуточным экзаменам и т.д.
Данное учебное пособие и предназначено для того, чтобы обеспечить методическое руководство самостоятельной работой студентов, изучающих курс «Химия», ее целенаправленность, планомерность, многогранность, систематичность.
Предлагаемая модульная технология обучения применяется более пяти лет на кафедре «Общей химии и экспертизы товаров» Бийского технологического института АлтГТУ им. И. И. Ползунова и показала свою эффективность.
Модуль 2
РАСТВОРЫ. ДИСПЕРСНЫЕ СИСТЕМЫ
1 ОБЩИЕ ПОЛОЖЕНИЯ
Изучение курса «Химия» ведется по единой схеме, включающей в себя два уровня:
- на первом уровне изучаются физическая сущность химических явлений, осваивается принятая терминология, рассматриваются основные закономерности химических явлений;
- на втором уровне изучаются практические вопросы, методы расчета и применение химических процессов.
Преследуя цель повышения качества подготовки специалистов, необходимо активно осуществлять управление процессом получения и усвоения знаний студентами, особенно при их самостоятельной работе.
Применяемая в данном учебном пособии модульно-рейтинговая технология обучения имеет целью поставить студента перед необходимостью регулярной самостоятельной учебной работы в течение всего семестра, обеспечить «мягкое» управление педагогическим процессом, стимулировать процессы самоорганизации учебной деятельности студента.
При изучении курса по учебникам, учебным пособиям и конспекту лекций необходимо пользоваться содержанием разделов и тем, предварительно ознакомившись с кратким содержание тем по рабочей программе дисциплины. При первом чтении не надо задерживаться на математических выводах, составлении уравнений реакций; нужно стараться получить общее представление об излагаемых вопросах, а также отметить трудные или неясные места. Необходимо внимательно читать текст, напечатанный особым шрифтом. При повторном изучении темы нужно стараться усвоить все теоретические положения, математические зависимости и их выводы, а также принципы составления уравнений реакций.
Вникайте в сущность того или иного вопроса, а не пытайтесь запомнить отдельные факты и явления. Изучение любого вопроса на уровне сущности, а не на уровне отдельных явлений способствует более глубокому и прочному усвоению материала. Чтобы лучше запомнить и усвоить изучаемый материал, надо обязательно иметь рабочую тетрадь и заносить в нее формулировки законов и основных понятий химии, новые незнакомые термины и названия, формулы и уравнения реакций, математические зависимости и их выводы. Во всех случаях, когда материал поддается систематизации, составляйте графики, схемы, диаграммы, таблицы. Они очень облегчают запоминание и уменьшают объем конспектируемого материала. Пока тот или иной раздел не усвоен, переходить к изучению новых разделов не следует. Краткий конспект курса будет полезен при повторении материала в период подготовки к экзамену. Изучение разделов модуля должно обязательно сопровождаться выполнением упражнений и решением задач.
1.1 Цели обучения
Изучение модуля «Растворы. Дисперсные системы» должно способствовать достижению следующих целей у студентов:
– освоению основных понятий и классификации растворов;
– усвоению общих законов растворов, теории электролитической диссоциации, кислот и оснований;
– формированию представлений о сильных и слабых электролитах, о гидролизе солей, ионном обмене и буферных растворах, о строении и свойствах коллоидных систем, а также зависимости реакционной способности химических соединений от свойств растворов;
– овладению умениями применять полученные знания для объяснения разнообразных химических явлений и свойств веществ, оценки роли химии в развитии современных технологий и получении новых материалов.
1.2 Программа модуля
Тема 8. «Основные понятия»
Химические системы: общие понятия о дисперсных системах. Классификация дисперсных систем.
Классификация растворов. Идеальные и реальные растворы. Способы выражения состава растворов и других дисперсных систем. Растворимость. Насыщенные и ненасыщенные растворы.
Тема 9. «Теоретические основы»
Общие свойства растворов. Законы Генри и Рауля. Следствия из законов Рауля. Осмос и осмотическое давление. Равновесие в растворах. Теория электролитической диссоциации. Теории кислот и оснований: теория С. Аррениуса, протонная теория Брёнстеда − Лаури, электронная теория Льюиса.
Тема 10. «Водные растворы электролитов»
Слабые электролиты. Константа диссоциации. Степень диссоциации. Закон разбавления Оствальда. Ионное произведение воды. Водородный показатель. Кислотно-основные индикаторы.
Сильные электролиты. Теория сильных электролитов Э. Хюккеля и П. Дебая. Активность и коэффициент активности. Ионная сила растворов.
Тема 11. «Особенности реакций в растворах электролитов»
Произведение растворимости. Условия выпадения осадка. Гидролиз солей. Отсутствие гидролиза в растворах. Три случая гидролиза. Буферные растворы. Случай полного и необратимого гидролиза солей. Способы подавления гидролиза солей. Ионный обмен. Катиониты. Аниониты. Буферные растворы.
Тема 12. «Гетерогенные системы»
Избыточная поверхностная энергия гетерогенных систем. Сорбция и ее виды. Адсорбция на границе твердое тело – газ. Адсорбция твердым адсорбентом из раствора. Адсорбция из растворов электролитов.
Тема 13. «Тонкодисперсные системы»
Коллоидные растворы. Основные понятия. Строение мицеллы. Методы получения коллоидных растворов. Оптические свойства коллоидных растворов. Кинетические свойства коллоидных растворов. Электрические свойства коллоидных растворов. Кинетическая и агрегативная устойчивость коллоидных растворов. Коллоидные растворы в природе и технике.
Тема 14. «Грубодисперсные системы»
Суспензии. Эмульсии. Пены.
Повторить материал из школьного курса:
Насыщенные и пересыщенные растворы. Растворимые и нерастворимые вещества. Качественная и количественная оценка растворимости. Таблица растворимости. Разбавленные и концентрированные растворы.
Качественный и количественный состав раствора. Массовая доля и молярная концентрация растворенного вещества.
Электролиты и неэлектролиты. Слабые и сильные электролиты.
1.3 Тематический план модуля
Тематический план второго модуля «Растворы. Дисперсные системы» представлен в таблице 1.1.
Таблица 1.1 − Тематический план модуля
| Наименование тем и разделов | Количество часов на изучение | |||
| Всего | В том числе | |||
| лекции | лабораторные работы | самостоятельная работа | ||
| Модуль 2 «Растворы. Дисперсные системы» | 32 | 8 | 8 | 16 |
| Истинные растворы | 21 | 5 | 8 | 8 |
| Коллоидные растворы | 8 | 2 | - | 6 |
| Грубодисперсные системы | 3 | 1 | - | 2 |
1.4 Перечень необходимых средств для выполнения
программы модуля
1.4.1 Лабораторная установка: растворы.
1.4.2 Учебники [1, 2, 3, 4, 5].
1.4.3 Методические указания [10].
1.4.4 Электронные диски: учебно-методический комплекс «Химия».
1.4.5 Сетевой учебно-методический комплекс «Химия».
1.5 План-график изучения модуля «Растворы. Дисперсные
системы»
План-график модуля, представленный в таблице 1.2, составлен исходя из того, что студент еженедельно 4−5 часов самостоятельно выполняет задания.
Таблица 1.2 − План-график изучения модуля
| Номер недели | Номер темы | Темы лекций | Лабораторные работы | Самостоятельная работа студентов содержание | Форма контроля |
| 7 | 8, 9 | Химические системы: об-щие понятия. Классификация дисперсных систем. Классификация растворов. Способы выражения состава растворов. Растворимость. Общие свойства растворов | Занятие 3 Выполнение лабораторной работы «Растворы» | Проработка учебников, учебных пособий, специальной методической литературы: темы 8, 9. Проработка конспектов лекций | Проверка конспектов лекций, тестов, индивидуальных расчетных заданий |
| 8 | 9,10 | Теория электролитической диссоциации. Теории кислот и оснований: С. Аррениуса, протонная теория Брёнстеда − Лаури, электронная теория Льюиса. Слабые электролиты. Константа диссоциации. Степень диссоциации. Закон разбавления Оствальда. Ионное произведение воды. Водородный показатель. Кислотно-основные индикаторы. Сильные электролиты | | Проработка учебников, учебных пособий, специальной методической литературы: темы 9, 10. Проработка конспектов лекций. Выполнение индивидуального расчетного за-дания [11] | |
| 9 | 11, 12 | Особенности реакций в растворах электролитов. Произведение растворимости. Гидролиз солей. Ионный обмен. Буферные растворы. Гетерогенные системы. Избыточная поверхностная энергия. Адсорбция | Занятие 4 Проведение текущего тестирования. Решение задач. За- щита лабораторной работы | Проработка учебников, учебных пособий, специальной методической литературы: темы 11, 12. Проработка конспектов лекций. Выполнение индивидуального расчетного задания [11] | |
| 10 | 13, 14 | Тонкодисперсные системы. Коллоидные растворы. Строение мицеллы. Методы получения. Свойства коллоидных растворов. Грубодисперсные системы. Суспензии. Эмульсии. Пены | - | Проработка учебников, учебных пособий, специальной ме-тодической литературы: темы 13, 14. Проработка конспектов лекций. Выполнение индивидуального расчетного за-дания [11] | |
| ПРОВЕДЕНИЕ ВТОРОГО ПРОМЕЖУТОЧНОГО ЭКЗАМЕНА | |||||
1.6 Планы лабораторных занятий
Планы лабораторных занятий представлены в таблице 1.3.
Таблица 1.3 − Планы лабораторных занятий
| Номер занятия | Наименование и краткое содержание,характер занятия и цель | Объем в часах |
| 1 | Подготовка и выполнение лабораторной работы «Растворы». Цель занятия: познакомиться с мерной химической посудой и освоить технику приготовления растворов заданного состава различными способами | 4 |
| 2 | Текущий тестовый опрос. Решение задач на тему «Растворы». Защита лабораторной работы. Цель занятия: освоить теоретические основы и научиться решать задачи на тему «Растворы», защитить лабораторную работу | 4 |
Лабораторные работы проводятся группой из 2−4 студентов.
Выполнению работы предшествует устный опрос по теории работы и собеседование по методике ее проведения, принципу работы лабораторной установки и входящих в нее химической посуды и устройств, а также уяснение вопросов, связанных с техникой безопасности проведения работ.
После выполнения работы преподаватель подписывает таблицу исходных данных, после чего студенты составляют отчет по лабораторной работе, содержащий:
1) титульный лист;
2) теоретическую часть;
3) зарисовку экспериментальной установки;
4) таблицу экспериментальных данных;
5) обработку результатов опыта;
6) выводы.
Итогом работы является защита полученных в ней результатов, защита проводится устно или письменно, но обязательно индивидуально.
Отчеты по лабораторным работам составляются каждым студентом и после защиты сдаются преподавателю.
Защита лабораторной работы №2
Тема: Свойства растворов и дисперсные системы.
Цель занятия: освоить теоретические основы темы «Растворы и дисперсные системы», научиться решать задачи.
План занятия:
- Текущий тестовый опрос.
- Решение задач по темам:
− приготовление растворов;
− общие свойства растворов;
− гидролиз солей.
- Защита лабораторной работы.
