Під загальною редакцією проф. Малого В. П. проф. Кратенко I. С. Харків 2006
| Вид материала | Диплом |
- Матер І а л и науково-практичної конференції з міжнародною участю 1-2 березня 2007, 7242.75kb.
- Под общей редакцией проф. Малого В. П., проф. Кратенко И. С. Харьков 2008, 8344.22kb.
- Р. А. Хальфин 08. 12. 2006 г. N 6530-рх методические рекомендации, 1062.91kb.
- За загальною редакцією, 1428.32kb.
- Программа студенческой олимпиады мгмсу по стоматологии 30. 10., 33.94kb.
- М. А. Рыбалко (отв редактор), проф, 973.68kb.
- Реферат циклу підручників «Україна в світовій політиці», 148.74kb.
- Колективу авторів у складі: проф. Гаращенко Ф. Г., проф. Закусило О. К., проф. Зайченко, 259.94kb.
- Программа по курсу "Уголовное право" / Сост проф. Б. С. Волков, проф. И. Д. Козочкин,, 638.15kb.
- Квалификационные тесты по дерматовенерологии Москва, 2267.11kb.
ЭКСТРАГЕНИТАЛЬНЫЕ ПРОЯВЛЕНИЯ ПРИ АКУШЕРСКО-ГИНЕКОЛОГИЧЕСКОМ СЕПСИСЕ
Джавахадзе М.В, Дараселия М.И., Мгалоблишвили Э.А., Гогелиани М.Г., Каджая Л.Л.
Противосепсисный Центр им. акад. В. Г. Бочоришвили, г. Тбилиси
В начале XXI-го века сепсис остается одной из актуальных медицинских и социальных проблем (Манухин И.Б., 2000). На сегодня научные исследователи подтверждают высокую частоту гнойно-септических осложнений после родов и абортов, которые несмотря на успехи достигнутые в критической медицине, не имеют тенденцию к снижению.
Целью нашего исследования являлось характеристика проявлений экстрагенитальных осложнений при акушерско-гинекологическом сепсисе.
Мы провели ретроспективные исследования историй болезней пациентов гинекологического отделения противосепсисного центра им. акад. В.Г.Бочоришвили (ПСЦ). В частности пациенток, которые лечились в ПСЦ-е с 1987-2000 г.г. с диагнозом послеродового и послеабортного сепсиса. Нами были исследованы экстрагенитальные проявления, которые были в основном причиной тяжелого течения заболевания.
Материал статистически разработан статистическим программным пакетом SPSS, 11 версией.
Из 2569 пациенток, госпитализированных 1987-2000 гг. диагноз сепсиса был поставлен у 524-х, из которых выздоровело 478 пациенток.
Мы разделили всех пациенток на 3 группы. В I группу были включены пациентки, у которых сепсис развился после родов через естественные родовые пути – их было 217 пациенток (45 %), II группу составили пациентки с сепсисом после кесарева сечения -167 (35 %) и III группу – пациентки с сепсисом после аборта – 105 (22 %).
Схема 1. Экстрагенитальные проявления при акушерско-гинекологическом сепсисе
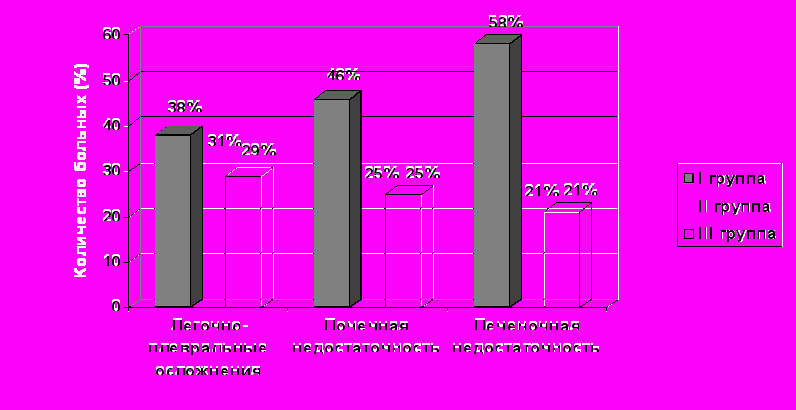
Легочно-плевральные осложнения отмечалис у 40% больных. Из клинических проявлений наиболее часто встречалась септическая пневмония – 65 пациенток (34%), бронхопневмония – 39 (21%), деструктивная пневмония 32 (17%), гнойный плеврит – 14 (3%), пневмоторакс 13 (3%), пиопневмоторакс 13 (3%) и в единичных случаях сухие и эксудативные плевриты. Такие больные поступали в клинику в тяжелом состоянии, была выражена дыхательная недостаточность, нарушена вентиляционная функция легких. Из мокроты и плевральной жидкости в основном высеивалис золотистый стафилокок (70 % ) и синегнойная палочка.
Между частотой легочно-плевральных осложнений и формой акушерско-гинекологического вмешательства достоверной связи не выявлено (p>0,01), хотя осложнения доминировали при сепсисе после родов через естественные родовые пути (40%).
Острая почечная недостаточность имелась у 19 % больных (Схема 1). Почти аналогичные результаты отмечают зарубежные авторы, в частности 23% - случаев при тяжелом сепсисе и 51 % - при септическом шоке. Острая почечная недостаточность развилась чаще (46 %) при послеродовом сепсисе (p>0,05).
Острая печеночная недостаточность с токсическим гепатитом выявлена у 33 больных (7%), среди которых преобладали пациенты с послеродовым сепсисом (p<0,05).
В единичных случаях встречались септический менингоэнцефалит (10 больных), церебральный васкулит (8) инфекционный психоз (4) , шизофренический синдром (3), септический эндокардит (4), септический перикардит ( 2).
Таким образом, по нашим клиническим материалом из экстрагенитальных проявлений при акушерско-гинекологическом сепсисе более часто встречались легочно-плевральные осложнения, почечная и печеночная недостаточность, которые сравнительно часто проявлялись при сепсисе после родов через естественные родовые пути.
Опримизация диагностики и лечения больных с ангионенным сепсисом
Доминяк А.Б., Чернуха Л.И., Ящук Ю.И., Влайков Г.Г., Чебурахин В.Н.
Гнойно–септические осложнения, которые возникают после реконструктивных операций на брюшной части аорты, подвздошных и бедренных артериях являются наиболее опасными осложнениями, которые угрожают жизни больных и достигают 12% (И. И. Затевахин и соавт., 1998). Воспалительные процессы приводят к распространению патогенной флори, на область сосудистых аллопротезов, их инфицированию, имунным нарушениям и возникновению ангиогенного сепсиса.
Цель исследования – оптимизировать методы диагностики, выбор показаний и методов хирургического лечения гнойно–септических осложнений аорто–бедренного протезирования.
Материалы и методы. Проанализированы результаты 5216 первичных операций на брюшной части аорты и периферических артериях из которых у 186 (3,5%) случаях послеоперационный период осложнился инфицированием трансплантата (ИТ), из которых у 31 (0,5%) наблюдалось инфицирование ложных аневризм. В зависимости от выраженности клинических проявлений и распространенности инфекции выделяем: локальное инфицирование трансплантата (ЛИТ), которое наблюдали у 63 (34%); тотальное инфицирование (ТИ) – у 70 (37,6%); ангиогенный сепсис (АС) – у 53 (28,4%). Возраст больных с АС был в пределах от 48 до 74 лет, все больные были мужчины.
Всем больным первично реваскуляризированно аорто–бедренный (АБ) сегмент: бифуркационное АБ аллопротезирование у 22 больных, бифуркационное АБ аллошунтирование – у 18; односторонее АБ шунтирование – у 13 больных.
У 53 больных с гнойно–септическими осложнениями клиническая картина проявилась нагноением послеоперационной раны во всех случаях, у 35 – сформировался незаживающий парапротезный, свищ (у 11 – в паховой области, и у 16 – в области рубца забрюшинного доступа), у 7 – мочеточниковый свищ, инфицирование ЛА – у 11 больных. У 35 больных возникло аррозивное кровотечение, острая ишемия нижних конечностей – у 10 больных.
Гнойно–септические осложнения диагнозированы на основании результатов клинического обследования, ультразвукового дуплексного сканирования, радиоизотопного с лейкоцитами меченными 99mТс, компьютерной томографии, бактериологическим исследованием аллопротеза и отделяемого из ран, рентгенконтрастной аортоартериографии, фистулографии, иммунологических методов исследования (определение воспалительного интерликина–6 (ИЛ–6), противоспалительного итерликина–4 (ИЛ–4).
Результати и их обсуждение. У всех больных клиническими проявлениями сепсиса были: наличие местного очага инфекции, лихорадка, анемия и гиперпротеинемия, лейкоцитоз, ускоренное СОЕ, значительный рост среднего уровня ИЛ–6 в сыворотке крови до 555,3 мг/мл, и ИЛ–4 до 130,6 мг/мл.
В зависимости от храктера и вида осложнений мы выделили три группы больных: 1 группа – с инфицированными аорто–бедренными аллопротезами; 2 группа – с ложными аневризмами дистальных и проксимальных анастомозов; 3 группа – с аррозивным кровотечением из анастомоза.
Бактериологическое исследование подтвердило, что преобладает стафилококовая флора (51,3%). Грамположительные бактерии колонизированы у 28% случаев; грамотрицательные – у 41%. Бактериемия выявлена у 44% больных. При подозрении на наличие инфекции протеза у всех больных высеяна микробная флора.
При ультразвуковом сканировании о наличии инфекции протеза – у 76% больных свидетельствовало скопление жидкости возле анастомоза или вдоль протеза. Радиоизотопное сканирование определило повышение накопления меченых лейкоцитов в области инфекции. При выборе метода и срока выполнения повторной операции учитывали локализацию инфицирования, вовлечения в гнойный процесс анастомозов, сохранение проходимости протеза, степень недостаточности кровоснабжения, анатомическую возможность обходного шунтирования, общее состояние больного и выраженость проявления гнойной инфекции.
При аррозивном кровотечении из анастомозов, обусловленным инфицированием аллотрансплантатов, безальтернативно удаляли инфицированный протез. Попытки хирургов наложения дополнительных швов, укрыть трансплантат предлежащими тканями были неэффективными. В то же время, угроза ампутации конечности диктовала необходимость в атипичном размещении нового сосудистого трансплантата (11), у больных с АС – полное удаление ИТ с одномоментной аутотканной реконструкцией магистральных артерий, проведением дезинтоксикационной, антибактериальной терапии и аутотканевой защитой области анастомоза: аутовенозное бифуркационное АБ шунтирование (20) или одностороннее аутовенозное АБ шунтирование (12). У больных с АС и развившейся полиорганной недостаточностью удаляли протез без восстановления кровотока (10).
Положительные результаты лечения получены у 41 больного, ампутации конечности на уровне средней трети бедра выполнена у 5 больных. На высоте кровотечения умерло 3 больных с инфицированием проксимального анастомоза и с аорто–кишечным свищом.
Дифференцированный подход к лечению больных с ангиогенным сепсисом и выполнением повторных реконструктивных операций до развития аррозивного кровотечения с использованием аутотрансплантатов позволяет получить хорошие и удовлетворительные результаты у 77,6% больных и значительно снизить летальность.
