Хімія є однією з основних природознавчих наук, що розвивається останнім часом дуже швидко
| Вид материала | Документы |
- Програми для профільного навчання в загальноосвітніх навчальних закладах Рекомендовано, 103.17kb.
- Останнім часом у літературознавстві з’явилося багато нових підходів до аналізу літературного, 126.23kb.
- 12 штучний інтелект. Експертні системи, 633.04kb.
- Енергозбереження в нашій країні останнім часом набуває все більшої актуальності, 66.58kb.
- Голоду не нова в історії світового письменства, оскільки йдеться, 136.43kb.
- «Про особисте селянське гос подарство», 924.69kb.
- Розпорядження, 26.48kb.
- Матеріал для виступу на педагогічній раді, 57.83kb.
- Єчимало класифікацій природних ресурсів, 682.02kb.
- Робоча програма навчальної дисципліни екоаналітична хімія напряму підготовки 040101, 154.06kb.
ПРАКТИЧНА РОБОТА № ОХ-2
МЕТОДИ ОЧИЩЕННЯ ТА ІДЕНТИФІКАЦІЇ РІДКИХ
ОРГАНІЧНИХ РЕЧОВИН
ДОСЛІД 1. Визначення температури кипіння
Реактиви: пропан-2-ол або інша органічна речовина з температурою кипіння 80–150°С.
О
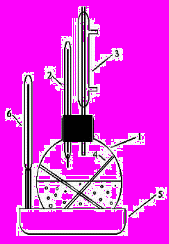
Мал. 2.1. Прилад
для визначення
температури кипіння:
1- колба; 2 - термометр;
3 - холодильник;
4 - капіляри; 5 - баня;
6 – технічний термометр
бладнання: скляні капіляри, круглодонна колба, водяний холодильник Лібіха, термометр, штатив з лапкою, прилад для визначення температури плавлення, нагрівний прилад.
1. Температура кипіння, на відміну від температури плавлення, дуже залежить від тиску і її точне визначення ускладнене перегрівом парів, вадами приладу, коливаннями атмосферного тиску. Тому в літературі часто для однієї речовини наводяться різні значення температури кипіння. Найпростішим приладом для визначення температури кипіння є прилад на мал.2.1. В круглодонну колбу 1 з широким горлом, місткість якої має бути не менше 50 мл, влийте на 1/4 її об’єму рідину, температуру кипіння якої будете виміряти. У рідину помістіть декілька капілярів 4 (запаяні кінці зверху). Колбу закрийте пробкою, в яку вставлений термометр 2 і зворотній холодильник 3. Нагрійте прилад на водяній або повітряній бані до початку процесу кипіння. Інтенсивність нагріву відрегулюйте так, щоб з кінця холодильника падало 20–30 крапель за хвилину, стежачи за тим, щоб краплі конденсату з холодильника не потрапили на термометр. За температуру кипіння беруть таке її значення, при якому температура залишатиметься постійною протягом 5–8 хвилин.
2
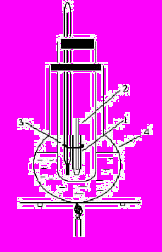
Мал.2.2. Прилад для визначення температури кипіння за Сиволобовим:
1 - пробірка; 2 - капіляр;
3 - гумове кільце;
4 - прилад для визначення
температури плавлення
. Іншим методом визначення температури кипіння є метод Сиволобова (мал.2.2). За Сиволобовим, маленьку скляну пробірку 1 довжиною 50 мм і діаметром 3 мм заповніть на 7–10 мм досліджуваною речовиною і помістіть в неї запаяний з одного кінця капіляр 2 (довжиною 55 мм, діаметром 1 мм) так, щоб його відкритий кінець був занурений у рідину. При-кріпіть пробірку до термометра за допомогою гумового кільця 3, помістіть її в прилад для визначення температури плавлення 4 і нагрійте, слідкуючи за тим, щоб швидкість нагрівання не перевищувала 3–5°С за хвилину. В ту мить, коли із капіляра почне виділятись безперервний ланцюг маленьких бульбашок пари досліджуваної рідини, відзначте показання термометра. Цю мить вважають точкою кипіння речовини. Визначення повторіть 3–4 рази, використовуючи кожного разу новий капіляр і нову порцію досліджуваної речовини.
3. Остаточним результатом вважають середнє арифметичне з усіх визначень.
● Якщо отримана Вами величина відрізняється від табличної, дайте цьому пояснення.
ДОСЛІД 2. Перегонка за атмосферного тиску
Реактиви: пропан-2-ол або інша органічна речовина з температурою кипіння 80–150°С.
Обладнання: колба Вюрца, водяний холодильник Лібіха, алонж, колби-приймачі, кип'ятильні камінці (шматочки пористих матеріалів, наприклад, уламки глиняного посуду, мармуру), термометр, два штативи, лапки, муфти, кільце, нагрівний прилад, скляна лійка.
1. Зберіть прилад, як показано на малюнку 2.3. Колбу закріпіть у штативі, затиснувши її лапкою вище газовідвідної трубки. В іншому штативі закріпіть холодильник. На кінці холодильної трубки закріпіть алонж і підставте під нього приймач.
2. У колбу Вюрца налийте пропанол (через лійку, щоб краплі рідини не потрапили у відвідну трубку) таким чином, щоб рідина, що переганяється, займала не більше 2/3 об'єму колби і вмістіть кілька кип'ятильних камінців для забезпечення рівномірного кипіння. Вставте пробку з термометром так, щоб кінець термометра розміщувався на 0,5 см нижче отвору відвідної трубки колби. Подайте в холодильник воду.
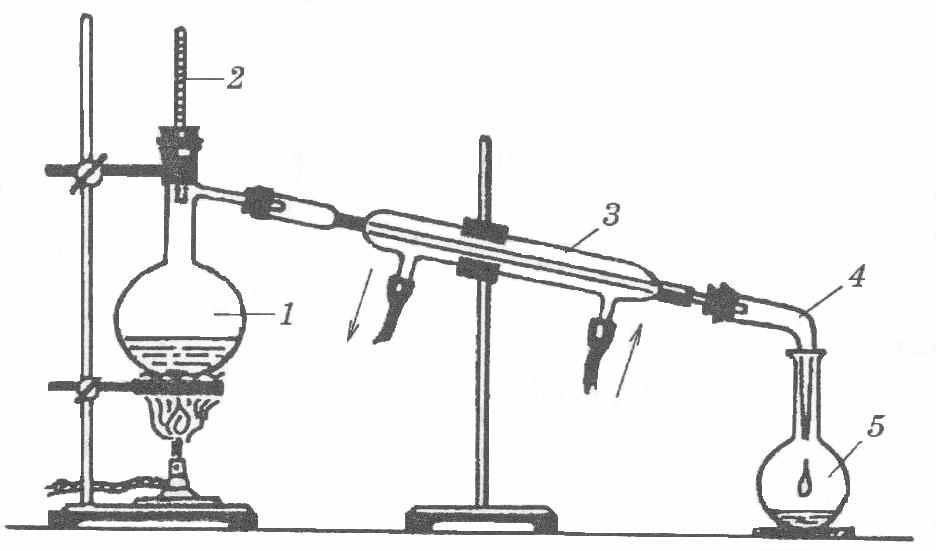

3. Обережно і рівномірно нагрівайте рідину (полум'я не повинно торкатися стінок колби вище від рівня рідини) і стежте за показаннями термометра. Коли температура залишатиметься сталою на протязі 1–2 хвилин, замініть приймач. Швидкість перегонки має бути ~1 крапля за секунду.
4. Зберіть кілька мілілітрів чистої рідини і припиніть перегонку.
ДОСЛІД 3. Розділення двох взаємно нерозчинних
рідин за допомогою ділильної лійки
Реактиви: тетрахлорметан, вода.
Обладнання: скляна лійка, ділильна лійка, хімічний стакан, колба, штатив з лапкою або кільцем.
1. Суміш води та неполярної органічної рідини, наприклад, тетрахлорметану, налийте за допомогою скляної лійки в ділильну лійку, яку потім закрийте пробкою і ретельно перемішайте. Після цього лійку переверніть догори носиком, обережно притримуючи пробку, і відвернувши в сторону від свого обличчя та інших осіб, відкрийте і знову закрийте краник. Якщо при перемішуванні в лійці змінився тиск, ви почуєте характерний свист повітря, яке проходить через кран. В цьому випадку процедуру відкриття–закриття крану між перемішуваннями треба повторювати до повного врівноваження тиску всередині лійки з атмосферним.
2. Ділильну лійку закріпіть в лапці або кільці штатива і почекайте, доки не утвориться чітка межа розділу фаз.
3. Для відділення органічної речовини відкрийте пробку і розташований знизу лійки кран, зберіть тетрахлорметан у чисту суху колбу. (Для усунення незначних кількостей води звичайно користуються осушувачами ― безводними кальцій хлоридом або натрій сульфатом, які надалі відфільтровують за допомогою складчастого фільтра).
СЕМІНАРСЬКЕ ЗАНЯТТЯ № ОХ-2
МЕТОДИ ОЧИЩЕННЯ ТА ІДЕНТИФІКАЦІЇ РІДКИХ
ОРГАНІЧНИХ РЕЧОВИН
Контрольні питання
- Що таке температура кипіння? Як вона залежить від складу та будови речовин?
- Якими способами можна визначити температуру кипіння? Які переваги у кожного з них? Які вади?
- *Як залежить температура кипіння від тиску? Як приводять результати вимірювань до нормального тиску?
- Що таке перегонка? Які види перегонки Вам відомі?
- З якою метою застосовують перегонку за атмосферного тиску? У вакуумі?
- Чи можна перегонкою користуватися не тільки для очищення, а й для розділення речовин? Які суміші можна розділити таким чином?
- Що таке фракційна перегонка? У яких випадках її застосовують?
- Назвіть основні деталі приладу для звичайної перегонки. Чим від нього відрізняється прилад для фракційної перегонки?
- Яким чином можна розділити суміш ацетону (т.кип. 56,2оС) й етанолу (т.кип. 78,3оС)?
- Які деталі приладу для вакуумної перегонки? Яких правил техніки безпеки треба дотримуватись при проведенні перегонки під вакуумом?
- Які деталі будуть потрібні для збирання приладу для перегонки діетилового етеру (т.кип. 35,6оС)? Які з них треба замінити, щоб перегнати додекан (т.кип. 216оС)? Чому?
- *Що таке азеотропна суміш? Яку речовину отримає експериментатор першою при повільній фракційній перегонці суміші двох речовин, що здатні утворювати азеотропну суміш? Що не здатні?
- *Що таке азеотропна сушка? Як виглядає і для чого служить насадка Дина-Старка?
- Чи можна перегонкою отримати чистий етиловий спирт виходячи з водно-спиртового розчину? А чисту воду?
- *Який склад рідини в колбі-приймачі Ви очікуєте при простій перегонці за атмосферного тиску:
а) 9% водного розчину оцтової кислоти (т.кип. 118оС);
б) 40% водного розчину етанолу;
в) 50% ацетоно-водної суміші?
- Що таке відстоювання (седиментація)? Декантація? Наведіть приклади використання цих процесів в народному господарстві.
- Чому вода і метанол (СН3ОН) необмежено розчиняються одне в одному, а метан в воді не розчиняється?
- Наведіть три приклади речовин з відповідними розчинниками, які відповідають принципу «подібне розчиняється в подібному».
- Що таке перегонка з водяною парою? Для очищення яких речовин можна її використовувати?
- Які властивості мають бути у речовин, щоб їх можна було розділити за допомогою ділильної лійки?
- Які речовини використовують в якості «осушувачів» рідких, твердих і газоподібних органічних речовин?
- На складі прохудла стеля і вночі через дощ в залишену відкритою бочку з олією набралася дощова вода. Яким чином повинен діяти завскладом щоб вернути олію і не сплачувати збитки?
- *Поділ методів очищення за агрегатним станом дуже відносний. Які методи очищення і розділення є загальними для твердих та рідких органічних речовин? Рідких та газоподібних речовин? Наведіть приклади.
