Хімія є однією з основних природознавчих наук, що розвивається останнім часом дуже швидко
| Вид материала | Документы |
СодержаниеДОСЛІД 3. Визначення температури плавлення Семінарське заняття № ох-1 |
- Програми для профільного навчання в загальноосвітніх навчальних закладах Рекомендовано, 103.17kb.
- Останнім часом у літературознавстві з’явилося багато нових підходів до аналізу літературного, 126.23kb.
- 12 штучний інтелект. Експертні системи, 633.04kb.
- Енергозбереження в нашій країні останнім часом набуває все більшої актуальності, 66.58kb.
- Голоду не нова в історії світового письменства, оскільки йдеться, 136.43kb.
- «Про особисте селянське гос подарство», 924.69kb.
- Розпорядження, 26.48kb.
- Матеріал для виступу на педагогічній раді, 57.83kb.
- Єчимало класифікацій природних ресурсів, 682.02kb.
- Робоча програма навчальної дисципліни екоаналітична хімія напряму підготовки 040101, 154.06kb.
ДОСЛІД 3. Визначення температури плавлення
Реактиви: бензойна кислота.
Обладнання: капіляри, скляна паличка, предметне скло, скляна трубка довжиною 50–70 см, прилад для визначення температури плавлення.
1. Температура плавлення є характерною константою твердих речовин. Залежно від приладу та швидкості нагрівання температура плавлення може бути визначена з точністю від десятих часток градуса до одного градуса. Чиста речовина плавиться при строго визначеній температурі. Цими властивостями користуються для встановлення ідентичності певної речовини з еталоном. Для цього змішують рівні кількості кристалів обох речовин, ретельно перетирають і визначають температуру плавлення суміші. Якщо температура плавлення суміші не змінюється в порівнянні з температурами плавлення кожного компоненту, то вважають, що ці дві речовини ідентичні. Якщо температура плавлення змішаної проби нижче т
 емператури плавлення вихідних компонентів (депресія температури плавлення), то суміш складається з двох різних сполук. Для визначення температури плавлення використовують скляний капіляр з внутрішнім діаметром 1 мм і довжиною 40–50 мм у приладі з подвійними стінками. Прилад для визначення т
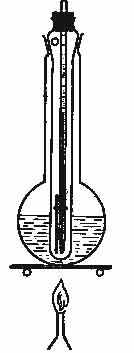
емператури плавлення вихідних компонентів (депресія температури плавлення), то суміш складається з двох різних сполук. Для визначення температури плавлення використовують скляний капіляр з внутрішнім діаметром 1 мм і довжиною 40–50 мм у приладі з подвійними стінками. Прилад для визначення т Мал.1.5. Прилад для визначення температури плавлення
емператури плавлення нижче за 200°С складається з к
Мал.1.5. Прилад для визначення температури плавлення
руглодонної колби з довгим горлом, в яку налита сульфатна кислота, силіконове масло або гліцерол. В горло колби вставлена широка пробірка (мал. 1.5). (Визначення температури плавлення речовин, які плавляться вище за 200°С, здійснюють у приладах з подвійними стінками без рідини або у спеціальних металевих блоках.) Увага! При визначенні температури плавлення у приладах, які вміщують рідину, обов’язково надівати захисні окуляри або маску.
2. На початку роботи запаяйте один кінець капіляра, обережно вносячи його у полум’я пальника. На предметному склі роздрібніть перекристалізовану речовину за допомогою скляної палички. Отвір капіляра занурте у речовину. Для переміщення речовини на дно капіляра киньте його декілька разів запаяним кінцем вниз всередину скляної трубки довжиною 50–70 см, яку перед тим поставте вертикально на тверду поверхню. Таким чином капіляр щільно набивається речовиною стовпчиком заввишки 0,3–0,5 см.
3. Капіляр укріпіть на термометрі за допомогою гумового кільця таким чином, щоб кінець капіляра з речовиною був на рівні кульки термометра. Термометр з капіляром помістіть у пробірку і закріпіть їх в отворі пробірки на пробці з вирізом (внутрішній простір колби повинен сполучатися з атмосферою).
4. Починайте обережно нагрівати прилад таким чином, щоб підвищення температури відбувалось на 5–10°С за хвилину, а поблизу очікуваної температури плавлення ― на 1–2°С за хвилину. (Температурою плавлення даної речовини вважається температурний інтервал з моменту появи рідкої фази до повного розплавлення речовини. Чим чистіше речовина, тим менший інтервал ― для чистих речовин він дорівнює 0,1–0,5°С).
СЕМІНАРСЬКЕ ЗАНЯТТЯ № ОХ-1
МЕТОДИ ОЧИЩЕННЯ ТА ІДЕНТИФІКАЦІЇ
ТВЕРДИХ ОРГАНІЧНИХ РЕЧОВИН
Контрольні питання
- На які два класи можна розділити всі хімічні речовини за їх складом? Які речовини вважаються органічними?
- Яка різниця між властивостями органічних та неорганічних речовин?
- За якими фізико-хімічними характеристиками можна вважати хімічну речовину чистою? Які фізичні константи використовуються для ідентифікації речовин?
- Які Ви знаєте методи очищення твердих речовин?
- Чим відрізняються методи очищення від методів розділення?
- Що таке фільтрування і декантація, чим вони схожі і в чому різниця цих методів?
- Які види фільтрування Вам відомі? Які приладдя для цього необхідні? З якою метою використовують складчастий фільтр?
- Назвіть основні деталі приладу для фільтрування під вакуумом. В яких випадках доцільно його використовувати?
- В чому полягає основний принцип очищення речовин за допомогою перекристалізації?
- Якими правилами керуються при виборі розчинників для перекристалізації?
- Чому для перекристалізації беруть мінімальний об'єм розчинника?
- Якими діями можна ініціювати утворення кристалів в насиченому розчині?
- *Охарактеризуйте метод «дрібної кристалізації». В яких випадках його використовують?
- Що таке сублімація? В яких випадках для очищення речовин використовують сублімацію?
- Яким основним обладнанням користуються при возгонці за атмосферного тиску? В вакуумі? Чи можна таким чином очищати речовини в промислових кількостях? Чому?
- Чи можна для розділення суміші піску та цукру використати сублімацію? Чому?
- Яким способом Ви збираєтесь розділити суміш піску та цукру?
- Господарка ненавмисне висипала щойнопридбаний пакет цукрової пудри в банку з крохмалем. Чи може вона відділити ці дві речовини одна від одної? Яким чином?
- Яким чином можна спробувати розділити суміш ошурків сірки, заліза та кристалів ферум(II) сульфіду?
- Як можна довести, що таблетка аспірину (ацетилсаліцилової кислоти) містить крім самої кислоти ще й домішки інших речовин?
- Назвіть основні деталі приладу для визначення температури плавлення.
- Чим відрізняються прилади для визначення температури плавлення легкоплавких та тугоплавких речовин?
- Чому для визначення температури плавлення бензойної кислоти капіляр запаюють з обох кінців?
- В чому полягає метод змішаної проби, для чого він використовується?
