Аналитические материалы предметной комиссии о проведении егэ по русскому языку в 2009 году
| Вид материала | Аналитические материалы |
- Кодификатор элементов содержания и требований к уровню подготовки выпускников общеобразовательных, 564.31kb.
- Рекомендации для учащихся по подготовке к егэ по английскому языку автор-составитель:, 428.85kb.
- Методические рекомендации по подготовке учащихся к егэ по русскому языку, 88.06kb.
- Данный курс предлагается ученикам 11 классов, чтобы качественно подготовиться к итоговой, 530.65kb.
- Сценарий школьной площадки для 10-классников «Готовимся к егэ по русскому языку», 51.85kb.
- Методическое письмо о проведении государственного выпускного экзамена по русскому языку, 188.03kb.
- Программа и методические рекомендации по русскому языку программа по русскому языку, 1693.32kb.
- Методические рекомендации по разработке заданий для школьного и муниципального этапов, 266.45kb.
- Обучение сочинению – рассуждению по плану – алгоритму, 235.82kb.
- Олимпиадное задание по русскому языку в 2010-2011 учебном году для осваивающих программу, 768.53kb.
Таблица №5
Количество учащихся, приступивших к выполнению заданий
-
Всего учащихся – 1345 чел.
Количество учащихся, приступивших к выполнению заданий
А
В
С
Чел.
1345
1345
1082
%
100%
100%
80,45%
В 2009 году положительный результат (зачет) получили 91,3 % выпускников, принимавших участие в экзамене, что выше на 2,3 %, чем в прошлом году (в 2008 году — 89 % выпускников, в 2007 — 88 %; в 2006 — 90,66 %).
Число выпускников, не справившихся с заданиями ЕГЭ по химии, составило 119 человек (8,84 %), что ниже на 2,16 %, чем в предыдущие годы (число выпускников получивших отрицательный результат в 2008 году составил 11 %, а в 2007 г. — 12 %). Из них два выпускника набрали нулевое количество баллов. Это позволяет предположить, что, как и в предыдущие годы, в экзамене принимало участие значительное число выпускников, которые имеют слабую подготовку, но рассчитывают получить более высокий балл.
В Красноярском крае в 2009 году максимальное количество баллов (80 — 100 баллов) набрали 46 человек (3,4 % от всех сдававших экзамен), что в два раза выше, чем в предыдущие годы (в 2008 году — 1,4 %; в 2007 году — 1,3 % выпускников; в 2006 году — 0,9 % от всех сдававших ЕГЭ по химии). Из них один выпускник набрал 100 баллов г. Заозерный (в прошлом году таких результатов не было, а в 2007 году было два выпускника, выполнивших все задания теста без единой ошибки). Средний балл (от 50 до 74 % выполнения) получили 33 % выпускников. Ниже среднего балла (от 33 до 49 баллов) набрали 54,76 % учащихся.
РЕЗУЛЬТАТЫ ЕГЭ ПО ТЕРРИТОРИЯМ КРАСНОЯРСКОГО КРАЯ
Решаемость тестов в среднем по Красноярскому краю составила 52,75 балла, что сопоставимо с результатами 2008 года (таблица № 6).
Таблица № 6
Распределение городов края и сельских районов по количеству
набранных баллов
| Территории | 2007 год | 2008 год | 2009 год |
| по 100-балльной шкале | по 100-балльной шкале | по 100-балльной шкале | |
| г. Красноярск | 55,94 | 55,93 | 52,41 |
| Города края | 48,46 | 54,83 | 54,51 |
| Сельские районы | 45,91 | 47,95 | 51,81 |
Результаты, приведенные в таблице № 5 свидетельствуют о незначительном понижении тестового балла по 100-балльной шкале, как в г. Красноярске, так и в сельских районах по сравнению с прошлыми 2008, 2007 годами.
Сравнивая результаты в различных территориях, можно отметить, что в 2009 году результаты выполнения тестовых заданий в городах края выше, чем в г. Красноярске и сельских районах.
Высокие результаты показали выпускники Советского (средний балл по 100-б. шкале 57,4 %) и Центрального районов (средний балл по 100-б. шкале 55,71 %); лучше выполнили работы по сравнению с 2008 годом, учащиеся Кировского района (повышение на 3,66 %). Однако следует отметить, что процент решаемости тестовых заданий выпускниками г. Красноярска в 2009 году несколько ниже, чем в прошлом году, значительное понижение тестового балла наблюдается в Центральном, Железнодорожном районах. Низкие результаты в Свердловском и Ленинском районах (47,52 % и 47,19 % соответственно).
Диаграмма результатов ЕГЭ — 2009 в разных районах г. Красноярска
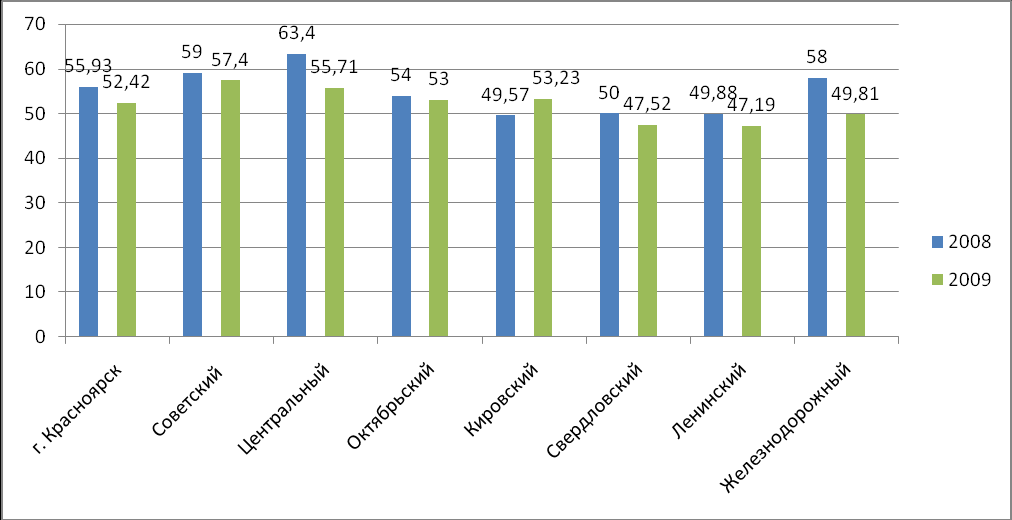
В 2009 году положительные результаты (без двоек) сдали экзамен по химии выпускники в 30 районах Красноярского края (см. приложение). Но, несмотря на то, что все (100 %) выпускников сдали ЕГЭ, процент решаемости остался низким в таких районах как Бирилюсский, Канский, Новоселовский, Саянский, Тюхтетский, Ужурский.
Сравнительные результаты ЕГЭ по химии в районах свидетельствуют, что из 42 районов Красноярского края в 20-ти высокие показатели среднего балла:
- Каратузский р-он — 72,7 б.,
- Дзержинский р-он — 69,63 б.,
- Северо-Енисейский р-он — 67,33 б.,
- г. Шарыпово — 66,70 б.,
- г. Назарово — 63,57 б.,
- Шушенский р-он — 61,5 б.,
- Уярский р-он — 61,25 б.,
- Балахтинский р-он — 60,56 б.,
- г. Заозерный — 60,33 б.,
- г. Канск — 59,24 б.,
- г. Зеленогорск (ЗАТО) — 59 б.,
- г. Ачинск — 57,84 б.,
- г. Минусинск — 57,41 %, г.
- Мотыгинский р-он — 56,81 б.,
- Сухобузимский р-он — 56,58 б.,
- Железногорск (ЗАТО) — 56,34 б.,
- Советский р-он (г. Красноярск) — 55,74 б.,
- Центральный р-он (г. Красноярск) — 55,71 б.,
- Иланский р-он — 55,6 б.,
- г. Лесосибирск — 55,11 б.,
На протяжении четырех лет без двоек сдают экзамен по химии выпускники Каратузского района. С минимальным количеством (1–2 чел.) не сдавших ЕГЭ по химии в городах: Ачинск, Канск, Зеленогорск (ЗАТО), Железногорск (ЗАТО); районах — Абанском, Березовском, Богучанском, Большемуртинском, Енисейском, Минусинском, Краснотуранском, Курагинском, Назаровском, Нижнеингашском, Сухобузимском.
По сравнению с прошлым годом наблюдается положительная динамика (улучшились результаты на 5–10 %) в гг. Ачинске, Канске, в районах: Ачинском, Балахтинском, Березовском, Богучанском, Большемуртинском, Ермаковском, Емельяновском, Иланском, Ирбейском, Кежемском, Краснотуранском, Нижнеингашском, Партизанском, Пировском, Сухобузимском, Уярском, Шарыповском. Однако, в городах Боготол, Дивногорск, Заозерный, Норильск, Сосновоборск, районах — Эвенкийском, Енисейском, Минусинском, Таймырском Долгано-Ненецком, Тюхтетском, Ужурском наблюдается понижение результатов на 3–10 %.
По сравнению с результатами ЕГЭ в Красноярском крае (средний балл 52,75) в некоторых территориях средний балл оказался ниже, например, в Березовском, Бирилюсском, Большемуртинском, Богучанском, Большеулуйском, Емельяновском, Канском, Нижнеингашском, Курагинском, Козульском, Назаровском, Новоселовском, Пировском, Саянском, Ужурском, Таймырском Долгано-Ненецком, Тасеевском, Тюхтетском, Эвенкийском районах, гг. Боготол, Дивногорск, Сосновоборск.
Диаграмма результатов ЕГЭ—2009 по территориям Красноярского края
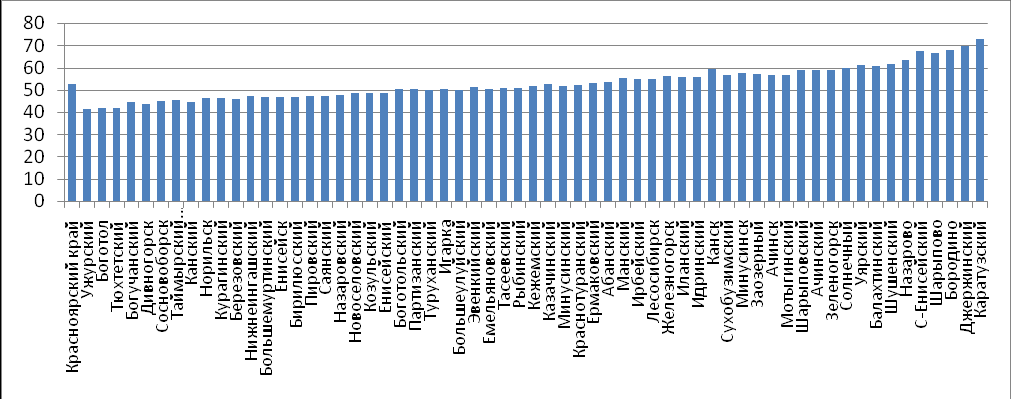
3.ФАКТОРЫ, ВЛИЯЩИЕ НА РЕЗУЛЬТАТЫ ЕГЭ
Положительная динамика результатов экзамена наблюдается вследствие влияния следующих факторов:
- выпускники, имеющие прочные знания по данному предмету и осознанно выбирающие химию для поступления в СФУ, КГПУ им. В.П. Астафьева, СибГТУ, Медицинский институт;
- участие выпускников в пробном экзамене, который позволяет с одной стороны, увидеть сам процесс проведения ЕГЭ (немного снимается нервное напряжение перед будущим экзаменом), а с другой, — попробовать свои силы, увидеть свои плюсы и минусы в знаниях и лучше подготовиться к экзамену;
- подробная информация о ЕГЭ и демоверсия позволяют учащимся прорешивая задания, не только проверить свой результат, но и на выставленном сайте задать любой вопрос, интересующий как учеников, так и их родителей;
- начиная с 2002 года, учителями накоплен большой опыт в подготовке учащихся к единому государственному экзамену — к выполнению стандартизованных тестовых заданий.
Причинами отрицательной динамики являются:
- не все учащиеся осознанно, заранее выбирают экзамен, чтобы к нему подготовиться, вероятно, завышенная самооценка учащихся позволяет выбрать предмет, которого они не знают;
- незнание некоторыми учащимися формата ЕГЭ (по всей видимости, нет доступа к Интернету в некоторых районах);
- зубрежка материала при подготовке к экзамену (рассчитано только на память), нет глубины понимания предмета;
- завышение итоговых оценок учителями при аттестации выпускников (три пишем, два в уме и т.д.), cубъективность в оценивании приводит к отрицательным показателям на экзамене;
- применение учителями традиционной системы обучения, которая в основном опирается на репродуктивные формы обучения и мало способствует осмысленному восприятию материала, не развивает у учащихся, как логического мышления, так и образного;
- нерациональное использование времени на уроке, отсутствие переконструированного тематического планирования, которое оптимально сочетало бы теоретическую и практическую его части;
- педагоги в основном недостаточно уделяют внимания решению расчетных задач по химии, слабо реагируя на современные представления о том, что именно через решение задач могут быть закреплены, доведены до функционального уровня (как того требует новый образовательный стандарт) теоретические положения;
- многие педагоги слабо ориентируются в конкретных требованиях государственного стандарта, ориентируясь на содержание авторских программ и стараясь равномерно преподать все их содержание, не разделяя материал, предназначенный для ознакомления, и материал, обязательный к усвоению каждым учащимся;
- большинство педагогов начинают подготовку учащихся к ЕГЭ в 11 классе (иногда в 10 классе), а эту работу необходимо начинать делать с 8 класса, еще в начале изучения курса химии, для того, чтобы выяснить пробелы в изучении теоретического материала и настроить учащихся на серьезную подготовку к выпускным экзаменам.
II АНАЛИЗ ВЫПОЛНЕНИЯ ЗАДАНИЙ
РЕЗУЛЬТАТЫ ВЫПОЛНЕНИЯ ЗАДАНИЙ ЧАСТИ А
На основе полученных статистических данных результатов выполнения вариантов, был проведен анализ и установлено следующее:
Выпускники образовательных учреждений из 30 заданий базового уровня на высоком уровне выполнены 3 задания, на среднем — 21 задание (что составляет 80 % от общего числа), на низком — 6 заданий (20 % от общего числа заданий базового уровня).
Как и в предыдущие годы, усвоение элементов содержания блока «Химический элемент» проверялось только на базовом уровне, т.е. заданиями с выбором ответа (А1 и А2). В соответствии с требованиями Федерального компонента образовательного стандарта по химии для средней школы (базовый уровень) эти задания проверяли сформированность знаний выпускников об электронном строении атомов и ионов, закономерностях изменения свойств химических элементов в зависимости от их положения в периодической системе Д.И.Менделеева. Результаты об усвоении данных элементов содержания выполнения заданий приведено в таблице № 7.
Диаграмма решаемости заданий по химии в 2009 году
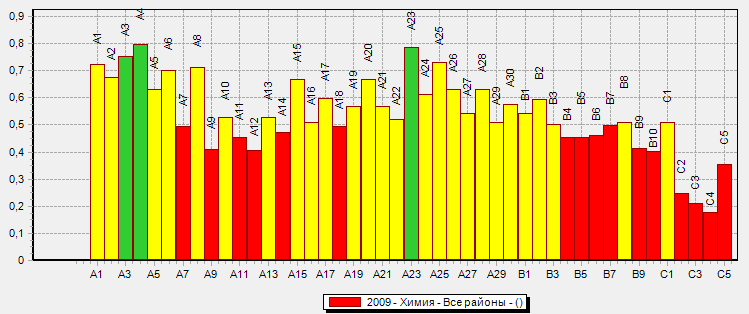
Учебный материал блока «Вещество» — важнейшая составляющая содержания курса химии средней школы. На его основе раскрываются идеи единства и многообразия неорганических и органических веществ, обусловленности свойств и применения веществ их составом и строением.
Значимость содержания данного блока в общей системе знаний выпускников
обуславливает традиционно высокий процент заданий экзаменационной работы, ориентированных на проверку усвоения этого материала. В соответствии с требованиями стандарта к общеобразовательной подготовке
выпускников задания, построенные на материале блока «Вещество», проверяли сформированность умений: называть изученные вещества по «тривиальной» или международной номенклатуре; определять валентность и степень окисления химических элементов, тип химической связи в соединениях, принадлежность веществ к различным классам; характеризовать строение и свойства изученных соединений; объяснять зависимость свойств веществ от их состава и строения.
Таблица № 7
Процент выполнения заданий части А в 2008, 2009 гг.
| Задания | Элемент содержания | Процент выполнения | |
| 2008 | 2009 | ||
| А 1 | Формулы существования химических элементов. Современные представления о строении атомов. Изотопы. Строение электронных оболочек атомов элементов первых четырех периодов. Атомные орбитали, s- и p – элементы. Основное и возбужденное состояние атомов. | 81,3 | 72 |
| А 2 | Периодический закон и периодическая система химических элементов Д.И. Менделеева. Радиусы атомов, их периодические изменения в периодической системе. | 80 | 67 |
| А 3 | Химическая связь: ковалентная (полярная, неполярная), ионная, металлическая, водородная. Способы образования ковалентной связи. Характеристика ковалентной связи: длина, энергия связи. Образование ионной связи. | 65 | 75 |
| А 4 | Электроотрицательность. Степень окисления и валентность химических элементов. | 82,3 | 80 |
| А 5 | Вещества молекулярного и немолекулярного строения. Зависимость свойств веществ от кристаллической решетки. | 76,1 | 63 |
| А 6 | Классификация неорганических веществ. Классификация и номенклатура органических веществ. | 62 | 70 |
| А 7 | Общая характеристика металлов главных подгрупп I–III групп в связи с положением в периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. Характеристика переходных элементов — меди, цинка, хрома, железа — по их положению в периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. | 52 | 49 |
| А 8 | Общая характеристика неметаллов главных подгрупп IV–VII групп в связи с положением в периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. | 61 | 71 |
| А 9 | Характерные химические свойства простых веществ — металлов: щелочных, щелочноземельных, алюминия, переходных металлов — меди, цинка, хрома, железа. Характерные химические свойства простых веществ — неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния. | 55 | 40 |
| А 10 | Характерные химические свойства оксидов: основных, амфотерных, кислотных. | 44 | 53 |
| А 11 | Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот. | 53 | 45 |
| А 12 | Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка). | 50 | 40 |
| А 13 | Взаимосвязь неорганических веществ. | 49 | 53 |
| А 14 | Основные положения и направления развития теории химического строения органических веществ А.М Бутлерова. Гомологический ряд углеводородов. Изомеры углеводородов. Структурная и пространственная изомерия. | 77,3 | 47 |
| А 15 | Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа. Характерные химические свойства углеводородов: алканов, алкенов, диенов, алкинов. Характерные химические свойства ароматических углеводородов: бензола, толуола. | 59 | 67 |
| А 16 | Характерные химические свойства одноатомных и многоатомных спиртов; фенола. | 45 | 51 |
| А 17 | Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Биологически важные вещества: жир, углеводы (моносахарида, дисахариды, полисахариды), белки. | 47 | 59,7 |
| А 18 | Взаимосвязь органических веществ. | 49 | 49,3 |
| А 19 | Классификация химических реакций в органической и неорганической химии. | 78 | 57 |
| А 20 | Скорость реакции, ее зависимость от различных факторов. | 54 | 67 |
| А 21 | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение равновесия под действием различных факторов. | 59 | 57 |
| А 22 | Диссоциация электролитов в водных растворах. Слабые и сильные электролиты. | 79,7 | 52 |
| А 23 | Реакции ионного обмена. | 76,4 | 79 |
| А 24 | Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее. | 75,5 | 61 |
| А 25 | Гидролиз солей. Среда водных растворов: нейтральная, кислая, щелочная. | 57 | 73 |
| А 26 | Реакции, характеризующие основные свойства и способы получения углеводородов. | 49 | 63 |
| А 27 | Реакции, характеризующие основные свойства и способы получения кислородсодержащих соединений. | 49 | 54,5 |
| А 28 | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсическими веществами, средствами бытовой химии. Методы исследования объектов изучаемых в химии. Определение характера среды водных растворов веществ. Индикаторы. Качественные реакции на неорганические вещества и ионы, отдельные классы органических соединений. | 43 | 63 |
| А 29 | Общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного способа получения аммиака, серной, азотной кислот, чугуна, стали, метанола). Промышленное получение веществ и охрана окружающей среды. Природные источники углеводородов, их переработка. | 42 | 50 |
| А 30 | Расчеты объемных отношений газов при химических реакциях. Расчеты теплового эффекта реакции. | 75,1 | 53 |
Анализ результатов выполнения экзаменационной работы 2009 г. показал, что выпускниками на базовом уровне хорошо усвоены элементы содержания, которые являются важнейшим составляющими основных разделов и тем школьного курса химии: периодический закон и периодическая система химических элементов Д.И.Менделеева; современные представления о строении атома; электроотрицательность, степень окисления; виды химической связи и способы ее образования; классификация неорганических и органических веществ; гидролиз солей; обратимые и необратимые химические реакции; химическое равновесие и условия его смещения; окислительно-восстановительные реакции; реакции ионного обмена; качественные реакции на неорганические вещества и ионы, отдельные классы органических соединений.
