Министерство здравоохранния Украины Академия медицинских наук Украины Днепропетровская государственная медицинская академия Кафедра анестезиологии и интенсивной терапии перфторан в комплексе интенсивной терапии сепсиса (Методические рекомендации)
| Вид материала | Методические рекомендации |
- Министерство Здравоохранения Украины Донецкий национальный медицинский университет, 1639.98kb.
- Глюкокортикостероиды в интенсивной терапии сепсиса и септического шока, 148.14kb.
- Кафедра анестезиологии, реаниматологии и интенсивной терапии факультета последипломного, 135.04kb.
- Диагностика и лечение тяжелого сепсиса и септического шока, 138.15kb.
- «Российская медицинская академия последипломного образования Росздрава», 280.78kb.
- Министерство здравоохранения Республики Казахстан Семипалатинская государственная медицинская, 765.11kb.
- Казахский национальный медицинский университет им. С. Д. Асфендиярова центр непрерывного, 1610.51kb.
- Методические рекомендации (№38), 639.69kb.
- Домашнее задание для подготовки к практическим занятиям и внеаудиторной самостоятельной, 49.25kb.
- Рабочая программа по курсу анестезиологии и реаниматологии Специальность: 040100-«Лечебное, 136.97kb.
Местное лечение
Необходимо как можно раньше установить очаг инфекции: бактериемия, инфекции, связанные с центральным венозным катетером, вентилятор-ассоциированная пневмония, хирургические инфекции и интраабдоминальный сепсис, острый бескаменный холецистит, синуситы, инвазивные грибковые заболевания.
Методы хирургического лечения состоят в радикальном иссечении нежизнеспособных тканей раны. При абдоминальной инфекции используются: чрезкожное дренирование, открытое непрерывное промывание, лапаротомия («открытый живот»), чаще плановые, программированные релапаротомии с этапным лаважем.
При выявлении жидкости в придаточных полостях проводится пункция и дренирование синусов до начала антибиотикотерапии.
^
Общее лечение
Общее лечение включает антибактериальную терапию, гемодинамическую, респираторную, нутритивную поддержку, иммунотерапию, профилактику тромбоэмболических и других осложнений.
Антибактериальная терапия
Раннее назначение адекватной антибиотикотерапии резко снижает риск неблагоприятного исхода.
Выбор антибиотиков определяется вероятным возбудителем и его чувствительностью к ним, характером основного заболевания, на фоне которого развилось инфекционное осложнение, состоянием иммунитета, фармакодинамикой антибиотика.
Предварительные данные о возбудителе можно получить по микробиологическому пейзажу после окраски мазка по Грамму: палочки или кокки, грамотрицательная или грамположительная инфекция, ассоциация микробов или монокультура. Кроме того, можно заподозрить анаэробную неклостридиальную инфекцию.
До получения окончательного бактериального диагноза применяется эмпирическая антибиотикотерапия.
Целесообразно применение деэскалационной антибактериальной терапии, характеризующейся широким стартовым спектром, дающим максимальную возможность охвата наиболее вероятных возбудителей с последующим (от 48 до 72 часов) переходом на терапию суженного спектра на основании микробиологических данных.
При кандидемии проводится антифунгинальная терапия. Противогрибковые препараты эмпирически не назначаются.
При выборе антибиотиков следует руководствоваться не только данными чувствительности микрофлоры к антибиотику, но и его возможностью создавать терапевтическую концентрацию в очаге инфекции (не менее, чем в 2 раза превышающую МПК).
Гемодинамическая поддержка
Нарушение гемоциркуляции является одним из основных признаков тяжелого сепсиса. Первоочередным мероприятием, направленным на восстановление тканевой перфузии и нормализацию окислительного метаболизма следует считать коррекцию ОЦК. Инфузионно-трансфузионная терапия должна проводиться с учетом конечных величин таких клинических показателей, как артериальное давление, пульс, сердечный выброс, диурез, концентрация лактата в крови, сатурация смешанной венозной крови кислородом, концентрация гемоглобина. Последний должен удерживаться в пределах не ниже 80-100 г/л, а при остающемся низком сердечном выбросе, десатурации смешанной венозной крови, лактат-ацидозе или у больных с ИБС – 100-120 г/л.
Среди инфузионных сред заслуживают внимания кровезаменители с газотранспортной функцией (перфторан), препараты ГЭК.
Если нормализация ОЦК не приводит к адекватному устранению артериальной гипотензии и восстановлению органной перфузии следует начинать вазопрессорную терапию.
Для этой цели используются допамин и норадреналин, при этом последний обладает более выраженным вазопрессорным эффектом. В случаях рефрактерной гипотензии назначается адреналин.
При низком сердечном выбросе после достижения адекватной жидкостной ресусцитации препаратом первого выбора является добутамин (добутрекс), который оказывает положительное инотропное влияние на сердце, улучшает кровообращение.
Респираторная терапия
Исходы при критических состояниях в большой мере обусловлены своевременной и адекватной коррекцией кислородного гомеостаза.
Поддержание адекватной оксигенации – на уровне SaO2>90%, обеспечивающей достаточную доставку кислорода к тканям, достигается путем проведения оксигенотерапии с использованием разных концентраций кислорода во вдыхаемой смеси. При эндотрахеальной интубации для снижения FiO2<0,6 может быть применено ПДКВ.
У больных с СОПЛ/ОРДСВ при тахипноэ > 40 в мин., участии в акте дыхания вспомогательных мышц, нарушении ментального статуса, тяжелой гипоксемии, несмотря на проведение оксигенотерапии, показаны ранняя интубация и ИВЛ.
При проведении ИВЛ у больных с ОРДСВ с высоким давлением на вдохе, риске баротравмы или волюмтравмы допустимы гиперкапния с уменьшением ДО до 6 мл/кг и поддержанием экспираторного плато менее 30 см вод.ст.
В случаях зависимости больного от высокого уровня FiO2 следует применять prone position. При угрожающей жизни гипоксемии, резистентной к традиционной терапии, показан оксид азота.
Отлучение от респиратора производится постепенно после стабилизации жизненно важных функций и кислородного гомеостаза.
Нутритивная поддержка
Септическое состояние организма характеризуется гиперметаболическим состоянием, которое требует повышенного удовлетворения энергетических запросов для репарации тканей и поддержания его защитных механизмов. С целью предупреждения потери массы тела и поддержания метаболических процессов назначается парентеральное, предпочтительнее энтеральное питание.
Парентеральное питание назначается при наличии противопоказаний к энтеральному питанию.
Рекомендуется исходить из следующих расчетов ежедневных потребностей: калории – 25-30 ккал/кг, протеин – 1,3-2 г/кг, глюкоза – 30-70 % от общих небелковых калорий, эссенциальных жирных кислот – 1 г/кг.
Иммуномодулирующая терапия
Коррекция иммунологических нарушений и целенаправленное влияние на отдельные звенья иммунной системы проводятся на основании иммунологического диагноза.
У больных сепсисом выраженный эффект наблюдается при использовании рекомбинантного цитокина иммунной системы – интерлейкина-2 (ронколейкина); деривата натрия, представляющего собой набор фрагментов ДНК, необходимых для ускоренного деления клеток, в т.ч. и иммунокомпетентных; индуктора интерферона неовира, который стимулирует клетки моноцитного ряда.
Целесообразно фармакологическую иммунотерапию сочетать с экстракорпоральными методами (плазмаферез, плазмосорбция, ультрафильтрация).
Глюкокортикоиды не рекомендуется использовать в высоких дозах (30 мг/кг) и коротким курсом (1-2 дня). Они могут быть эффективными при рефрактерном септическом шоке. При этом назначается гидрокортизон в дозе 100 мг 3 раза в день в течение 5-10 дней.
Из других видов интенсивной терапии не следует забывать о необходимости профилактики ТЭО (низкие дозы гепарина, предпочтительнее НМГ), профилактики стресс-язв и гастроинтестинальных кровотечений.
В последние десятилетия несколько снизилась летальность при тяжелом сепсисе и септическом шоке за счет мониторного контроля, улучшения диагностики и качества заместительной и поддерживающей интенсивной терапии в созданных специализированных отделениях интенсивной терапии сепсиса. Вместе с тем даже в ведущих зарубежных центрах с современными техническими возможностями диагностики, мониторинга и лечения летальность, как было указано ранее, остается высокой.
Одним из методов дальнейшего повышения результатов патогенетической и поддерживающей интенсивной терапии, направленных на улучшение общей и регионарной оксигенации, включая легкие, почки, гепатоспланхнитический регион, представляющие собой органы-мишени и пейсмейкеры развития СПОН является использование в комплексе интенсивного лечения перфторана, как системное, так и локальное.
^
СВЕДЕНИЯ О ПЕРФТОРАНЕ
Перфторан – это 10% субмикронная эмульсия перфторорганических соединений (ПФОС) с газотранспортными свойствами, обладающий полифункциональным действием. Основными газотранспортными компонентами перфторана являются перфтордекалин и перфторметилциклогексилпиперидин. ПФОС являются химически инертными, не подвергаются в организме человека метаболическим превращениям. Состав и основные свойства перфторана отражены в таблице 2.
Таблица 2. Состав и основные физико-химические свойства перфторана
| ^ Компонент эмульсии | Содержание |
| Перфтордекалин | 7 об% |
| Перфторметилциклогексилпиперидин | 3 об% |
| Проксанол 268 | 4 % |
| NaCl | 102 ммоль/л |
| KCl | 4,8 ммоль/л |
| MgCl2 | 1,8 ммоль/л |
| NaHCO3 | 7,7 ммоль/л |
| NaH2PO4 | 1,7 ммоль/л |
| D-глюкоза | 11 ммоль/л |
| Ион фтора | 10-20 мкмоль/л |
| рН | 7,2-7,8 |
| Осмолярность | 280-340 мосм/л |
| Относительная вязкость | 2,5 сП |
| Средний размер частиц эмульсии | 0,07 мкм |
Эмульсия перфторана белого цвета с голубоватым оттенком, отчего получила название «голубая кровь». Без запаха. Выпускается в стеклянных флаконах по 100, 200 и 400 мл.
Период полувыведения перфторана из кровотока 22-24 часа. Выводится в основном через легкие (93%), в меньшей степени через почки (4%), с желчью (3%). Частицы эмульсии ПФОС временно аккумулируются в макрофагах печени, селезенки, костного мозга. Период полувыведения ПФОС из макрофагов после замещения им у крыс 65% ОЦК для перфтордекалина составляет 14 дней (полное выведение 1 месяц), для перфторметилциклогексилпиперидина – 90 дней (полное выведение 18-24 месяца).
Эффекты перфторана при внутривенном его введении отражены в табл. 3.
^ Таблица 3. Эффекты перфторана при внутривенном введении.
| Показатели | Эффекты | |
| Кислородная емкость, об% | 7,0 | Дополнительная емкость |
| Вязкость, сП | 2,5 | Уменьшение вязкости, дезагрегация эритроцитов |
| Растворимость в жирах | Растворяется в мембране эритроцитов | Уменьшение вязкости крови за счет повышения эластичности и деформируемости мембран эритроцитов |
| 1 мл перфторана связывает 10 мг липидов | Предупреждает и устраняет жировую эмболию сосудистого русла | |
| Размеры, мкм | 0,07 против 7,0 у эритроцитов | Частички перфторан в отличие от эритроцитов свободно проходят через спазмированные, склерозированные, частично тромбированные и сладжированные сосуды |
| Первичный гемостаз | Дезагрегация тромбоцитов, что способствует реканализации сосудистого русла | |
| Вторичный гемостаз | Повышение фибринолитической активности, снижение концентрации фибриногена, фактора XIII, что устраняет последствия свертывания крови и способствует реканализации сосудистого русла | |
| Суммарная поверхность газообмена, м2/100 мл | 847 против 70 у эритроцитов | Возрастает суммарная поверхность газообмена |
| Растворимость кислорода в среде, об% | До 40 (ПФОС) | Из частичек ПФОС в кровотоке образуются каналы типа «жемчужных нитей», проводимость кислорода по которым в 20-25 раз выше, чем по окружающей их плазме. Эстафетный клиренс кислорода в системе «альвеолы/капил-ляры легких/эритроциты/ткань» возрастает |
| Осмолярность, мосм/л | 280-340 | Осмотический диурез |
| Стабилизация клеточных мембран | Противоотечный | |
Как видно из таблицы, субмикронные эмульсии ПФОС, кроме кислородотранспортных свойств, обладают реологическим эффектом. Последний обусловлен не только тем, что частицы перфторана, размеры которых почти в 100 раз меньше размеров эритроцитов, проникают в кровяное русло, куда эритроциты в условиях стресса проникнуть не могут, но и свойствами эмульгатора проксанола, который, являясь поверхностно-активным веществом, улучшает текучесть и препятствует агрегации клеток крови за счет увеличения поверхностного заряда эритроцитов.
Перфторан также обладает кардио- и нейропротекторным действием, имеет сорбционные свойства, оказывает дозозависимое иммунотропное действие. В дозе до 10 мл/кг в первые часы – до суток происходит незначительное увеличение макрофагальной функции нейтрофилов с последующей её существенной активацией на длительное время – до 7 суток.
Перфторан хранится в замороженном состоянии при tº –18 ºС – 3 года, в размороженном состоянии при tº +4 ºС – 2 недели.
Рекомендуется самопроизвольное размораживание препарата при комнатной температуре или при tº +4 ºС. После этого препарат необходимо осторожно встряхнуть до полной однородности состава. Перед инфузией согреть до +21-+23 ºС. Допускается 5-кратное размораживание/замораживание.
Препарат непригоден к применению при расслоении эмульсии (даже после встряхивания), помутнении её (до молочного цвета), появление осадка (прозрачные маслянистые капли на дне флакона).
Запрещается хранить перфторана при tº ниже –18 ºС и размораживать при tº выше + 30 ºС.
Противопоказанием к его применению являются гемофилия, аллергические и аутоиммунные заболевания, повышенная чувствительность к препарату. При беременности использование перфторана возможно по жизненным показаниям.
Перфторан – это первый и единственный препарат, введенный ВОЗ в Международную анатомо-клинико-химическую классификацию (АТС) в рубрику «кровезаменители и перфузионные растворы» под кодом В05А А03. В настоящее время – это единственный препарат, разрешенный к широкому клиническому применению. Он допущен для клинического использования и на всей территории Украины (регистрационное свидетельство № Р 06.99/00716 от 225.06.1999 г.).
^
ПЕРФТОРАН У БОЛЬНЫХ СЕПСИСОМ
ПРИ РАЗЛИЧНЫХ ПУТЯХ
ЕГО ВВЕДЕНИЯ
Выбор перфторана для оптимизации интенсивной терапии у больных сепсисом обусловлен его полифункциональным действием, среди которого особого внимания у этих больных заслуживает его противоишемическое действие, способность предупреждать развитие шунтирующего кровотока в паренхиматозных органах и создавать условия для адекватного энергообеспечения, быть «интракорпоральным сорбентом» для биологически активных веществ, иммунотропное действие.
Исходя из патогенеза сепсиса, выраженности поражения того или иного органа мы использовали различные пути введения перфторана: системный – внутривенный и локальный – энтеральный и эндотрахеальный. Клинические эффекты при его применении представлены на рис.2.
Внутривенный путь введения перфторана
Внутривенный путь введения перфторана является наиболее распространенным. Это связано с тем, что первоначально этот препарат разрабатывался как заменитель крови при кровопотере. Особенностью этого пути введения является возможность ликвидации ишемии и гипоксии в любом органе и ткани.
Важно подчеркнуть, что введение эмульсии ПФОС не влияет на скорость и качество проведения анализов на групповую совместимость крови.
^ Перфторан совместим в одной линии с донорской кровью, альбумином, изотоническим солевым раствором, глюкозой, мафусолом, полиоксидином.
Перфторан не совместим с декстранами и препаратами ГЭК в виду их влияния на биологические и физико-химические свойства препарата. При необходимости следует использовать другую вену или ту же, но после окончания инфузии перфторана.
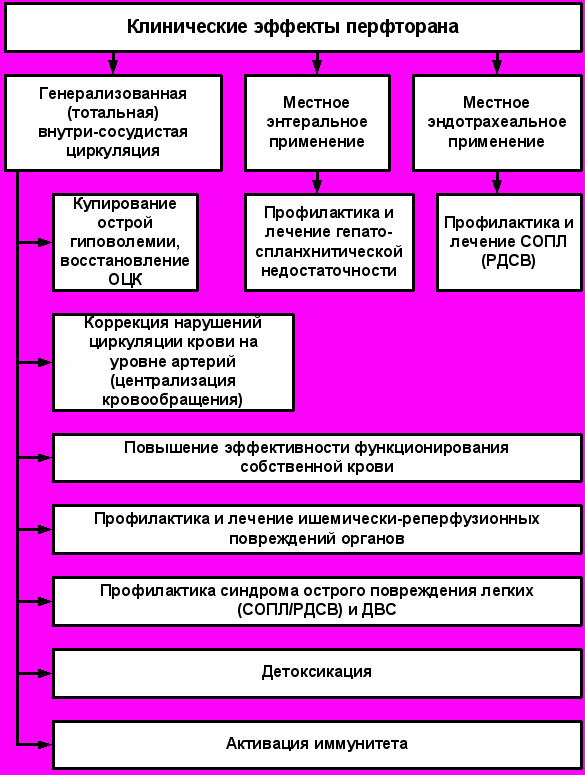
Рис. 2. Клинически эффекты перфторана у больных сепсисом
при различных путях его введения.
