Структурно-кинетические закономерности и механизм термораспада полифункциональных нитро- и азидосоединений 02. 00. 04 физическая химия
| Вид материала | Закон |
СодержаниеКинетические и термодинамические параметры разложения 2-замещенных Таблица 3.6 Кинетические параметры термораспада соединений XXIV |
- Синтез и исследование полифункциональных люминофоров на основе алюминатов стронция, 307.95kb.
- Рабочая программа дисциплины (модуля) «математический анализ», 424.74kb.
- Рабочая программа дисциплины (модуля) «Уравнения математической физики», 266.58kb.
- Рабочая программа дисциплины «физическая химия», 80.79kb.
- Рабочая программа дисциплины (модуля) «Линейная алгебра и аналитическая геометрия», 275.82kb.
- Программа дисциплины дпп. Ф. 05 Физическая химия, 267.17kb.
- «Кинетика и механизм реакции поликонденсации аминокислот» 02. 00. 04 физическая химия, 332.67kb.
- И в свет разрешаю на основании "Единых правил", п 14 Заместитель первого проректора-, 350.14kb.
- Физико-химические закономерности удерживания производных адамантана в высокоэффективной, 432.05kb.
- Физико-химические закономерности формирования и деградации органосиликатных покрытий, 977.75kb.
Таблица 3.5
Кинетические и термодинамические параметры разложения 2-замещенных
5,5-динитро-1,3-диоксанов XXIII
| Шифр | Условия распада | ΔТ, C | k 200С105, c–1 | Еa, кДж/моль | lgA | S200С, Дж/(мольК) |
| XXIII.1 | Расплав Раствор | 180–200 195–215 | 3,89 3,05 | 176,8 174,6 | 15.09 14,75 | 31,8 25,3 |
| XXIII.2 | Расплав Раствор | 180–200 190–210 | 3,68 2,48 | 175,8 177,9 | 14,97 15,03 | 29,5 30, 7 |
| XXIII.3 | Расплав Раствор | 180–200 195–215 | 2,73 2,27 | 178,5 177,1 | 15,12 14,90 | 32,4 28,2 |
| XXIII.4 | Раствор | 185–205 | 2,18 | 176,3 | 14,79 | 26,1 |
| XXIII.5 | Раствор | 190–215 | 5,63 | 174,2 | 14,97 | 29,5 |
| XXIII.6 | Раствор | 190–210 | 4,96 | 175,8 | 15,1 | 32,0 |
| XXIII.7 | Расплав Раствор | 190–210 190–210 | 4,78 4,09 | 179,3 175,4 | 15,44 14,97 | 38,5 29,5 |
| СH3C(NO2)2CH3 | Газ* | 175–210 | 0,74 | 211,6 | 18,20 | 91,4 |
* [Flournoy J.M., 1962]
Природа заместителя в цикле слабо влияет на скорость распада изученных соединений (константы скорости изменяются не более чем в три раза). В то же время скорость распада соединений XXIII в сравнении с 2,2-динитропропаном в 3–8 раз больше. Причина этого, возможно, заключается в меньшей конформационной подвижности 5,5-динитро-1,3-диоксанового цикла по сравнению с 2,2-динитропропаном.
Термораспад соединений R1N(NO2)CH2C(NO2)2R2 (XXIV), где R1 = C2H5, R2 = F (1), CH3 (2), CH2N(NO2)СH3 (3), NO2 (4), Cl (5), CH2C(NO2)2СH3 (6), Br (7),
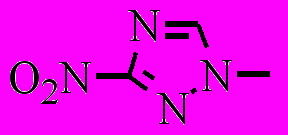 (8), I (9),
(8), I (9), 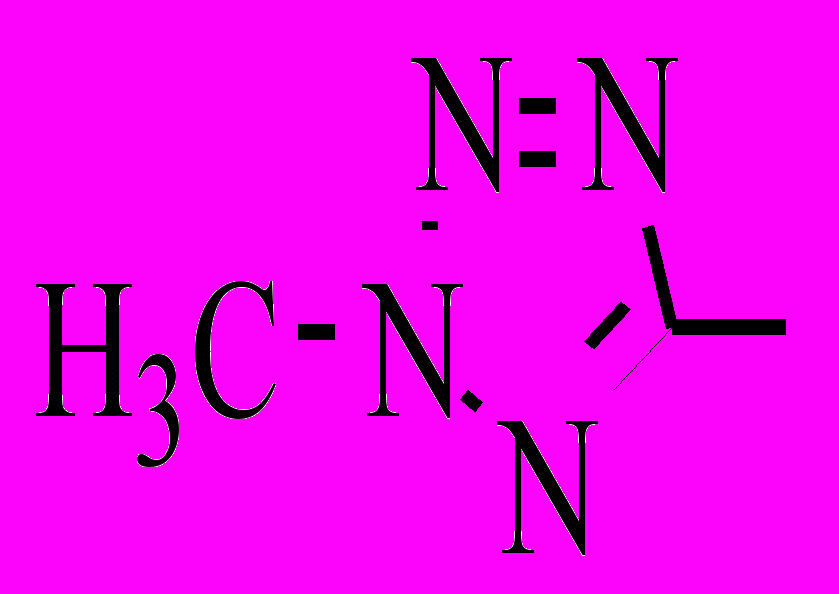 (10), R1= СH3, R2= СH3 (11), NO2 (12), Cl (13), а также R2= NO2, R1= СH3 (12), C2H5 (4), C3H7 (14), C2H4OH (15), C2H4ONO2 (16), C2H4CN (17), CH2COOСH3 (18), CH2C(NO2)2СH3 (19) и CH2C(NO2)3 (20), изучали в 1-10 % (масс.) растворах ДНБ, ТНБ и ДБФ, где концентрация вещества и диэлектрическая проницаемость растворителя не влияли на константу скорости. До глубины превращения 40-50 % реакция описывается уравнением первого порядка. Большинство результатов было получено в растворе ДНБ. Параметры уравнения Аррениуса представлены в табл. 3.6.
(10), R1= СH3, R2= СH3 (11), NO2 (12), Cl (13), а также R2= NO2, R1= СH3 (12), C2H5 (4), C3H7 (14), C2H4OH (15), C2H4ONO2 (16), C2H4CN (17), CH2COOСH3 (18), CH2C(NO2)2СH3 (19) и CH2C(NO2)3 (20), изучали в 1-10 % (масс.) растворах ДНБ, ТНБ и ДБФ, где концентрация вещества и диэлектрическая проницаемость растворителя не влияли на константу скорости. До глубины превращения 40-50 % реакция описывается уравнением первого порядка. Большинство результатов было получено в растворе ДНБ. Параметры уравнения Аррениуса представлены в табл. 3.6.Таблица 3.6
Кинетические параметры термораспада соединений XXIV
| Шифр | Температурный интервал, С | Еа, кДж/моль | lg A | k150 105, с-1 | S150C, Дж/мольК | Es | * |
| XXIV.1 | 180-215 | 170,0 | 14,81 | 0,068 | 27,4 | 1,56 | |
| XXIV.2 | 165-200 | 183,8 | 16,71 | 0,107 | 63,8 | 0 | |
| XXIV.3 | 180-200 | 173,8 | 15,87 | 0,27 | 47,7 | -0,58 | |
| XXIV.4 | 140-165 | 166,6 | 16,28 | 5,23 | 55,5 | -2,14 | -0,10 |
| XXIV.5 | 140-160 | 160,4 | 15,93 | 13,96 | 48,8 | -2,81 | |
| XXIV.6 | 140-160 | 157,8 | 15,62 | 21,1 | 42,9 | -3,22 | |
| XXIV.7 | 135-155 | 154,1 | 15,65 | 43,8 | 43,5 | -3,44 | |
| XXIV.8 | 140-160 | 155,0 | 15,78 | 43,9 | 11,0 | -3,50 | |
| XXIV.9 | 105-130 | 149,9 | 15,20 | 50,5 | 34,9 | -3,62 | |
| XXIV.10 | 100-125 | 150,3 | 15,79 | 175,1 | 46,2 | -4,25 | |
| XXIV.11 | 175-190 | 166,2 | 14,58 | 0,117 | 23,0 | 0 | |
| XXIV.12 | 130-165 | 168,7 | 16,53 | 5,13 | 60,3 | -2,14 | 0 |
| XXIV.13 | 140-160 | 152,0 | 14,83 | 11,9 | 27,7 | -2,81 | |
| XXIV.14 | 145-165 | 166,4 | 16,26 | 5,2 | 49,9 | | -0,12 |
| XXIV.15 | 135-165 | 161,3 | 15,78 | 7,3 | 45,0 | | 0,20 |
| XXIV.16 | 145-165 | 165,9 | 16,42 | 8,7 | 58,3 | | 0,48 |
| XXIV.17 | 140-160 | 163,7 | 16,21 | 10,0 | 54,3 | | 0,50 |
| XXIV.18 | 145-165 | 159,9 | 15,89 | 14,1 | 48,1 | | 0,71 |
| XXIV.19 | 140-160 | 156,0 | 15,63 | 23,4 | 43,2 | | 1,16 |
| XXIV.20 | 130-150 | 154,0 | 15,74 | 52,3 | 45,3 | | 1,79 |
lg k150C = (0,7420,016)Es (5,9530,047) r=0,998; Sy=0,067; n=12 (56)
lg k150C = (0,5360,018)* (4,2550,014) r=0,996; Sy=0,091; n=9 (57)
Ea = (181,76 ±0,35) + (7,96 ±0,14)Es r=0,953; Sy=4,68; n=11 (58)
Для соединений XXIV при постоянстве структурных факторов у тринитрометильной группы (соединения XXIV.4, XXIV.12, XXIV.(14-20), уравнение (57)) наблюдается корреляция между константой скорости и * Тафта .
Соединения XXIV, имеющие два реакционных центра, судя по активационным параметрам, могут разлагаться гомолитически по двум механизмам, с первичным разрывом C-NO2 или N-NO2 связи. Влияние структурных факторов [табл. 3.6, уравнения (56), (58)], за исключением соединения XXIV.1, указывают на первичный гомолиз по связи C-NO2. Для подтверждения этого на примере соединения XXIV.11 проведено масс-спектрометрическое изучение продуктов распада с привлечением масс-спектров веществ-свидетелей.
В интервале температур 165-200С термораспад соединений XXIV.2-XXIV.3 и XXIV.11 протекает, по крайней мере, по двум параллельным реакциям гомолитического разрыва связей C-NO2 и N-NO2. Из-за близости констант скорости термораспада соединений XXIV.2-XXIV.3 и XXIV.1 (табл. 3.7) можно сделать такое же допущение и в отношении соединения XXIV.1. Термическое разложение соединений XXIV.4-XXIV.10 и XXIV.12-XXIV.20 предпочтительно протекает с первичным разрывом связи C-NO2, на прочность которой влияют стерические и электронные эффекты заместителей (уравнения 56-58).
Нами установлена единая корреляционная зависимость для всех изученных динитросоединений общей формулы R1C(NO2)2R2 между суммой стерических констант заместителей Es и константой скорости (энергией активации) термораспада:
lg k100C = - (0,773±0,016) Es - (9,245±0,088) (59)
r=0,992; Sy=1,410; n=36 (XVII.1-5, XVIII, XIX.3-8, XX.1-4, XXI.1-3, XXII.1-5, XXIV.2-13)
Ea = (6,72±0,31) Es + (179,86±1,67) (60)
r=0,964; Sy=26,963; n=36 (XVII.1-5, XVIII, XIX.3-8, XX.1-4, XXI.1-3, XXII.1-5, XXIV.2-13)
Уравнения (59)-(60) для соединений общей формулы R1-C(NO2)2-R2 позволяют выбрать вещества для производства и применения, а также прогнозировать синтез соединений с заданными параметрами по термостабильности.
