Автори: Богатирьова О. В., Бакурова О. М., Скоробогатова З. М., Соколовська Л. В., Турсунова Ю. Д., Хомутов Є. В., Швець Т. А
| Вид материала | Документы |
- Хомутов Геннадий Федорович член Союза писателей России; руководитель областного литературного, 493kb.
- В. Г. Швець, д-р екон наук, проф, 4046.01kb.
- Практикум з української мови: 10-11 класи (автори Л. Скуратівський, Г. Шелехова,, 49.77kb.
- Дипломант Всероссийского конкурса «Школа года» 1997,1998,1999, 631.22kb.
- 3 Исследование биосинтеза и катаболизма пуриновых нуклеоти- дов. Определение конечных, 1840.77kb.
- Акустико-эмиссионный комплекс неразрушающего контроля тяговых хомутов и корпусов автосцепного, 15.3kb.
- Скоробогатова Татьяна Николаевна Вишневое, 2010 Цель урок, 93.69kb.
- Скоробогатова Татьяна Николаевна Вишневое, 2010 Цель урок, 98.24kb.
- Скоробогатова Татьяна Николаева С. Вишневое 2008 пояснительная записка, 106.96kb.
- Реферат, 198.16kb.
ТЕМА 2.1. ДОСЛІДЖЕННЯ БІОСИНТЕЗУ ТА КАТАБОЛІЗМУ ПУРИНОВИХ НУКЛЕОТИДІВ. ВИЗНАЧЕННЯ КІНЦЕВИХ ПРОДУКТІВ ЇХНЬОГО ОБМІНУ
Актуальність теми
В організмі обмін нуклеотидів тісно пов'язаний з їхніми важливими біологічними функціями. Навіть якщо їжа багата нуклеопротеїнами, клітини людини однаково синтезують попередники нуклеїнових кислот з амфіболічних проміжних речовин. Пурини та піримідини їжі в мінімальній кількості можуть використовуватись для синтезу тканинних нуклеїнових кислот. Більшість їх під дією нуклеозидфосфорилаз розщеплюються до фосфопентоз та азотних основ. Більшість пуринових основ розщеплюється до сечової кислоти, піримідинові основи також підлягають розпаду до кінцевих продуктів – NH3, CO2, β-амінокислот.
Фізіологічні потреби організму в цих сполуках задовольняються переважно за рахунок основного синтезу із простих попередників – синтезу de novo. В той же час втрата регуляторних механізмів цього шляху, або інтенсифікація іншого, більш швидкого механізму синтезу нуклеотидів шляхом повторного включення в метаболізм вільних азотистих основ (шлях реутилізації), відіграють вирішальну роль під час пухлинної трансформації, при системних захворюваннях сполучної тканини. Для патогенезу інших станів, навпаки, характерними є порушення реутилізації нуклеотидів, що призводить до виникнення подагри, синдрому Леша-Ніхана. В той же час шляхи обміну нуклеотидів є мішенями для хіміотерапевтичних препаратів, які використовуються для лікування пухлинних процесів, а також для препаратів, що пригнічують утворення токсичної кількості метаболітів нуклеотидного обміну. Наприклад, структурний аналог гіпоксантину алопуринол використовують для корекції гіперурікемії. Таким чином, метаболічні перетворення нуклеотидів можуть підпадати під фармакологічну корекцію при цілому ряді патологічних станів.
Тепер ознайомтеся із цілями заняття.
Загальна мета
Уміти оцінювати стан пуринового обміну й інтерпретувати його можливі порушення на основі кількісного визначення сечової кислоти в крові й сечі для наступної правильної діагностики на клінічних кафедрах .
Конкретні цілі: Мети вихідного рівня:
Уміти:
| 1.Інтерпретувати процеси синтезу пуринових нуклеотидів, їхню регуляцію. | 1.Інтерпретувати структуру пуринових азотистих підстав (каф. медичної й фарм. хімії). |
| 2.Інтерпретувати процеси розпаду пуринових нуклеотидів | |
| 3. Пояснити порушення пуринового обміну на молекулярному рівні. | 3.Аналізувати структуру й розчинність сечової кислоти і її солей (каф. медичної й фарм. хімії). |
| 4. Інтерпретувати механізм дії аллопуринола й інгібіторів синтезу пуринових нуклеотидів. | |
| 5. Використовувати дані визначення сечової кислоти в сечі й крові для діагностики порушень пуринового обміну. | |
Для перевірки вихідного рівня Вам пропонується виконати ряд завдань
Завдання для самоперевірки й самоконтролю вихідного рівня з.
Завдання 1. У лабораторії проведений кислотний гідроліз нуклеинових кислот із дріжджів. Які з даних з'єднань могли бути виявлені серед продуктів цієї реакції при розщепленні РНК?
А. Глюкоза
В. Урацил
С. Тимин
Д. Дезоксирибоза
Е. Сечова кислота
Завдання 2. Після проведення повного гідролізу АТФ у гидролизате було за допомогою срібної проби відкрита пуринова підстава. Назвіть його.
А. 2,6 -диоксипурин
В. 6-оксипурин
С. 2, 4-диоксипиримидин
Д. 6- аминопурин
Е. 4- оксипурин
Завдання 3. До амонійної солі сечової кислоти додали трохи краплі розчину Нсl. Спостерігалося часткове розчинення осаду й наступне утворення кристалів. Які властивості сечової кислоти доводить дана проба?
А. Здатність зв'язуватися із НСl
В. Погану розчинність у кислому середовищі
С. Гарну розчинність у кислому середовищі
Д. Здатність утворювати солі
Е. Виражені кислотні властивості
Завдання 4. При дослідженні мочекислих каменів, витягнутих із нірки хворого, були виявлені нерозчинні кристали, які добре розчинялися при додаванні Nаон. Яка речовина виявлена в складі каменів?
А. Двузамещенная калієва сіль
В. Двузамещенная натрієва сіль
С. Однозаміщена натрієва сіль
Д. Однозаміщена літієва сіль
Е. Двузамещенная літієва сіль.
Правильність рішення перевірте, зіставивши їх з еталонами відповідей.
Еталони відповідей до рішення завдань для самоперевірки й самоконтролю вихідного рівня знань-умінь:
1. - В; 2, -Е; 3.- В.;. 4 - З
Інформацію для заповнення вихідних знань-умінь можна знайти в наступній літературі.
1. Тюкавкина Н.А.,Бауков Ю.И. Біоорганічна хімія. -М.: “Медицина”, 1991. - С. 296-298, 301-304.
2.А.Я.Рево, В.В.Зеленкова «Малий практикум по органічній хімії».-«Висш. школа»,1980, С. 154-156.
- Лекції по біоорганічній хімії.
Зміст навчання.
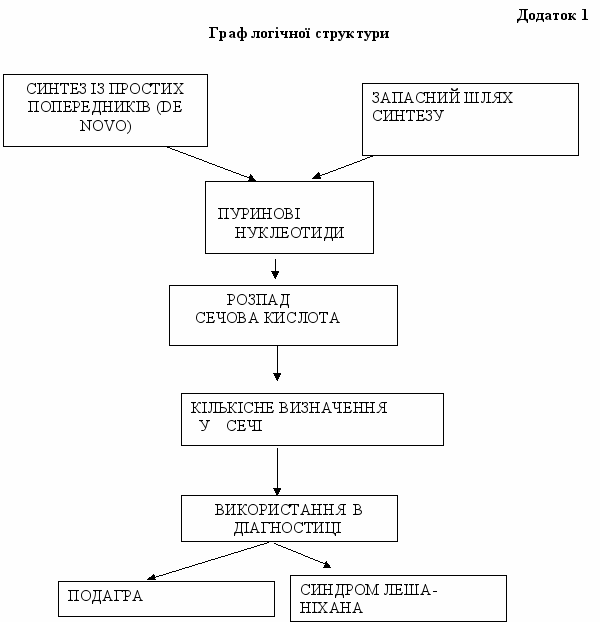
Зміст навчання повинне забезпечувати досягнення цілей навчання, чому сприяє граф логічної структури досліджуваної теми (Додаток 1).
Основні теоретичні питання, що дозволяють виконати цільові види діяльності:
1. Біохімічні функції нуклеотидів. Компоненти нуклеотидів та нуклеозидів. Вільні нуклеотиди та їх біохімічні функції: участь в метаболічних реакціях (АТФ, НАД, НАДФ, ФАД, ФМН, ЦТФ, УТФ).
2. Біосинтез пуринових нуклеотидів; cхема реакцій синтезу ІМФ; утворення АМФ, ГМФ, АТФ, ГТФ. Регуляція біосинтезу пуринових нуклеотидів за принципом негативного зворотного зв’язку (ретроінгібірування).
3. Біосинтез дезоксирибонуклеотидів. Утворення тимідилових нуклеотидів; інгібітори біосинтезу дТМФ як протипухлинні засоби (структурні аналоги дТМФ, похідні птерину)
4. Катаболізм пуринових нуклеотидів; cпадкові порушення обміну сечової кислоти. Клініко-біохімічна характеристика гіперурикемії, подагри, синдрому Леша-Ніхана.
5.. Біохімічні аспекти використання інгібітору ксантиноксидази- аллопуринола.
6. Клініко-діагностична цінність визначення сечової кислоти в біологічних рідинах (крові й сечі).
7. Принцип методу й хід роботи з визначення сечової кислоти в сечі.
Знайти матеріал для освоєння цих питань можна в одному з наступних джерел:
Обов'язкова література.
- Вороніна Л.М., Десенко В.Ф., Мадієвська Н.М., Кравченко В.М., Сахарова Т.С., Савченко Л.Г., Шоно Н.А. Біологічна хімія: Підручник. – Харьків: Основа; Вид-во НФАУ, 2000. – 81 -94 с.
- Губський Ю.Г. Біологічна хімія.- Київ-Тернопіль.:Укрмедкнига, 2000.-С. 270-275, 281- 282.
- Тестовые задания по биологической химии/ Под ред. Б. Г. Борзенко.-Донецк,2002.-С. 111-117
4. Лекції з біохімії
5. Граф логічної структури
6. Инструкції до практичних занять
Додаткова література
- Марри Р., Греннер Д., Мейес П., Родуэлл В. Біохімія людини.- М.: “Мир”, 1993. Т.II.-С. 15-34.
- Ленинджер А. “Основи біохімії”. - М.: Мир, 1985.-С. 665-668, 672-674
- Маршалл В. Дж. Клінічна біохімія.- М.- З-П.: “Видавництво Біном-Невський Діалект”, 1999. -368 с.
- Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1998.-С. 470-474,
500-501.
- Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1990.-С. 369-373,
390- 392.
- Миколаїв А.Я. Біохімія. -М.:” Гэотар-Мед”, 2001.-С. 258-261.
- Пустовалова Л.М. Практикум по біохімії.- Ростову-на-Дону.: “Фенікс”, 1999.-С. 215-219.
Після вивчення переліченних вище питань для самоперевірки засвоєння матеріалу по даній темі пропонується вирішити наступні цільові навчальні завдання.
Цільові навчальні завдання
Завдання 1. Вивчення регуляції синтезу пуринових нуклеотидів в експерименті показало, що надлишок АМФ і ГМФ гальмує синтез ІМФ - попередника цих нуклеотидів, за рахунок інгібування одного з ферментів. Назвіть цей фермент.
А. ІМФ-циклогідролаза
В. Гліцинамідосинтетаза
- С. ФРПФ-амідотрансфераза
D. Аденілосукциназа
- E. Формілтрансфераза
Завдання 2. Для симптоматичного лікування подагри хворому призначено алопуринол, синтетичний аналог гіпоксантину. Це призвело до зростання екскреції гіпоксантина з сечею. Який фермент інгібується цим препаратом?
А. Аденозиндезаміназа
В. Ксантиноксидаза
С. Нуклеозидфосфорилаза
D. Карбамоїлфосфатсинтетаза
Е. Аденінфосфорибозилтрансфераза
Завдання 3. У хлопчика спадкова форма гіперурикемії (синдром Леша-Ніхана). З дефектом якого ферменту пов'язана ця хвороба?
А. Гіпоксантин-гуанін-фосфорибозилтрансферази
В. Ксантиноксидази
С. Аденозиндезаминази
Д. Карбамоїлфосфатсинтетази
Е. Тимідилатсинтази
Завдання 4. Для симптоматичного лікування подагри хворому призначений препарат алопуринол, синтетичний аналог гіпоксантину, що призвело до зростання екскреції останнього із сечею. Який фермент інгібується цим препаратом?
А. Аденозиндезаміназа
В. Ксантиноксидаза
С. Нуклеозидфосфорилаза
Д. Карбамоїлфосфатсинтетаза
Е. Аденінфосфорибозилтрансфераза
Завдання 5. У клініку надійшов чоловік 48 років з гострим приступом подагри. Вміст сечової кислоти в сироватці крові хворого 0,68 ммоль/л, у сечі добова кількість сечової кислоти підвищена. Часткова втрата активності якого ферменту призводить до даної патології?
А. Ксантиноксидази
В. Фосфорибозиламідотрансферази
С. Гуанинфосфорибозилтрансферази
Д. Аденозиндезамінази
Е. Тимідинкінази
Завдання 6. У хворого з довготривалим захворюванням печінки вміст сечової кислоти в плазмі крові складає 0,08 ммоль/л, в сечі значно збільшена кількість гіпоксантину та ксантину. До недостатності якого ферменту призвела патологія печінки?
А. Аденозиндезамінази
В. Ксантиноксидази
С. ФРПФ-синтетази
D. Тимідинфосфорилази
Е. Дигідропіримідинази
Завдання 7. На прийом до терапевта прийшов чоловік 37 років зі скаргами на періодичні інтенсивні больові приступи у суглобах великого пальця стопи та їхню припухлість. На підвищення концентрації якої речовини в сечі слід чекати ?
A. Сечової кислоти
B. Хлоридів
C. Солей амонію
D. Фосфату кальцію
E. Сульфату магнію
Правильність рішення завдань перевірте, зіставивши їх з еталонами відповідей.
Еталони відповідей до рішення цільових навчальних завдань.
1.- C; 2. - В; 3.- А; 4. - В; 5.- С.
Короткі методичні рекомендації до проведення заняття
На занятті проводиться тестовий контроль вихідного рівня знань студентів і його корекція. Перевіряється виконання домашнього завдання. Потім студенти приступають до виконання лабораторної роботи, використовуючи при цьому інструкцію.
Після виконання лабораторної роботи необхідно оформити протокол, зробити висновки до роботи, які перевіряє й контролює викладач.
Інструкція до практичного заняття «Кількісне визначення сечової кислоти в сечі»
Принцип методу. Метод заснований на здатності сечової кислоти відновлювати фосфорно-вольфрамовий реактив у фосфорно-вольфрамову синю, інтенсивність фарбування якої пропорційна змісту сечової кислоти. Кількість фосфорно-вольфрамової синьої визначається шляхом титрування червоною кров'яною сіллю К3 [Fе(СN)6]. Остання окисляє фосфорно-вольфрамову синю й синє фарбування зникає.
Матеріальне забезпечення: сеча, розчин карбонату натрію, фосфорно–вольфрамовийо реактиву Фолина, розчин К3 [Fе(СN)6], хімічні склянки, бюретка.
Хід роботи. ДО 1,5 мол сили додають 1 мол 20% розчину карбонату натрію й 1 мол фосфорно-вольфрамового реактиву Фолина, перемішують і титрують 0,01 н розчином
ДО3 [Fе(СN)6] до зникнення синього фарбування. Паралельно проводять такий же досвід зі стандартним розчином сечової кислоти.
Розрахунок: Зміст сечової кислоти (у мг) у добовій сечі обчислюють по формулі:
А х В
Х = 0,75--------- мг/сут; Х =
Ао х 1,5
де:
А-Кількість мл червоної кров'яної солі,витрачене на титрування досліджуваної сили,
Ао-Кількість мл червоної кров'яної солі, пошедшее на титрування стандартного розчину сечової кислоти,
0,75 - кількість мол сечової кислоти в стандартному розчині в мг,
У - обсяг добової сили в мол (1500мол).
Для перерахування результатів у системі “СИ” (ммоль/сут.) результат потрібно помножити на коефіцієнт 0,0059.
Норма змісту сечової кислоти в сечі 1, 6-3,5 ммоль/сут або 276-600 мг/сут.
Клініко-діагностичне значення. Гіпоурикурія (зменшення виділення сечової
кислоти із сечею) відзначається при подагрі, нефриті, нирковій недостатності; гиперурикурія (збільшення виділення сечової кислоти із сечею) - при лейкемії, посиленому розпаді нуклеопротеїнів. У дітей виділяється дещо більше сечової кислоти, ніж у дорослих. Виділення сечової кислоти залежить від змісту пуринів у їжі й інтенсивності обміну нуклеопротеїнів. При подагрі солі сечової кислоти (урати) відкладаються в хрящах, м'язах і слизистої сумці суглобів. Зміст сечової кислоти в крові може бути підвищене, а в сечі знижене.
ВИСНОВКИ:
Підпис викладача.
ТЕМА 2.2. ДОСЛІДЖЕННЯ МЕТАБОЛІЗМУ ПІРИМІДИНОВИХ НУКЛЕОТИДОВ. ДОСЛІДЖЕННЯ СКЛАДУ НУКЛЕЇНОВИХ КИСЛОТ
Актуальність теми
Нуклеотіди є мономірами ДНК і РНК. Саме піримідинові нуклеотиди та модифікована пентоза надають структурній специфічності ДНК. Проліферуючі клітини для реплікації генома потребують дезоксинуклеозидтрифосфати як субстрати для синтезу ДНК. Відновлення рибози в дезоксирибозу відбувається тільки у складі нуклеозиддифосфатів, причому, безпосереднім відновником є білок тіоредоксин Для синтезу тимідинмонофосфату, що є обличчям ДНК, необхідно ввести в дезоксиуридинмонофосфат (дУМФ) метильну групу (-СНЗ). Її донором є N5, N10 -метилен-ТГФК (активна форма вітаміну росту; в утворенні цього радикалу також бере участь вітамін В12). Швидкість синтезу піримідинових нуклеотидів є об'єктом тонкої регуляції, що може порушуватися при різних захворюваннях. Пухлинам є притаманною висока інтенсивність синтезу нуклеотидів за „запасним” шляхом. Вважається, що рівень дТТФ лімітує швидкість синтезу ДНК, тому його синтез є мішенню протипухлинної терапії. Структурні аналоги фолієвої кислоти – аміноптерину та метотрексат - інгібітори дигідрофолатредуктази, отже теж зупиняють утворення дТМФ. Препарати застосовуються у хіміотерапії пухлин.
Тепер ознайомтеся із цілями заняття
Загальна мета
Вміти оцінювати механізм синтезу піримідинових нуклеотидів і нуклеїновых кислот для розуміння патогенезу спадкоємної оротацидурії та механізму дії хіміотерапевтичних препаратів при онкологічних захворюваннях.
Конкретні цілі: Цілі вихідного рівня:
Уміти:
| 1. Інтерпретувати процеси синтезу піримідинових нуклеотидів, їхню регуляцію | 1. Інтерпретувати структуру піримідинових азотистих сполук (каф. медичної та фарм. хімії) |
| 2. Інтерпретувати процеси розпаду піримідинових нуклеотидів та їхню регуляцію | 2. Інтерпретувати структуру нуклеїнових кислот (каф. медичної та фарм. хімії) |
| 3. Пояснити порушення піримідинового обміну на молекулярному рівні | |
| 4. Інтерпретувати механізм дії противопухлинних препаратів - інгібіторів синтезу нуклеотидів | |
Для перевірки вихідного рівня Вас пропонується виконати ряд завдань
Завдання 1. У гидролизате дріжджів було відкрито пиримидиновое підставу урацил. Яку структуру має гетероцикл, що входить у його сполуку? Напишіть його формулу.
А. 1,2 диазин
В. 1,3 диазин
С. 1,4 диазин.
Д. Піридин
Е. Бензол
Завдання 2. Після гідролізу речовини, що не мало відбудовну активність, утворилися рибоза й этанол, причому розчин придбав властивості, що відновлюють.
1. Яка сполука була піддана гідролізу?
А. Складний ефір.
В. Пептид
С. Гликозид
Д. Дисахарид
Е. Простий ефір
- Що являє собою це похідне моносахаридов?
А. Відновлена рибоза
В. Окислена рибоза
С. Простий ефір за рахунок полуацетального гідроксилу ( у першого атома З рибози)
Д. Простий ефір за рахунок ВІН- у п'ятого атома З
Е. Складний ефір з фосфорною кислотою.
Правильність рішення завдань перевірте, зіставивши їх з еталонами відповідей.
Еталони відповідей до рішення завдань для самоперевірки й самоконтролю вихідного рівня знань-умінь:
1.-В, 2.1 - Е., 2.2 - С..
Інформацію для заповнення вихідного рівня можна знайти в наступній літературі:
1. Тюкавкина Н.А.,Бауков Ю.И. Біоорганічна хімія. -М.: “Медицина”, 1991. - С. 297-298, 302-304.
2.А.Я.Рево, В.В.Зеленкова «Малий практикум по органічній хімії».-«Висш. школа»,1980, С. 154-156.
- Лекції по біоорганічній хімії.
Зміст навчання.
Зміст навчання повинне забезпечувати досягнення цілей навчання, чому сприяє граф логічної структури досліджуваної теми (Додаток 1).
Основні теоретичні питання, що дозволяють виконати цільові види діяльності:
1. Біосинтез піримідинових нуклеотидів: реакції; регуляція. Оротацидурія як порушення біосинтезу піримідинових нуклеотидів.
2. Розпад піримідинових нуклеотидів.
3. Біохімічні аспекти хіміотерапії ( 5-фторурацил, метотрексат, аминоптерин, меркаптопурин)
4. Структура, властивості та біологічні функції ДНК.
5. Структура, властивості та біологічні функції РНК. Типи РНК: мРНК, тРНК, рРНК; особливості структурної організацїї (вторинної а третинної) різних типів РНК.
6. Молекулярна організація ядерного хроматину та рибосом еукаріотичних клітин.
7. Принцип методу й хід роботи з визначення складених компонентів нуклеопротеидов.
Знайти матеріал для освоєння цих питань можна в одному з наступних джерел:
Обов'язкова література
- Вороніна Л.М., Десенко В.Ф., Мадієвська Н.М., Кравченко В.М., Сахарова Т.С., Савченко Л.Г., Шоно Н.А. Біологічна хімія: Підручник. – Харьків: Основа; Вид-во НФАУ, 2000. – 81 -94 с.
- Губський Ю.Г. Біологічна хімія.- Київ-Тернопіль.:”Укрмедкнига”, 2000.-С. 275-281, 282.
- Тестові завдання по біологічній хімії/ Під ред. Б. Г. Борзенко.-Донецьк,2002.-С. 111-117
- 3. Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1998.-С. 474-478,
501-503.
- Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1990.-С. 373-376,
393- 394.
6. Миколаїв А.Я. Біохімія. -М.:” Гэотар-Мед”, 2001.-С. 261-267.
7. Пустовалова Л.М. Практикум по біохімії.- Ростову-на-Дону.: “Фенікс”, 1999.-С. 215-
219.
8. Лекції по біохімії.
9. Граф логічної структури (Додаток 1).
10 .Інструкція до практичного заняття.
Додаткова література
1. Марри Р., Греннер Д., Мейес П., Родуэлл В. Біохімія людини.- М.: “Мир”, 1993. Т.II.-С.
15-34.
2.Ленинджер А. “Основи біохімії”. - М.: Мир, 1985.-С. 668-670.
3. Маршалл В. Дж. Клінічна біохімія.- М.- З-П.: “Видавництво Біном-Невський Діалект”, 1999. -368 с.
4. Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1998.-С. 474-478,
501-503.
5. Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1990.-С. 373-376,
393- 394.
6. Миколаїв А.Я. Біохімія. -М.:” Гэотар-Мед”, 2001.-С. 261-267.
7. Пустовалова Л.М. Практикум по біохімії.- Ростову-на-Дону.: “Фенікс”, 1999.-С. 215-219.
Після вивчення переліченних вище питань для самоперевірки засвоєння матеріалу по даній темі пропонується вирішити наступні цільові навчальні завдання.
Цільові навчальні завдання
Завдання 1. Онкологічному хворому був призначений 5-фторурацил. На гальмуванні якого процесу заснована його протипухлинна дія?
А. Синтезу пуринів
В. Утворення сечовини
С. Синтезу піримідинів
D. Розпаду глікогену
Е. Розпаду простих білків
Завдання 2. В онкологічного хворого після проходження курсу рентгенотерапії збільшилася екскреція аміноізобутирата із сечею. Прискорення якого процесу відображує цей тест?
А. Катаболізму пуринів.
В. Утворення сечовини
С. Катаболізму піримідинів
Д. Розпаду глікогену
Е. Розпаду простих білків
Завдання 3. При обстеженні дитини лабораторно підтверджена оротидинурія та оротовая ацидурія, мегалобластична анемія. При пероральному прийомі препарату уридину наступила ремісія. Для дефекту якого ферменту характерні зазначені ознаки хвороби?
А. ОМФ-декарбоксилази
В. Рибонуклеотидредуктази
С. Карбамоїлфосфатсинтетази
Д. ГТФ-синтетази
Е. Уридинфосфорилази
Завдання 4. Протипухлинний препарат. метотрексат шнгібує дігідрофолатредуктазу, зв’язуючись з її активним центром. Активність ферменту може бути відновлена збільшенням концентрації субстрату. Який тип інгібування спостерігається?
А. Конкурентне
В. Незворотне
С. Стереохімічне
Д. Алостеричне
Е. Неконкурентне
Завдання 5. Онкологічному хворому проводиться курс хіміотерапії лікарським препаратом метотрексатом - антивітаміном фолієвої кислоти, що блокує дигідрофолатредуктазу та таким чином порушує утворення ТГФК. Який етап синтезу ДНК клітин, що діляться, найбільш чутливий до інгібіторів цього ферменту?
А. Синтез пуринових нуклеотидів по”запасному” шляху
В. Синтез УМФ
С. Утворення ЦМФ із УМФ
Д. Утворення АМФ із ІМФ
Е. Утворення тимідилату з dУМФ
Правильність рішення завдань перевірте, зіставивши їх з еталонами відповідей.
Еталони відповідей до рішення цільових навчальних завдань.
1 - , 2 -С, 3 - А, 4 - А, 5 - Е.
Короткі методичні рекомендації до проведення заняття
На занятті проводиться тестовий контроль вихідного рівня знань студентів і його корекція. Перевіряється виконання домашнього завдання. Потім студенти приступають до виконання лабораторної роботи, використовуючи при цьому інструкцію.
Після виконання лабораторної роботи необхідно оформити протокол, зробити висновки до роботи, які перевіряє й контролює викладач.
Інструкція до практичного заняття
Гідроліз нуклеопротеинов. Якісні реакції на складові частини нуклеопротеинов
Принцип методу: у результаті процесу кислотного гідролізу дріжджів утвориться суміш складених компонентів складних білків - нуклеопротеинов: пентоз, фосфорної кислоти, азотистих підстав і білка.
Матеріальне забезпечення: гидролизат дріжджів, розчин сульфату міді, розчин гидроксида натрію, пробірки, штативи.
Хід роботи. Студенти одержують для роботи готовий гидролизат.
1. Биуретовая проба на білок.
Принцип методу: У лужному середовищі розчин білка при взаємодії з іонами міді здобуває синьо-фіолетове фарбування. Цією реакцією відкривають пептидную зв'язок у білках.
Матеріальне забезпечення: гидролизат дріжджів, розчин сульфату міді, розчин гидроксида натрію, пробірки, штативи.
Хід роботи: до 10 крапель гидролизата дріжджів додають 10 краплі 10% розчину лугу й 1 краплю 1% розчину сульфату міді (2+). Через 15 мінут з'являється фіолетове фарбування.
2. Реакція Молиша на пентози.
Принцип методу: При взаємодії концентрованої сірчаної кислоти з пентозами відбувається їхня дегідратація й утвориться фурфурол, що дає з тимолом продукти конденсації червоного кольору.
Матеріальне забезпечення: гидролизат дріжджів, спиртовий розчин тимолу, концентрована сірчана кислота, пробірки, штативи.
Хід роботи: ДО 10 крапель гидролизата додають 3 краплі спиртового розчину тимолу й по стінці пробірки обережно(!) додають 10 краплі концентрованої сірчаної кислоти. При струшуванні на дні пробірки утвориться продукт червоного кольору.
3. Реакція на рибозу й дезоксирибозу.
Принцип методу: Дифеніламін з дезоксирибозой дає синє фарбування, а з рибозой – зелене
Матеріальне забезпечення: гидролизат дріжджів, розчин дифеніламіну, пробірки, штативи, водяна лазня.
Хід роботи. ДО 5 крапель гидролизата дріжджів додають 20 краплі 1% розчину дифеніламіну й кип'ятять пробірку на водяній лазні 15 мінут. При цьому розчин офарблюється в синьо-зелений колір.
- Молібденова проба на фосфорну кислоту.
Матеріальне забезпечення: гидролизат дріжджів, молібденовий реактив, пробірки, штативи, водяна лазня.
Хід роботи: до 10 крапель гидролизата доливають 20 краплі молібденового реактиву й кип'ятять. Рідина офарблюється в лимонно-жовтий колір. Пробірку прохолоджують у холодній воді й на дні з'являється кристалічний лимонно-жовтий осад фосфорномолибденовокислого амонію.
ВИСНОВКИ:
Підпис викладача:
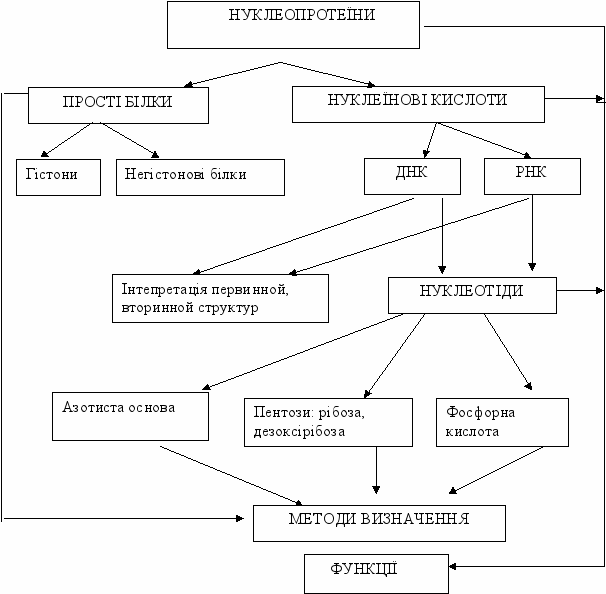
Додаток 1
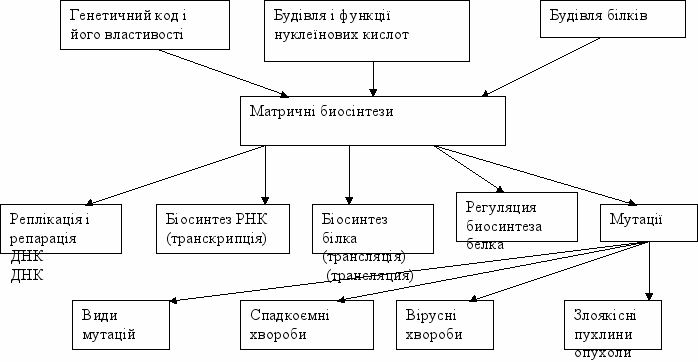
Граф логічної структури
ТЕМА 2.3. ДОСЛІДЖЕННЯ РЕПЛІКАЦІЇ ДНК І ТРАНСКРИПЦІЇ РНК. АНАЛІЗ МЕХАНІЗМІВ МУТАЦІЙ І РЕПАРАЦІЇ ДНК
Актуальність теми
У новому XXI віці перед біохімією стоять нові завдання, що мають не тільки науково-пізнавальне, але й практичне значення. Дотепер не розкриті в деталях механізми передачі генетичної інформації, закодованої в ДНК. Генетична інформація в ДНК реалізується шляхом програмованого через мРНК синтезу білків, котрі визначають фенотипічні ознаки живих організмів.
Регуляція експресії генів - це один з фундаментальних механізмів адаптації живих організмів до умов зовнішнього середовища. Всі живі організми на землі піддаються постійній дії мутагенних факторів, що супроводжується нестабільністю ДНК, пов'язаної з постійними точковими (генними) мутаціями. У процесі еволюції живих організмів виникли спеціальні молекулярні механізми, які протидіють постійним ушкодженням молекул ДНК і репарують зміни в її будові, які відбулися.
Біотехнологічні методи генної інженерії дозволяють у майбутньому створити нові медичні технології терапії спадкоємних захворювань практично невиліковних у наш час, а також синтез лікарських речовин: інтерферонів, гормонів, ферментів, імунобіологічних препаратів.
Студенту-фармацевту тема не тільки допомагає зрозуміти молекулярні основи та механізми фізіологічних та патологічних процессів, але й сприяє формуванню наукового світогляду.
Джерела інформації
Обов'язкова література
1. Вороніна Л.М., Десенко В.Ф., Мадієвська Н.М., Кравченко В.М., Сахарова Т.С., Савченко Л.Г., Шоно Н.А. Біологічна хімія: Підручник. – Харьків: Основа; Вид-во НФАУ, 2000. – 94 - 108с.
2. Губський Ю.Г. Біологічна хімія.- Київ-Тернопіль.:Укрмедкнига, 2000.-С. 284-299, 322-329.
3. Тестовые задания по биологической химии/ Под ред.Б.Г.Борзенко.-Донецк,2000.-С.206-222.
4. Лекції з біологічної хімії
5. Граф логічної структури
Додаткова література
1.Березов Т.Т., Коровкин Б.Ф. Биологическая химия.-М.: “Медицина”,1998.-С.478-493
2.Березов Т.Т., Коровкин Б.Ф. Биологическая химия.-М.: “Медицина”,1990.-С.81-91, 377-387
3. Николаев А.Я. Биологическая химия. -М.:Высшая школа, 1989.-С.92-115
4. Николаев А.Я. Биологическая химия. -М.:Высшая школа, 1998.-С.92-115
5. Маршалл В.Дж. Клиническая биохимия.- М.-С-П.: “Издательство БИНОМ-Невский Диалект”, 1999. -368 с.
6. Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека.- М.: “Мир”,1993.-384 с.
Цілі навчання
Загальна мета. Вміти інтерпретувати інформацію про біосинтез і функціонування нуклеїнових кислот для пояснення адаптації організму до умов, що змінюються, а також для рішення питань діагностики, лікування спадкоємних та онкозахворювань.
Конкретні цілі : Цілі вихідного рівня:
Уміти:
| 1. Інтерпретувати інформацію про потік генетичної інформації - експресії генів. | 1. Використовувати знання про комплементарність азотистих сполук для розуміння вторинної структури ДНК (каф. медичної та фармацевтичної хімії) |
| 2. Інтерпретувати інформацію про матричні синтези ДНК і РНК та їхньої регуляції | 2. Інтерпретувати первинну, вторинну структуру ДНК і всіх видів РНК (каф. медичної та фармацевтичної хімії) |
| 3. Застосовувати знання про молекулярні механізми спадковості та реалізації генетичної інформації для діагностики, лікування й профілактики спадкоємних та інших хвороб | 3. Аналізувати структуру речовин, що є антагоністами азотистих сполук і порушують синтез нуклеїнових кислот (каф. медичної та фармацевтичної хімії) |
Для перевірки вихідного рівня Вам пропонується виконати ряд завдань.
Завдання для самоперевірки й самокорекції вихідного рівня .
Завдання 1.При аналізі складу очищеної ДНК було виявлено, що кількість аденина й цитозина дорівнює
А. Кількості аденина й гуаніну
В. Кількості аденина й тимина
С. Кількості гуаніну й тимина
Д. Кількості гуаніну й цитозина
Е. Кількості тимина й цитозина
Завдання 2.При аналізі складу очищеної ДНК було виявлено, що кількість аденина й гуаніну дорівнює:
А.Кількості аденина й тимина
В. Кількості цитозина й тимина
С.Кількості гуаніну й тимина
Д.Кількості аденина й цитозина
Е.Кількості цитозина й гуаніну.
Завдання 3. Фрагмент одного ланцюга ДНК має наступну нуклеодидную послідовність - ААЦГТ. Яким образом виглядає комплементарний фрагмент іншого ланцюга ДНК ?
А. ГТГЦА
В. ТГГЦЦ
С. ААЦГТ
Д. ТТГАЦ
Е. ТТГЦА
Завдання 4.Фрагмент однієї з ланцюгів ДНК має наступну нуклеотидную послідовність ГЦАГТТ. Яким образом виглядає комплементарний фрагмент іншого ланцюга ДНК?
А. ГТЦАГЦ
В.ЦГТЦАА
С.ГГТЦАГ
Д. ТТТГАА
Е. ЦТТЦАА.
Завдання 5. При вивченні вторинної структури РНК було встановлено , що вона має форму «конюшинового листа».Що це за вид РНК?
А. мРНК
В.гяРНК
С. рРНК
Д. тРНК
Е.мя РНК
Завдання 6.При вивченні первинної структури РНК виявлені мінорні азотисті підстави: дигидроурацил, метилированние гуанозин і инозин. У який РНК вони втримуватися?
А. мРНК
В.гя РНК
С.рРНК
Д.ТРК
Е.мяРНК
Завдання 7. У якості противоопухолевого препарату хворому був призначений 5-фторурацил . У ролі антагоніста якої азотистої підстави він виступає?
А.Гипоксантина
В.Цитозина
С.Аденина
Д.Тимина
Е.Гуаніну
Завдання 8. У якості противоопухолевого препарату була запропонована речовина 6-меркаптопурин. У ролі антагоніста якої азотистої підстави він виступає?
А.Гипоксантина
В.Цитозина
С.Аденина
Д.Тимина
Е.Гуаніну.
Правильність рішення перевірте, зіставивши їх з еталонами відповідей.
Еталони відповідей до рішення завдань для самоперевірки й самоконтролю вихідного рівня :
1.- З; 3.- Е; 5.- Д; 7.- Д.
Інформацію для заповнення вихідного рівня можна знайти в наступних підручниках:
1. Тюкавкина Н.А., Бауков Ю.И. Біоорганічна хімія. М., “Медицина”, 1991. - С. 431-448.
2. Лекції по біоорганічній хімії.
Зміст навчання.
Зміст навчання повинне забезпечити досягнення цілей навчання, чому сприяє граф-логічної структури досліджуваної теми (Додаток 1).
Основні теоретичні питання, що дозволяють виконати цільові види діяльності:
1. Поняття про генетичну інформацію. Види її передачі.
2. Будову хроматину, ДНК, РНК
3. Біологічне значення реплікації ДНК. Сутність відкриття Дж.Уотсона та Ф.Кріка . Напівконсервативний механізм реплікації.
4. Загальна схема біосинтезу ДНК. Ферменти реплікації ДНК у прокаріотів та еукаріотів.
5. Біологічне значення та механізми репарації ДНК. Репарація УФ-індукованих генних мутацій; пігментна ксеродерма.
6. Загальна схема транскрипції; кодуючі та некодуючі ланцюги ДНК. РНК-полімерази прокаріотів та еукаріотів. Етапи та ферменти синтезу РНК. Сигнали транскрипції: промоторні, ініціаторні, термінаторні ділянки генома.
7. Процессинг - пострансляционная модифікація РНК
8. Поняття про генні мутації: заміщення (миссенс і нонсенс мутації), вставка, делеция, інверсія. Біохімічні механізми дії хімічних мутагенів - аналогів азотистих основ, дезамінуючих, алкілуючих агентів, ультрафіолетового та іонізуючого випромінювання.
9. Ампліфікація генів. Клонування генів з метою отримання біотехнологічних лікарських засобів та діагностикумів (гормонів, ферментів, антибіотиків, інтерферонів та ін.).
Знайти матеріал для освоєння цих питань можна в одному з наступних джерел.
Обов'язкова література
1. Вороніна Л.М., Десенко В.Ф., Мадієвська Н.М., Кравченко В.М., Сахарова Т.С., Савченко Л.Г., Шоно Н.А. Біологічна хімія: Підручник. – Харьків: Основа; Вид-во НФАУ, 2000. – 94 - 108с.
2. Губський Ю.Г. Біологічна хімія.- Київ-Тернопіль.:Укрмедкнига, 2000.-С. 284-299, 322-329.
3. Тестовые задания по биологической химии/ Под ред.Б.Г.Борзенко.-Донецк,2000.-С.206-222.
4. Лекції з біологічної хімії
5. Граф логічної структури
Додаткова література
1.Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1998.-С. 478-493. 2. 2. Березов Т.Т., Коровкин Б.Ф. Біологічна хімія.-М.: “Медицина”,1990.-С. 81-91, 377-387.
3. Миколаїв А.Я. Біологічна хімія. -М.:”Вища школа”, 1989.-С. 92-115.
4. Миколаїв А.Я. Біологічна хімія. -М.:”Вища школа”, 1998.-С. 92-115.
5. Маршалл В.Дж. Клінічна біохімія.- М.- З-П.: “Видавництво Біном-Невський Діалект”, 1999. -368 с.
6. Марри Р., Греннер Д., Мейес П., Родуэлл В. Біохімія людини.- М.: “Мир”,1993.-384 с.
Після вивчення переліченних вище питань для самоперевірки засвоєння матеріалу по досліджуваній темі пропонується вирішити наступні цільові навчальні завдання.
Цільові навчальні завдання
Завдання 1. В процесі транскрипції в ядрі клітини здійснюється біосинтез комплементарного РНК-транскрипту на матриці ДНК. Який фермент каталізує цей процес?
А. ДНК-залежна РНК-полімераза
В. ДНК-полімераза
С. ДНК-лігаза
Д. Праймаза.
Е. ДНКаза
Завдання 2. В організм людини потрапив онкогенний вірус. Яким образом здійснюється реплікація його генома?
А. РНК вірусу РНК
В. РНК вірусу ДНК РНК-вируса
С. РНК вірусу→білок
Д. ДНК вірусу→ДНК
Е. ДНК вірусу мРНК
Завдання 3. Пошкоджені ділянки ДНК, які мають димери тиміну, що утворені під час дії ультрафіолетового світла, відновлюються потім репарацією. Який процес при цьому відбувається?
А. Видалення пошкоджених нуклеотидів
В. Синтез фрагментів Оказакі
С. Утворення репликативної виделки
Д. Видалення праймеру
Е. Видалення інтронів
Завдання 4. Під дією УФ - випромінювання в одному з нуклеотидних ланцюгів ДНК утворився дімер тимідилової кислоти. Який із зазначених ферментів бере участь у реплікації ДНК й її репарації?
А. ДНК-залежна РНК-полімераза
В. Хеліказа
С. ДНК-полімераза Ш
Д. ДНК-полімераза 1
Е. Зворотна транскриптаза
Завдання 5. У результаті генної мутації почався синтез «модіфікованого» білка, кодує- мого ушкодженим геном зі зрушенням рамки зчитування. При яких мутаціях це відбувається?
А. Вставка тринуклеотида
В. Делеція тринуклеотидів
С. Вставка нуклеотида
Д. Випадання цистрона
Е. Інверсія
Завдання 6. Процес репарації ДНК починається з розщеплення ланцюга ДНК. Назвіть фермент даної реакції.
А. УФ-специфічна ендонуклеаза
В. ДНК-полімераза
С. ДНК-лігаза
Д. Кіназа
Е. Аміноацил-тРНК синтетаза
Завдання 7. Відомо, що процес реплікації на відстаючому ланцюгу здійснюється фрагментами. Як вони називаються.
А. Фрагменти Оказакі
В. Фрагменти Поля
С. Фрагменти Кребса
Д. Екзони
Е. Інтрони
Правильність рішення перевірте, зіставивши їх з еталонами відповідей.
Еталони відповідей до рішення цільових навчальних завдань.
1.- В, 2 – В; 3-А; 4- Д.
Короткі методичні рекомендації до проведення заняття
- На занятті проводиться тестовий контроль вихідного рівня знань і його корекція. Перевіряється виконання домашнього завдання. Потім студенти приступають до виконання самостійної роботи, використовуючи при цьому інструкцію.
- По закінченні самостійної роботи проводиться її аналіз і корекція.
- Наприкінці заняття проходить поточний тестовий контроль, підводяться підсумки заняття.
Додаток 1
Граф логічної структури