Автори: Богатирьова О. В., Бакурова О. М., Скоробогатова З. М., Соколовська Л. В., Турсунова Ю. Д., Хомутов Є. В., Швець Т. А
| Вид материала | Документы |
- Хомутов Геннадий Федорович член Союза писателей России; руководитель областного литературного, 493kb.
- В. Г. Швець, д-р екон наук, проф, 4046.01kb.
- Практикум з української мови: 10-11 класи (автори Л. Скуратівський, Г. Шелехова,, 49.77kb.
- Дипломант Всероссийского конкурса «Школа года» 1997,1998,1999, 631.22kb.
- 3 Исследование биосинтеза и катаболизма пуриновых нуклеоти- дов. Определение конечных, 1840.77kb.
- Акустико-эмиссионный комплекс неразрушающего контроля тяговых хомутов и корпусов автосцепного, 15.3kb.
- Скоробогатова Татьяна Николаевна Вишневое, 2010 Цель урок, 93.69kb.
- Скоробогатова Татьяна Николаевна Вишневое, 2010 Цель урок, 98.24kb.
- Скоробогатова Татьяна Николаева С. Вишневое 2008 пояснительная записка, 106.96kb.
- Реферат, 198.16kb.
Обов'язкова література
1.Вороніна Л.М., Десенко В.Ф., Мадієвська Н.М., Кравченко В.М., Сахарова Т.С., Савченко Л.Г., Шоно Н.А. Біологічна хімія: Підручник. – Харьків: Основа; Вид-во НФАУ, 2000. – 431 - 442с.
2.Губський Ю.Г. Біологічна хімія. - Київ-Тернопіль.: Укрмедкнига, 2000. - С. 411-417.
3. Тестовые задания по биологической химии/ Под ред.Б.Г.Борзенко. - Донецк, 2000. -С. 44-73.
4. Лекції з біохімії
5. Граф логічної структури (Додатки 1,2).
6. Інструкція до практичного заняття.
Додаткова література
1. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. - М.: Медицина, 1998.-С. 210-219 313-316
2. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. - М.: Медицина, 1990. - С. 138-147
3. Николаев А.Я. Биологическая химия. - М.: Высшая школа, 1998.- С. 161, 167-171, 386-388, 478-480.
4. Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека. - М.: Мир, 1993. - С.111-139
Після вивчення перерахованих вище питань для самоперевірки засвоєння матеріалу по досліджуваній темі пропонується вирішити наступні цільові навчальні завдання.
Цільові навчальні завдання.
Завдання 1.В експерименті встановлено, що окислювання субстрату в клітині відбувається по оксигеназному шляхи. Підберіть відповідну характеристику процесу:
А. Реакцію катализирует анаэробная дегидрогеназа
Б. Сприяє включенню кисню в субстрат
В. Супроводжується утворенням ендогенної води
М. Супроводжується синтезом АТФ
Д. Здійснюється в мітохондріях
Завдання 2. Одним з методів боротьби з гіпоксією є гипербарическая
оксигенация. При недотриманні режиму цієї процедури висока доза
кисню може викликати гостре отруєння, навіть із появою
“кисневих “ судорог. Активація якої реакції біологічного
окислювання особливо небезпечна для тканини мозку при тривалому вдиханні
кисню під тиском?
А. Пероксидазной
В. Оксигеназной
С. Оксидазной
Д. Свободнорадикального окислювання
Е. Микросомального окислювання
Завдання3 .Порушення функції товстого кишечника викликало у хворого пови-
шенное утворення токсичного бензолу. Який з нижеуказанних процес-
сов бере участь у його знешкодженні?
А. Вільно-радикальне окислювання
В. Микросомальное окислювання
С. Тихорєцький подих
D. Окисне фосфорилирование
Е. Окисне декарбоксилирование
Завдання 4 При обстеженні хворого з діагнозом пелагра виявлена
зниження утворення АТФ у міокарді. У чому причина розвитку гипоэнер-
гетического стану в пацієнта?
А. Інгібування монооксигеназних реакцій
В. Гіпоксія
С. Зменшення гемоглобіну
D. Порушення структури мітохондрій
Е. Інгібування піридинових дегидгогеназ
Завдання 5. Під дією твердого ультрофиолетового опромінення розвивається м'язова
дистрофія. Яка речовина може перешкоджати цьому порушенню?
А. ?-токоферол
В. 1, 25-диоксихолекальциферол
С. Ретинол
Д. Вітамін Д3
Е. Филлохтнон
Завдання 6 У рятувальника, що працює в радіаційному вогнищі, почалися некрозо-дистрофічні процеси в печінці. Що йому варто призначити в комплексі лікування?
А. Ретинол
В. Аскорбінову кислоту
С. Вітамін ДО
D. Лецитин
Е. (-токоферол
Завдання 7 Вітамін D регулює мінеральний обмін в організмі. Для засвоєння яких мінеральних елементів він необхідний?
А. Натрію
В. Калію
C. Кальцію
D. Заліза
Е. Кобальту
Завдання 8 Складний процес утворення в організмі кальцитриола проходять через кілька стадій. Для якої з них потрібне ультрафіолетове опромінення?
А. 7-дегидрохолестерин( холекальциферол
В. Холестерин ( холевая кислота
С. Холекальциферол ( 25-гидроксихолекальциферол
D. 25(ВІН)-Д3 1,25(ВІН)2 -Д3)
Е. Сквален ( ланостерин
Правильність рішення перевірте, зіставивши їх з еталонами відповідей.
Еталони відповідей до рішення цільових навчальних завдань:
2-Д; 3-В; 4-Е ; 5-А; 6 - Е
Завдання для самостійної роботи до заняття «Дослідження типів біологічного окислення»
- Заповнити таблицю «Типи реакцій біологічного окислення».
Тип реакції
Схема процесу
Ферменти
Біологічна роль
1
2
3
4
- Виписати в загальному виді рівняння реакцій катализируемих піридин- і флавінзалежними дегідрогеназами.
SH2 + НАД+→
SH2 + ФАД→
Привести активні структури в молекулах НАД+ і ФАД, які є акцепторами протонів і електронів у дегідрогеназних реакціях.
Короткі методичні рекомендації до проведення заняття.
На занятті проводиться тестовий контроль вихідного рівня знань студентів і його корекція. Перевіряється виконання домашнього завдання. Потім студенти приступають до виконання лабораторної роботи, використовуючи при цьому інструкцію.
Після виконання лабораторної роботи необхідно оформити протокол,зробити висновки до роботи, які перевіряє й контролює викладач.Проводиться підсумковий тестовий контроль по темі, підводять підсумки роботи.
Інструкція до практичного заняття «Дослідження типів біологічного окислювання».
РОБОТА №1: Відкриття альдегиддегидрогенази в молоці.
Принцип роботи: Фермент виробляється мікроорганізмами, що попадають у молоко ззовні. По хімічній природі він належить до флавопротеїнів, здатним окислювати альдегіди, зокрема формальдегід. При додаванні до некип'яченого молока формальдегіду метиленової сині альдегіддегидрогеназа окисляє формальдегід у мурашину кислоту, а вивільнюваний при цьому водень переноситься на метиленову синь, відновлює її в безбарвне з'єднання.
Матеріальне забезпечення: кип'ячене молоко, не кип'ячене молоко, 0,04% розчин формальдегіду, 0,01% розчин метиленової сині, пробірки, піпетки.
Хід роботи: В одну пробірку вносять 15 краплі кип'яченого молока, а в іншу – 15 краплі не кип'яченого. У кожну пробірку вносять по краплі 0,4% розчину формальдегіду й по краплі 0,01% розчину метиленової сині. Пробірки струшують і закривають пробками, щоб створити відносні анаэробние умови.
Пробірки поміщають у термостат при 37? З і відзначають через п'ять мінут поступове знебарвлення метиленової сині.
ВИСНОВКИ:
РОБОТА №2 Виявлення каталази крові
Принцип роботи: Фермент каталаза належить до класу оксидоредуктаз. Цей фермент утримується у всіх тканинах і рідинах організму, але особливо багато його в стромі еритроцитів і печінки. У процесі окислення деяких речовин утворюється перекис водню, отрутна для організму, що може в ньому накопичуватися.
Біологічна роль каталази полягає в розкладанні шкідливої для організму перекису водню на молекулярний кисень і воду:
2
 Н2О2 2Н2О + О2
Н2О2 2Н2О + О2каталаза
Фермент каталаза містить гем.
Матеріальне забезпечення: 3% розчин перекису водню, кров.
Хід роботи: У пробірку вносять 10-15 краплі 3% Н2О2 і 1 краплю крові. Відзначають виділення пухирців кисню.
Клінічно-діагностичне значення. Визначення активності каталази крові має значення для діагностики раку, анемії, туберкульозу.
Підпис викладача:
Додаток 1
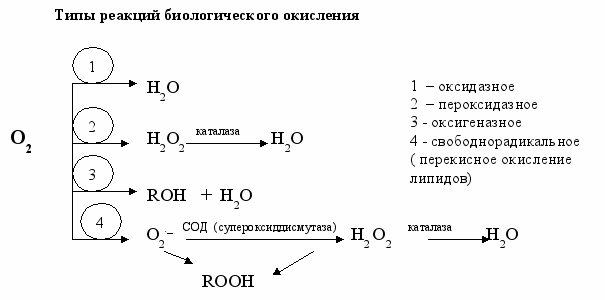
2. Процеси катаболізму в клітинах тварин супроводжуються споживанням кисню, що необхідний для реакцій окислення. Ферменти, катализирующие окислювально-відновні реакції, називаються оксидоредуктазами. Їх підрозділяють на 4 групи:
2.1. Дегидрогенази катализируют перенос водню від субстрату (S) на кофермент акцептор (А).
SН2 + А → S + АН2 є: дві основні групи дегидрогеназ, які розрізняються по використовуваних коферментах.
2.1.1. Піридинзавасимие дегидрогенази (кофермент НАД+ або НАДФ+). Никотинамид синтезується в організмі із триптофану або надходить із їжею (вітамін РР).
2.1.2. Флавиновие дегидрогенази (кофермент ФАД або ФМН). ФМН і ФАД утворяться в організмі з рибофлавіну (вітамін В2).
2.2. Оксидази - катализируют перенос електронів від S на молекулярний кисень
SН2 +1/2ПРО2 → S + Н2ПРО SН2 +ПРО2 → S + Н2ПРО2.
2.3. Оксигенази катализирует включення кисню в молекулу органічного субстрату. Їх підрозділяють на дві групи, залежно від :
-диоксигенази, кількість атомів кисню, що взаємодіє з S:
S + ПРО2→SО2
- монооксигенази: S -Н + ПРО2 + АН2 → SОН + А + Н2 ПРО
- гидропероксидази (пероксидази й каталази) катализируют руйнування перекису водню. 2Н2ПРО2 → 2Н2ПРО +ПРО2.
2.4 Свободнорадикальное окислювання
Окислювання субстратів вільними радикал-аніонами: супероксидом ПРО2· -, Н2О2, и наиболее активним радикалом – гидроксил анионом ОН·
Шляхи утворення вільних радикалів;
- Реакції відновлення кисню до Н2 О в дихальні ланцюги - основний: джерело вільних радикалів

- Деякі метаболические процеси ( микросомальное окислювання, розпад пуриеових нуклеотидов, фагоцитоз идр.)
Вільні радикали викликають утворення органічних гидропероксидов (ROOH) ДНК, білків і ліпідів. сления органических молекулоть в качестве переносчика олигосахаридныъ
Додаток 2.
Г р а ф логічної структури
окисление


Оксидазное
Оксигеназное
Пероксидазное
Свободно-радикальное окисление

Активные формы кислорода
Синтез макроэргических соединений, образование конечных продуктов СО2 и Н2О
Метаболизм экзо- и эндогенных соединений
Механізм антиоксидантного дії
ЖИРОРОЗЧИННИХ вітамінів
Обнаружение альдегиддегидрогеназы и каталазы крови
Клинико-диагностическое значение определения активности ферментов окислительных процессов
ЗАВДАННЯ ДЛЯ САМОПЕРЕВІРКИ ТА САМОКОРЕКЦІЇ ЗМІСТОВОГО МОДУЛЯ «БІОХІМІЯ ТА ПАТОБІОХІМІЯ КРОВІ І ПЕЧІНКИ»
Завдання 1
При мобілізації жиру з жирових депо в кров надійшла велику кількість жирних кислот. Якими білками плазми крові вони будуть транспортуватися?
А. Альбумінами
В. α1-глобулінами
С. α2-глобулінами
D. Бета -глобулінами
Е. Гама-глобулінами
Завдання 2
У пацієнта з печінковою недостатністю виявлене зниження показника залишкового азоту крові. За рахунок якого компонента відбулося зниження цього показника ?
А. Сечовини
В. Аміаку
С. Амінокислот
D. Білірубіну
Е. Сечової кислоти
Завдання 3
У пацієнта, що страждає захворюванням нирок, з'явилися набряки. Зміною вмісту яких білків плазми крові це спричинено?
А. Альбумінів
В. α1 -глобулінів
С. α2-глобулінів
D. Бета-глобулінів
Е. Гама-глобулінів
Завдання 4
У пацієнта, що страждає схильністю до тромбоутворення, досліджена антизгортальна система крові . Яка із речовин належить до цієї системи ?
А. Фактор П
В. Плазмін
С. Урокіназа
D. α2 –макроглобулин
Е. Стрептокіназа
Завдання 5
Перспективним вважається використання тканинного активатора плазміногена для відновлення прохідності коронарних артерій. З активацією якого процесу пов'язаний його терапевтичний ефект?
А. Антизгортальної системи
В. Фібринолізу
С. Утворенням брадикініну
D. Утворенням гепарину
Е. Утворенням білого тромбу
Завдання 6
У пацієнта, що страждає кровоточивістю, виявлена неможливість утворення стабільного фібринового згустку. З недостатністю якого фактора згортання крові це пов'язано ?
А. Фактора ХШ
В. Фактора ХП
С. Фактора ХI
D. Фактора V
Е. Протромбіну
Завдання 7
Відомо, що тромб протягом декількох днів після утворення розсмоктується. Якому ферменту належить головна роль у цьому процесі?
А. Урокіназі
В. Стрептокіназі
С. Плазміногену
D. Плазміну
Е. Гепарину
Завдання 8
Після отриманої травми на гомілці дитини з'явилася гематома, що із часом змінила свій колір з пурпурного на жовтий. Який процес обумовив таку зміну фарбування?
А. Зв'язування білірубіну з альбумінами
В. Утворення білірубіндиглюкуроніду
С. Перетворенням гему в білірубін
D. Утворенням мезобілірубіну
Е. Перетворенням гему в гемоглобін
Завдання 9
Отруєння грибами призвело до токсичного ушкодження паренхіматозних клітин печінки та появленню жовтяниці. Підвищення вмісту якої речовини в крові призвело до появи жовтяниці?
А. Гемоглобіну
В. Білівердину
С. Порфобіліногену
D. Протопорфірину 1Х
Е. Білірубіну
Завдання 10
У печінці пацієнта, що страждає залізодефіцитною анемією, виявлене порушення утворення залізовмісного білка, що є джерелом заліза для синтезу гему. Як називається цей білок?
А. Трансферин
В. Гемосидерин
С. Феритин
D. Міоглобін
Е. Цитохром
ПЕРЕЛІК ПИТАНЬ ДЛЯ ПІДСУМКОВОГО КОНТРОЛЯ МОДУЛЯ II
«МОЛЕКУЛЯРНА БІОЛОГІЯ. БІОХІМІЯ МІЖКЛІТИННИХ КОМУНІКАЦІЙ. БІОХІМІЯ ТА ПАТОБІОХІМІЯ КРОВІ І ПЕЧІНКИ »
1. Синтез пуринових нуклеотидів.
2. Катаболізм пуринових нуклеотидів та його можливі порушення.
3. Перетворення рибонуклеотидів на дезоксирибонуклеотиди.
4.Утворення тимідилових нуклеотидів. Інгібітори синтезу дТМФ як протипухлинні засоби.
5. Метаболізм пиримідинових нуклеотидів та його можливі порушення.
6. Структура та біологічна роль ДНК.
7. Структура та біологічна роль різних типів РНК.
8. Генетичний код і його властивості.
9. Біосинтез ДНК (реплікація).
10. Молекулярні механізми мутацій. Репарація ДНК.
11.Транскрипція РНК.
12. Основні етапи біосинтезу білків у рибосомах: ініціація, елонгація, термі нація.
13. Структура та роль транспортних РНК у біосинтезі білків. Активація амінокислот і їхнє приєднання до тРНК.
14. Посттрансляційні модифікації білків.
15. Загальна теорія регуляції синтезу білка (Ф.Жакоб, Ж. Моно).
16. Антибіотики як інгібітори синтезу білка. Механізм дії дифтерійного токсину на біосинтез білка.
17. Фізіологічні та біохімічні функції крові.
18. Біохімічний склад крові. Білки крові: загальна характеристика, роль, окремі представники.
19. Біохімічний склад крові. Небілкові складові плазми крові. Залишковий азот плазми крові. Поняття азотемії та причини її виникнення.
20. Біохімічний склад крові. Ферменти сироватки крові. Їхнє походження та значення для діагностики.
21. Кислотно-лужний стані буферні системи крові. Порушення кислотно-лужної рівноваги
22.Біохімія згортальної системи крові: компоненти, механізми активації та функціонування каскадної системи згортання крові. Роль вітаміну К в процесі згортання крові. Спадкові порушення процесу згортання крові.
23. Антизгортальна система крові. Антикоагулянти природного та синтетичного походження.
24. Фібринолітична система крові.
25. Дихальна функція еритроцитів. Гемоглобін: структура, біологічна роль. Молекулярні форми гемоглобінів.
26. Патологічні форми гемоглобінів. Гемоглобінози.
27. Синтез гемоглобіну. Роль і механізм процесу. Спадкові порушення обміну порфіринів:
еритропоетична та печінкова порфірії.
28. Катаболізм гемоглобіну та обмін жовчних пігментів.
29. Патобіохімія жовтяниць. Гемолітична, паренхіматозна, обтураційна жовтяниці. Ферментативні (спадкові) жовтяниці. Механізм дії фенобарбіталу для попередження жовтяниці новонароджених.
30. Роль печінки в обміні білків.
31. Роль печінки в обміні ліпідів. Ліпопротеїни, їхня біологічна роль.
32. Роль печінки в обміні вуглеводів.
33. Важливіші механізми детоксикації сполук у печінці: мікросомальне окиснення, реакції .кон’югації. Приклади детоксикації ксенобіотиків і продуктів гниття білків у товстій кишці.
34. Роль печінки у метаболізмі фармацевтичних препаратів.
35. Хімічний канцерогенез.
36. Нейромедіатори: структура, роль, дезактивація.
37. Ієрархія регуляторних систем. Роль гормонів в системі регуляції метаболізму та функцій організму.
38. Механізми обратного зв’язку в регуляції утворення та дії гормонів.
39. Класифікація гормонів згідно з хімічною структурою.
40. Механізми трансдукції гормональних сигналів до клітин-мішеней.
41. Гормони гіпоталамуса: структура та механізм дії. Біологічна роль ліберинів і статинів.
42. Гормони передньої, середньої та задньої часток гіпофізу. Механізм дії гормонів гіпофізу на метаболізм вуглеводів, ліпідів, білків. Гіпо- та гіперфункція гіпофізу.
43. Гормони щитоподібної залози. Біосинтез тироксину. Механізм дії йодтиронинів на вуглеводний, ліпідний, білковий, мінеральний та енергетичний обміни. Порушення метаболізму при гіпо- та гіперфункції щитоподібної залози.
44. Гормони підшлункової залози: інсулін і глюкагон. Їхній вплив на метаболізм. Біохімічні прояви порушень при цукровому діабеті та його ускладненнях.
45. Гормони надниркових залоз. Біосинтез адреналіну та норадреналіну. Регуляція метаболізму за участю гормонів мозкового шару надниркових залоз. Хімічна природа та біосинтез гормонів коркового шару надниркових залоз. Механізм дії глюкокортикоїдів на метаболізм. Біохімічні прояви гіпо- та гіперфункції кори надниркових залоз. Взаємозв’язок системи «гіпофіз – кора надниркових залоз».
46. Статеві гормони. Структура та біосинтез жіночих та чоловічих статевих гормонів, їхній вплив на репродуктивну функцію та метаболізм. Адреногенітальний синдром. Синтетичні статеві гормони, їхнє використання в клініці.
47. Регуляція водно-сольового обміну. Структура та механізм дії вазопресину та альдостерону. Ренін-ангіотензинова система. Порушення водно-сольового обміну.
48. Регуляція обміну кальція та фосфатів. Роль паратгормону, кальцитоніну та кальцитріолу в регуляції обміну кальція та фосфатів. Порушення обміну кальція та фосфатів.
49. Тканинні гормони. Синтез та вплив на метаболізм ейкозаноїдів.
50. Біохімічні методи діагностики ендокринних порушень. Використання гормонів і їхніх синтетичних аналогів при лікуванні ендокринних захворювань.
51. Жиророзчинні вітаміни A, D, E, K, F: функції в органімі, ознаки гіпо- та авітамінозів. Використання жиророзчинних вітамінів як лікарських засобів.
