Клинико-функциональные и иммунопатогенетические механизмы формирования усиления рефракции 14. 00. 36 аллергология и иммунология 14. 00. 08 глазные болезни
| Вид материала | Автореферат диссертации |
| Внедрение в практику Апробация работы Материалы и методы исследования. Полученные результаты и их обсуждение ИЛ-4/ ИНФ-γ |
- Клинико-функциональные результаты коррекции пресбиопии с использованием различных хирургических, 371.89kb.
- Клинико-лабораторная характеристика и лечение хламидийной инфекции, ассоциированной, 311.6kb.
- Клинико иммунологические особенности аллергодерматозов на фоне урогенитальной инфекции, 335.48kb.
- Изучение влияния постоянной слабомиопической дефокусировки изображения на динамику, 291.68kb.
- Образовательный стандарт послевузовской профессиональной подготовки специалистов Специальность:, 1035.98kb.
- Клинико-иммунологическая характеристика и иммунотерапия пневмонии у новорожденных,, 653.89kb.
- Диагностика и лечение аллергического ринита с сопутствующей патологией лор-органов, 740.73kb.
- Иммунные механизмы инвазивности эндометриальных клеток при эндометриозе 14. 00. 36., 247.97kb.
- Клинико-патогенетическое обоснование комбинированного лазерно-медикаментозного лечения, 270.48kb.
- Методы оценки и клиническое значение биомеханических свойств роговицы (клинико-экспериментальное, 429.56kb.
ВНЕДРЕНИЕ В ПРАКТИКУ
Результаты исследований используются в работе детского глазного отделения и детской поликлиники ГЛПУ ТО «ОКБ № 2» г. Тюмени, Тюменского областного офтальмологического диспансера, лечебного бюро ЗОА «Газпромоптика», а также в учебном процессе кафедры глазных болезней ГОУ ВПО «Тюменская государственная медицинская академия» Росздрава.
АПРОБАЦИЯ РАБОТЫ
По теме диссертации опубликовано 175 работы, из них 18 в рекомендуемых журналах ВАК. Основные положения работы доложены на следующих форумах: 3-й научно-практической конференции «Вопросы диагностики и лечения глазных заболеваний» (Новосибирск, 1995); межрегиональной научно-практической конференции «Медико-социальная реабилитация офтальмологических больных» (Тюмень, 1997); международном симпозиуме «Медицина и охрана здоровья-98» (Тюмень, 1998); межрегиональной научно-практической конференции «Медико-социальная реабилитация офтальмологических больных» (Тюмень, 1999); I всероссийской конференции «Актуальные проблемы эволюционной и популяционной физиологии человека» (Тюмень, 2001); X научно-практической конференции Екатеринбурского центра МНТК «Микрохирургия глаза» (Екатеринбург, 2002); международной конференции, посвященной 95-летию со дня рождения П.И. Мельникова «Криосфера земли как среда жизнеобеспечения» (Пущино, 2003); объединенном иммунологическом форуме (Екатеринбург, 2004); международной конференции «Криосфера нефтегазоносных провинций» (Тюмень, 2004); VIII Всероссийском научном форуме с международным участием им. Академика В.И. Иоффе «Молекулярные основы иммунорегуляции, иммунодиагностики и иммунотерапии» (Санкт-Петербург, 2004); научно-практической конференции «Избранные вопросы рефракционной офтальмологии. Оптический рынок в условиях ВТО: прогнозы и перспективы» (Тюмень, 2004); международной конференции «Приоритетные направления в изучении криосферы земли» (Пущино, 2005); VIII съезде офтальмологов России (Москва, 2005); научно-практической конференции «Роль гигиены зрения в профилактике формирования близорукости и ее прогрессирования» (Тюмень, 2005); научно-практической конференции, посвященной 25-летию Центральной научно-исследовательской лаборатории Челябинской государственной медицинской академии, «Новые лабораторные технологии в диагностике и лечении заболеваний человека» (Челябинск, 2006); международной конференции «Теория и практика оценки состояния криосферы земли и прогноз ее изменений» (Тюмень, 2006); международной конференции «Криогенные ресурсы полярных регионов» (Салехард, 2007); VIII конгрессе «Современные проблемы аллергологии, иммунологии и иммунофармакологии» (Москва, 2007); международной конференции «Рефракционные и глазодвигательные нарушения» (Москва, 2007); научно-практической конференции «Офтальмоиммунология: итоги и преспективы» (Москва, 2007); международной конференции «Криогенные ресурсы полярных и горных регионов. Состояние и перспективы инженерного мерзлотоведения» (Тюмень, 2008); II региональной научно-практической конференции «Галанинские чтения – 2008» (Исетское, 2008); научно-практической конференции «Учебный центр в реализации здоровьесберегающих технологий. Офтальмоиммунорефрактология» (Тюмень, 2008); региональной научно-практической конференции «Нижнетавдинский район: история и перспективы развития» (Нижняя Тавда, 2008).
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ.
Обследованы группы малочисленных народов Крайнего Севера (1013 чел.) и населения юга Тюменской области (1110 чел.), в том числе тюменских староверов Исетского района (146 человек). Установление у них ВИДС осуществлялось клинико-анамнестическим методом с выявлением частого рецидивирования вирусных и бактериальных воспалительных процессов.
Проводилась идентификация различных популяций и субпопуляций иммунокомпетентных клеток и их функциональной активности методами флюресцентной микроскопии и иммуногистохимии с использованием МАТ к дифференцировочными антигенам МНК (Хаитов Р.М. и др., 1995), производства НПЦ «Медбиоспектр» и лаборатории клинической радиоиммунологии НИИ клинической онкологии ВОНЦ РАМН г. Москва (Барышников А.Ю., 1990): CD3, -4, -8, -16, -22, -34, -38, HLA-DR, -25, -71, Ki 67, -95.
Оценивались фагоцитарная активность нейтрофилов методом фагоцитоза пекарских дрожжей (Фримель Г., 1987) через 30 и 90 мин от начала соприкосновения нейтрофилов с чужеродными частицами; функциональная активность моноцитов по методу восстановления нитротетразолиевого синего (NST), розеткообразования и фагоцитоза. Определялись концентрация сывороточных IgA, M, G методом радиальной иммунодиффузии в геле (Mancini G., Carbowara A.O., Hereman J.F., 1965); количество циркулирующих иммунных комплексов (ЦИК) методом преципитации раствором полиэтиленгликоля (ПЭГ) с концентрацией 3,5 % и 7,0 %; концентрация ИНФ-γ и ИЛ-4 твердофазным ИФА методом с использованием набора реагентов «PrCon IFgamma» (ООО «Протеиновый контур», С.-Петербург); определение сыворочных IgE, аутоиммунных антител (IgG) к нативной и денатурированной ДНК, IgG к ВПГ и ЦМВ ИФА методом с использованием набора реагентов «Вектор-Бест» (г. Новосибирск).
Демографические и генеалогические данные собирались с помощью анализа похозяйственных книг и статистических материалов, путем прямого и перекрестного опроса взрослых лиц. Изучение системы гистосовместимости включало иммуногенетическое типирование I и II класса антигенов HLA-системы с использованием антисыворотки из республиканского центра тканевого типирования (г. Санкт-Петербург). Группы крови АВО (А1, А2, В, О), MNSs (M, N, S, s), Rhesus (C, Cw, c, D, E, e), Duffy (Fy, Fy), P (P1), Kell (K, k) определяли в полевой лаборатории с помощью методов прямой и непрямой гемагглютинации, используя антисыворотки: anti-A, -B, -A1, -H, -M, -N, -S, -s, -K, -k, - P1, -C, - Cw, -c, -D, -E, -e, - Fy, -Fy («Biotest», Германия). Частота аллелей и гаплотипов рассчитывались по описанной методике (Осипова Л.П., Кашинская Ю.О., Посух О.Л. с соавт., 1997).
Для оценки экзогенного поступления питательных веществ в организм использовали дневник питания за 2 дня. Количество потребляемой пищи (грамм/сутки) оценивали с помощью «Альбома порций продуктов и блюд» (Мартинчик А.Н. с соавт., 1995). Для анализа химического состава пищевого рациона использовали программный пакет «Dietmast – ассистент диетолога», разработанный сотрудниками Тюменского филиала НИИ клинической иммунологии СО РАМН. Микроэлементы в сыворотке крови определялось атомно-эмиссионным спектральным анализом (Шелпаков И.Р., Гаранин В.Г., Лабусов В.А., 1999).
Оценивались параметры зрительного восприятия методами визометрии; визиоконтрастной периметрии; скиаскопии; авторефрактометрии; кератометрии; определения резервов аккомодации, положительной и отрицательной части и объема относительной аккомодации; общей электроретинографии; фосфена; термометрии глазного яблока в области проекции цилиарного тела; эхобиометрии глазного яблока и наружных прямых мышц; офтальмотонометрии, тонографии по А.П. Нестерову и эластотонометрии аппланационным тонометром Маклакова; биомикроскопии; офтальмоскопии.
Полученные данные обрабатывались на ПЭВМ IBM/РС при помощи стандартных статистических пакетов «SPSS 11,5 for Windows» (среднее значение, дисперсия средних, непараметрическое сравнение по критерию Стъюдента, коэффициента корреляций Спирмена с определением коэффициентов ранговой корреляции, частотный анализ, многофакторный регрессивный анализ).
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
При изучении распространенности ВИДС и близорукости в различных возрастных периодах было установлено, что между кривыми распространенности ВИДС и близорукости имеется определенный параллелизм (рис. 1).
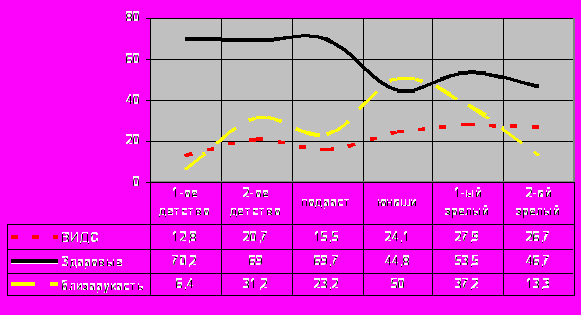 Рисунок 1. Характеристика распространенности ВИДС и близорукости по возрастам.
Рисунок 1. Характеристика распространенности ВИДС и близорукости по возрастам.Обращает внимание тот факт, что в период первого детства частота встречаемости ВИДС выше распространенности близорукости в 2 раза, а в последующих возрастных группах начинает преобладать близорукость. С периода 1-го детства до 1-ого периода зрелого возраста частота встречаемости ВИДС увеличивается в 2,2 раза, а близорукость – в 5,8 раз.
Установлена высокая частота встречаемости близорукости во всех обследуемых группах (рис. 2).
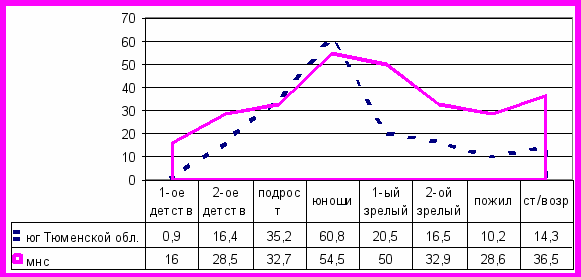 Рисунок 2. Сравнительная характеристика распространенности близорукости среди населения юга Тюменской области и малочисленных народов Крайнего Севера.
Рисунок 2. Сравнительная характеристика распространенности близорукости среди населения юга Тюменской области и малочисленных народов Крайнего Севера.Так в юношеском возрасте удельный вес близорукости достигает 60,8 + 3,8 %, а среди малочисленных народов Севера (МНС) – 54,5 + 4,5 %. Близорукость слабой степени у МНС юношеского возраста составила 29,8 + 4,1 %, средней – 13,2 + 3,1 %, высокой – 11,6 + 2,9 %. За годы обучения в школе отмечается рост частоты встречаемости близорукости в 3,4 раза. В том числе, количество лиц с близорукостью слабой степени увеличивается в 2,6 раз, средней – в 6,9 раз, высокой – в 4,1 раз. При этом в группе лиц без клинических признаков ВИДС («практически здоровые») между жителями юга Тюменской области и коренного населения Севера достоверных различий по степеням близорукости не было, а в группе лиц с ВИДС были.
Так у коренного населения Севера близорукость в сочетании с ВИДС слабой степени встречается в 2,7 раз чаще, средней степени – в 15,0 раз, высокой степени – в 2,1 раз. Очевидно, распространенность близорукости среди МНС связано именно с ВИДС. У коренного населения Севера с клиническими признаками ВИДС близорукость в 3,4 раза встречается чаще в сравнении с аналогичной группой населения юга Тюменской области. Об этом же свидетельствуют полученные данные корреляционного анализа: между частотой встречаемости близорукости и ВИДС имеются высокие корреляционные взаимосвязи (КК=0,676 при p<0,05).
Учитывая то, что среди патогенетических причин развития ВИДС и близорукости выделяют генетическую предрасположенность, морфологическую незрелость мезенхимальной (соединительной) ткани и нарушения пищевого рациона, было проведено изучение их на примере различных этнических групп (тундровые ненцы и староверы), сохранивших в той или иной степени (при достаточно длительной изоляции) относительную генетическую однородность. Выбранные группы являются адекватными и до некоторой степени уникальными объектами для выяснения анализируемых патологических состояний.
В ходе изучения эритроцитарных генетических антигенов было установлено, что близорукость имеет более широкий генетический полиморфизм наследственной предрасположенности по отношению к ВИДС. Так если при ВИДС обнаружены ассоциативные связи c ABO (B и A2B), MNSs (М, NN, NSs и Ns) и Rhesus (Ccddee, ccDEE и CwcDEe), то при близорукости – с ABO (А2), MNSs (MNSs), Kell (КК и Кк), Rhesus (CcDEe, Ccddee и ccDEe), Duffy (Fy+-) аллелями и фенотипами.
При анализе антигенов ядерных клеток крови с последующим определением величины диагностического коэффициента (анализ Вальда) обнаружены ассоциации близорукости с HLA-антигенами В15 (ДК=4,61; RR=6,67), В40 (ДК=11,1; RR=16,45), В51 (ДК=11,1; RR=16,45), B62 (ДК=12,7; RR=27,56), B7 (ДК=-9,58; RR=-11,73) и HLA фенотипами В15-В15 (ДК=10,66; RR=14,45), Cw0-Cw3 (ДК=9,44; RR=13,0) и DR0-DR5 (ДК=12,89; RR=35,0). При этом для носителей антигена HLA-В62 вероятность развития близорукости составила около 95 %, а при его сочетании с HLA-В40 и -В51 – до 99,0 %. В качестве протекторного фенотипа выступает Cw0-Cw4 (ДК=-8,69; RR=-8,81). Сочетание фенотипов HLA DR0-DR5 и В40-В15 повышает вероятность реализации прогноза развития близорукости до 99,0 %.
Примечательно то, что обнаружены (табл. 1) общие иммуногенетические предрасположенности, как в плане формирования близорукости, так и ВИДС – это ассоциативные HLA-А24, -А25, -В62 и протекторный HLA-В41 антигены с высоким коэффициентом относительного риска (RR>3,0).
Таблица 1
Общие HLA-антигены, ассоциированные с предрасположенностью к ВИДС и близорукости
| HLA-антигены | ВИДС | близорукость | ||
| ДК | RR | ДК | RR | |
| А 24 | 4,53 | 3,1 | 8,87 | 8,64 |
| А 25 | 11,04 | 14,56 | 8,87 | 8,64 |
| В 41 | -7,85 | -6,67 | -4,42 | -3,09 |
| В 62 | 4,72 | 3,26 | 12,7 | 27,56 |
Полученные результаты наглядно демонстрируют наличие ассоциации близорукости с иммуногенетическими маркерами тканевых антигенов и их сочетанием, что подтверждает результат корреляционного анализа. Обнаружены статистически достоверные взаимосвязи степени рефракции с HLA-A26 (КК=-0,53 при p<0,01) и B44 (КК=-0,66 при p<0,01). Установлено также, что выявленные значимые HLA-антигены связаны с иммунными показателями: HLA-В15 с уровнем CD3+ клетками (КК=-0,82 при p<0,05); HLA-В41 с уровнем ЦИК, IgA и M (КК=0,47; КК=0,5 и КК= 0,65 соответственно при p<0,05); HLA-B62 и А25 с уровнем ЦИК (КК=0,5 и КК=-0,46 соответственно при p<0,05).
Таким образом, близорукость необходимо рассматривать в контексте с функциональным состоянием иммунной системы. При этом известно, что морфологическое становление иммунной и зрительной систем происходит в эмбриональный период развития плода, а функциональное – в постнатальный период жизни ребенка.
Из представленной диаграммы (рис. 3) и таблицы 2 видно, что у детей с различными сроками гестации в период новорожденности имеет место целый ряд особенностей иммунной системы.
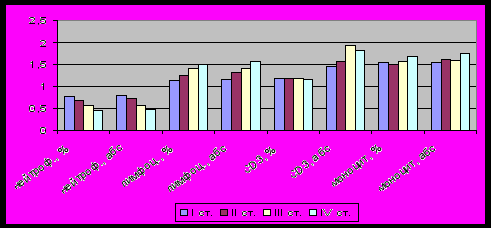
Рисунок 3. Характеристика показателей клеточного звена иммунной системы у новорожденных, в усл. ед. к показателям доношенных детей
Таблица 2
Характеристика показателей клеточного звена иммунной системы у новорожденных
| Показатели | Ед. изм. | Доношенные дети | Недоношенные дети | ||
| I | II | III | |||
| Лактоферрин | нг/мл | 1444,6+74,0 | 842,5+97,1*** | 837,5+79,4*** | 240,0+36,4*** |
| ИЛ-4 | пг/мл | 68,83+28,11 | 50,92 + 18,9 | 12,4 + 1,11 * | 65,4 + 9,3 |
| ИНФ-γ | пг/мл | 0,4+0,097 | 5,06+0,91 *** | 46,07+9,9 *** | 31,85+5,5 *** |
| ИЛ-4/ ИНФ-γ | усл. ед. | 172,1+37,5 | 10,06+7,3 *** | 0,27+0,08 *** | 2,05+0,81 *** |
| IgA | г/л | 0,014+0,001 | 0,02 + 0,003 | 0,02 + 0,002 | 0,025 + 0,002 |
| IgM | г/л | 0,25 + 0,02 | 0,71+0,09 *** | 0,41+0,08 * | 1,1 + 0,18 *** |
| IgG | г/л | 9,16 + 0,07 | 8,77+0,1 * | 8,85 + 0,15 * | 9,25 + 0,02 |
| IgE | МЕ/мл | 1,95 + 0,76 | 25,33+8,6 *** | 12,0 + 4,46 ** | 0,8 + 0,25 |
| IgG/IgA+M | усл.ед | 34,7 | 12,0 | 20,6 | 8,2 |
| ЦИК с ПЭГ 3,5 | усл. ед. | 7,37 + 0,78 | 15,0+2,57 * | 7,25 + 0,79 | 55,0+10,5 *** |
| ЦИК с ПЭГ 7,0 | усл. ед. | 35,43 + 5,09 | 80,75 + 15,2 * | 82,75 + 7,75 * | 123,5+7,37*** |
| ААТ к ДНК: - денатурир.; - нативной. | усл. ед. | 0,38 + 0,04 1,97 + 0,29 | 0,97+0,08*** 1,12 + 0,08 * | 0,7+0,05 *** 1,07+0,04 ** | 0,65+0,02 *** 0,85+0,02 ** |
| Титр а/т ВПГ: - 0; - 1:200; - 1:400; - 1:800. | % | 0,0 25,0+10,8 12,5+8,3 62,5+12,1 | 0,0 0,0 75,0+15,3 25,0+15,3 | 0,0 0,0 25,0+15,3 75,0+15,3 | 0,0 0,0 100,0 0 |
| Титр а/т ЦМВ - 0; - 1:200; - 1:400; - 1:800. | % | 50,0+12,5 12,5+8,3 0 37,5+12,1 | 25,0+15,3 0,0 50,0+17,7 25,0+15,3 | 0,0 25,0+15,3 75,0+15,3 0,0 | 0,0 0,0 100,0 0,0 |
