Клинико-функциональные и иммунопатогенетические механизмы формирования усиления рефракции 14. 00. 36 аллергология и иммунология 14. 00. 08 глазные болезни
| Вид материала | Автореферат диссертации |
- Клинико-функциональные результаты коррекции пресбиопии с использованием различных хирургических, 371.89kb.
- Клинико-лабораторная характеристика и лечение хламидийной инфекции, ассоциированной, 311.6kb.
- Клинико иммунологические особенности аллергодерматозов на фоне урогенитальной инфекции, 335.48kb.
- Изучение влияния постоянной слабомиопической дефокусировки изображения на динамику, 291.68kb.
- Образовательный стандарт послевузовской профессиональной подготовки специалистов Специальность:, 1035.98kb.
- Клинико-иммунологическая характеристика и иммунотерапия пневмонии у новорожденных,, 653.89kb.
- Диагностика и лечение аллергического ринита с сопутствующей патологией лор-органов, 740.73kb.
- Иммунные механизмы инвазивности эндометриальных клеток при эндометриозе 14. 00. 36., 247.97kb.
- Клинико-патогенетическое обоснование комбинированного лазерно-медикаментозного лечения, 270.48kb.
- Методы оценки и клиническое значение биомеханических свойств роговицы (клинико-экспериментальное, 429.56kb.
* - достоверность различий с миопией слабой степени (*-p<0,05; **-p<0,01; ***-p<0,001); # - достоверность различий с миопией средней степени (#-p<0,05; ##-p<0,001).
Установлено, что близорукость слабой степени сопряжена с повышением содержания HLA-DR+ клеток (12,87+0,91 по сравнению с 7,42+0,22 при эмметропии), CD16+ клеток (19,8+2,28 по сравнению с 14,74+0,87), CD8+ (29,13+1,44 по сравнению с 23,05+1,74 при эмметропии) и IgG (12,28+0,57 и 10,81+0,36 соответственно), а также снижением фагоцитарной активности нейтрофилов (ФИ через 90 мин: 2,82+0,14 и 3,22+0,08 соответственно) и крупномолекулярных ЦИК (12,28+2,83 и 26,52+2,07 соответственно).
При близорукости средней степени обнаружена более выраженная дисрегуляция активационно-пролиферативных процессов – с одной стороны дальнейшее повышение фагоцитарной активности нейтрофилов (85,0+1,45 и 78,33+2,84 соответственно) и количества пролиферирующих клеток (CD71+ до 0,57+0,14), а с другой стороны достоверное снижение количества клеток, экспрессирующих маркер мономорфных детерминант HLA-антигенов II класса (HLA-DR: 7,24+0,7 и 12,87+0,91 соответственно), CD38+ клеток (15,29+1,05 и 24,3+3,76 соответственно), а также В-лимфоцитов (9,7+0,85 и 14,0+1,16 соответственно) и IgА (1,48+0,12 и 2,17+0,1 соответственно) при значительном увеличении содержания крупных молекулярных ЦИК в сыворотке крови (24,13+3,03 и 12,28+2,83 соответственно). По сути, выявленные отклонения можно охарактеризовать как дисрегуляционное состояние процессов активации иммунной системы.
Характеристики иммунного статуса при близорукости высокой степени существенно отличаются от близорукости слабой и средней степени, что выражается снижением маркеров активационно-пролиферативных процессов: HLA-DR+ (5,25+0,78 и 7,24+0,7 соответственно) и CD71+ клеток (0,13+0,06 и 0,57+0,14 соответственно), фагоцитарной активности нейтрофилов (ФИ через 30 и 90 мин в 1,8 и в 1,2 раза). При этом снижается уровень CD8+ субпопуляций лимфоцитов (27,76+0,69 и 29,59+0,67 соответственно) и повышаются CD16+ клетки (22,26+1,49 и 17,67+1,41 соответственно), крупные молекулярные ЦИК (34,0+4,0 и 24,13+3,03 соответственно) в периферической крови. Выявленные отличительные черты в иммунном статусе при близорукости высокой степени можно с полным основанием отнести к болезни регуляции, которая может опосредовать осложнения со стороны органа зрения.
Таким образом, изучение характеристик иммунного статуса, используя общепринятые градации близорукости по степени, позволило получить сопоставимые данные по однородным группам и выделить иммунопатогенетические критерии, связанные с переходом биологического варианта нормы (близорукости слабой степени) в предболезнь (близорукость средней степени) и в патологический процесс (близорукость высокой степени). Так близорукость слабой степени характеризуется напряжением всех звеньев иммунного ответа (клеточного, гуморального и фагоцитарного) с высокой вероятностью формирования болезни регуляции, близорукость средней степени – дисбалансом активационно-пролиферативных процессов иммунной системы, супрессией клеточного и гуморального звеньев иммунного ответа, а близорукость высокой степени – супрессией всех звеньев иммунного ответа.
Известно, что близорукость может протекать стационарно или прогрессировать. Быстро прогрессирующая близорукость даже слабой степени является неблагоприятным прогностическим признаком. К сожалению, в настоящее время, одной из нерешенных проблем в офтальмологии остается выяснение механизмов, приводящих к прогрессирующему течению близорукости. Изучение данного аспекта с использованием иммунологических методов может позволить понять суть происходящего и дать основу для разработки новых методов лечения прогрессирующей близорукости. При анализе показателей иммунной системы у лиц с близорукостью средней и высокой степени были установлены следующие особенности (рис. 6).
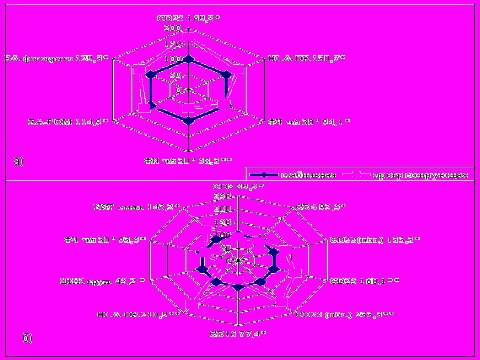
Рисунок 6. Характер изменений показателей иммунной системы при прогрессирующем течении близорукости средней (а) и высокой (б) степени (* - p<0,05; ** - p<0,01)
Так прогрессирующее течение близорукости ассоциировано с повышением уровня ряда активационных маркеров: повышение содержания лимфоцитов, экспрессирующих ИЛ-2 (2,92+0,39 и 1,72+0,2 соответственно при средней степени и 3,21+0,42 и 1,38+0,36 соответственно при высокой степени) и DR-рецепторы (8,16+0,65 и 6,54+0,46 соответственно при средней степени и 11,07+1,65 и 5,25+0,78 соответственно при высокой степени), снижение фагоцитарной активности нейтрофилов (80,0+1,15 и 85,0+1,45 соответственно при средней степени и 79,71+1,65 и 85,25+0,62 соответственно при высокой степени). Наряду с этим в группе лиц со средней степенью близорукости выявлено повышение функциональной активности моноцитов (ЕА-РОМ: 12,79+0,4 и 11,13+0,54 соответственно; ЕА-фагоцитоз: 11,16+0,91 и 8,63+0,93 соответственно), а при близорукости высокой степени относительное снижение CD8 (24,96+1,12 и 27,76+0,69 соответственно) и CD4 (29,31+0,78 и 31,7+0,86 соответственно) позитивных лимфоцитов.
Таким образом, близорукость и ее прогрессирующее течение ассоциировано в первую очередь с нарушением (дисбалансом) активационной составляющей иммунной системы, а также дефектом (дефицитом) компонентов иммунной системы при близорукости более 6,0 дптр., что типично для ВИДС. Логично предположить, что ВИДС может влиять на возникновение и прогрессирование близорукости. Поэтому следующим этапом исследования явилось изучение характеристик иммунной и зрительной систем при близорукости в сочетании с ВИДС (рис. 7).
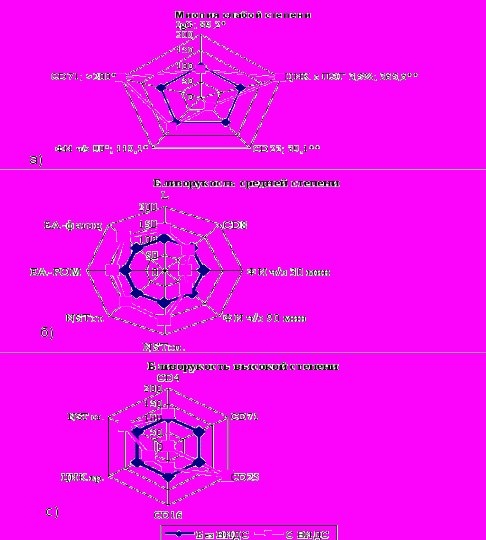
Рисунок 7. Сравнительная характеристика иммунных показателей при близорукости различной степени в зависимости от наличия ВИДС, %
Было установлено, что для ВИДС с соразмерной рефракцией (эмметропией) в первую очередь характерно нарушение (дисбаланс) взаимосвязей между компонентами иммунной системы с повышением активационно-пролиферативных характеристик иммунной системы.
При близорукости слабой степени с наличием ВИДС по сравнению с группой «близорукость слабой степени без ВИДС» направленность выявленных отклонений в иммунной системе была практически однотипна, но более выражена (рис. 7а), что проявилось в повышении крупномолекулярных ЦИК на 265,6%, интенсивности фагоцитоза нейтрофилов на 19,1%, количества CD71+ клеток более чем в 2 раза, также снижение В-лимфоцитов на 60,9% и IgG на 10,8%.
При близорукости средней степени в сочетании ВИДС по сравнению с близорукостью той же степени, но без ВИДС, выявлена (рис. 7б) более выраженная дисрегуляция активационно-пролиферативных процессов. С одной стороны повышение функциональной активности моноцитов: NST-спонтанный (10,63+1,22 и 6,75+0,88 соответственно) и NST-стимулированный (11,75+0,98 и 8,38+0,91 соответственно), ЕА-РОМ (14,75+0,54 и 11,13+0,54 соответственно) и ЕА-фагоцитоз (12,75+0,89 и 8,63+0,93 соответственно). С другой стороны – признаки иммуносупрессии: снижение фагоцитарной активности нейтрофилов (ФИ через 30 и 90 мин в 1,9 и в 1,2 раза соответственно) и повышение уровня CD8+ лимфоцитов (26,79+0,92 и 29,59+0,67 соответственно).
Близорукость высокой степени с ВИДС в сравнении с близорукостью высокой степени без ВИДС ассоциирована (рис. 7с) со значительной депрессией активационно-пролиферативных процессов, о чем свидетельствует снижение CD71+ (0,0 и 0,13+0,06 соответственно), CD16 (16,22+1,62 и 22,26+1,49 соответственно) и CD8 (27,5+1,24 и 27,76+0,69 соответственно) позитивных лимфоцитов при повышении уровня CD4+ (34,65+0,55 и 31,7+0,86 соответственно) и CD25+ (4,18+0,5 и 1,38+0,36 соответственно) лимфоцитов.
Таким образом, рефракционный статус органа зрения связан с морфо-функциональным состоянием иммунной системы. При этом в случае сочетания близорукости с клиническими признаками ВИДС по мере роста степени близорукости происходит изменение иммунных характеристик. Так близорукость слабой степени сопровождается с повышением активационной составляющей иммунной системы, близорукость средней степени – с дисрегуляцией активационно-пролиферативных процессов, близорукость высокой степени – с функциональной депрессией иммунной системы. Аналогичная картина наблюдается при близорукости без ВИДС. Однако присутствие ВИДС является явным отягощающим фактором, усугубляющим течение рефракционной офтальмопатологии. Иммунологические характеристики при близорукости с ВИДС формируются раньше, чем при близорукости без ВИДС, где они наблюдаются при более высокой степени близорукости.
Установлено также, что наличие клинических признаков ВИДС существенно оказывает влияние и на характер течения близорукости (рис. 8).
При прогрессирующем течении близорукости обнаружена дисрегуляция функциональной активности иммунной системы: увеличение содержания в периферической крови DR+ лимфоцитов (на 27,2% и 91,8% соответственно при средней и высокой близорукости) при снижении на 33,2% и 22,2% соответственно уровня лимфоцитов, экспрессирующих ИЛ-2 рецепторы, и функциональной активности моноцитов (способности к розеткообразованию с эритроцитами барана на 24,6% и 21,9%, ЕА-фагоцитоз на 34,3% и 38,5% соответственно).
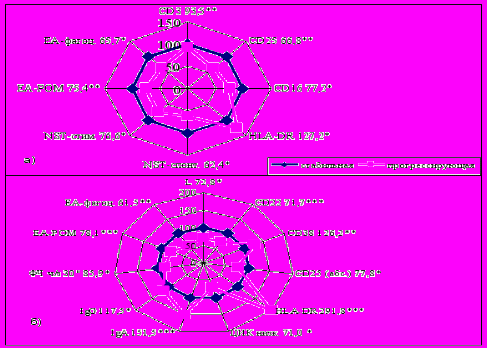 Рисунок 8. Характер изменений показателей иммунной системы при прогрессирующем течении близорукости средней (а) и высокой (б) степени при ВИДС, %.
Рисунок 8. Характер изменений показателей иммунной системы при прогрессирующем течении близорукости средней (а) и высокой (б) степени при ВИДС, %.Кроме того, выявлено снижение популяции зрелых Т-лимфоцитов (CD3+ на 6,5%), клеток с естественной цитотоксичностью (CD16+ на 22,8%) и бактерицидной активности моноцитов в спонтанном и стимулированном NST-тесте (на 37,6% и 23,4% соответственно) при прогрессирующей близорукости средней степени. Увеличение содержания активированных лимфоцитов (на 26,2%), IgA (на 51,5%), G (на 17,5%), явное снижение общего количества лейкоцитов (на 27,2%) в периферической крови, В-лимфоцитов (CD22+ на 28,3%), фагоцитарной активности нейтрофилов (на 14,1%), низкомолекулярных ЦИК (на 29,0%) при прогрессирующей близорукости высокой степени.
Если существуют взаимосвязи между состоянием иммунной и зрительной системами, то патологические процессы иммунной системы (ВИДС) должны оказывать влияние на анатомо-оптические, функциональные и другие составляющие процесса обеспечения четкого изображения на сетчатке. Поэтому выявление влияния ВИДС на рефракционные, аккомодационные и электрофизиологические характеристики органа зрения чрезвычайно важно.
Согласно широко распространенным взглядам, в основе формирования близорукости и ее прогрессирования лежат нарушения сопротивляемости склеры, что ведет к ее растяжению под влиянием повышения внутриглазного давления (ВГД). При ВИДС имеет место системная «просадка» фиброзной ткани всего организма. Разрушение коллагеновых белков ведет к образованию большого количества низкомолекулярных коллагеновых пептидов (КП). КП являются биологически активными веществами по отношению ко многим типам клеток. В частности КП активируют миграцию нейтрофилов в коллагенновый матрикс и ингибируют аналогичную функцию макрофагов. Обработка нейтрофилов КП приводит к усилению продукции активных форм кислорода, тогда как макрофаги отвечают на добавление КП ее ингибированием. При этом в отношении нейтрофилов КП выступают, с одной стороны, как хемотаксический фактор, а с другой – как праймирующий агент. Кроме того, снижая уровень спонтанного апоптоза нейтрофилов КП очевидно не позволяет им погибнуть, не реализовав своих функций (инициируют и обеспечивают фазу альтерации). КП ингибируют миграцию макрофагов, продукцию ими свободных радикалов и поддержание их жизнеспособности за счет снижения апоптоза, это может свидетельствовать о том, что КП регулируют переход воспаления от альтернативных процессов к репаративным (Козлов И.Г., Емельянов А.Ю., Давыдова Н.В. с соавт., 1999).
Некоторые свойства соединительной ткани глаза в условиях ВИДС иллюстрируют полученные результаты при анализе эластотонометрической кривой (рис. 8).
У
Рисунок 8. Эластонометрия при близорукости и эмметропии в зависимости от наличия ВИДС.
становлено, что присутствие клинических признаков ВИДС при эмметропии сопровождается снижением внутриглазного давления (14,6+0,6 и 15,7+0,3 мм.рт.ст. соответственно при p<0,05), измеряемое тонометром в 5,0 граммов, а также укорочение размаха эластонометрической кривой – признак нарушения ригидности соединительнотканной оболочки глазного яблока (склеры).
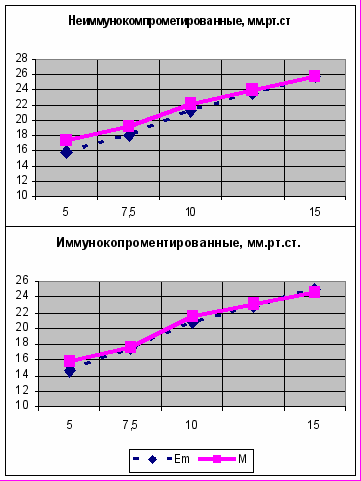 Так, если у «практически здоровых» эмметропов размах эластотонометрической кривой составил в пределах 4,4-15,6 мм рт.ст., то у лиц с клиническими признаками ВИДС – 5,2-15,4 мм рт.ст. (достоверно укорочен), а в группе «близорукость высокой степени с ВИДС» - 4,5-10,0 мм рт.ст.. У «практически здоровых» излом эластокривых при различных видах рефракции не был выявлен, а при близорукости в сочетании с ВИДС излом имел место. Обнаруженные факты свидетельствуют о снижении ригидности фиброзной оболочки глазного яблока, что и подтверждают результаты дисперсионного анализа. Так, острый характер течения ОРЗ в анамнезе с высокой температурной реакцией организма, а также затяжной характер течения ОРЗ (более 7 дней) имеют прямую взаимосвязь с повышением тонометрического ВГД (КК=0,22 при p<0,01 и КК=0,17 при p<0,05 соответственно) и являются одними из определяющих факторов в повышении тонуса глазного яблока (F=4,87 при p<0,01). Обнаружено, что ВГД является одним из определяющих факторов в усилении рефракции. Однако при исследовании истинного внутриглазного давления было установлено, что у лиц с близорукостью оно достоверно не изменяется, а при высокой степени близорукости в сочетании с ВИДС даже снижается (15,8+0,6 и 16,9+0,5 мм.рт.ст при p<0,05).
Так, если у «практически здоровых» эмметропов размах эластотонометрической кривой составил в пределах 4,4-15,6 мм рт.ст., то у лиц с клиническими признаками ВИДС – 5,2-15,4 мм рт.ст. (достоверно укорочен), а в группе «близорукость высокой степени с ВИДС» - 4,5-10,0 мм рт.ст.. У «практически здоровых» излом эластокривых при различных видах рефракции не был выявлен, а при близорукости в сочетании с ВИДС излом имел место. Обнаруженные факты свидетельствуют о снижении ригидности фиброзной оболочки глазного яблока, что и подтверждают результаты дисперсионного анализа. Так, острый характер течения ОРЗ в анамнезе с высокой температурной реакцией организма, а также затяжной характер течения ОРЗ (более 7 дней) имеют прямую взаимосвязь с повышением тонометрического ВГД (КК=0,22 при p<0,01 и КК=0,17 при p<0,05 соответственно) и являются одними из определяющих факторов в повышении тонуса глазного яблока (F=4,87 при p<0,01). Обнаружено, что ВГД является одним из определяющих факторов в усилении рефракции. Однако при исследовании истинного внутриглазного давления было установлено, что у лиц с близорукостью оно достоверно не изменяется, а при высокой степени близорукости в сочетании с ВИДС даже снижается (15,8+0,6 и 16,9+0,5 мм.рт.ст при p<0,05). Полученные результаты свидетельствуют о том, что при близорукости в сочетании с ВИДС имеет место более выраженные изменение биомеханических свойств фиброзной оболочки глазного яблока, а именно снижение ригидности его соединительнотканных структур, что составляет патогенетическую основу формирования усиленного типа рефракции в условиях ВИДС.
Другой важный момент, который также подтверждает вышесказанное, - это характер изменения анатомо-оптических характеристик органа зрения в условиях ВИДС. Так при близорукости слабой степени они выражаются в уплощении роговицы (радиус роговицы составил 7,66+0,04 против 7,5+0,02 мм при p<0,01) и соответственно в снижении ее преломляющей силы (44,1+0,22 против 44,8+0,2 дптр. при p<0,05). При близорукости высокой степени присутствие клинических признаков ВИДС ассоциировано с выраженным увеличением переднезадних размеров хрусталика (3,73+0,09 и 3,63+0,05 мм при p<0,05), разницы радиусов кривизны (0,36+0,07 и 0,2+0,05 мм при p<0,05) и преломляющей силы роговицы в двух меридианах (2,06+0,4 и 1,21+0,31 мм при p<0,05) с формированием роговичного астигматизма большей степени. Параллельно с этим наличие ВИДС оказывает влияние и на работу ресничной мышцы глаза.
Длительное время в литературе шли споры по поводу того, как влияет интенсивная зрительная нагрузка на работоспособность ресничной мышцы и формирование близорукости. По мнению одних исследователей, она вызывает увеличение объема аккомодации и приближение к глазу ближайшей точки ясного зрения, по данным других – напротив, способствует снижению работоспособности ресничной мышцы при близорукости и практически не влияет на аккомодационную функцию эмметропов. Имеются данные о наличии двухфазности изменения аккомодации: сначала работоспособность цилиарных мышц повышается, а затем снижается (Кузнецова М.В., 2004).
Установлено, что при усилении рефракции в сочетании с частыми ОРЗ происходит (p<0,05) увеличение положительной части объема относительной аккомодации (ОА) и объема ОА, а в группе лиц с частыми и длительными обострениями хронических инфекционно-воспалительных процессов в период ремиссии – снижение положительной части ОА. Результаты дисперсионного анализа свидетельствуют, что положительная часть и объем ОА являются определяющими факторами в отклонении рефракционного статуса в сторону близорукости (F=7,62 и F=5,4 соответственно при p<0,001). Выявлено, что если при стабильном течении близорукости средней степени у лиц с клиническими признаками ВИДС резервы аккомодации (RA) достоверно ниже (2,44+0,31 и 3,52+0,38 дптр при p<0,05), то при прогрессирующем течении близорукости вне зависимости от ее степени RA выше в 1,9-2,4 раза.
Мышечные сокращения сопровождаются выработкой большого количества тепла, а значит, работающие мышцы участвуют в теплообразовании. Концентрация продуктов распада в клетке является одним из регуляторов интенсивности мышечного сокращения. При увеличении концентрации интенсивность сокращения снижается, а при достижении определенного уровня сокращение становиться невозможным. Таким образом, клетка предохраняет себя от выполнения чрезмерной работы. Установлено, что в группе «близорукость - ВИДС» (на момент обследования считающих себя соматически здоровыми) средняя температура в области проекции ресничного тела на 0,31°С выше. Это соответствует повышению уровня метаболизма на 3,6 %. Более выраженные (p<0,01) изменения были выявлены в темпоральной точке измерения, где повышение температуры было на 0,5°С и соответственно уровня метаболизма на 6,4 %. R.W. Swift и K.H. Fischer (1964) установили, что при физической активности и специфическом динамическом действии энергетические потребности увеличиваются на 6 %. Таким образом, наличие ВИДС сопровождается повышением уровня основного обмена, который соответствует активной физической работе и требует соответствующего обеспечения нутриентного и субстратного микроокружения для его покрытия.
При близорукости в сочетании с ВИДС после тренировочных упражнений ресничной мышцы выявлена парадоксальная температурная реакция (рис. 9).
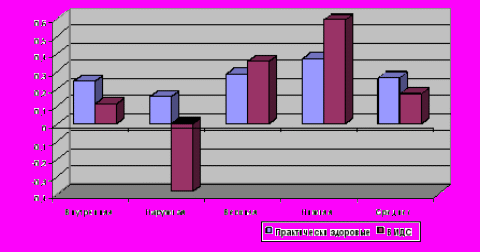
Рисунок 9. Разница температур в области проекции ресничного тела до и после аккомодативных тренировок.
Так в верхней и нижней точках измерения наблюдается достоверное повышение температуры на 0,3°С, в наружной достоверное (p<0,05) снижение на 0,4° С, а в среднем достоверное изменение температуры не происходит. При этом установлено, что если у «практически здоровых» лиц с близорукостью после физической нагрузки средняя температура в области проекции ресничного тела снижается в 15,6% случаев, то при ВИДС – в 25,0% случаев (в 1,6 раз чаще). Обнаруженный факт свидетельствует о том, что при близорукости в сочетании с ВИДС имеет место повышение скорости и интенсивности обмена веществ в ресничном теле, а значит и концентрации продуктов распада в процессе теплообразования, вывод которых затруднен из-за снижения скорости тока крови, кровенаполнения кровеносных сосудов, внутриглазной гидродинамики. При увеличении концентрации продуктов распада интенсивность сокращения снижается, а по достижению определенного уровня сокращение становиться невозможным. Таким образом, клетка предохраняет себя от выполнения чрезмерной работы. Все это вызывает снижение запаса работоспособности ресничной мышцы. По-видимому, при близорукости в сочетании с ВИДС интенсивность акоммодативных тренировок должна быть меньше, мышечная нагрузка – дозированной, а лечебно-профилактические курсы – более длительными.
Таким образом, определено влияние функционального состояния иммунной системы на аккомодативную работоспособность органа зрения. Однако описанным феноменом данное влияние не ограничивается. В результате корреляционного и дисперсионного (факторного) анализов установлено, что при стабильном течении близорукости средней степени RA положительно коррелируют с ЕА-фагоцитозом моноцитов (КК=0,95 при p<0,001), а при прогрессирующем течении – обратно пропорционально с фагоцитарной активностью нейтрофилов (ФЧ ч/з 30 мин: KK=-0,59 при p<0,01). При этом независимо от течения близорукости средней степени, снижение RA сопряжено со снижением DR+ клеток (F=69,8 при p<0,001 и КК=0,23), фагоцитарной активности моноцитов (F=3,23 при p<0,05 и КК=0,31) и замедлением интенсивности фагоцитоза нейтрофилов (ФИ ч/з 30 мин: F=5,26 при p<0,01 и КК=0,16). Кроме того, при стабильном течении близорукости снижение RA сопряжено со снижением ЕА-РОМ (F=112,5 при p<0,001 и КК=0,24), а при прогрессирующем течении близорукости с их ростом (F=3,11 при p<0,05 и КК=-0,04).
Полученные результаты демонстрируют, что зрительный анализатор является структурно-функциональным производным, встроенным в билатерально-асимметричную организацию единой иммуно-эндокрино-нервной системы, в то же время, по всей вероятности, участвует в иммунорегуляции. Аккумулирующим центром подобных взаимодействий, очевидно, является гипоталамус, в ядрах которого оканчиваются аксоны ганглиозных клеток сетчатки. Для подтверждения этого были изучены электрофизиологические характеристики зрительной системы при близорукости с учетом наличия клинических признаков ВИДС (рис. 10). Установлено, что при близорукости слабой степени ВИДС ассоциируется с одной стороны с разобщением биоэлектрогенеза между нейронами I и II порядка (увеличивается амплитуда b-волны общей ЭРГ: 301,55+8,13 и 256,75+13,84 мкв соответственно при p<0,05), а с другой стороны со снижением моно- и бинокулярного визирования в более широком диапазоне пространственных частот (с 3,4 до 18,0 цикл/град) и в большей степени (монокулярное визирование на 10,4-24,5%, бинокулярное – на 7,4-23,4%), чем при близорукости слабой степени без ВИДС. Подобная картина наблюдается у лиц с близорукостью средней степени без клинических признаков ВИДС.
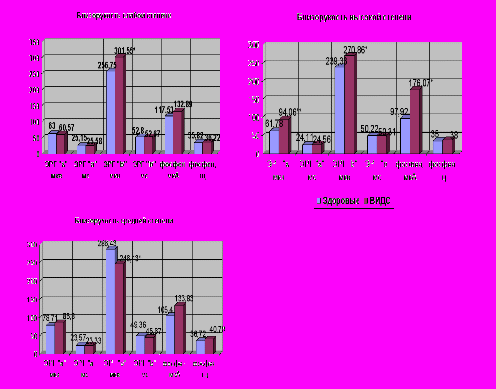
Рисунок 10. Электрофизиологическая характеристика близорукости различной степени в зависимости от наличия клинических признаков ВИДС.
При средней степени близорукости ВИДС ассоциируется со снижением амплитуды b-волны общей ЭРГ (246,43+17,2 и 286,43+6,76 мкв соответственно при p<0,05) и укорочение времени достижения максимума b-волны (45,67+1,52 и 49,36+0,61 мс соответственно при p<0,05). При этом соотношение амплитуд волн b/a общей ЭРГ снижается в 1,5 раз – свидетельство развития тормозных процессов в сетчатке вследствие аноксии пострецепторных клеток и снижения электрической активности нейронов II порядка. Возможно, это является следствием чрезмерного раздражения фоторецепторов сетчатки либо обусловлено нарушением проведения возбуждения по ретиноталамическим центробежным тормозящим волокнам, что также характерно для близорукости более высокой степени при отсутствии ВИДС.
Интерес представляет факт отсутствия у лиц с близорукостью средней степени достоверного снижения моно- и бинокулярного ПКЧ в диапазоне низких пространственных частот (0,37-1,0 цикл/град) в отличие от «практически здоровых» лиц с близорукостью средней степени. Тем не менее, снижение в других диапазонах было выражено в большей степени (монокулярного ПКЧ на 16,6-65,9 %, бинокулярного ПКЧ на 31,2-75,0 %). Известно, что каждый нейрон центральных отделов зрительного анализатора реагирует на оптимальную для него пространственную частоту. Так, нейроны Х-типа, располагающиеся в зрительной коре и связанные в основном с макулярной областью сетчатки, относятся к каналам средней и высокой пространственной частоты; Y-нейроны имеют большие размеры, им не свойственно комбинировать возбуждающие и тормозящие сигналы с рецептивных полей по линейному закону. В отличие от Х-нейронов, они лучше реагируют на стимулы низкой пространственной частоты (Шамшинова А.М., Волков В.В., 1998).
Таким образом, наличие признаков ВИДС оказывает селективное существенное влияние на возбуждающие и тормозящие сигналы с рецептивных полей сетчатки – тормозящее на опознавание стимулов, исходящих от макулярной области, и возбуждающее на опознавание стимулов с рецептивных полей от Y-нейронов.
При близорукости высокой степени ВИДС ассоциировано с дискоординацией электрогенеза сетчатки – рост амплитудных характеристик a-волны (94,06+8,49 и 61,78+5,74 мкв соответственно при p<0,01) и снижение амплитудных характеристик b-волны (270,86+8,71 и 239,33+10,15 мкв соответственно при p<0,05) общей ЭРГ на фоне достоверного повышения порога электрической чувствительности сетчатки (176,07+27,36 и 97,92+5,31 мкА соответственно при p<0,05).
Проведенные исследования свидетельствуют о том, что электрофизиологические показатели сетчатки и зрительного нерва при близорукости имеют множественные положительные и отрицательные корреляционные связи с различными показателями клеточного и гуморального иммунитета. Так снижение временных параметров «a» и «b» волн ЭРГ ассоциируется со снижением количества CD95+ клеток (КК=0,89 при p<0,05 и КК=0,95 при p<0,01 соответственно), крупномолекулярных ЦИК (КК=0,41 и КК=0,37 при p<0,01 соответственно) и с лейкоцитозом (КК=-0,49 при p<0,01 и КК=-0,38 при p<0,05 соответственно), ростом низкомолекулярных ЦИК (КК=-0,5 и КК=-0,54 при p<0,01 соответственно). Снижение временных параметров «b» волны ЭРГ ассоциируется также с низким уровнем содержания CD4+ лимфоцитов (КК=0,4 при p<0,05), ЕА-РОМ (KK=-0,47 при p<0,01), IgG (КК=-0,35 при p<0,05) и NST-стимулированных моноцитов (KK=-0,38 при p<0,05). При этом амплитуда a-волны ЭРГ прямопропорционально коррелирует с уровнем DR-позитивных клеток (КК=0,44 при p<0,05) и бактерицидной активностью моноцитов, определяемой в тесте NST-спонтанном и стимулированном (КК=0,4 при p<0,05 и КК=0,51 при p<0,01 соответственно), а порог электрической чувствительности сетчатки – с NST-спонтанным (КК=0,43 при p<0,01). Выявлены также корреляционные взаимосвязи между электрической лабильностью зрительного нерва и следующими иммунными показателями: низкомолекулярными ЦИК (КК=-0,28 при p<0,05), CD4+ лимфоцитами (КК=0,46 при p<0,01), ФИ нейтрофилов через 60 мин (КК=0,28 при p<0,05).
Таким образом, близорукость и ВИДС следует рассматривать как патогенетически взаимосвязанные состояния и процессы, каждый составляющий элемент которых характеризуется определенными периодами: стационарного или прогрессирующего течения близорукости и отсутствием или наличием острых инфекционно-воспалительных проявлений (в отношении ВИДС). При этом ВИДС совершенно определенным образом влияет на течение близорукости.
Другим общим лимитирующим фактором, влияющим на рефрактогенез и иммуногенез, является алиментарный фактор необходимый для метаболического обеспечения обмена веществ (распада и синтеза) в клетках иммунной и зрительной систем.
Установлено (табл. 4), что снижение энергетической ценности потребляемой пищи является одним из определяющих факторов риска не только роста степени близорукости (F=3,12; p<0,001), но и увеличения асимметрии рефракции двух глаз (F=1,42; p<0,05), степени астигматизма (F=1,68; p<0,01).
Таблица 4
Потребление основных нутриентов лицами с близорукостью в зависимости от состояния иммунной системы
| Нутриенты | Эмметропия | Близорукость сл. степени | Близорукость > 3,0 дпрт. | ||||
| Здоровые (n=105) | ВИДС (n=58) | Здоровые (n=57) | ВИДС (n=42) | Здоровые (n=34) | ВИДС (n=29) | ||
| Энергетическая ценность, ккал | 2401,3 + 103,3 | 2201,8 + 97,0 | 2337,2 + 191,2 | 2043,9 + 134,2 # | 2297,3 + 142,8 | 2198,9+ 170,0 | |
| Белок | Г | 67,51 + 3,12 | 70,63 + 4,96 | 81,22 + 9,72 | 63,69 + 6,96 | 79,53 + 6,52 | 72,25 + 4,63 |
| % | 14,1 + 0,65 | 16,02 + 1,12 | 16,53 + 1,98 | 15,71 + 1,72 | 16,75 + 1,37 | 15,73 + 1,01 | |
| Жиры | Г | 86,17 + 6,43 | 78,19 + 6,62 | 77,15 + 7,22 | 76,0 + 10,91 | 71,85 + 6,7 | 74,22 + 12,83 |
| % | 17,99 + 1,34 | 17,74 + 1,5 | 15,7 + 1,47 | 18,75 + 2,69 | 15,13 + 1,41 | 16,16 + 2,79 | |
| Сумма углеводов | Г | 325,3 + 13,22 | 292,0 + 12,3 | 333,0 + 37,1 | 265,7 + 20,3 | 323,5 + 25,0 | 312,9 + 24,5 |
| % | 67,91 + 2,76 | 66,24 + 2,79 | 67,77 + 7,55 | 65,54 + 5,0 | 68,12 + 5,26 | 68,11 + 5,33 | |
| Б : Ж : У | 1:1,3:4,8 | 1:1,1:4,1 | 1:0,9:4,1 | 1:1,2:4,2 | 1:0,9:4,1 | 1:1:4,3 | |
| Моно- и дисахариды | Г | 118,9 + 6,9 | 97,09 + 6,83 | 80,21 + 3,16 | 96,15 + 10,35 | 86,36 + 7,71 ** | 86,43 + 8,81 |
| % | 36,55 | 33,25 | 24,09 | 36,19 | 26,7 | 28,62 | |
| Вода | Мл | 1854,0 + 69,5 | 1830,8 + 72,7 | 1878,7 + 183,8 | 1444,8 + 98,9 # | 1654,5 + 102,8 | 1838,9 + 138,8 |
| Мл/ккал | 0,84+ 0,03 | 0,91+ 0,05 | 0,83+ 0,06 | 0,8+ 0,08 | 0,78+ 0,06 | 0,9+ 0,08 | |
| Метабо-лическая вода (мл) | Б | 27,7+ 1,3 | 29,0+ 2,0 | 33,3+ 4,0 * | 26,1+ 2,8 | 32,6+ 2,7 * | 29,6+ 1,9 |
| Ж | 92,2+ 6,9 | 83,7+ 7,1 | 82,5+ 7,7 | 81,3+ 11,7 | 76,88+ 7,2 | 79,4+ 13,7 | |
| У | 195,2+ 7,9 | 175,2+ 7,4 | 199,8+ 22,3 | 159,4+ 12,2 | 194,1+ 14,9 | 187,8+ 14,7 | |
| сумма | 315,0+ 13,0 | 287,8+ 12,0 | 315,7+ 27,5 | 266,9+ 20,3 | 303,6+ 18,9 | 296,8+ 24,1 | |
| Доля метаболической воды от потребляемой воды, % | 14,7+ 0,4 | 14,0+ 0,5 | 15,2+ 0,8 | 16,3+ 1,4 | 16,2+ 1,2 | 14,5+ 1,2 | |
* Достоверность различий с группой «здоровые эмметропы» (* - p<0,05; ** - p<0,01).
# Достоверность различий с группой «здоровых миопов слабой степени» (# - p<0,01).
Общеизвестно, что основным источником энергии являются углеводы и жиры. При этом при всех типах анизометропии практически здоровые лица достоверно больше потребляют простые углеводы (моносахариды) по сравнению с эмметропами. При анализе содержания углеводов в рационе в зависимости от наличия или отсутствия ВИДС выявлено, что при анизометропии в сочетании с клиническими признаками ВИДС наблюдается снижение потребления моносахаридов, а у гиперметропов также ди- и полисахаридов. При этом у лиц с близорукостью установлено снижение поступления с продуктами питания гемицеллюлозы (12,1+1,48 и 15,99+1,58 при p<0,05 соответственно).
Известно, что увеличение степени аметропии сопряжено с ростом астигматического компонента. Поэтому снижение потребления моносахаридов в группах лиц с аметропией в сочетании с ВИДС сопровождается соответственным ростом степени астигматизма. Учитывая то, что для коренного населения Крайнего Севера не характерен белково-углеводный тип питания, становится вполне объясним и обнаруженный в этой группе факт – влияние повышенного потребления практически всех групп углеводов на процесс усиления рефракции, а также влияние повышенного потребления простых углеводов на ослабление аккомодативной работоспособности органа зрения.
Известно, что липиды играют более значимую роль в структуре традиционного питания коренных жителей Крайнего Севера, чем углеводы. Для «практически здоровых» лиц с близорукостью со степенью рефракции более 3,0 дптр. характерно снижение в рационе питания моно- и полиненасыщенных жирных кислот по сравнению с эмметропами не имеющих клинических признаков ВИДС (19,49+2,56 по сравнению с 23,66+1,8 и 7,65+1,31 по сравнению с 12,9+2,06 соответственно при p<0,05). В ходе исследований определились факторы риска развития близорукости – недостаточность моно- и полиненасыщенных жирных кислот (F=1,89-2,8 при p<0,001); прогрессирования близорукости – недостаточность триглицеридов и суммы жирных кислот (F=4,0-5,4 при p<0,001); аккомодативной слабости – недостаточность триглицеридов (F=2,08 при p<0,05), суммы жирных кислот (F=2,43 при p<0,01) и холестерина (F=12,71 при p<0,001).
При сравнительном анализе потребления незаменимых и заменимых аминокислот, их составляющих в различных группах в зависимости от типа рефракции и состояния иммунной системы, каких-либо достоверных различий выявлено не было. Тем не менее, дисперсионным анализом установлено, что уровень содержания аминокислот в структуре питания является одним из определяющих факторов формирования аметропии и ВИДС. При этом направленность и существенность оказываемого влияния зависит как от типа рефракции, так и от наличия клинических признаков ВИДС.
Выявлена недостаточность потребления витаминов, являющихся катализаторами биохимических и физиологических процессов, – Е, β-каротина, Н, В5 и В9, которая и явилась фактором риска, способствующим формированию близорукости (F=2-4 при p<0,05 соответственно). Недостаточное содержание в пище пантотеновой кислоты (F=2,87 при p<0,05), кальциферолов (F=2,99 при p<0,05), аскорбиновой кислоты (F=20,5 при p<0,001) и повышенное содержание кобаламина (F=4,29 при p<0,01) является определяющим фактором в прогрессировании уже сформировавшейся близорукости.
Роль макро- и микроэлементов в многообразных функциях организма и каждой клетки в отдельности не вызывает сомнения. Установлено, что для лиц с близорукостью в сочетании с ВИДС характерно недостаточное поступление ряда элементов с продуктами питания, в частности Ca, Na, Cl, Co, Mo, Cr и F.
Анализ содержания элементов в сыворотке крови показал (рис. 11), что при близорукости выявлено достоверное снижение в сыворотке крови меди (1133,3 + 26,2 и 876,7 + 52,0 соответственно при p<0,05), магния (1,49 + 0,16 и 0,7 + 0,15 соответственно при p<0,05), селена (97,22 + 5,18 и 84,0 + 0,89 соответственно при p<0,001), олова (1,53 + 0,07 и 0,71 + 0,14 соответственно при p<0,001) и кобальта (0,8 + 0,07 и 0,41 + 0,11 соответственно при p<0,05). При этом алиментарная эссенциальная недостаточность установлена только по кобальту.
 Рисунок 11. Содержание микроэлементов в сыворотке крови у лиц с близорукостью по отношению к лицам с эмметропической рефракцией.
Рисунок 11. Содержание микроэлементов в сыворотке крови у лиц с близорукостью по отношению к лицам с эмметропической рефракцией.По-видимому, при близорукости потребность в данных микроэлементах повышена по сравнению с эмметропической рефракцией и потери данных элементов при близорукости превалируют над поступлением их с пищей. Показано также, что недостаточность Zn (F=40,5; p<0,001), Cu (F=17,4; p<0,001) и Ni (F=10,4; p<0,001) является одним из факторов, усиливающим степень астигматизма. При этом наиболее значимыми микроэлементами для полноценного функционирования иммунной системы является цинк и медь.
Кроме ухудшения зрения вдаль, первым признаком близорукости является повышенная зрительная утомляемость, затем появляются жалобы на головную боль в лобной части головы, слезотечение, плавающие мушки перед глазами и прочие. В результате статистического анализа было установлено влияние уровня содержания макро- и микроэлементов на вышеперечисленные симптомы у коренного населения Севера – это недостаточность Cu (F=2,4 при p<0,05), P (F=4,0 при p<0,01), Zn (F=3,4 при p<0,01) и повышение таких иммунотоксических микроэлементов, как Ni и Sb. Проведенный дисперсионный анализ в обследованной группе коренных народностей Севера достоверно показал наличие как протективных (Cu, Sn, Co, Zn) микроэлементов, сдерживающих прогрессирование уже сформировавшейся близорукости, так и ассоциативных микроэлементов (Se, Ni, Sb, V и Mo) в сыворотке крови, оказывающих влияние на рост степени близорукости.
Таким образом, насыщение нутриентами, обеспечивающими физиологические потребности функциональных структур органа зрения, зависит от их экзогенного поступления, транспорта и распределения в организме, а также от наличия или отсутствия ВИДС. Отсюда следует, что регуляция потока элементов дает возможность определенным образом обеспечивать деятельность не только зрительного анализатора, но и иммунной системы, их функциональную активность и определять принципы диетической коррекции близорукости и ВИДС.
Полученные результаты позволили сформулировать предположение о том, что позитивное терапевтическое влияние на один из патогенетически связанных процессов (ВИДС – близорукость) может позитивно сказаться как на течении частой инфекционно-воспалительной заболеваемости, так и близорукости. При проведении лечебных мероприятий группа ВИДС с близорукостью была разделена на две подгруппы. Первая получала традиционную схему терапии (схема 1), вторая - наряду с традиционной терапией иммуноактивную (схему 2). Иммуноактивная терапия включала тактивин в суммарной дозе 28 мл на курс, нуклеинат натрия в суммарной дозе 12 граммов и комплекс аминокислот, элементов, витаминов в виде пищевой добавки. Обследование проводилось дважды: первый раз – до назначения лечебных мероприятий, второй – через год после назначенного лечения. После лечения с использованием иммунотропных препаратов клиническая эффективность в 2,5-3 раза была выше, чем после лечения по базовому способу, что проявилось в стабилизации близорукости в 85,7 % случаев. При этом рост остроты зрения без коррекции в 2,3-4 раза был выше, увеличение аккомодативной способности в 1,7-2,8 раза, отмечалось снижение частоты развития, тяжести и длительности инфекционно-воспалительных заболеваний в 2-4 раза.
Клинические различия ассоциировались и с особенностями динамики лабораторных показателей (табл. 5; 6). Это проявилось достоверным ростом активированных лимфоцитов (CD38: 22,13+1,1 и 17,06+1,18 соответственно при p<0,01), Th лимфоцитов (CD4: 34,12+1,47 и 28,16+2,41 соответственно при p<0,05), NK-клеток (CD16: 17,62+1,37 и 12,44+1,0 соответственно при p<0,01) и снижением маркеров активации иммунокомпетентных клеток (CD25: 2,39+0,14 и 3,35+0,27 соответственно при p<0,01; CD34: 0 и 0,58+0,05 соответственно при p<0,05), апоптоза (CD95: 17,67+0,88 и 24,5+0,5 соответственно при p<0,001), IgM (1,66+0,13 и 2,2+0,18 соответственно при p<0,05).
Важным доказательством влияния зрительного анализатора на характеристики системы иммунитета является то, что у лиц с близорукостью в сочетании с ВИДС, получавших схему 1 (без иммуноактивной и метаболической терапии), наблюдались положительные изменения лабораторных показателей системы иммунитета – рост NK-клеток (19,92+4,38 и 9,93+0,59 соответственно при p<0,05) и клеток, экспрессирующих рецепторы к трансферрину (0,37+0,04 и 0,28+0,03 соответственно при p<0,05) на фоне снижения В-лимфоцитов (5,52+1,35 и 9,03+0,81 соответственно при p<0,05).
Таблица 5
Содержание субпопуляций МНК в группе «ВИДС-близорукость», пролеченных по различным схемам, %
| Показатели | Схема 1 (n=32 чел.) | Схема 2 (n=24 чел.) | |||
| До лечения | После лечения | До лечения | После лечения | ||
| Субпопуляции мононуклеарных клеток (CD) | 38 | 25,25 + 0,85 | 25,33 + 1,64 | 17,06 + 1,18 | 22,13 + 1,1 ** |
| 8 | 28,29 + 1,85 | 32,07 + 4,1 | 24,65 + 1,92 | 30,6 + 2,93 | |
| 4 | 37,24 + 2,71 | 38,7 + 2,3 | 28,16 + 2,41 | 34,12 + 1,47 * | |
| 3 | 59,06 + 1,49 | 60,9 + 2,7 | 54,45 + 3,53 | 55,78 + 3,59 | |
| DR | 10,58 + 0,81 | 14,27 + 2,6 | 12,97 + 0,88 | 11,56 + 0,43 | |
| 71 | 0,28 + 0,03 | 0,37 + 0,04 * | 0,23 + 0,05 | 0,23 + 0,05 | |
| 25 | 1,53 + 0,13 | 1,62 + 0,51 | 3,35 + 0,27 | 2,39 + 0,14 ** | |
| 34 | 0 | 0 | 0,58 + 0,05 | 0 * | |
| 16 | 9,93 + 0,59 | 19,92 + 4,38 * | 12,44 + 1,0 | 17,62 + 1,37 ** | |
| 95 | 27,48 + 1,79 | 29,0 + 1,77 | 24,5 + 0,5 | 17,67 + 0,88 *** | |
