Клинико-лабораторная характеристика и лечение хламидийной инфекции, ассоциированной с генитальными микоплазмами 14. 01. 10- кожные и венерические болезни 14. 03. 09- клиническая иммунология, аллергология
| Вид материала | Автореферат |
- Урогенитальный хламидиоз: клинико-иммунологическая характеристика, иммуногенетические, 872.18kb.
- Оптимизация лечения варикозной экземы, ассоциированной с микотической инфекцией,, 427.97kb.
- Клинико иммунологические особенности аллергодерматозов на фоне урогенитальной инфекции, 335.48kb.
- Расписание занятий на элективе для студентов 6 курса «Клиническая аллергология», 41.99kb.
- Обоснование применения пармелии в комплексной терапии экземы (клинико-экспериментальное, 349.46kb.
- Клиническая, медико-правовая оценка дефектов оказания дерматовенерологической помощи, 171kb.
- Оптимизация фармакотерапии плоского лишая 14. 00. 25. фармакология, клиническая фармакология, 214.56kb.
- Клинико-лабораторная характеристика вич-инфекции у беременных и рожденных ими детей, 295.89kb.
- Задачи по оказанию доврачебной помощи при неотложных состояниях 43 акушерство, 1884.21kb.
- Комплексная фармакотерапия тяжелых форм псориаза с учетом биохимических и иммунологических, 211.59kb.
На правах рукописи
Ахмедов Хотамджон Бахромалиевич
Клинико-лабораторная характеристика и лечение хламидийной инфекции, ассоциированной с генитальными микоплазмами
14.01.10- кожные и венерические болезни
14.03.09- клиническая иммунология, аллергология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва- 2011
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Российский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
| Научные руководители: | Доктор медицинских наук, профессор И.В. Хамаганова |
| | |
| | Доктор биологических наук, профессор С.С. Хромова |
| | |
Официальные оппоненты:
доктор медицинских наук, профессор В.И.Кисина
доктор медицинских наук, профессор И.Г. Козлов
Ведущее учреждение: Московский государственный медико-стоматологический университет
Защита диссертации состоится “30” мая 2011 г. в 14.00 часов на заседании диссертационного совета Д 208.072.10 при ГОУ ВПО РГМУ Росздрава по адресу: 117997, Москва, ул. Островиятнова, дом 1
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО РГМУ Росздрава по адресу: 117997, Москва, ул. Островиятнова, дом 1
Автореферат разослан «29» апреля 2011г.
Ученый секретарь диссертационного совета,
доктор медицинских наук, профессор И.В.Хамаганова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы
По данным Всемирной Организации Здравоохранения каждый день во всем мире около одного миллиона человек заражаются инфекциями, передаваемыми половым путем (ИППП). ВОЗ утвердила глобальную стратегию на 2005- 2015 гг. «Предотвращение и контроль инфекций, передаваемых половым путем». В последние годы в Российской Федерации были пересмотрены многие нормативно-правовые документы, которые касаются разработки и внедрения в практику здравоохранения новых подходов к тактике ведения больных ИППП. Особое внимание исследователей обращено на воспалительные заболевания урогенитального тракта (Рюмин Д.В., 2009, Brill J.R., 2010), которые характеризуются нарушением микробиоценоза и развитием иммунологической недостаточности. При этом дисбиотические изменения определяются не только присутствием патогенов, таких как хламидии и микоплазмы, но составом и степенью репродукции условно-патогенной микрофлоры ( Рахматулина М.Р., 2009, Meyer T., 2009). В результате, случаи микст-инфекций могут сопровождаться развитием урогенитальных заболеваний, вызванных моноинфекциями. Известно, что от процесса взаимодействия иммунной системы с возбудителем во многом зависит течение и исход инфекций. Клинические наблюдения показали, что лечение заболеваний урогенитального тракта (УГТ) осложняется персистирующим характером течения инфекций и развитием рецидивов примерно в 10-15 % случаев. Этот факт послужил основанием для применения иммунотропных препаратов в комплексной терапии хламидийной инфекции (Баринова А.Н., Плавинский С.Л., 2010;. Гриценко В.А., Андрейчев В.В., 2010).
Вопрос о выборе комплексной терапии и контроле ее эффективности активно изучается. Применение иммуномодулятора с прямым антимикробным действием диктует необходимость проведения иммунологического и микробиологического мониторинга. Собранная к настоящему времени научная информация свидетельствует об актуальности проблемы исследования микробиологического и иммунного статуса пациентов, страдающих воспалительными заболеваниями урогенитального тракта, обусловленными хламидийной инфекцией, ассоциированной с микоплазмами, как с диагностической целью, так и для контроля проводимой терапии.
Цель исследования: – Разработка тактики терапии хламидийной инфекции, ассоциированной с микоплазмами, на основе результатов изучения клинического, микробиологического и иммунного статуса пациентов.
В соответствии с целью исследования были поставлены следующие задачи:
1. Изучить состояние микробиоценоза органов мочеполовой системы больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами, с помощью микробиологического метода и метода амплификации нуклеиновых кислот (ПЦР в реальном времени).
2. Провести сравнительную оценку спектра клинических проявлений хламидийной инфекции, ассоциированной с генитальными микоплазмами, в зависимости от качественного состава и количественного содержания микробиоценоза органов мочеполовой системы обследованных больных.
3. Оценить интерфероновый статус больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами, путем определения продукции интерферонов α и γ (IFNα, IFNγ) в пробах периферической крови и клиническом материале органов мочеполовой системы.
4. Оценить цитокиновый профиль в пробах периферической крови и органов мочеполовой системы больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами, путем определения провоспалительных (ИЛ-1, ИЛ-6, ИЛ-8, ФНО. ФНОα) и противовоспалительных (ИЛ-2, ИЛ-10, ИЛ-12, ИЛ-18) цитокинов.
5. Провести лечение больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами, антибактериальным препаратом (азитромицин) изолированно и в сочетании с иммунотропным препаратом (суперлимф-комплекс природных цитокинов и противомикробных пептидов).
Научная новизна
- Анализ результатов бактериологических и молекулярно-биологических исследований, проведенных у больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами, позволил определить наличие дисбиоза органов мочеполовой системы, характеризующегося высоким уровнем диссеминации Ctaphylococcus spp., Streptococcus spp., Enterococcus, Corinebacterium spp., С.albicans, Gardnerella vag., достоверно превыщающим аналогичные показатели здоровых лиц.
- Получены клинико-лабораторные данные о спектре клинических проявлений хламидийной инфекции, ассоциированной с генитальными микоплазмами, в зависимости от видового состава и количественного содержания последних и сопутствующих нарушений микробиоценоза органов мочеполовой системы.
- На основании иммунологических исследований, проведенных у больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами, установлены снижение продукции α и γ-интерферонов, дисбаланс в системе цитокинов на системном и локальном уровне, что служит обоснованием для включения в комплексную терапию иммунотропного препарата (суперлимф).
Практическая значимость
Предложен эффективный этиопатогенетически обоснованный метод лечения хламидийной инфекции, ассоциированной с генитальными микоплазмами (M.genitalium, U.urealyticum), заключающийся в применении антибактериального препарата (азитромицин) и комплекса природных цитокинов и противомикробных пептидов (суперлимф), показавший высокую клиническую и микробиологическую эффективность.
В качестве лабораторных показателей при оценке эффективности терапии хламидийной инфекции, ассоциированной с генитальными микоплазмами, предложено использовать результаты бактериологической оценки состояния микробиоценоза органов мочеполовой системы, а также определения видового состава количественного содержания генитальных микоплазм (U.urealyticum, U.parvum, M.hominis).
Положения, выносимые на защиту
- Для клинического статуса пациентов с воспалительными урогенитальными заболеваниями, обусловленными хламидиями и микоплазмами, характерно нарушение состава микробиоценоза урогенитального тракта, снижение уровня продукции интерферонов ИФН и ИФН , дисбаланс в системе провоспалительных и противовоспалительных цитокинов.
- Применение иммунотропного препарата в комбинированной терапии пациентов с хламидийной инфекцией, ассоциированной с микоплазмами, приводит к нормализации состава микрофлоры УГТ, повышению продукции интерферонов и выявлению ранее не определяемых интерлейкинов с восстановлением баланса в системе цитокинов.
- Применение монотерапии препаратом джозамицин и комплексной терапии (антибиотик азитромицин и иммунотропный препарат) приводит к этиологическому выздоровлению у 97 % обследованных пациентов с урогенитальной хламидийной инфекцией, ассоциированной с микоплазмами.
Внедрение результатов работы.
Результаты работы используются в клинической практике КВКД №1
Апробация работы. Материалы диссертации доложены в МОНИКИ на конференции «Актуальные вопросы дерматовенерологии и дерматоонкологии», 2008г., на юбилейной конференции РГМУ «Актуальные проблемы диагностики и терапии в дерматовенерологии, 2009г., на конференции РМАПО «Урогенитальные инфекции и репродуктивное здоровье», 2010 г.
Публикации. По материалам диссертации опубликовано 9 научных работ в отечественной и зарубежной печати, в том числе 3 статьи в журналах, рекомендованных ВАК Российской Федерации.
Структура и обьем диссертации. Работа изложена на 122 страницах машинописного текста. Состоит из введения, обзора литературы, материалов и методов исследования, результатов собственных исследований, обсуждения, выводов, практических рекомендаций и списка литературы, который включает 107 ссылок (на 60 отечественных и 47 зарубежных публикации).
СОДЕРЖАНИЕ РАБОТЫ
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Клиническое обследование и лечение пациентов проводилось на кафедре дерматовенерологии РГМУ, исследование микробиологического и иммунного статуса - на кафедре микробиологии и вирусологии РГМУ. В период с 2007г. по 2010 г. на базе кафедры дерматовенерологии лечебного факультета и кафедры микробиологии и венерологии РГМУ им. Н.И.Пирогова проведены комплексное клинико-лабораторное обследование и лечение 140 пациентов в возрасте от 22 до 47 лет, которые условно были разделены на 2 группы. Основную группу составили 98 больных урогенитальными заболеваниями, обусловленными хламидийной инфекцией (30 пациентов) или хламидийной инфекцией, ассоциированной с генитальными микоплазмами (M.genitalium. M.hominis, U.urealyticum, U.parvum) (68 больных). Контрольную группу составили 42 пациента аналогичного возраста, обратившихся на амбулаторный прием в КВД № 1 для профилактического обследования. Фармакотерапия проведена 98 больным основной группы, условно разделенных на 3 группы: больные группы I (30 больных хламидийной инфекцией) получали стандартное лечение однократной дозой азитромицина 1,0 г в сутки; больные группы II (44 больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами) получали лечение азитромицином один раз в сутки по схеме: 1-й день – 500 мг, следующие 4 дня – по 250 мг внутрь. Пациентам группы III (24 больных) одновременно с курсовым лечением азитромицином (аналогично больным группы II) назначали препарат, содержащий комплекс природных цитокинов и противомикробных пептидов – суперлимф. Препарат назначали один раз в сутки в дозе 25 мкг в форме свечей, вводимых per rectum (мужчины) и per vaginus (женщины) в течение 10 дней.
Методы исследования
| Наименование метода |
|
При изучении микробиоты УГТ примененяли культуральний метода (посев материала из урогенитального тракта на селективные питательные среды)
Иммунологические исследования включали:
1. определение продукции интерферонов на системном (пробы периферической крови) и локальном (соскобы УГТ) уровнях;
2. оценку продукции провоспалительных(IL-1, IL-6, IL-8, TNF) и противовоспалительных цитокинов (IL-2, IL-12, IL-18), регуляторного фактора IL-10 с помощью метода обратной транскрипции-амплификации (ОТ-ПЦР) на присутствие мРНК цитокинов в пробах периферической крови и соскобов УГТ.
В работе были использованы пары праймеров для следующих цитокинов: ИФН-и , ИЛ-6, ИЛ-8, ИЛ-1ß, ИЛ-2, ИЛ-4, ИЛ-10 ФНО, ИЛ-18 , ИЛ-12 .
Иммунологические исследования проводили одновременно с оценкой клинического и микробиологического статуса данного пациента.
До и после лечения всем пациентам проводилось исследование местного статуса, клинических лабораторных показателей с констатацией результатов иммунологических и микробиологических исследований.
В контрольную группу были включены клинически здоровые лица, обратившиеся в КВКД № 1 на амбулаторный прием с целью профилактического обследования. Лицам в контрольной группе (n= 42; средний возраст 25,5± 2,5 года) проводилось клиническое и лабораторное обследование в том же объеме, что и в основной группе.
Статистическая обработка данных
Анализ и обработка статистических данных выполнялись на персональном компьютере с использованием пакета программ EXCEL 2003 и STATISTICA 6. Проводилось сравнение групп данных с использованием непараметрических критериев: Sign test (знаковый критерий) и Wilcoxon test (критерий Вилкоксона). Вычислялись также коэффициенты корреляции по Спирмену (Spearman Rank Order Correlations) для выявления связи с дискретными показателями. Результаты представлены с использованием следующих уровней значимости различий p< 0,05; p < 0,01; p< 0,001.
Результаты исследования и их обсуждение
Этиологическая структура микробиоценоза урогенитального тракта пациентов перед проводимой терапией
Перед терапией были обследованы 98 пациентов. Анализ результатов молекулярно-биологических методов исследований (ПЦР и ПЦР в реальном времени) показал, что C.trachomatis обнаружены у всех 98 пациентов основной группы, при этом в сочетании с генитальными микоплазмами (M.genitalium, U.urealyticum, U.parvum, M.hominis) – у 68 обследованных (31 мужчина и 37 женщин)
При использовании метода ПЦР в реальном времени у 47 пациентов I группы (20 мужчин и 27 женщин) U.urealyticum, U.parvum, M.hominis были обнаружены в количестве более 104/мл, у остальных больных количественное содержание микроорганизмов составило менее 103/мл
Выявленные возбудители находились в ассоциации с патогенной (C.trachomatis) и условно-патогенной микрофлорой (табл. 1- 3).
Фармакотерапия проведена 98 больным основной группы, условно разделенных на 3 группы: больные группы I (30 больных хламидийной инфекцией) получали стандартное лечение однократной дозой азитромицина 1,0 г в сутки; больные группы II (44 больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами) получали лечение азитромицином один раз в сутки по схеме: 1-й день – 500 мг, следующие 4 дня – по 250 мг внутрь. Пациентам группы III (24 больных) одновременно с курсовым лечением азитромицином (аналогично больным группы II) назначали препарат, содержащий комплекс природных цитокинов и противомикробных пептидов – суперлимф. Препарат назначали один раз в сутки в дозе 25 мкг в форме свечей, вводимых per rectum (мужчины) и per vaginus (женщины) в течение 10 дней.
Таблица 1 Результаты микробиологического исследования клинического материала урогенитального тракта пациентов перед проводимой терапией (данные представлены в КОЕ/мл клинического материала и Log10)
| Состав микрофлоры УГТ | КОE/мл (Log 10 ) | Норма |
| Staphylococcus spp. | 10 4 -109 (3-7,58) | 103-104 (3-4) |
| Streptococcus spp. | 104 - 108 ( 6-8 ) | 104- 05 (4-5) |
| Peptostreptococcus spp. | 105 - 10 7 (5, 89-7,7) | 10 3 -10 4 (3-4) |
| Gardnerella vaginalis | 104 - 109 (4,7-10,4 ) | < 104 (<4) |
| Дрожжеподобные грибы рода Candida | 104 - 109 (3,41-9) | < 105 (<5) |
| Corinebacterium spp. | 103- 109 (3,4-10) | 103-104 (3-4) |
| Bacterides spp. | 104 - 108 (4-8,6) | 102 (<2) |
| Enterococcus spp. | 104- 108 (4-8) | 102 (<2) |
| Lactobacillus | (-) - 107 | 106-8 |
Таблица 2 Показатели микробиологического исследования клинического материала урогенитального тракта обследуемых пациентов основной группы перед проведением комплексной терапии (с учетом показателей нормы для женщин и мужчин)
| Состав микрофлоры УГТ | Показатель КОЕ/мл клинического материала | |||
| min | max | норма | ||
| жен | муж | |||
| Staphylococcus spp. | 104 | 109 | 104 | 102 |
| Streptococcus spp. | 104 | 108 | <103-5 | 102 |
| Peptostreptococcus spp. | 105 | 107 | 104 | 102 |
| Gardnerella vaginalis | 104 | 109 | 104 | 102 |
| Дрожжеподобные грибы рода Candida | 104 | 109 | <103 | 102 |
| Corinebacterium spp. | 102 | 109 | 102 | 102 |
| Bacterides spp. | 104 | 108 | <104 | 102 |
| Enterococcus spp. | 104 | 108 | 102-4 | 102 |
| Lactobacillus | (-) | 108 | 106-8 | 102 |
Таблица 3. Показатели состава микрофлоры в клиническом материале урогенитального тракта пациентов перед проведением терапии (КОЕ/мл клинического материала Log10)
| Микроорганизмы | Показатели уровня роста микроорганизмов до терапии / норма | |
| женщины | мужчины | |
| Staphylococcus spp. | 4-7,6 / <4 | 3-7 / <3 |
| Streptococcus spp. | 5-8 / <5 | 6-8 / <5 |
| Peptostreptococcus spp. | 4-7,7 / <4 | 3-7 / <3 |
| Gardnerella vaginalis | 7-9,9 / <4 | 4,7-6 / <3 |
| Дрожжеподобные грибы рода Candida | 4-9 / <5 | 4-6 / <3 |
| Corinebacterium spp. | 3-9 / <3 | 4,3-9 / <3 |
| Bacterides spp. | 4-7 / <4 | 3-6 / <3 |
| Enterococcus spp. | 5,8-7 / <5 | 6-8 / <5 |
| Lactobacillus | Отсут-6 / 6-8 | Отсут-3 / <3 |
Группу сравнения составили 25 здоровых добровольцев.
Были получены достоверные данные (р<0,05) относительно уровней значимости различий при сравнении результатов обследования пациентов 1) до терапии и 2) после комплексной терапии, а также и 3) монотерапии. Комплексная терапия приводила к восстановлению нормальной микрофлоры УГТ. До терапии отмечены случаи с нормальным уровнем отдельных видов микробиоты.
Установлено, что проводимая терапия целесообразна в плане как элиминации патогенов, так и восстановления степени роста нормальной микрофлоры. Это указывает на целесообразность определения состава микробиоты УГТ в качестве критерия диагностики и контроля проводимой терапии.
Результаты оценки интерферонового статуса пациентов перед
проводимой терапией
а) Определение интерферон - продуцирующей способности клеток периферической крови (исследование на системном уровне)
При тестировании проб периферической крови учитывали тот факт, что интерфероны I типа, в частности IFN (ИФН), вырабатывают преимущественно фагоциты и лейкоциты ( В-клетки ), а IFN (ИФН) - активированные Т - и NK-клетки). Оценка продукции интерферонов α- и - показала следующее:
- у всех пациентов снижена продукция IFN. Титры составили от 1:10 до 1:40 (Log10 =3,3-5,32) , при норме 1:128-1:640;
-у большинства пациентов продукция IFN резко снижена или соответствует нижней границе нормы. Титры составили от 1:4 до 1:32 (Log10= 2-5) при норме 1:32- 1:256 (5-8)
б) Определение интерферон-продуцирующей способности клеток в пробах соскобов УГТ (исследование на локальном уровне) (Рис.2 и 3)
- продукция IFN в соскобах УГТ снижена у всех больных. Определяемые титры находились в пределах 1:10 -1:40 или были ниже нормы ( у добровольцев титры IFN в соскобах составили 1:40 – 1:160, Log10 =5,32- 7,3)
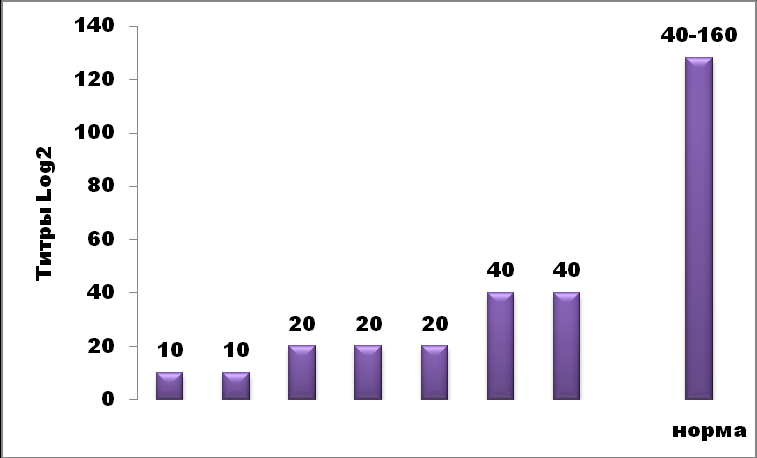
Рис 1. Титры IFN в пробах соскобов перед терапией у 7 пациентов с урогенитальной хламидийной инфекцией, ассоциированной с микоплазмами
- продукция IFN (титры1:2-1:16) была также снижена ( у добровольцев титры IFN в соскобах составили 1:16-1:32)

Рис 2. Титры IFN в пробах соскобов у 8 пациентов с урогенитальной хламидийной инфекцией, ассоциированной с микоплазмами
Данные по исследованию уровней интерферонов у пациентов до лечения суммированы в таблице 2.
Таблица 4. Показатели продукции интерферона у обследованных пациентов до лечения, Ед\мл [Log2 (титр-1), Mm]
| Уровень ИФН | Периферическая кровь | Клинический материал УГТ |
| ИФН Мm (min -max) c присутствием хламидий микоплазм Норма ИФНα | *4,5 0,87 (3,32 - 5,3) *4,54 1,0 (3,3 - 6,3) 7,8 0,8 (7- 9) | 3,8 0,9 (3,32 – 5,3) 3,9 1,0 (3,32 - 5,3) 6,301,0 (5,3-7,3) |
| ИФН Mm (min -max) c присутствием хламидий микоплазм | *3,3 0,9 (2,3-4,8) *3,6 1,2 (2,4-4,8) | * 2,0 0,9 (1,0 - 3,8) * 2,2 0,6 (1,8 – 3,8) |
| Норма ИФН | 6,50 0,27 (5-8) | 3,60 1,0 (3,0 5,0) |
* достоверные отличия относительно нормы (P< 0,05)
Результаты показали следующее: - в пробах крови больных уровень IFNα составил в среднем Log2= 4,5 по сравнению с показателями Log10 от 7 до 9 в норме; уровень IFN составил в среднем Log2= 3,3 (3,6) по сравнению с показателями от 5 до 8 в норме. - в пробах соскобов УГТ больных уровень IFNα в целом ряде случаев достоверно отличался от нормы, составляя в среднем Log2 = 3,8-3,9 по сравнению с показателями от 5 до 7 в норме. При оценке уровня IFN в соскобах УГТ у большинства пациентов также выявлены достоверные отличия.
Таким образом, полученные данные указывают на достоверное снижение продукции интерферонов на системном и локальном уровнях, что предполагает целесообразность проведения анализа соскобов УГТ при диагностическом обследовании пациентов.
Микробиологический контроль проводимой терапии
При исследовании этиологической структуры УГТ и факторов иммунной системы пациентов после препаратом азитромицин установлено, что монотерапия азитромицином приводит к элиминации патогенов (хламидий, микоплазм). Однако одновременно отмечено резкое снижение роста сопутствующих микроорганизмов (ниже значений нормы), что приводило к изменению количественного и качественного состава нормальной микрофлоры и развитию у части больных дисбиотических нарушений на уровне урогенитального и желудочно-кишечного трактов.
Учитывая полученные данные, была использована комплексная терапия, включающая сочетание азитромицина и иммунотропного препарата (суперлимф), который, как ранее было установлено в системе in vitro, способствует выходу патогена из состояния с замедленным репликативным уровнем жизненного цикла (цитоплазматические включения), повышению доступности к антибиотикам, что в определенной мере было продемонстрировано при лечении больных с хронической хламидийной инфекцией. Результаты микробиологического мониторинга после комплексной терапии препаратами азитромицин+ иммуномодулятор представлены в таблице 3, рис. 6-8.
Таблица 5 Показатели состава микрофлоры УГТ пациентов до и после проведения комплексной терапии антибиотик+суперлимф, Log
| Возбудители | Перед лечением М±m | После лечения М±m | Р (U-test) | P |
| Staphylococcus spp. | 5,91±1,00 | 3,91±0,80 | 0,14 | >0,05 |
| Gardnerella vaginalis | 7,90±0,87 | 4,54±1,04 | 0,04 | <0,05 |
| Streptococcus spp. | 6,65±0,56 | 1,85± 0,05 | 0017 | <0,05 |
| Дрожжеподобные грибы рода Candida | 5,38±0,57 | 1,93±0,13 | 0,0001 | <0,001 |
| Enterococcus spp. | 7,37±0,58 | 4,07±0,53 | 0,02 | <0,05 |
Рис. 3 Стафилококки
Уровень роста стафилококков до (1) и после (2) комплексной терапии у 5 пациентов с хламидийной инфекцией, ассоциированной с микоплазмами

Рис.4 Энтерококки
Уровень роста энтерококков до(1) и после (2) комплексной терапии у 4-х пациентов с хламидийной инфекцией, ассоциированной с микоплазмами
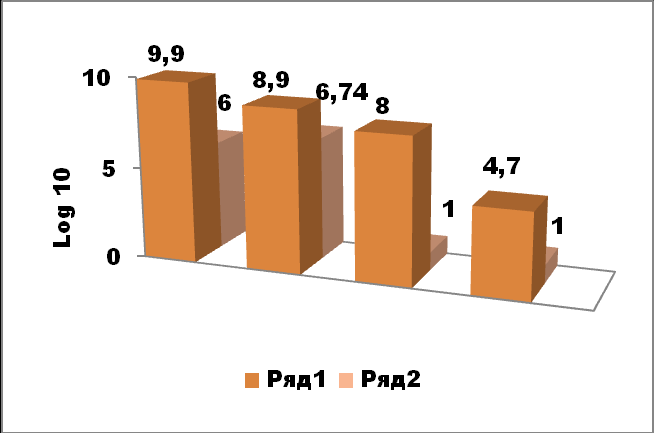
Рис.5 Гарднереллы
Уровень роста гарднерелл до (1) и после (2) комплексной терапии у 4-х пациентов с хламидийной инфекцией, ассоциированной с микоплазмами

Рис.6 Дрожжеподобные грибы рода Candida
Уровень роста Candida до(1) и после (2) комплексной терапии у 7 пациентов с хламидийной инфекцией, ассоциированной с микоплазмами
Таким образом, микробиологический контроль служит важным звеном оценки эффективности терапии с применением иммунотропных средств при урогенитальной хламидийной инфекции, ассоциированной с микоплазмами.
Оценка интерферонового статуса пациентов после проводимой терапии
Результаты оценки продукции интерферонов у обследованных пациентов представлены в Таблице 4 и на Рис. 8-12.
Таблица 6. Оценка продукции ИФН до и после комплексной терапии джозамицин+ иммунотропный препарат ( n=18)
| Уровень ИФН | Периферическая кровь | Соскобы УГТ |
| ИФН Мm( min-max) Перед терапией (а) Комплексная терапия(б) Монотерапия (в) Норма | 4,320,771 (3,3 – 5) 6,0 0,798 (4,32-6,3) 4,36 0,6 (3,3 - 4,32) 7,8 0,8 (7- 9) | 3,8 0,687 (3,3-4,32) 5,180,611 (4,32- 6,3) 3,500,6 (3,3 -4,32) 6,301,0 (5,3-7,3) |
| ИФН Mm (min-max) Перед терапией (а) Комплексная терапия(б) Монотерапияв\(в) Норма | 3,3 0,632 (2,3-4,8) 4,90 0,502 (4,32-5,3) 3,3 0,6 (2,3 – 4,32) 6,50,27 (5 -8 ) | 2,00,680 (1,0 -4,32) 4,740,592 (4,32-5,3) 2,0 0,6 (1,0-4,32) 4,01,0 (4,0-5,0) |
Достоверные отличия: (а)- (б) р<0,05; (б) - (в) р<0,05. Недостоверные отличия: (а) – (в) р>0,5

Рис. 7 Уровни IFN в периферической крови 5 пациентов до (1) и после (2) комплексной терапии азитромицин +иммунотропный препарат
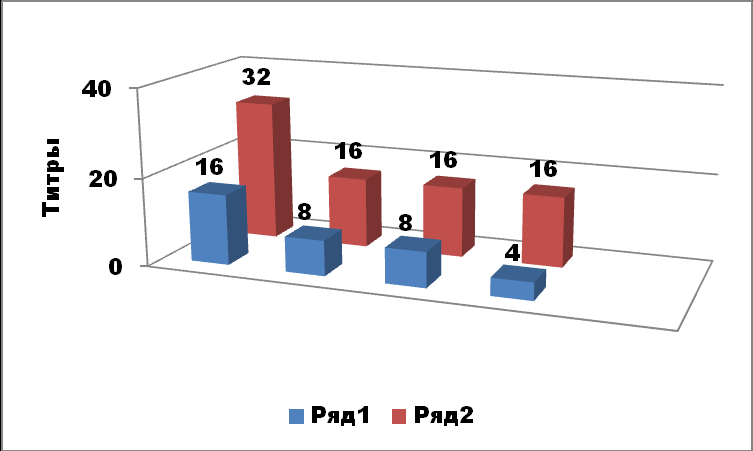
Рис. 8 Уровни IFN в соскобах УГТ 4-х пациентов до (1) и после (2) комплексной терапии азитромицин+ иммунотропный препарат

Рис. 9 Уровни IFN в периферической крови 4-х пациентов до(1) и после (2) монотерапии азитромицином
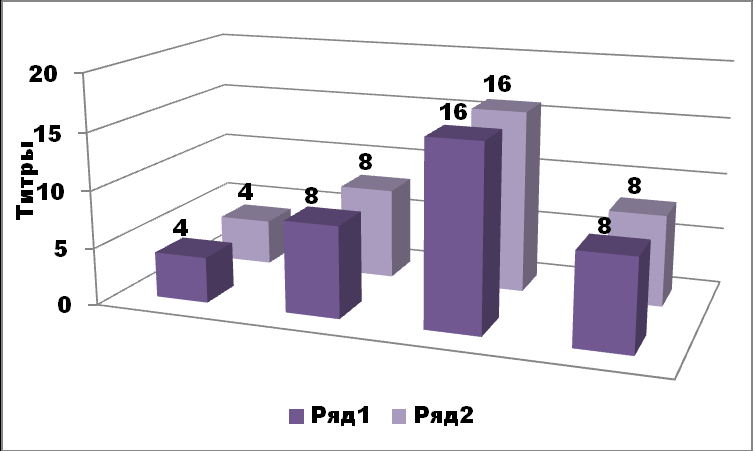
Рис. 10 Уровни IFN в соскобах УГТ 4-х пациентов до (1) и после (2) монотерапии азитромицином (исходные титры 1:4 -1:16 остались без
изменения)
Результаты оценки интерферонового статуса пациентов указывают на достоверное повышение ( р< 0,05) уровней интерферонов у 16 из 24 обследованных (66,6%) после проведения комплексной терапии.
Статистический анализ включал сравнение данных с использованием непараметрических критериев Sign test (знаковый критерий) и Wilcoxon test (критерий Вилкоксона), что позволило установить
а) достоверные различия в уровне продукции интерферонов в периферической крови и соскобах УГТ относительно исходного уровня;
б) закономерность – чем выше исходный уровень, тем выше уровень ИФН после терапии.
При вычислении коэффициентов по Спирмену (Spearman Rank Order Correlations) было показано, что существует корреляция между повышением уровней ИФН в крови и соскобах УГТ: r=0,675 (p<0,05).
Рис.11. Результаты оценки уровня интерферонов α – и - (А) и
уровня роста микрофлоры (Б) в материале из УГТ пациента Пав-ва с урогенитальной микст-инфекцией (С.trachomatis+M.hominis)
Комплексная терапия
А. Б.

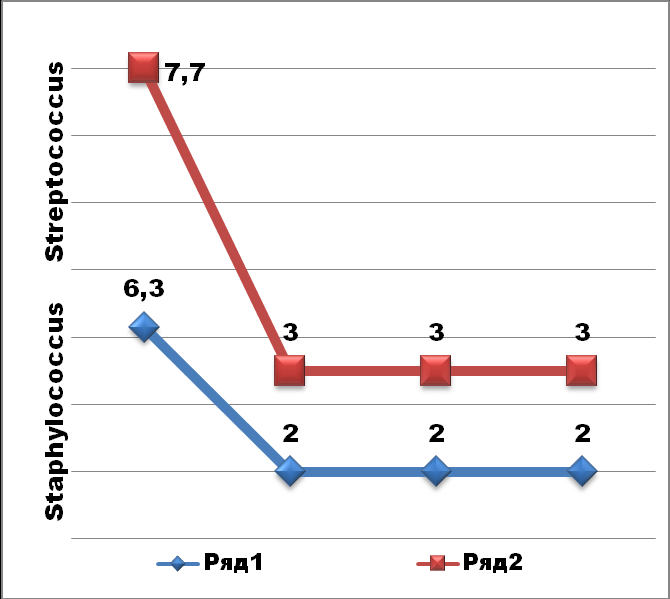
Рис.12. Показатели уровня интерферона α (А) и интерферона (Б) в материале из УГТ пациента И. с микст-инфекцией (C.trachomatis +M.genitalium+G.vaginalis). Комплексная терапия.
А. Б.

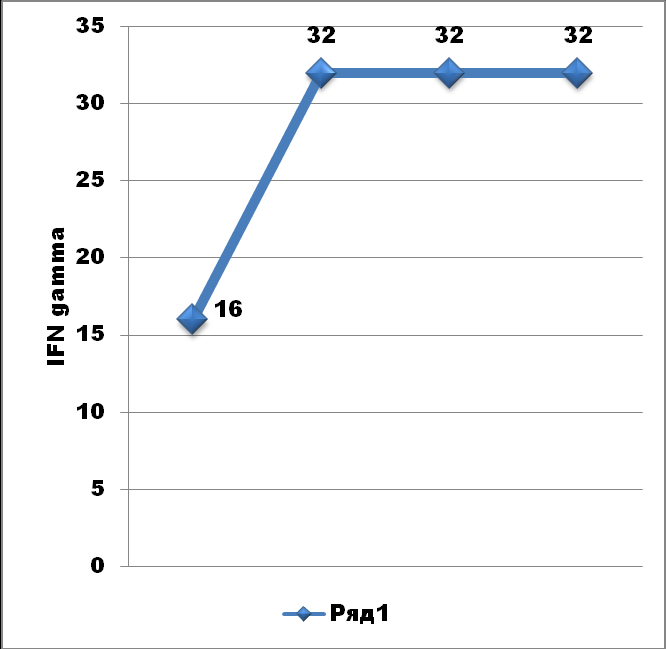
Рис.13. Показатели роста стрептококков и коринебактерий (А), энтерококков и гарднерелл (Б) в материале УГТ пациента И. с урогенитальной микст-инфекцией Комплексная терапия
А. Б.
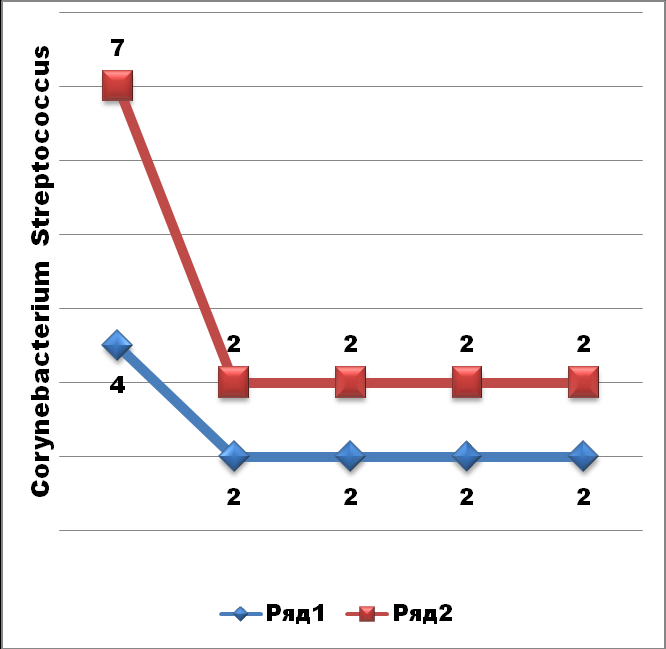

Определение мРНК цитокинов в пробах периферической крови
и соскобах УГТ
При исследовании цитокинов было установлено, что инфекции УГТ могут ассоциироваться с дисбалансом в системе цитокинов. При этом принимали во внимание механизмы действия интерлейкинов, в частности,
IL-1, который активирует лимфоциты и стимулирует макрофаги, до лечения отсутствовал в периферической крови у 20 % больных,
IL-2, фактора активации Т-клеток и макрофагов, который до терапии отсутствовал у 30 % больных, .
Определен исходно повышенный показатель выявления мРНК IL-6, который участвует в индукции белков острой фазы, а также IL-8 (хемокин), влияющего на секрецию нейтрофилами супероксида свободных радикалов.
Выявлены изменении в продукции IL-12, участвующего в индукции Th1-клеток, и IL-18, известного как кофактор индукции Th1-клеток в направлении выработки IFN и повышения активности NK-клеток (Таблица 5).
Таблица7. Показатели выявления мРНК цитокинов методом
ОТ-ПЦР до и после проведения комплексной терапии
(азитромицин+ иммунотропный препарат)
| Цитокины (периферическая кровь, соскобы) | Количество пациентов,% а) до терапии: б) после терапии: в) здоровые с выявленной изменение лица (%) с состава выявленной выявляемой в крови (* ) мРНК цитокинов _____________ | |
| IL-1 кровь соскобы УГТ | 20 10 | + 10 35 + 10 |
| IL-2 кровь соскобы | 10 10 | + 10 5 + 10 |
| IL-4 кровь соскобы | 50 50 | - 5 5 - 10 |
| IL-6 кровь соскобы | 60 65 | - 20 20 - 10 |
| IL-8 кровь соскобы | 20 30 | - 10 10 - 15 |
| IL-10 кровь соскобы | 20 10 | + 20 20 + 10 |
| IL-12 кровь соскобы | 50 50 | + 10 70 + 10 |
| IL-18 кровь соскобы | 40 20 | + 5 30 + 5 |
| TNF кровь соскобы | 60 70 | - 5 75 - 10 |
(*) данные Центра интерферонов и интерлейкинов ЦНИИЭМ им.Н.Ф.Гамалеи
Учитывая роль цитокинов как факторов иммунорегуляции, выявленное частичное восстановление состава цитокинов в крови и соскобах служит указанием положительного ответа организма на проводимую антибактериальную и цитокинотерапию.
ВЫВОДЫ
1 Установлено, что при хламидийной инфекции, ассоциированной с генитальными микоплазмами ( M.genitalium, U.urealyticum) отмечаются выраженные нарушения микробиоценоза органов мочеполовой системы – высокий исходный уровень диссеминации Staphylococcus spp., Streptococcus spp., Enterococcus spp., Corynebacterium spp., грибов Candida, Gardnerella vag., что достоверно превышает аналогичные показатели у здоровых лиц.
2. Диагностическое обследование пациентов с воспалительными заболеваниями урогенитального тракта, обусловленных хламидиями и/или микоплазмами, показало, что их клинический статус характеризуется нарушением микробиоценоза урогенитального тракта, снижением продукции - и - интерферонов и дисбалансом в системе цитокинов на системном (пробы периферической крови) и локальном (соскобы УГТ) уровнях. Это служит обоснованием для включения в комплексную терапию иммунотропных препаратов в сочетании с антибиотиками.
3. Установлено, что хламидийная инфекция, ассоциированная с генитальными микоплазмами ( M.genitalium, U.urealyticum) у 90% обследованных характеризуется:
- снижением продукции IFN; титры составили от 1:10 до 1:40 (Log2 =3,3-5,32) при норме 1:128-1:640; и резким снижением продукции IFN (в ряде случаев уровень достигал нижней границе нормы; титры составили от 1:4 до 1:32 (Log2= 2-5) при норме 1:32-1:256 (5-8);
- дисбалансом в системе цитокинов с выявлением провоспалительных цитокинов и отрицательным тестом на противовоспалительные цитокины (метод обратной транскрипции – ПЦР).
4. Доказана эффективность монотерапии антибиотиком (азитромицин) и комплексной терапии (антибиотик+суперлимф) для элиминации Chlamydia trachomatis, Mycoplasma genitalium (91% и 95 % соответственно) у больных хламидийной инфекцией, ассоциированной с генитальными микоплазмами, при этом комплексное лечение сопровождалось нормализацией состояния микробиоценоза органов мочеполовой системы.
5. Установлена высокая клиническая эффективность лечения хламидийной инфекции, ассоциированной с генитальными микоплазмами антибиотиком в комплексе с суперлимфом, а также нормализация показателей цитокинового и интерферонового статуса обследованных больных.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ Полученные результаты позволяют рекомендовать микробиологический анализ, исследование цитокинового и интерферонового статуса у пациентов со смешанными инфекциями урогенитального тракта, передаваемыми половым путем. Обоснована монотерапия азитромицином и комплексная терапия, включающая применение азитромицина в сочетании с иммуномодулятором (комплекс природных цитокинов противомикробных пептидов).
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Хамаганова И.В. Иммунотропные и фитотерапевтические средства в лечении больных с инфекциями урогенитального тракта / Хамаганова И.В. Погорельская Л.В., Хромова С.С., Ганковская Л.В.,. Ахмедов Х.Б, Башлыкова Г.В. // Сб. труд. науч.-практ.конф. МОНИКИ «Актуальные вопросы дерматовенерологии и дерматоонкологии». - М., 2008.- С.45- 47.
- Хамаганова И.В. Джозамицин в терапии смешанных инфекций, передаваемых половым путем /Хамаганова И.В., Карамова А.Э., Ахмедов Х.Б. // Сб.труд. юбилейной конф. РГМУ «Актуальные проблемы диагностики и терапии в дерматовенерологии», - М., 2008.- С.174-175.
- Хамаганова И.В. Современные подходы к диагностике смешанных инфекций урогенитального тракта. /Хамаганова И.В., Хромова С.С., Ахмедов Х.Б., Дегтярева Л.А. //В сб.труд. науч-практ. конф., посвященной 135-летию каф. кож. и вен. бол. Казанского мед.ин-та, - К., 2008.- С.27.
- Хромова С.С. Новый подход к терапии смешанных инфекций урогенитального тракта с применением иммунотропного препарата Суперлимф /Хромова С.С., Хамаганова И.В., Ганковская Л.В., Ахмедов Х.Б., Ковальчук Л.В. //Российский иммунологический журнал.- 2008.-Том 2 (11), - №2-3. - С.205.
- Хромова С.С. Микробиологические и иммунные аспекты развития инфекций урогенитального тракта /Хромова С.С. Хамаганова И.В. Тарабрина Н.П. Дегтярева Л.А., Ахмедов Х.Б., Кафарская Л.И. //Стерилизация и госпитальная инфекция. - 2009.- № 1.- С. 14-18.
- Хамаганова И.В. . Распространенность смешанной хламидийно-микоплазменной инфекции в условиях мегаполиса / Хамаганова И.В., Хромова С.С., Ахмедов Х.Б., Пивень Н.П., Разакова Р.Ю. // Российский журнал кожных и венерических болезней.-2009.-№2.-С.57-59.
- Ахмедов Х.Б.. Контроль эффективности комплексной терапии при урогенитальных хламидийных и/или микоплазменных инфекциях, передаваемых половым путем /Ахмедов Х.Б., Хамаганова И.В., Тарабрина Н.П., Ганковская Л.В., Мезенцева М.В., Хромова С.С. //Урогенитальные инфекции и репродуктивное здоровье. Материалы конференции 24-25 мая 2010г. Российская Ассоциация по Генитальным Инфекциям и Неоплазии, С. 13-14.
- Хамаганова И.В. Комплексная терапия антибиотиками, иммунотропными и пробиотическими. препаратами в реабилитации больных с инфекциями УГТ. /Хамаганова И.В., Хромова С.С., Тарабрина Н.П., Ахмедов Х.Б., Дегтярева Л.А. Материалы XI Межд.Конгресса по реабил. в медицине и иммунореабилитации Дубай- //Аллергология—Иммунология. - 2009,- т.10, - №1, - С.79.
- Хамаганова И.В. Эффект комбинированной терапии с использованием комплекса природных цитокинов и противомикробных пептидов при урогенитальных хламидийных и микоплазменных инфекциях /Хамаганова И.В., Ахмедов Х.Б., Тарабрина Н.П., Хромова С.С., Мезенцева М.В., Ковальчук Л.В., Ганковская Л.В., Дегтярева Л.А.//ЖМЭИ-2011г.- №1.- С.90-93.
СПИСОК СОКРАЩЕНИЙ
ИЛ (IL) - интерлейкин
ИФН (IFN) - интерферон
КОЕ - колониеобразующая единица
УГТ - урогенитальный тракт
ОТ-ПЦР - реакция обратной транскрипции – ПЦР (амплификации)
ПЦР (PCR) - полимеразная цепная реакция
ФНО (TNF) - фактор некроза опухоли
