Современная тактика системной радиотерапии хлоридом стронция-89 в комплексном лечении больных с метастатическим поражением костей 14. 00. 14 онкология 14. 00. 19 -лучевая диагностика и лучевая терапия
| Вид материала | Автореферат диссертации |
- Лучевая терапия различными видами ионизирующего излучения в комплексном лечении больных, 785.18kb.
- Комплексная лучевая диагностика в оценке репаративного процесса при лечении больных, 429.1kb.
- Стратегия и тактика лучевой терапии в многокомпонентном лечении местно-распространенного, 1026.52kb.
- Адъювантная лучевая терапия рака желудка. 14. 00. 14 онкология 14. 00. 19 лучевая диагностика,, 304.24kb.
- Рефлексотерапия в реабилитации больных поздними лучевыми повреждениями и паллиативной, 426.37kb.
- Нейтронная и нейтронно-фотонная терапия злокачественных новообразований слюнных и щитовидной, 340.88kb.
- Ультразвуковое исследование в комплексной лучевой диагностике злокачественных опухолей, 485.88kb.
- Селиверстов Павел Владимирович лучевая диагностика диспластически-дистрофического синдрома, 488.65kb.
- Селиверстов Павел Владимирович лучевая диагностика диспластически-дистрофического синдрома, 488.95kb.
- Трухачёва Наталия Геннадьевна офтальмосонография в комплексной диагностике опухолей, 456.47kb.
На правах рукописи
РЫЖКОВ АЛЕКСЕЙ ДМИТРИЕВИЧ
СОВРЕМЕННАЯ ТАКТИКА СИСТЕМНОЙ РАДИОТЕРАПИИ ХЛОРИДОМ СТРОНЦИЯ-89 В КОМПЛЕКСНОМ ЛЕЧЕНИИ БОЛЬНЫХ С МЕТАСТАТИЧЕСКИМ ПОРАЖЕНИЕМ КОСТЕЙ
14.00.14 - онкология
14.00.19 –лучевая диагностика и лучевая терапия
Автореферат диссертации на соискание учёной
степени доктора медицинских наук
МОСКВА – 2008
Работа выполнена в лаборатории радиоизотопной диагностики НИИ клинической онкологии ГУ Российского онкологического научного центра им. Н. Н. Блохина Российской академии медицинских наук (директор – академик РАН и РАМН, профессор М.И.Давыдов)
Научный консультант:
Заслуженный Деятель науки РФ,
доктор медицинских наук, профессор Р.И.Габуния
Официальные оппоненты:
доктор медицинских наук, профессор В.П. Летягин
доктор медицинских наук, профессор С.Б. Петерсон
доктор медицинских наук В.В. Крылов
Ведущая организация:
ФГУ Российский научный центр рентгенорадиологии Росздравсоцразвития РФ, г. Москва
Защита состоится «_____»___________2009 г. в_____ часов на заседании диссертационного учёного совета (Д 001.17.01) ГУ Российского онкологического научного центра им. Н. Н. Блохина РАМН по адресу 115478, г.Москва, Каширское шоссе, 24.
С диссертацией можно ознакомиться в библиотеке ГУ РОНЦ им. Н.Н. Блохина РАМН
Автореферат диссертации разослан «___»____________2008 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук, профессор Ю.В. Шишкин
^ Актуальность темы
Злокачественные новообразования занимают одно из ведущих мест среди причин смертности людей моложе 65 лет. Частота развития костных метастазов у онкологических больных высока. Так, из 1000 патологоанатомических исследований, выполненных у пациентов, умерших от злокачественных образований, в 25-30% случаев выявляются костные метастазы. Рак предстательной железы и молочных желез имеют особенную предрасположенность к развитию метастазов в кости (Кондратьева А.П., 2000). Так рак молочной железы у женщин в структуре заболеваемости злокачественными опухолями занимает первое место. За последние 15 лет отмечено двукратное увеличение уровня заболеваемости и имеется тенденция к дальнейшему повышению этого показателя (Аксель Е.М., 2006). Метастазы в кости встречаются достаточно часто и при таких злокачественных опухолях как рак легкого, почки, желудка и других нозологических формах (Модников О.П. с соавт., 2004). Определено, что у 30%-70% пациентов с первично установленным диагнозом рака уже имеются костные метастазы, способствующие развитию болевого синдрома - наиболее часто встречаемого и трудно поддающегося лечению. Болевой синдром, нарастающий по мере прогрессирования процесса, резко снижает качество жизни, способствует развитию тревоги, депрессии и приводит к стойкой инвалидизации. (Исакова М.Е. с соавт., 2000). В предотвращении боли ведущую роль играет медикаментозная терапия. Однако применение анальгетиков не обеспечивает стопроцентный результат. Кроме того, существуют побочные эффекты, ограничения по длительности применения и индивидуальная чувствительность или невосприимчивость к препаратам.
Развитие специфической противоопухолевой лекарственной терапии (прежде всего при раке молочной железы, гормоночувствительной форме рака предстательной железы) позволило добиться успехов в плане продолжительности жизни, однако при некоторых опухолях (рак почки, гормонорезистентная форма рака предстательной железы) успехи не столь значимы. Кроме того, проводимая терапия не всегда сопровождается значительным улучшением общего состояния больного. Дистанционная лучевая терапия безусловно является мощным оружием в борьбе с костными метастазами, однако ее применение ограничено при множественном поражении.
Проблема борьбы с метастазами в кости и их клиническими проявлениями заставляет искать дополнительные возможности для лечения. В последние десятилетия в медицинскую практику внедрены методы системной радионуклидной терапии (РНТ) метастазов в кости с использованием различных радионуклидов. Результаты их применения дают основание считать перспективным развитие в ядерной медицине направления по лечению костных метастатических поражений с помощью системной радионуклидной терапии.
^ Цель исследования
Целью настоящего исследования является повышение клинической эффективности лечения пациентов с костными метастазами на основе совершенствования тактики применения системной радиотерапии хлоридом стронция-89.
^ Задачи исследования
1. Оценить анальгезирующую эффективность радионуклидной терапии хлоридом стронция-89 при метастатическом поражении скелета у больных с метастазами в кости рака молочной железы, предстательной железы и злокачественных опухолей других локализаций, как при применении хлорида стронция-89 в монорежиме, так и в сочетании с основным противоопухолевым лечением.
2. Проанализировать анальгезирующую эффективность системной радиотерапии хлоридом стронция-89 при остеопластических, остеолитических и смешанных метастазах в кости.
3. Провести сравнительный анализ эффективности системной радиотерапии хлоридом стронция-89 при различном количестве метастазов в кости скелета.
4. Изучить зависимость анальгезирующей эффективности системной радиотерапии хлоридом стронция-89 от данных остеосцинтиграфии.
5. Изучить возможности системной радиотерапии хлоридом стронция-89 в достижении репарации при лечении больных с костными метастазами.
6. Определить условия максимально эффективного клинического применения системной радиотерапии хлоридом стронция-89.
7. Оценить изменение качественных и количественных характеристик остеосцинтиграфической картины в процессе мониторинга при радиотерапии хлоридом стронция-89 и других видах лечения метастазов в кости.
8. Оценить информативность определения уровня остеокальцина с помощью радиоиммуноферментного метода в мониторинге костных метастазов на фоне терапии хлоридом стронция-89.
9. Определить степень гематологической токсичности при радионуклидной терапии хлоридом стронция-89.
Научная новизна
Впервые на большом клиническом материале разработаны оптимальные подходы к применению хлорида стронция-89 для лечения болевого синдрома при метастазах в кости различных злокачественных опухолей, основанные на оценке остеосцинтиграфической картины и учете диагноза и исходного симптомокомплекса. Оценена перспективность радиотерапии хлоридом стронция-89 в сочетании с другими видами противоопухолевого лечения.
Определена противоопухолевая активность системной радиотерапии хлоридом стронция-89 при костных метастазах злокачественных опухолей различных локализаций.
Впервые определены закономерности изменений остеосцинтиграфической картины при метастатическом поражении костей в зависимости от проведённого лечения, что дало возможность повысить диагностическую ценность остеосцинтиграфии.
Впервые установлена информативность РИА-метода определения уровня остеокальцина в сыворотке крови при мониторинге больных с костными метастазами рака предстательной и молочной железы при лечении хлоридом стронция-89.
Впервые предложена методика дозиметрического контроля системной радиотерапии хлоридом стронция-89 по регистрации тормозного излучения.
^ Практическая значимость
Разработаны показания для практического применения в онкологических учреждениях лечения болевого синдрома при костных метастазах с помощью хлорида стронция-89, предложены рекомендации по повышению клинической эффективности системной радионуклидной терапии.
Установленная радионуклидная семиотика костных метастазов повышает диагностическую значимость остеосцинтиграфии в оценке динамики лечения костных метастазов.
Показана целесообразность определения сывороточного остеокальцина в диагностике и оценке эффективности лечения у больных с костными метастазами.
Предложена новая методика расчета очаговых доз при системной радиотерапии хлоридом стронция-89.
ВНЕДРЕНИЕ
Метод системной радиотерапии отечественным препаратом - хлоридом стронция-89 при генерализованном метастатическом поражении скелета с выраженным болевым синдромом у пациентов с опухолями различных локализаций по совместной разработке ФГУ Российский научный центр рентгенорадиологии Росздравсоцразвития и ГУ Российский онкологический научный центр им. Н.Н. Блохина РАМН зарегистрирован в Федеральной службе по надзору в сфере здравоохранения и социального развития.
^ Апробация работы
Диссертация апробирована 17 октября 2008 года на совместной конференции лаборатории радиоизотопной диагностики отдела лучевой диагностики и рентгенохирургических методов лечения, поликлиники, отделения радиохирургии, хирургического отделения диагностики опухолей, отделения опухолей опорно-двигательного аппарата, хирургического отделения опухолей молочных желёз, урологического отделения, отделения клинической фармакологии и химиотерапии НИИКО ГУ РОНЦ им.Н.Н. Блохина РАМН. Материалы работы докладывались на III и IV Съездах онкологов и радиологов СНГ Минск, 2004, Баку, 2006, II Евразийском конгрессе по медицинской физике и инженерии «Медицинская физике -2005» Москва 2005, на III Съезде МОО «Общество ядерной медицины», Всероссийской научно-практической конференции «Актуальные вопросы ядерной медицины и фармацевтики» Дубна, Ратмино, 2004, на Международной конференции «Современные проблемы ядерной медицины и радиофармацевтики», Обнинск, 2000, на Невском Радиологическом форуме, «Наука – клинике», Санкт-Петербург, 2005, 2006.
Публикации
По материалам диссертации опубликовано 12 научных статей, 4 главы в монографиях, 14 тезисов докладов.
^ Объем и структура диссертации
Диссертация изложена на 245 страницах машинописного текста, содержит таблиц, 51 рисунок, 11 диаграмм.
Содержание работы
В исследование включено 400 больным с метастатическим поражением костей. Во всех случаях диагноз злокачественной опухоли был верифицирован после патологоанатомического исследования материалов пункционной биопсии или послеоперационного материала. Метастазы в кости выявлены с помощью радиологических исследований: остеосцинтиграфии с обязательным подтверждением рентгенологическими методами - планарной рентгенографией и (или) компьютерной томографией. При обращении в лабораторию радиоизотопной диагностики РОНЦ оценивалось субъективное состояние, выяснялись жалобы. Проводилось ознакомление с историей болезни или амбулаторной картой. При осмотре пациента устанавливались двигательная активность, возможность самообслуживания, локализация боли и её интенсивность с оценкой по шкале ВОЗ (ECOG): 0-отсутствие боли, 1-слабые, 2-умеренные, 3-сильные, 4-очень сильные боли. Проводилась оценка общего статуса по шкале Карновского. Оценивалась эффективность применяемых анальгетиков. Затем всем пациентам с костными метастазами в обязательном порядке осуществлялось комплексное рентгенорадионуклидное обследование костной системы до назначения системной радиотерапии хлоридом стронция-89. На первом этапе выполнялась остеосцинтиграфия, по результатам которой проводилось рентгенографическое исследование костей скелета, в которых были сцинтиграфически выявлены очаги патологического включения РФП.
Оценка анальгезирующего эффекта проводилась путем периодического контроля состояния пациентов через 2 недели после введения хлорида стронция-89 и далее через каждые 4 недели с оценкой состояния по шкале ВОЗ (ECOG). Анальгезирующий (обезболивающий) эффект от системной радиотерапии оценивался следующим образом: полным эффектом считалось купирование болей на срок не менее 2-х месяцев (балльная оценка «0»), частичным эффектом — любое значимое снижение болей на тот же срок (снижение балльной оценки на 1 пункт по пятибалльной шкале). Устанавливался индекс Карновского, а также выяснялась частота суточного применения анальгетиков. По истечении 3-х месяцев делалось контрольное рентгенорадионуклидное обследование, при котором отмечались изменения картины костных нарушений. В последующем, подобные контрольные обследования проводились каждые 3 - 6 месяцев в зависимости от клинической картины и субъективного состояния (при стабилизации процесса и удовлетворительном самочувствии промежутки между временем обследования увеличивались). Такой режим обследования выдерживался до и после каждого введения хлорида стронция - 89.
Исследование уровней сывороточного остеокальцина.
В исследование вошли 97 пациентов, которым была проведена системная радиотерапия хлоридом стронция-89. Из них: рак простаты – 49, рак молочной железы – 48. Уровни остеокальцина определялись в плазме крови с помощью РИА-наборов фирмы CIS biointernational (Франция). Радиоиммунологические исследования и исследования по визуализации проводились непосредственно перед введением 89-стронций-хлорида, через 2-3 недели, 3-6 и более месяцев после начала лечения.
Методика системной радиотерапии хлоридом стронция-89.
В качестве лечебного препарата применялся отечественный хлорид стронция-89 (ФСП 42-0225-0809-01), регистрационный номер 000291/01-2001 от 26.02.01, регистрационное удостоверение № 99.128.1. Эффективная доза облучения пациента при терапии с использованием препарата 89Sr составляет 3,1 мЗв/МБк. Препарат вводился внутривенно в объеме 4.0 мл, активность во флаконе - 150 МБк (4,08 мКи), в процедурном кабинете радиоизотопной лаборатории с соблюдением мер радиационной безопасности.
- Радиационно-техническое обеспечение радионуклидной терапии и контроль очаговых доз облучения
- Под руководством профессора Б.Я. Наркевича разработана методика подобного контроля, основанная на радиометрии патологических очагов по тормозному излучению, которое генерируется бета-частицами при их замедлении в тканях тела больного.
- Для этого необходимы следующие условия:
- 1. создается гетерогенный фантом, который с максимально возможной степенью подобия имитирует участок тела больного с локализованным в нём патологическим очагом.
- 2. накопленный в реальном патологическом очаге радиофармпрепарат (РФП) выводится из него по моноэкспоненциальной зависимости с известным периодом полувыведения.
Методика реализуется следующим образом:
1. Проводится радиометрия фантома в интегральном режиме с помощью сцинтилляционного радиометра, обладающего энергетическим порогом регистрации импульсов не более 20 кэВ, после чего флакон с порцией РФП извлекается из фантома, и больному сразу же производится внутривенное введение всей активности РФП из этого флакона (момент времени t=0).
2. По формуле
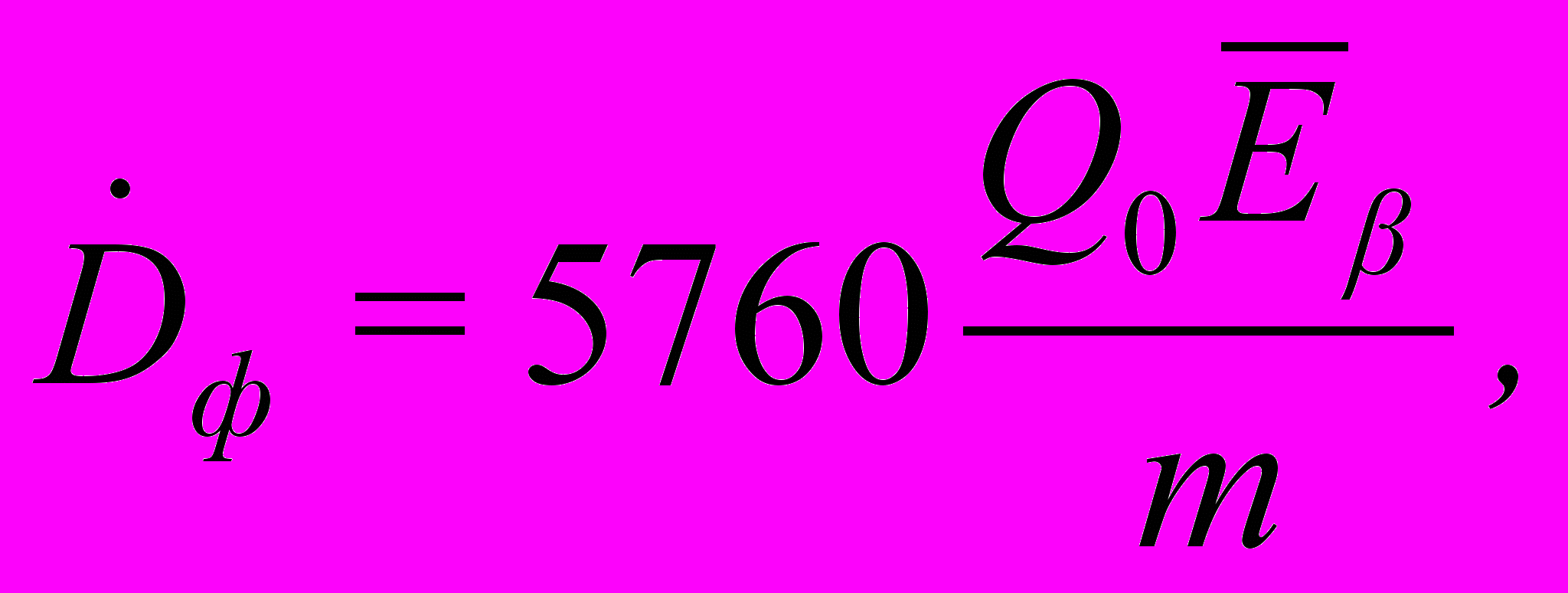
вычисляется мощность дозы бета-излучения
 в имитированном патологическом очаге фантома.
в имитированном патологическом очаге фантома.3. Через 1 – 2 недели после инъекции РФП (момент времени t=t*) проводится радиометрия участка тела больного с патологическим очагом, причём геометрия и режим радиометрии должны полностью совпадать с таковыми при радиометрии фантома.
4. Радиометрия повторяется для участка тела рядом с патологическим очагом с целью учёта вклада в скорость счёта от тормозного излучения, которое возникает в мягких тканях, лежащих выше и ниже поражённого позвонка по направлению к детектору радиометра.
5. По формуле
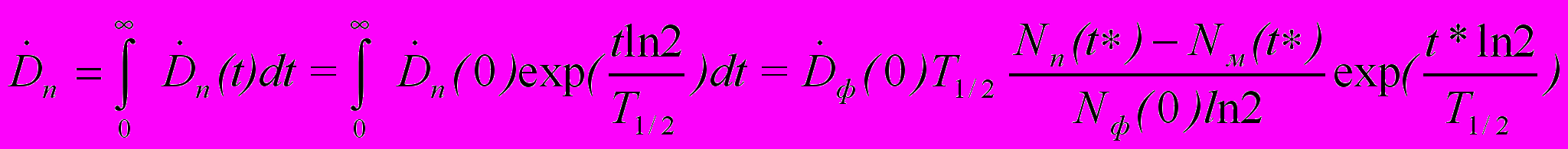
вычисляется полная доза, полученная тканями патологического очага за весь курс РНТ.
Проведенные нами предварительные измерения уровней накопления 89Sr у 4-х больных в области метастазов в позвоночник при раке молочной железы показывают, что регистрация тормозного излучения от них с помощью стандартного радиометра-дозиметра МКС-1117А обеспечивает реальную возможность контроля очаговых доз облучения бета-частицами 89Sr. Было установлено, что поглощённая доза бета-излучения в костных метастазах варьирует от 24 до 78 Гр (среднее значение 53 Гр).
^ Гематологический контроль при системной радиотерапии
хлоридом стронция-89.
Контроль за картиной крови проводился с помощью предварительного (не ранее, чем за 2 недели до проведения курса системной радиотерапии) и периодического дальнейшего (спустя 2 недели после инъекции хлорида стронция-89 и далее через каждые 4 недели) исследования клинического анализа крови. При оценке угнетения кровяного ростка использована общепринятая шкала миелотоксичности по CNC – NCIC, version 3.0.
Все больные, получившие системную радиотерапию хлоридом стронция-89, были разделены на 3 группы.
В первую группу вошли больные раком предстательной железы (125 пациентов) в возрасте от 50 до 81 года (65,14±3,61 лет). Из 125 больных 50-ти больным параллельно с системной радиотерапией проводилось противоопухолевое лечение: 20 пациентов находились в режиме гормонотерапии (МАБ), 19 больных получали бисфосфонаты (зомета), 5-ти больным проводилась дистанционная гамма-терапия, 4 больных получали химиотерапию, 1 больной получал химиотерапию+зомету, 1 больной - химиотерапию+локальное лучевое лечение. 75 больных получали только системную радиотерапию хлоридом стронция-89. Все больные ранее получали специфическое противоопухолевое лечение по поводу основного заболевания.
Во вторую группу включены больные раком молочной железы (195 пациентов) в возрасте от 31 до 80 лет (54,1±2,14 лет). Из 195 больных с метастазами рака молочной железы 140 больным параллельно проводилось противоопухолевое лечение: 81 пациентка находилась в режиме гормонотерапии (тамоксифен, аримидекс), 28 больных на фоне гормонотерапии получали бисфосфонаты (бонефос, аредиа, зомета), 13 больных получали химиотерапию, 10 больных получали химиотерапию+бисфосфонаты, 5 больных - химиотерапию+локальное лучевое лечение, 3-м больным проводилась дистанционная гамма-терапия. 55 больных получали только системную радиотерапию хлоридом стронция-89.
В 3-ю группу вошли 43 мужчины в возрасте от 17 до 78 лет (53,5±15,6 лет) и 37 женщин в возрасте от 15 до 82 лет (54,6±14,1 лет). На момент начала системной радиотерапии 30 больным было проведено оперативное лечение по поводу первичной опухоли, в 50 случаях первичная опухоль не была удалена. Во всех случаях диагноз злокачественной опухоли был верифицирован после патологоанатомического исследования материалов пункционной биопсии или послеоперационного материала.
У 22-х пациентов кроме метастазов в кости имелись метастазы в другие органы (печень, лёгкие и др.). По поводу метастазов в кости системная радиотерапия хлоридом стронция-89 проводилась на фоне химиотерапии 11 больным, комбинации двух различных видов лечения – 11 больным (химиолучевое лечение — 6 пациентов, иммунотерапия/бисфосфонаты — 2 пациента, гормонотерапия/бисфосфонаты — 2 пациента, лучевая терапия/бисфосфонаты – 1 пациент), бисфосфонаты получали 6 больных, лучевое лечение – 3 больных, гормонотерапию - 2 пациента.
Структура данной группы по нозологическим формам представлена в следующей таблице:
Таблица 1
^ Нозологические формы опухолей различных локализаций
| Нозологическая форма | Количество больных | ^ Нозологическая форма | Количество больных |
| Рак почки | 17 | Рак легкого | 16 |
| ^ Рак желудка | 7 | Остеосаркома | 4 |
| Рак яичников | 3 | ^ Рак толстой кишки | 3 |
| Рак тела матки | 3 | Рак мочевого пузыря | 3 |
| Меланома | 2 | Прочие* | 22 |
Примечание:
* - саркома Юинга -2, лейомиосаркома - 1, рак щитовидной железы -1, карциноид брюшной полости -1, рак подчелюстной железы -1, рак носоглотки -1, феохромоцитома -1, хемодектома -1, параганглиома -1, рабдомиосаркома -1, рак ротоглотки -1, метастазы в кости из невыявленного первичного очага -10.
^ Статистическая обработка данных
На основании анамнеза, клинических данных и результатов, полученных при остеосцинтиграфии, рентгенологических исследованиях и in vitro-диагностике уровней остеокальцина была составлена база данных - кодификатор в программе Excel.
Данные обрабатывались с помощью стандартного пакета «Statistica», ver.7.
Оценка достоверности различия средних групповых величин между исследуемыми группами проводилась с использованием параметрического t-критерия Стьюдента для парных и непарных выборок. Результаты представлены как групповые средние, со среднеквадратичным отклонением (standard deviation – cd).
Оценка гематологической токсичности проведена с использованием общепринятой шкалы миелотоксичности по CNC – NCIC, version 3.0.
