Учебное пособие к дисциплине для студентов заочной формы обучения по специальности 140211 «Электроснабжение»
| Вид материала | Учебное пособие |
- Учебное пособие к дисциплине для студентов заочной формы обучения по специальности, 1219.34kb.
- Методические указания к дисциплине и задания к контрольной работе для студентов заочной, 126.92kb.
- Методические указания к дисциплине и темы рефератов для студентов заочной формы обучения, 102.72kb.
- Учебное пособие для студентов заочной формы обучения Санкт-Петербург, 1247.83kb.
- Методические указания к итоговому междисциплинарному экзамену по специальности «электроснабжение», 382.82kb.
- Н. Н. Кувшинова экология учебное пособие, 1072.88kb.
- Учебное пособие для самостоятельной работы студентов специальности 040600 «Сестринское, 1354.95kb.
- Методические указания: краткий курс лекций для студентов заочной формы обучения Санкт-Петербург, 1540.61kb.
- Учебное пособие Для студентов всех специальностей Москва 1999, 1603.73kb.
- Учебное пособие для студентов специальности «Экономика и управление на предприятии», 1271.5kb.
Негосударственное образовательное учреждение
высшего профессионального образования
Московский институт
энергобезопасности и энергосбережения
Кафедра
Электротехника и Электроника
МАТЕРИАЛОВЕДЕНИЕ. ТЕХНОЛОГИЯ КОНСТРУКЦИОННЫХ МАТЕРИАЛОВ
Учебное пособие
к дисциплине для студентов заочной формы обучения по специальности
140211 «Электроснабжение»
Учебно-методический комплекс
Часть 5.
Москва 2007
Содержание
1. Введение 3
2. Структура кристаллов. 3
3. Основные свойства материалов. 7
3.1. Механические свойства. 7
3.1.1. Особенности структуры и свойств полимерных материалов. 8
3.2. Теплофизические свойства материалов. 15
3.2.1. Теплоёмкость. 16
3.2.2. Теплопроводность. 16
3.2.3. Тепловое расширение. 17
3.2.4. Температуры фазовых переходов. 17
3.3. Электрические свойства. 18
3.3.1. Проводники, полупроводники и диэлектрики. 18
3.3.2. Основные электрические характеристики материалов. 20
3.4. Магнитные свойства. 26
3.5. Химическая и радиационная стойкость материалов различной природы. 29
4. Проводниковые материалы. 32
4.1. Металлические проводниковые материалы. 32
4.1.1. Термо-ЭДС. 33
4.1.2. Материалы высокой проводимости. 34
4.1.3. Материалы высокого удельного сопротивления. 35
4.1.4. Сплавы для термопар. 36
4.1.5. Контактные материалы. 36
4.1.6. Припои. 37
4.2. Сверхпроводники и гиперпроводники. 37
4.3. Неметаллические проводники. 38
4.3.1. Углеродные материалы и композиции. 38
4.3.2. Ионные проводники. 42
5. Диэлектрические материалы. 43
5.1. Газообразные диэлектрики. 43
5.2. Жидкие диэлектрики. 45
5.2.1. Нефтяные масла. 45
5.2.2. Синтетические жидкие диэлектрики. 46
5.3. Твёрдые диэлектрики. 47
5.3.1. Органические полимеры. 47
5.3.1.1. Термопластичные полимеры. 48
5.3.1.2. Термореактивные полимеры – реактопласты. 57
5.3.1.3. Эластомеры (каучуки и резины). 60
5.3.1.4. Лаки, эмали и компаунды. 64
5.3.1.5. Полимерные композиционные материалы (ПКМ). 65
5.3.2. Неорганические диэлектрики. 67
5.3.3. Ситаллы. 70
5.3.4. Техническая керамика. 71
5.3.4.1. Традиционная электротехническая керамика. 73 5.3.4.2. Конденсаторная керамика. 78
6. Полупроводниковые материалы. 79
6.1. Элементарные полупроводники. 79
6.2. Полупроводниковые соединения. 80
7. Магнитные материалы. 82
7.1 Магнитомягкие материалы 82
7.2. Магнитотвёрдые материалы 85
8. Рекомендуемая литература 86
1. Введение
Материаловедение – наука о материалах, методах их получения, переработке, об их свойствах и областях их использования. Правильный выбор материалов даёт важный, иногда определяющий эффект в создании высокоэффективных и экономичных приборов, машин и механизмов.
Материалы могут находиться в различных фазовых и агрегатных состояниях. По электрическим свойствам они подразделяются - на проводники, полупроводники и диэлектрики (включая электроизоляционные материалы). По магнитным свойствам - на сильномагнитные и слабомагнитные.
Свойства материалов определяются их строением и видами связей, которыми атомы и молекулы связаны между собой.
Существует 3 типа химических связей – ионная, ковалентная и металлическая. Ковалентная связь заключается в образовании общих электронных пар атомов, ионная – в переходе валентных электронов от одного атома к другому и образованию разноимённо-заряженных ионов. Металлическую связь можно рассматривать как разновидность ковалентной связи с тем отличием, что общая пара электронов делокализована, т.е. не имеет постоянного места. Этим объясняется электропроводность, теплопроводность, ковкость, пластичность металлов.
Эти 3 типа химических связей являются идеализированными представлениями о химическом связывании. В действительности реализуется некоторое промежуточное состояние и когда говорят, например, что какое-либо вещество является ковалентным, то подразумевают, что в химической связи вклад ковалентности преобладает.
Прочность ковалентных химических связей достаточно велика. Так, прочность связи в молекуле водорода составляет 436 кДж/моль, связь Н – СН3 435 кДж/моль, связь СН3-СН3 - 368 кДж/моль, связь СН3-С6Н5 – 389 кДж/моль, связь Si-О – 432 кДж/моль.
Ковалентные связи могут быть полярные и неполярные. Связь полярна, если она образуется между атомами с различной электроотрицательностью. Если в молекуле имеются полярные ковалентные связи и молекула не симметрична, то она будет полярной. Мерой её полярности является электрический момент диполя . Момент диполя есть вектор, направленный от положительного заряда к отрицательному и равный произведению заряда q и расстояния L между зарядами = q L. Размерность – Дебай D. 1D = 3,3310-30 Клм. Наиболее полярные связи – ионные. Например, в КВr дипольный момент равен 10 D. Ковалентные связи менее полярны, = 0,5 4 D.
Важную роль играют более слабые (4 – 40 кДж/моль) межмолекулярные связи (силы Ван-дер-Ваальса). Эти связи существенны в жидкостях, в аморфных веществах, в биологических структурах. Особенно прочны межмолекулярные водородные связи, например, между атомами Н и О в воде, Н и N в аммиаке. Межмолекулярные связи обусловливают склеивание и прилипание.
2. Структура кристаллов
Одно и то же твёрдое вещество в зависимости от условий затвердевания может быть в кристаллическом или в аморфном состоянии. Для твёрдого вещества обычным является кристаллическое состояние – это состояние почти полной упорядоченности материальных частиц – атомов, ионов или молекул, из которых состоит вещество. Упорядоченность расположения этих частиц в значительных объёмах вещества обозначают термином «дальний порядок». В аморфных веществах дальнего порядка нет, – там существует «ближний порядок». Под этим термином подразумевается, что с определённой долей вероятности можно судить о среднем количестве частиц в ближайшем окружении интересующей нас частицы. В газообразном состоянии вещество полностью неупорядоченно.
Вещество в кристаллическом состоянии может находиться в виде собственно кристаллов, например, NaС1, алмаз, или в виде поликристаллических агрегатов (мрамор, большинство металлов). Кристаллическое состояние, в отличии от аморфного, характеризуется определённой температурой плавления Тпл, часто – геометрической формой, во многих случаях – анизотропией свойств.





 Обычно из более простых и симметричных частиц получаются более простые и симметричные кристаллические постройки. Так, шарообразные частицы, например, атомы или ионы, образуют кристаллические структуры, которые почти буквально повторяют наиболее плотные упаковки подшипниковых шариков или мячей настольного тенниса – по гексагональному закону.
Обычно из более простых и симметричных частиц получаются более простые и симметричные кристаллические постройки. Так, шарообразные частицы, например, атомы или ионы, образуют кристаллические структуры, которые почти буквально повторяют наиболее плотные упаковки подшипниковых шариков или мячей настольного тенниса – по гексагональному закону. 



Рис.2.1. Плотнейшая упаковка шаров в одном слое.
В зависимости от того, как будут укладываться такие последующие слои шаров относительно предыдущих, могут образовываться как «гексагональная плотнейшая упаковка», так и «кубическая плотнейшая упаковка».
Чтобы установить тип упаковки, нужно определить тип симметрии данного атомного расположения и выделить соответствующую структурную единицу. Сначала остановимся на структурной единице. Всякий повторяющийся узор можно разделить на «мотивные единицы», совершенно одинаковые, соприкасающиеся друг с другом без промежутков. Рис. 2.2. Повторяющийся узор.
След овательно, в принципе выбор мотивной единицы произволен.
Обычно наиболее удобно считать единицей узора – структурной единицей
параллелограмм с кратчайшими сторонами и с углами, наиболее близкими к
прямым. По тем же принципам анализируются пространственные узоры,
которые всегда можно разделить на единицы в форме ящиков, называемых
Рис.2.2. «элементарными ячейками».
Элементарная ячейка полностью определена тогда, когда известны:
- все три ребра повторяющегося параллелепипеда;
- углы, которые образуют между собой три ребра ячейки;
- тип, число и положение структурных единиц (атомов, ионов, молекул), из которых состоит ячейка.
Число частиц, окружающих данную частицу, называется «координационным числом». К.ч. 12.
Всего известно 14 видов пространственных решёток, которые различаются между собой по симметрии и формам элементарных ячеек. Эти 14 видов решёток геометрически вывел французский кристаллограф О.Браве. 14 решёток Браве подразделяются на 4 типа: 1) примитивные – имеют узлы (т.е. материальные частицы – атомы, ионы, молекулы) в вершинах ячейки;
2) базоцентрированные – узлы находятся в вершинах и в центрах двух противоположных граней;
3) объёмноцентрированные – узлы находятся в вершинах и в центре ячейки;
4) гранецентрированные – узлы находятся в вершинах и в центре каждой грани.
Плотность упаковки ячеек возрастает от 1-го к 4-му типу.
Русский учёный Е.С.Фёдоров показал, что 14 элементарных решёток в кристаллических многогранниках могут совмещаться (взаимное проникновение), образуя 230 возможных комбинаций или пространственных групп.
Способ упаковки материальных частиц или, иначе, вид элементарной ячейки, определяет форму кристаллов. Кристаллы ограничиваются плоскими гранями, пересекающимися на рёбрах, которые, в свою очередь, пересекаются в вершинах. Форма кристаллов весьма разнообразна, но симметрична. В кристаллах различают следующие элементы симметрии:
- плоскость симметрии – воображаемая плоскость, делящая кристалл на 2 части, являющимися зеркальными отражениями друг друга;
- ось симметрии – линия, при вращении вокруг которой кристалл некоторое число раз совмещается сам с собой. Это число определяет порядок оси. Доказано, что в кристаллах возможны оси симметрии только 2, 3, 4 и 6 порядков;
- центр симметрии – точка внутри кристалла, в которой пересекаются и делятся пополам линии, соединяющие соответственные точки на поверхности кристалла.
В кристаллах элементы симметрии могут встречаться как поодиночке, так и в сочетании друг с другом. Полная совокупность элементов симметрии многогранника называется видом симметрии. . Русский академик А.В.Гадолин в 1867 г. доказал, что возможны 32 вида симметрии, которые сгруппированы в 7 кристаллографических систем или сингоний.
Таблица 1.
КРИСТАЛЛОГРАФИЧЕСКИЕ СИНГОНИИ
| КАТЕГОРИЯ | СИНГОНИЯ | Углы между осями | Длина осей |
| Низшая | триклинная моноклинная ромбическая | 900 = = 900 = = = 900 | x y z x y z x y z |
| Средняя | Тригональная Тетрагональная Гексагональная | = = 900 = = = 900 ось z перпендикулярна к осям х, у, u, которые расположены под углом 600 или 1200 | x = y = z x = y z |
| Высшая | Кубическая | = = = 900 | x = y = z |
У различных веществ, принадлежащих к одной сингонии, углы между гранями иногда могут несколько отличаться, но у всех кристаллов данного вещества одной кристаллической формы углы между гранями постоянны. Это установили Стено в 1669 г. и Роме де Лиль в 1772 году.
В природе встречаются вещества, кристаллизующиеся одинаковым образом в одной кристаллической системе. Такие вещества называют изоморфными. Точные измерения показали, что кристаллы изоморфных веществ не всегда строго одинаковы по форме, а только относительно близки. Так
ZnCO3 MgCO3 FeCO3 MnCO3 CdCO3 CaCO3 кристаллизуются в тригональной сингонии в форме ромбоэдров, однако характерные углы ромбоэдра для них несколько различны:
103028’ 103021’ 103004’ 102050’ 102030’ 101055’
Обнаружилось, что изоморфные вещества в ряде случаев способны кристаллизоваться совместно с образованием смешанных кристаллов переменного состава.
Не все вещества с одинаковой кристаллографической формой и химически сходные между собой способны образовывать смешанные кристаллы. Для этого необходимо, чтобы радиусы соответствующих атомов или ионов , т.е. тех, которые замещают друг друга в кристаллической решётке, не отличались друг от друга более, чем на 15%. Если в узлах кристаллической решётки находятся молекулы, имеющие сложную форму, то требование подобия размеров становятся более жёсткими. А для полимерных кристаллов различия в поперечниках макромолекул должны быть менее 1%, поэтому образование смешанных полимерных кристаллов – очень редкое явление.

 Смешанные кристаллы чаще называют «изоморфно-замещёнными кристаллами» или «твёрдыми растворами замещения» или «фазами переменного состава». Последний термин более общий, он включает в себя и другие структуры, например, твёрдые растворы внедрения, дефицитные структуры. Термин «твёрдые растворы» подчёркивает аналогию с распределением одного компонента в другом, наблюдаемую в обычных растворах, а именно, - в среднем равномерное, но случайное распределение компонентов. Для жидких растворов состояние их описывается «фазовой диаграммой». Если компонента смешиваются друг с другом неограниченно, то диаграмма состояния имеет вид, представленные на рис. 2.3.
Смешанные кристаллы чаще называют «изоморфно-замещёнными кристаллами» или «твёрдыми растворами замещения» или «фазами переменного состава». Последний термин более общий, он включает в себя и другие структуры, например, твёрдые растворы внедрения, дефицитные структуры. Термин «твёрдые растворы» подчёркивает аналогию с распределением одного компонента в другом, наблюдаемую в обычных растворах, а именно, - в среднем равномерное, но случайное распределение компонентов. Для жидких растворов состояние их описывается «фазовой диаграммой». Если компонента смешиваются друг с другом неограниченно, то диаграмма состояния имеет вид, представленные на рис. 2.3. 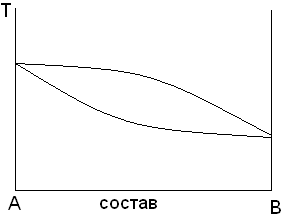
Рис.2.3. Фазовая диаграмма системы с неограниченной взаимной растворимостью.
Верхняя кривая характеризует состав пара, а нижняя кривая – состав жидкости. Точно так же выглядит диаграмма состояния для твёрдого раствора замещения, только названия кривых будет иным. Верхняя называется линией ликвидуса, а нижняя – линией солидуса. В твёрдых растворах параметры кристаллических решёток изменяются пропорционально составу. Знание фазовой диаграммы для данной смеси веществ позволяет изготовить твёрдый раствор заданного состава
Другой разновидностью твёрдых растворов являются «твёрдые растворы внедрения». В этом случае в кристаллическую решётку (чаще всего металлическую) в междоузлия внедряются атомы неметалла. Очевидно, что это возможно тогда, когда в кристаллической решётке матричного вещества имеются «пустоты», а внедрённые атомы малы и их размеры соизмеримы с этой «пустотой». Понятно, что возможны только ограниченные твёрдые растворы. К атомам, которые могут располагаться в междоузлиях металлической решётки, относятся Н, С, N, O, B, Si. Присутствие внедрённых атомов вызывает напряжение в материнской решётке, искажение кристаллической решётки вплоть до изменения её симметрии, например, переход кубической симметрии в тетрагональную.
Кроме явления изоморфизма в кристаллических веществах проявляется полиморфизм. Явление полиморфизма состоит в том, что в зависимости от условий (температуры, давления) одно и то же вещество может образовывать разные по симметрии и форме кристаллы. Эти формы, называемые полиморфными разновидностями или модификациями ,принято обозначать буквами , , и т.д., причём обычно относится к модификации, стабильной при наиболее низкой температуре.
Вопросы для самопроверки.
1. В чём отличие дальнего порядка от ближнего?
2. Каков принцип выбора формы элементарной ячейки кристалла?
3. Какой тип элементарной решётки имеет наибольшую плотность упаковки, наименьшую плотность упаковки?
4. Какими элементами симметрии могут обладать кристаллы?
5. Что такое «кристаллографические сингонии»? В чём заключается их отличия?
6. Что такое изоморфные вещества? Изоморфно-замещённые кристаллы?
Приведите синоним термину «изоморфно-замещённые кристаллы».
7. Приведите примеры фаз переменного состава.
3. Основные свойства материалов
Основные свойства материалов – механические, электрические, магнитные, теплофизические.
3.1. Механические свойства
Механические свойства материала проявляются в виде ответной реакции на нагружение и формоизменение, когда в нём возникают внутренние напряжения.
Механические свойства твёрдых тел характеризуются прочностью (сопротивление разрушению), жёсткостью (сопротивление упругой деформации), твёрдостью (сопротивление пластической деформации), ударной вязкостью (сопротивление хрупкому разрушению).
Наиболее распространённым является испытание материалов на растяжение, выполняемое на разрывных машинах. Результаты эксперимента представляют в виде графика в координатах относительное удлинение % - напряжение в Па. На рис.3.1 представлены диаграммы растяжения разных материалов – керамики, металла, стеклообразного полимера, эластомера.
 , МПа
, МПа  В
В
 1
1
 2 3 К 1. Керамика, стекло.
2 3 К 1. Керамика, стекло.А 2. Металл.

 С D 3. Стеклообразный
С D 3. Стеклообразный 4 полимер.
4. Эластомер.
 О ,%
О ,%Рис.3.1. Кривые нагрузка – удлинение ( - ) материалов различной природы.
На первом участке (ОА) напряжение пропорционально деформации: = Е (закон Гука), где Е – модуль упругости. Модуль упругости характеризует сопротивление материала упругой деформации, которая обратима.
Затем, на втором участке (АВ), наблюдается отклонение от линейности, А – предел нарушения пропорциональности.
Хрупкие материалы (неорганическое стекло, керамика) разрушаются на первом участке, например, в точке Х. Аналогично ведут себя пластмассы – реактопласты и композиты – композиционные материалы на основе реактопластов с волокнистыми наполнителями (стеклопластики, углепластики и др.).
Упруго-вязкие материалы (металлы, пластмассы) при дальнейшем растяжении достигают максимума – предела текучести (точка В).
При достижении предела текучести у полимеров и мягких материалов при дальнейшем деформировании может наблюдаться уменьшение напряжения, при этом в материале образуется так называемая «шейка» – скачкообразное уменьшение поперечного сечения. Металлы вскоре после этого разрушаются, полимеры при постоянном напряжении можно деформировать до точки D, т. е. до тех пор, пока весь материал не перетечёт в «шейку» (участок СD). На этом участке происходит ориентирование макромолекул полимера и увеличение его прочности. На участке DК происходит деформация и разрушение уже ориентированного полимера.
Кривая растяжения эластомеров более плавная и напряжения существенно ниже.
Испытания на растяжение позволяют определить предел прочности при растяжении р, разрывное удлинение р %, модуль упругости Е, предел пропорциональности, предел текучести. Обычно для расчётов конструкций задаются определённой жёсткостью или вибропрочностью по величине напряжений, при которых пластическая деформация достигает малой нормированной величины, например 0,001; 0,005; 0,02; 0,05%.
Прочность материалов в первую очередь зависит от энергии связи между частицами (атомами, ионами, молекулами), их образующими. Для кристаллических веществ, расстояния между частицами в которых строго определённо, можно рассчитать теоретическую прочность исходя из количества связей, попадающих в сечение разрыва. Поскольку идеальных кристаллов, т.е. кристаллов с идеальной кристаллической решёткой, не существует, имеющиеся дефекты кристаллической решётки будут снижать реальные значения прочности по сравнению с теоретическими.
Решающее влияние на реальную (физическую) прочность оказывают поверхностные дефекты в виде микротрещин. Именно они в состоянии понизить прочность по сравнению с теоретической в сотни раз. Впервые это было экспериментально доказано исследованиями, проводившимися в Физико-техническом институте Академии наук под руководством А. Ф. Иоффе на примере кристаллов каменной соли. Теоретическая прочность на растяжение кристаллов NaCl приблизительно составляет 2 ГПа, а реально при комнатной температуре прочность не превышает 5 МПа, т.е., в 400 раз ниже. В то же время при испытаниях, проводившихся в горячей воде, прочность повышалась в десятки раз и, в ряде случаев, приближалась к теоретической. Горячая вода растворяет дефектный поверхностный слой, содержащий трещины (концентраторы напряжения), и прикладываемое напряжение при этом распределяется на всё поперечное сечение.
Эти закономерности чётко прослеживаются на материалах любого типа. Так, нитевидные кристаллы железа, представляющие собой практически монокристалл с малым количеством дислокаций, имеют предел прочности при растяжении порядка 10 ГПа, а поликристаллическое железо, очищенное методом зонной плавки, имеют предел прочности при растяжении всего 0,1 ГПа. Легированные стали после специальной термообработки обладают прочность порядка 2 – 3 ГПа.
Керамика по механическим свойствам характеризуется высокой твёрдостью, но, к сожалению, хрупкостью и чувствительностью к термическим ударам. Прочность керамических материалов во многом определяется её многофазностью, в частности, наличием газовой фазы, присутствие которой обусловлено технологией керамики. Механические испытания керамики обычно сводятся к определению предела прочности при сжатии и при изгибе и реже – при растяжении. Наибольшей прочностью обладают керамики на основе чистого оксида алюминия А12О3 или А12О3 с добавками других соединений, например, карбида титана ТiC. При этом чем меньше пористость (чем меньше размер зерна), тем выше прочностные характеристики. Так, керамика на основе чистого А12О3 при диаметре зерна 2 – 3 мкм имеет предел прочности при сжатии сж 3,5 – 4 ГПа, предел прочности при изгибе изг 0,4 – 0,6 ГПа, а при размере зерна 0,5 – 1,6 мкм изг = 0,8 ГПа. Керамика А12О3 с добавкой 20 – 40 % ТiC обладает более высокими характеристиками: при размере зерна 1 – 2 мкм сж = 4 – 5 ГПа, изг = 0,7 – 0,8 ГПа, при размере зерна 0,3 – 1,2 мкм изг = 0,9 ГПа.
Прочность обычных стёкол как правило лежит в диапазоне 70 – 100 МПа, термически упрочнённое (закалённое) – 210 МПа, химически упрочнённое – 390 МПа, а стекловолокно – 2 – 3,8 ГПа.
Полимерные материалы в неориентированном состоянии имеют предел прочности при растяжении 20 – 80 МПа, а при высокой степени ориентации прочность достигает 6 – 10 ГПа, т.е., находится на уровне нитевидных кристаллов железа и во много раз превышают прочностные характеристики металлических сплавов. Если учесть, что плотность полимеров обычно составляет 0,9 – 1,4 т/м3, то удельные значения прочности полимеров превосходят удельные значения прочности металлических материалов в десятки раз.
3.1.1. Особенности структуры и свойств полимерных материалов.
Как видим, полимерные материалы сильно отличаются от металлов, стекол, керамики. Эти отличия обусловлены специфической структурой полимеров. Полимеры – это высокомолекулярные соединения, макромолекулы которых построены из многократно повторяющихся одинаковых групп атомов – звеньев. Количество звеньев, составляющих макромолекулу, называется степенью полимеризации (СП).
Полимеры с молекулярной массой от 500 до 10000 называют олигомерами, больше 104 – высокополимерами или просто полимерами.
Свойства полимеров, особенно физико-механические, определяются их цепным строением и зависят от химической природы, структуры макромолекул и характера надмолекулярных образований. Проследим влияние отдельных факторов на свойства полимеров.
Молекулярная масса.
Из трёх агрегатных состояний вещества – твёрдого, жидкого и газообразного, полимерам присущи только твёрдое и жидкое. Газообразное состояние для полимеров не известно. Это связано с их большой молекулярной массой, приводящей к тому, что величина взаимодействия макромолекул друг с другом, так называемая энергия когезии, оказывается выше, чем прочность химической связи. В результате при нагревании испарению полимера предшествует его деструкция, т.е. распад макромолекул на фрагменты меньшей массы.
Измеримой механической прочностью полимеры обладают только при достижении некоторой минимальной степени полимеризации. До СП порядка 250 наблюдается приблизительно прямая пропорциональность между СП (или молекулярной массой М) и р (предел прочности при растяжении). Дальнейшее увеличение СП всё слабее сказывается на росте р и при СП порядка 600 рост р практически прекращается. Следует учесть, что при синтезе полимеров образуются макромолекулы с различной СП.
Структура макромолекул.
Понятие «структура макромолекул» чрезвычайно ёмкое и в зависимости от рассматриваемого уровня имеет различный смысл. Сюда входит и внутреннее строение макромолекул, т.е. последовательность соединения атомов друг с другом, и пространственное расположение атомов или групп атомов относительно оси макромолекулы и форма самой макромолекулы.
О





 т структуры макромолекул зависят такие важные свойства полимеров, как гибкость макромолекул, способность кристаллизоваться, механическая прочность, плотность, стойкость к химическому старению и пр. По форме макромолекулы бывают (см. рис. 3.2) линейные (1), циклоцепные (2), спироцепные (3), лестничные (4) и паркетные (5), схемы которых представлены на рис. 2. По мере усложнения структуры макромолекул (от 1 к 5) уменьшается гибкость, увеличивается термостойкость, механическая прочность. Отличными эксплуатационными свойствами обладают полимеры циклоцепного и лестничного строения.
т структуры макромолекул зависят такие важные свойства полимеров, как гибкость макромолекул, способность кристаллизоваться, механическая прочность, плотность, стойкость к химическому старению и пр. По форме макромолекулы бывают (см. рис. 3.2) линейные (1), циклоцепные (2), спироцепные (3), лестничные (4) и паркетные (5), схемы которых представлены на рис. 2. По мере усложнения структуры макромолекул (от 1 к 5) уменьшается гибкость, увеличивается термостойкость, механическая прочность. Отличными эксплуатационными свойствами обладают полимеры циклоцепного и лестничного строения.






















1 2 3 4 5
Рис.3.2. Схемы молекулярных структур полимеров.
При синтезе полимеров, особенно линейного и циклоцепного строения, часто образуются макромолекулы с разветвлениями. Эти разветвления, в свою очередь, могут разветвляться, могут химически соединяться друг с другом как в пределах одной макромолекулы, так и между различными макромолекулами. В последнем случае образуются так называемые сетчатые полимеры.
Разветвления препятствуют кристаллизации, уменьшают плотность, понижают температуру плавления Тпл, повышают растворимость и газопроницаемость, уменьшают гидродинамическое сопротивление при течении, уменьшают сопротивление раздиру.
Полимеры с линейной или разветвлённой структурой называются термопластичными или термопластами. Они при нагревании могут переходить в вязкотекучее состояние, обратимо изменяют свои свойства.
Полимеры, имеющие сетчатую структуру, при нагревании не расплавляются, а могут лишь разрушаться (деструкция). Их называют термореактивными или реактопластами. При небольшом количестве поперечных связей полимер может обладать даже высокой эластичностью (резина). С увеличением количества поперечных связей повышается твёрдость и хрупкость реактопластов, понижается их набухание в растворителях.
Такое различное отношение к нагреву термопластов и реактопластов обусловлено различной природой сил, действующих между макромолекулами. В полимерах с линейной структурой макромолекулы связаны между собой Ван-дер-Ваальсовыми силами электростатического характера, не превышающими нескольких десятков кДж/моль. При разветвлённой структуре чем больше длина ответвлений, тем дальше отстоят молекулы друг от друга и тем меньше энергия межмолекулярной связи. При сетчатой структуре макромолекулы связаны между собой не только электростатическими, но и химическими связями, энергия которых в 10 – 30 раз выше.
Химическая природа полимера влияет как на внутри-, так и на межмолекулярные связи и, соответственно, - на гибкость макромолекул, прочностные, электрофизические и физико-химические свойства полимера. Присутствие в основной цепи или в боковых заместителях атомов с различной электроотрицательностью обычно приводит (если не наблюдается компенсации, как в случае мономеров симметричного строения) к возникновению диполей и, соответственно, к возрастанию межмолекулярного взаимодействия за счёт образования водородных связей. При этом гибкость макромолекул уменьшается, прочность возрастает, диэлектрические свойства ухудшаются, возрастает стойкость к маслам, бензину и др. неполярным растворителям.
Широкие возможности для модификации свойств полимеров открываются при синтезе полимеров из различных по химической структуре мономеров. Полимеры, образующиеся при этом, называются сополимерами. Например, политетрафторэтилен (фторопласт Ф-4) является продуктом полимеризации тетрафторэтилена СF2=CF2. Ф-4 обладает уникальными химическими, физическими, электрическими свойствами. Однако он ни в чём не растворяется и при нагревании не переходит в жидкое состояние. Это существенно затрудняет его переработку в изделия. Если же провести сополимеризацию тетрафторэтилена с каким-либо другим мономером (этиленом СН2=СН2, винилиденфторидом СН2=СF2, трифторхлорэтиленом CF2=CFCl и др.), то образующийся сополимер, практически сохраняя достоинства Ф-4, приобретает способность растворяться или расплавляться.
Фазовые состояния полимеров.
Полимеры в твёрдом агрегатном состоянии могут находиться как в аморфном (не кристаллическом), так и в кристаллическом фазовых состояниях. Зная механизм кристаллизации, можно регулировать структуру полимеров и, соответственно, их физико-механические свойства.
Кинетика процесса кристаллизации характеризуется двумя величинами – скоростью образования зародышей кристаллизации и скоростью роста кристаллов. Устойчивый зародыш (или зародыш критического размера) представляет собой микрокристалл, который по своим размерам находится в равновесии со средой, поэтому вероятность его роста и растворения одинаковы.
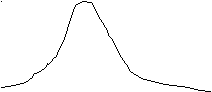
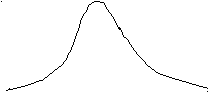
Скорость образования зародышей максимальна при температуре значительно ниже Тпл, в то время, как линейная скорость роста кристаллов имеет максимум немного ниже Тпл (рис.3.3). Максимальная скорость кристаллизации наблюдается при температуре 8/9 от Тпл. При высокой температуре, близкой к Тпл, устойчивые зародыши имеют большие размеры, но их очень мало. В результате вырастают крупные кристаллы.
 V Vобр. зарод. Vроста кристаллов
V Vобр. зарод. Vроста кристаллов Т
ТРис. 3.3. Кинетические кривые процесса кристаллизации
При низкой температуре появляется много мелких зародышей, - в результате образуется мелкокристаллическая структура.
При очень быстром охлаждении можно проскочить область роста кристаллов и получить в принципе кристаллизующийся полимер в аморфном состоянии.
Эти представления о кинетике кристаллизации применимы к материалам любой природы.
Физические состояния полимеров.
Гибкость цепных молекул обусловливает существование трёх физических состояний – стеклообразного, высокоэластического и вязкотекучего. Стеклообразное и вязкотекучее состояния наблюдаются и в низкомолекулярных веществах. Высокоэластическое состояние присуще только полимерам. Каждому физическому состоянию соответствуют свои механические, электрические, физические свойства. Наблюдая изменение соответствующих характеристик, например, модуля упругости, деформируемости, теплоёмкости, теплопроводности, тангенса угла диэлектрических потерь и пр., можно определить температурные области существования физических состояний конкретного полимера. Часто для изучения физических состояний полимеров проводят термомеханические исследования, то есть изучают деформацию полимера в зависимости от температуры Т при постоянных нагрузках Р и времени действия нагрузки .
Т
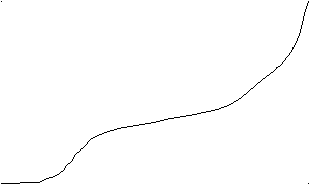 ипичная термомеханическая кривая для аморфного линейного полимера представлена на рис. 3.4.
ипичная термомеханическая кривая для аморфного линейного полимера представлена на рис. 3.4.
L/L

Тс Тт Т
Рис. 3.4. Термомеханическая кривая аморфного линейного полимера.
Для аморфного полимера при переходе из одного физического состояния в другое ряд физических характеристик изменяется, однако фазовое состояние не изменяется. Более того, высокоэластическое состояние по многим показателям ближе к жидкому агрегатному состоянию, чем к твёрдому. Для выяснения причин, вызывающих различия деформационных свойств полимеров в различных физических состояниях, рассмотрим, что происходит с полимером в этих состояниях.
В вязкотекучем состоянии под действием приложенной к расплаву силы макромолекулы перемещаются друг относительно друга. Однако, в отличие от низкомолекулярных веществ, это перемещение осуществляется ступенчато, оно складывается из ряда перемещений отдельных частей гибких макромолекул и напоминает движение червей. Часть макромолекулы, способную в определённых пределах к самостоятельному перемещению, независимо от перемещения самой макромолекулы в целом, называют сегментом, тем самым подчёркивая аналогию с движением червей. Таким образом, в вязкотекучем состоянии за время действия силы макромолекулы успевают переместиться целиком и занять новое равновесное состояние. Так осуществляется течение полимеров.
В высокоэластическом состоянии за время действия силы макромолекулы не успевают перемещаться целиком, происходит только движение сегментов. После снятия силы сегменты возвращаются в исходное состояние. Так осуществляются большие обратимые деформации полимеров.
По мере понижения температуры вязкость полимера растёт, что затормаживает сегментальное движение. При достижении вязкости 1012 – 1013 Пас сегментальное движение становится невозможным (при прежних временах действия прежней силы) и полимер будет находиться в стеклообразном состоянии. Агрегативно это соответствует твёрдому состоянию.
Тот или иной тип физического состояния зависит, следовательно, как от температуры, так и от величины и продолжительности действия силы (скорости приложения силы). Всё определяется тем, насколько успевают макромолекулы отреагировать на изменение напряжённого состояния или, как говорят, отрелаксировать.
Понятие «релаксация» применимо к любым процессам и обозначает переход из неравновесного состояния в равновесное. При этом в системе уменьшаются внутренние напряжения, вызванные изменением внешних условий. Само слово «релаксация» происходит от латинского слова relaxatio- ослабление.
Существует простая зависимость, связывающая время механической релаксации р с температурой Т и приложенным напряжением .
( U - )/RT
р = 0 . е (3.1)
где 0 10-11с; U – энергия активации вязкого течения; - коэффициент; R – универсальная газовая постоянная. Как видно, Т и уменьшают время релаксации.
Именно уменьшением времени релаксации при больших напряжениях до уровня, соответствующего высокоэластическому состоянию, объясняются наблюдаемые большие деформации стеклообразных полимеров (рис.1.1). Эти деформации получили название «вынужденно-эластические». Вынужденно-эластическая деформация по своей природе является высокоэластической и обратимой. Обратимость осуществится, если полимер нагреть выше Тс, т.е., если ускорить релаксационные процессы.
Обратимся вновь к рис. 1.1. На этом рисунке кривая 4 описывает деформацию полимера, находящегося в высокоэластическом состоянии. При малых напряжениях и температурах, близких к Тс, наблюдается начальный крутой участок (1), переходящий затем в прямолинейный пологий участок (2) и крутой участок (3). По участку 1 можно определить Еупр, по участку 2 – Евыс-эласт. На участке 3 растяжению подвергается уже ориентированный образец.
Высокоэластическая деформация имеет энтропийный характер, т.е. связана с изменением конформации макромолекул. При деформации происходит выпрямление свёрнутых макромолекул и энтропия системы уменьшается. При нагревании каучукоподобного тела тепловое движение увеличивает беспорядок, иначе говоря, приводит к возрастанию энтропии. Следовательно, при нагревании резины должно возрастать сопротивление деформированию. Действительно, с ростом температуры модуль эластичности каучукоподобных полимеров увеличивается.
Как известно, энтропия системы есть логарифм термодинамической вероятности S = k ln W. Для применения этого уравнения к рассмотрению высокоэластической деформации делается предположение о структуре полимера, как сетчатой, при этом не важно, будет ли эта сетка химической или физической. Это нужно для исключения процессов течения. Место соединения нескольких цепей называется узлом сетки, а молекулярная масса отрезков цепей между узлами сетки обозначается Мс. Частотой сетки N тогда будет N = d/Mc, где d – плотность полимера.
Между модулем эластичности Ев-э, плотностью, Мс и температурой Т существует простое соотношение:
Ев-э = 3RTd/Мс . (3.2)
Таким образом, по значению Ев-э можно рассчитать параметры сетки.
В действительности полностью исключить процесс течения при наличии физической сетки нельзя и высокоэластической деформации сопутствует некоторая доля пластической деформации.
В реальных эластомерах высокоэластическая деформация не является чисто энтропийной, но сопровождается изменением внутренней энергии. Это объясняется тем, что при деформации происходит изменение объёма, сопровождающееся изменением средних расстояний между полимерными цепями , при этом изменяется их энергия взаимодействия.
Полимеры не однородны по молекулярной массе, более того, они содержат два вида структурных элементов – звенья цепи и сами цепи. Размеры их значительно отличаются, отличается и их подвижность. Время релаксации звеньев составляет 10-4 – 10-6 с, а время релаксации цепей очень велико – от минут до лет. По этой причине высокоэластическая деформация по своей природе не равновесна, т.е. она развивается во времени и достижение равновесного значения может, в зависимости от температуры, происходить очень долго. Аналогично, после снятия нагрузки очень долго происходит восстановление прежней, исходной формы образца. Для линейных полимеров полное восстановление исходной формы может вообще не наблюдаться из-за наличия пластической деформации.
Разграничить виды деформации можно, изучая кривые ползучести ( - ). Ползучесть – это явление постепенного развития деформации. Для разделения общей деформации на виды проводят испытания в режиме нагружение – разгрузка.
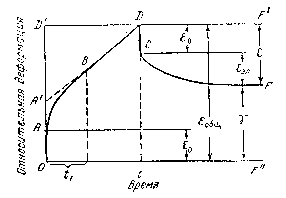
Рис. 3.5. Зависимость относительной деформации от времени (кривая ползучести).
На этом рисунке участок ОАВD соответствует изменению относительной деформации при нагружении, а участок DCE – при разгружении. Участок ОА отвечает условно - упругой деформации, участок АВ характеризует одновременно развивающиеся высокоэластическую деформацию и деформацию течения, участок ВD – необратимая (пластическая) деформация, являющаяся процессом установившегося течения.
Видно, что общ = упр + в-э + необр. (3.3)
Если продолжить прямую ВD до пересечения с осью ординат, то из треугольника А1DD1 можно найти величину относительной деформации течения
d/dt = /t = A1D1/D1D, откуда A1D1 = . (3.4)
По кривой ползучести можно не только разделить общую деформацию на виды, но и рассчитать целый ряд важных характеристик. Это:
1) вязкость = т/(d/d/t); (3.5)
2) Еупр = т/0 = т/ОА; (3.6)
3) Ев-э = т/в-э = т/АА1 (3.7)
Здесь т – действующее напряжение.
Ползучесть проявляется не только в высокоэластическом состоянии, но и в стеклообразном. Казалось бы, в стеклообразном состоянии времена релаксации очень велики и, кроме упругой, других видов деформации при небольших напряжениях не должно быть. Тем не менее, ползучесть наблюдается и в стеклообразном состоянии. Это объясняют наличием быстрых релаксационных процессов, обусловливающих деформацию, по своей природе являющуюся как бы промежуточной между упругой и вынужденно-эластической. Они получили названия деформации упругого последействия.
К явлениям упругого последействия, кроме ползучести, относятся:
- зависимость модуля упругости Еупр от скорости деформирования или частоты воздействия, механические потери (механический гистерезис);
- релаксация напряжения при постоянной деформации.
Отличием ползучести полимеров в стеклообразном состоянии от ползучести в высокоэластическом состоянии является значительно меньшая величина необратимой деформации, которая может развиться только при очень больших временах действия нагрузки.
Релаксация напряжения. Если образец аморфного полимера быстро растянуть и закрепить в этом положении, то напряжение в образце с течением времени уменьшается (по экспоненте). Это вызвано тем, что под действием этого напряжения макромолекулы, не успевшие изменить конформацию за время деформирования, изменяют конформацию – вытягиваются. В неполярных полимерах это происходит быстрее, чем в полярных, так как в неполярных межмолекулярное взаимодействие слабее.
Механический гистерезис – связан с несовпадением скоростей деформации при нагружении и разгрузке, при этом происходит отставание деформации от напряжения.
 |
| Рис. 3.6. График механического гистерезиса. |
Если за время действия нагрузки успела развиться пластическая деформация (вязкое течение), то образец уже никогда самопроизвольно не восстановит своей исходной формы. Если же цикл нагружения был проведён так быстро, что вязкое течение не успело начаться, то вся «остаточная деформация» впоследствии исчезнет.
Площадь петли гистерезиса характеризует необратимо рассеянную в виде тепла механическую энергию.
На примере вынужденно-эластической деформации можно было увидеть, что время релаксации уменьшается не только при увеличении температуры, но и напряжения. Скорость релаксационных процессов также увеличивается при введении в полимер пластификаторов.
Пластификаторы – это обычно низкомолекулярные высококипящие жидкости с низкой упругостью паров. Введение пластификаторов улучшает эластичность материала, придаёт ему морозостойкость и облегчает его переработку. Сущность пластификации заключается в изменении вязкости системы, увеличении гибкости макромолекул и подвижности надмолекулярных структур (НМС). Пластификаторы оказывают влияние на все физические свойства – прочность, эластичность, хрупкость, диэлектрические потери, Тс, Тт и т.п. Пластификаторы понижают Тс и Тт , однако Тс понижается сильнее, чем Тт, поэтому, наряду с повышением морозостойкости, наблюдается расширение области высокоэластического состояния. Однако, при больших содержаниях пластификатора снижение Тс замедляется, а Тт продолжает интенсивно уменьшаться. В результате область высокоэластического состояния сужается. Отсюда следует, что существует оптимум по содержанию пластификатора в полимере.
Всё это справедливо для аморфных полимеров. Для кристаллических полимеров введение пластификаторов сильно понижает Тс и практически не оказывает влияния на Тт, которая обычно совпадает с Тпл. Количественной мерой пластифицирующего эффекта является величина снижения Тс ( Тс).
Пластификаторы, хотя и являются слаболетучими жидкостями, тем не менее всё же летучими. С течением времени пластифицирующий эффект снижается. Единственными веществами, не способными испаряться, являются полимеры. Заманчиво для пластификации жёстких полимеров использовать гибкие полимеры – эластомеры. Отличные результаты достигаются при пластификации поливинилхлорида нитрильным каучуком СКН-40. К сожалению, не для всех полимеров можно подобрать соответствующий, совмещающийся с ним эластомер.
Вопросы для самопроверки
- Основные характеристики механических свойств материалов. Сравните механические свойства материалов различной природы.
- Какова роль сил межмолекулярного взаимодействия в полимерах?
- Теоретическая и реальная прочность материалов.
- Основные особенности свойств полимеров и причины их проявления.
- Что такое релаксация и как влияют внешние факторы на время релаксации?
- Влияние структуры макромолекул на свойства полимеров.
- Особенности кристаллической структуры полимеров.
