Клинико-иммунологическая характеристика и иммунотерапия пневмонии у новорожденных, инфицированных внутриутробно 14. 00. 36 Аллергология и иммунология 14. 00. 09 Педиатрия
| Вид материала | Автореферат диссертации |
- Клинико-лабораторная характеристика и лечение хламидийной инфекции, ассоциированной, 311.6kb.
- Сравнительный и исторический анализ методического прогресса в аллергологии: аллерген-специфическая, 383.99kb.
- Клинико иммунологические особенности аллергодерматозов на фоне урогенитальной инфекции, 335.48kb.
- Образовательный стандарт послевузовской профессиональной подготовки специалистов Специальность:, 1035.98kb.
- Урогенитальный хламидиоз: клинико-иммунологическая характеристика, иммуногенетические, 872.18kb.
- Клинико-функциональные и иммунопатогенетические механизмы формирования усиления рефракции, 788.74kb.
- Расписание занятий на элективе для студентов 6 курса «Клиническая аллергология», 41.99kb.
- Клинико-иммунологическая характеристика обострений бронхиальной астмы 14. 00. 43 пульмонология, 423.16kb.
- Адаптация недоношенных новорожденных детей при церебральной ишемии (клинико-функциональное, 394.95kb.
- Рабочая программа учебной дисциплины клиническая иммунология и аллергология для специальности:, 1167.83kb.
Полученные материалы были использованы при подготовке проекта «Программы клинических испытаний эффективности и безвредности иммунологического препарата Аффинолейкин в лечении пневмоний у детей в первые три года жизни», представленной в Комитет медицинских иммунологических препаратов Минздрава России.
Апробация работы. Материалы и выводы диссертации доложены и обсуждены на Российской научно-практической конференции «Актуальные вопросы педиатрии и детской хирургии», г. Ульяновск, ноябрь, 2000 г. ; на Областной конференции врачей-педиатров, посвященной «Дню педиатра», г. Ульяновск, май, 2001; на Российской конференции «Актуальные вопросы педиатрии, акушерства, гинекологии и детской хирургии» г. Ульяновск, ноябрь 2002 г. ; на VIII Международном конгрессе по иммунореабилитации «Аллергия, иммунология и глобальная сеть», Канны, Франция, апрель, 2002 г. (стендовый доклад); на XXXVII научно-практической межрегиональной конференции врачей «Здравоохранение Ульяновской области в XXI веке», г. Ульяновск, май, 2002 г. ; на Российском конкурсе молодых ученых, г. Москва, 2002 г. ; на V съезде иммунологов и аллергологов СНГ, июнь 2003 г., г. Санкт-Петербург (доклад). Апробация диссертации проведена 2 июля 2003 г. на межкафедральном заседании кафедр педиатрии, акушерства и гинекологии медицинского факультета Ульяновского государственного университета.
Публикации. По материалам диссертации сделано 11 публикаций, ещё 2 статьи приняты в печать.
Структура и объем диссертации:
- диссертация состоит из введения, обзора литературы, 4-х глав описания собственных исследований, обсуждения результатов, выводов, практических рекомендаций и указателя литературы, содержащего ссылки на работы отечественных (187) и иностранных (98) авторов.
- текст изложена на 151 страницах формата А4, количественные данные представлены в 20 таблицах и проиллюстрированы 45 рисунками.
Работа выполнена по плану Института медицины, экологии и физической культуры Ульяновского государственного университета. Код государственной регистрации 76.29.47, при поддержке Гранта «Университеты России» №1101018.
Исследования проводились на клинических базах кафедры педиатрии Ульяновского Государственного Университета - в Областной Детской Клинической больнице (главный врач – заслуженный врач России Губарева Т.А.) и родильном доме №3 Городского Перинатального центра (главный врач – Богомолова Л.К.).
Экспериментальная часть работы проведена в лаборатории мембранных процессов (заведующий лабораторией – к.м.н., доцент Мац А.Н.) НИИ вакцин и сывороток им. И.И.Мечникова РАМН (директор – академик РАМН, профессор Семенов Б.Ф.).
С О Д Е Р Ж А Н И Е Р А Б О Т Ы
Материал и методы исследований
Клинико-лабораторные исследования. Под наблюдением в стационарах находились 174 новорожденных: 135 – больных неонатальной пневмонией и 39 практически здоровых. Изучение преморбидного фона и клинического состояния детей проводили по специально разработанному протоколу обследования новорожденного. В группе больных пневмонией, было 75 доношенных и 60 недоношенных новорожденных; 63 девочки и 72 мальчика.
Диагноз пневмонии был сформулирован в соответствии с Международной классификацией болезней и причин смерти (Х пересмотр), с учётом методических рекомендаций Минздрава РФ и классификации Сотниковой К.А. (1985).
При общеклиническом обследовании производили общий анализ и биохимическое исследование крови, общий анализ мочи, копрограмму, электрокардиограмму, рентгенологическое исследование органов грудной клетки, нейросонографию в динамике и, по показаниям - ультразвуковое исследование сердца и органов брюшной полости; все дети проходили консультации невропатолога и офтальмолога.
У всех больных детей проводилась иммунохимическая диагностика сексуально-трансмиссивных инфекций – токсоплазменной, цитомегаловирусной, герпетической, хламидийной, уреаплазменной и трихомонадной – путём выявления специфических антигенов в отделяемом из бронхов при ИВЛ, в слюне, в смывах из глотки, в моче и сыворотке крови , а также определения сывороточных антител изотипа IgM и IgG в динамике:
- для диагностики токсоплазмоза по динамике гуморального ответа использовали иммуноферментные тест-системы «Векто-Токсо-IgМ-стрип» и «Векто-Токсо-IgG-cтрип» (ЗАО“Вектор-Бест”, Новосибирск), выявляющие антитела изотипов IgМ и IgG в сыворотке крови;
- антитела IgМ и IgG к вирусу цитомегалии, в частности к его предраннему белку, определяли также в иммуноферментном анализе;
- антитела IgG к трихомонадам определяли, используя иммуноферментную тест-систему “Трихомоно Бест-Ig G-стрип” (ЗАО “Вектор-Бест”, г.Новосибирск);
- антигены цитомегаловируса человека идентифицировали в реакции непрямой иммунофлюоресценции с помощью диагностикума “Цитомега Флюоскрин” фирмы “Ниармедик” (Москва); кроме того, в слюне и моче определяли пораженные цитомегаловирусом гигантские клетки типа «совиный глаз»;
- антигены Ureaplasma urealiticum выявляли в мокроте, промывных водах из трахеи и моче методом прямой иммунофлюоресценции (РИФ), применяя набор диагностических антител “УреаСлайд” (ЛАБдиагностика, г.Москва);
- антигены Micoplasma hominis выявляли в мокроте, слюне, моче, промывных водах из трахеи методом прямой иммунофлуоресценции, применяя диагностикум “МикогомоФлюоскрин” фирмы “Ниармедик” (г.Москва).
Для определения содержания IgG1, IgG2, IgG3 и IG4 субклассов в сыворотке применяли иммуноферментную тест-систему (ООО «Стибиум», Санкт-Петербург).
Концентрацию лактоферрина в сыворотке крови определяли также с помощью иммуноферментной тест-системы «Лактоферрин-стрип» ( ЗАО «Вектор-Бест», Новосибирск).
Содержание подклассов IgG и лактоферрина в сыворотке, а также количество лейкоцитов с токсической зернистостью у каждого ребёнка определяли трижды: I - при поступлении в стационар (на второй-третий день заболевания), II - через неделю после поступления, III - перед выпиской из стационара, при выздоровлении, т.е. в периоды разгара, стабилизации и инволюции неонатальных пневмоний.
Все больные получали специфическую этиотропную фармакотерапию (при условии адекватной этиологической диагностики): пенициллины с расширенным спектром активности, аминогликозиды II и III поколения, полусинтетические макролиды, линкосамиды, цефалоспорины II - IV поколения, видарабин, ацикловир и другие антимикробные средства, допущенные для лечения новорожденных. В качестве патогенетического и симтоматического лечения использовали препараты для дезинтоксикации – солевые растворы, кровезаменители, растворы глюкозы, компоненты и препараты крови человека; применяли кислородотерапия ( ИВЛ, маска, палатка), антиоксиданты и витамины, десенсибилизирующие, стероидные и нестероидные противовоспалительные средства.
Для лечения неонатальных пневмоний в дополнение к этиотропной и патогенетической терапии у 48 больных была применена вспомогательная иммунотерапия Аффинолейкином в инъекционной и сублингвальной
лекарственных формах – препарат вводили подкожно по 0,2 ед/кг или сублингвально по 1,0 ед/кг 2 - 3 раза в неделю, до 10 аппликаций на курс.
Экспериментальные исследования. Перед началом иммунотерапии неонатальных пневмоний было проведено дополнительное доклиническое исследование безвредности и иммуноадъювантной активности Аффинолейкина было проведено на новорожденных мышатах F1(СBА x C57BL/6J), которым в первый день жизни подкожно в объёме 0.05 мл 0.9% раствора хлористого натрия вводили по 0.07 ед препарата (эквивалентно переносу 3.5 х 107 лейкоцитов).В группе Аффинолейкина и интактного контроля было исходно по 25 мышат, которых оставили в клетках вместе с кормящими самками и в первую неделю жизни ежедневно взвешивали. Через месяц всех мышат иммунизировали Ещё через месяц брали кровь из ретроорбитального венозного сплетения и определяли антитоксическую активность индивидуальных сывороток в реакции нейтрализации дифтерийного токсина в коже кроликов по C.Jensen'y на уровне 1/3000 МЕ [Сиандартизованная методика ГИСК им. А.Л. Тарасевича]. Перед иммунизацией у животных брали кровь в 6% раствор цитрата натрия и определяли пороговую концентрацию дифтерийного анатоксина, вызывающую конгломерацию лейкоцитов [Matz A.N. et al., 1971].
Для оценки значимости (p) различий и корреляций в сравниваемых группах больных и экспериментальных животных пользовались критериями параметрической (t -критерий Стьюдента, 2- Пирсона) и непараметрической статистики (критерии U - Вилкоксона-Манна-Уитни, Q - Розенбаума, медианный - Ван дер Вардена и корреляции Спирмена).
Результаты исследования и их обсуждение
Клинико- лабораторные исследования.
Формы неонатальной патологии лёгких (Табл. 1). Чаще всего встречались одно- и двусторонние полисегментарные пневмонии; реже - пневмопатии и односторонние очаговые пневмонии. Более 70% одно- и 30% двусторонних полисегментарных пневмоний были осложненными - при одностороннем процессе, в основном, плевритом и долевым ателектазом, а при двустороннем - ателектазом одного легкого и напряженным пневмотораксом. Пневмопатия, характеризующаяся дыхательной недостаточностью и кислородной зависимостью, часто сочеталась с поражением ЦНС (в 62% случаев с церебральной ишемией II степени, а в 30% - с внутри-желудочковыми кровоизлияниями I-II степени) В 43% случаев односторонняя и в 55% - двусторонняя пневмония развивалась на фоне пневмопатии. Среди детей, больных двусторонней пневмонией, 67% были недоношенными, как правило, II-III степени ; среди больных с односторонним процессом было около 40% недоношенных и 18% детей с признаками внутриутробной гипотрофии.
Таблица 1.
Формы неонатальной патологии лёгких
.
| Характер пневмонии | Течение | Всего | ||||
| осложненные | неосложненные | |||||
| n | % | n | % | N | % | |
| Пневмопатия | 1 | 6,6 | 12 | 93,3 | 13 | 9,6 |
| Односторонняя очаговая | 9 | 63,4 | 4 | 37,6 | 13 | 9,6 |
| Двусторонняя очаговая | 6 | 40 | 9 | 60 | 15 | 11,2 |
| Одностор.полисегмент. | 21 | 28,7 | 52 | 71,3 | 73 | 54,1 |
| Двустор.полисегмент. | 7 | 33,3 | 14 | 66,7 | 21 | 15,5 |
По клинической картине неонатальная полисегментарная пневмония отличалась от очаговой меньшей выраженностью, но большей продолжительностью дыхательной недостаточности и кислородной зависимости. В первые дни стационарного лечения при аускультации как при очаговой, так и при полисегментарной пневмонии отмечались крепитирующие хрипы при ослаблении везикулярного дыхания; но наблюдались несколько больший лейкоцитоз (среднее число лейкоцитов, соответственно, 25 1 и 20 2 × 109/л) и анемия (содержание гемоглобина - 118 5 и 128 7 г/л), а также повышенный ЛИИ ( 6,5 0,4 и 5,8 0,4 – в норме 1,3 0,2).
Возбудители неонатальных пневмоний. Частота выявления отдельных возбудителей сексуально-трансмиссивных инфекций у обследованных новорожденных представлена на рис. 1. Они были идентифицированы во всех случаях неонатальных пневмоний при моно- и микс-инфекциях. Наиболее часто был обнаружен вирус простого герпеса (ВПГ) 1 и 2 серотипов (48%) и цитомегаловирус
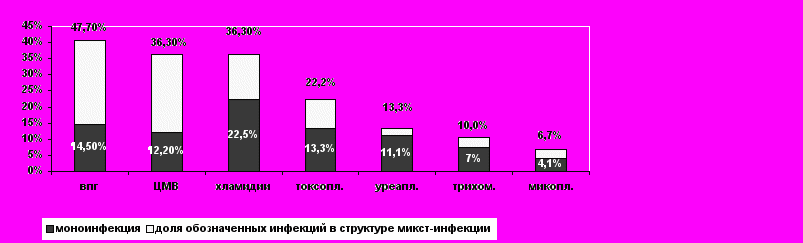 Рисунок 1. Частота различных инфекций у новорожденных, больных пневмонией.
Рисунок 1. Частота различных инфекций у новорожденных, больных пневмонией.(ЦМВ) (36%), а также хламидии (36%). Хламидии чаще других (22%) были представлены моноинфекцией, при этом диагноз хламидийной пневмонии был поставлен лишь в 8% случаев. ВПГ (33%) чаще, чем ЦМВ (24%) и хламидии (14%), диагносцировался при микс-инфекциях. В 21% случаев имела место герпесвирусная (ВПГ + ЦМВ), а в 36% - герпесвирусно-хламидийная (ВПГ + ЦМВ + хламидии) микст-инфекция.
Клиническое течение неонатальной пневмонии, которой сопутствует герпесвирусно-хламидийная инфекция, было наиболее тяжёлым и имело наименее благоприятный прогноз. Герпесвирусно-хламидийная инфекция чаще, чем герпесвирусная, сопровождала двустороннюю очаговую пневмонию, соответственно, в 12,5% и 7,1% (р 0,01); одностороннюю полисегментарную – в 60% и 42,9% (р 0,01), двустороннюю полисегментарную пневмонию - в 20% и 16,9% (р 0,01) случаев. При герпесвирусно-хламидийной пневмонии чаще, чем при герпесвирусной встречались гипоксически-ишемические поражения ЦНС II и III степени, соответственно - 46,4% и 32,5% (р 0,01); 25% и 20% (р 0,05), а также гораздо чаще выявлялись внутрижелудочковые кровоизлияния III степени, соответственно - 10% и 3,6% (р 0,01).
Пренатальные и интранатальные предпосылки внутриутробного инфицирования. Выявленные возбудители сексуально-трансмиссивных инфекций в большинстве случаев поражают плод транспланцентарно во время беременности или во время вагинального родоразрешения. Однако, нельзя исключить их перинатальную передачу от матери при грудном кормлении, либо от медицинского персонала и других детей воздушно-капельным или контактным путём, а главное, при инвазивных лечебных и диагностических мероприятиях (ИВЛ, катетеризация и т.п.). Тем не менее, согласно собранным нами данным, единственный источник инфекции - это мать, и само инфицирование и условия его реализации в воспаление лёгочной паренхимы зависят от пренатальных и интранатальных факторов риска.
Половина больных неонатальной пневмонией рождены от первой беременности. У половины матерей анамнез был отягощен: самопроизвольным выкидышем (20%), медицинским абортом (19%); замершей беременностью (6%). У 71% матерей находили анемию анемию I-II степени; у 21% - заболевания щитовидной железы; у 13% - повышение внутричерепного давления; 7% женщин страдали ожирением, 4% - врожденными пороками сердца. У 15% женщин часто отмечались острые респираторные заболевания в анамнезе. Нередко встречались хронические заболевания, обусловленные условнопатогенной инфекцией - кольпит (56%), пиелонефрит (34%), аднексит (8%). Установлено, что матери детей, больных герпесвирусно-хламидийной пневмонией, в два раза чаще страдали обострениями хронического пиелонефрита и кольпита во время беременности, и у 73% из них находили анемию.
Высокая частота осложнений имела место и при последней бременности. У 33% женщин она осложнилась нефропатией I степени, у 31% - возникла угроза преждевременных родов. В 13% случаев у матерей отмечались герпетические высыпания на губах. У матерей новорожденных с ЦМВ- и ВПГ-инфекцией наблюдались частые ОРЗ не только в анамнезе, но и в ходе последней беременности. У 33% матерей околоплодные воды были окрашены меконием, у большинства – в сочетании с многоводием, что было свидетельством внутриутробной гипоксии плода. Родоразрешение более чем в половине случаев было осложненным: дети родились в тяжелой (29%) или среднетяжелой (37%). асфиксии. Наличие всех этих факторов риска в нашем материале, согласно общепринятой точке зрения, косвенно свидетельствует именно о внутриутробном заражении плода выявленными условнопатогенными возбудителями.
Известно, что наличие условнопатогенной инфекции, свидетельствующее о внутриутробном заражении, вовсе не доказывает её значения как причины пневмонии, и совокупное влияние всех перечисленных выше пре- и интранатальных факторов не всегда приводит к неонатальной пневмонии. Например в нашем наблюдении, пневмопатии были диагносцированы при недоношенности I-II степени у детей, рожденных с признаками внутриутробной гипотрофии II степени матерями, страдающими соматической патологией: анемией (39%); заболеваниями щитовидной железы (20%), кольпитом (48%), хроническим пиелонефритом (24%) без обострений процесса во время беременности. Тем не менее, эти пневмопатии , по лабораторным данным, собранным в динамике, нельзя было отнести к проявлениям острого инфекционного процесса. Следовательно, существует какой-то дополнительнй неизвестный перинатальный фактор, от которого зависит, эволюционирует ли пневмопатии в пневмонию. Таким фактором может быть глубина и особенности «неонатальной физиологической иммунодефицитности».
Сывороточный лактоферрин при неонатальных пневмониях. Лактоферрин - многофункциональный белок, который в форме ненасыщенного железом аполактоферрина обладает противомиикробными свойствами, проявляющимися в крови и на слизистых оболочках дыхательных путей. Это – один из инструментов врождённого иммунитета у плода и новорожденного, направленный против ряда видов бактерий, вирусов и грибов [Farnand S., Evans R.W., 2003]. Концентрация лактоферрина в сыворотке крови при патологии легких имеет патогенетическое (отражение активности и обширности воспаления) и диагностическое (прогностическое) значение. Как выяснилось, этот показатель в крови новорожденных при неонатальных пневмониях был примерно в 100 раз ниже, чем у здорового взрослого человека ( 1 мкг/мл сыворотки в норме и до 200 мкг/мл при воспалении), но широко варьировал ( от 0,15 до 1,1 мкг/мл). Концентрация лактоферрина была пропорциональна распространенности процесса (таблица 2) и различалась в зависимости от вида возбудителя инфекции (таблица 3).
Таблица 2.
Динамика концентрации лактоферрина в сыворотке крови при патологии лёгких у новорожденных
| Характеристика пневмонии | n | Лактоферрин (нг/мл) Мm | ||
| периоды заболевания | ||||
| | | начальный | разгара | выздорав. |
| Пневмопатия | 11 | 141,512,3 | 503,615,4 | 151,216,2 |
| Односторонняя очаговая | 10 | 257,916,4 | 705,021,1 | 174,517,3 |
| Двусторонняя очаговая | 12 | 268,719,7 | 819,814,7 | 198,713,5 |
| Односторонняя полисегмент. | 54 | 197,515,9 | 682,917,9 | 112,812,9 |
| Двусторонняя полисегмент. | 17 | 312,018,9 | 1118,619,4 | 198,618,4 |
| Здоровые новорожденные | 22 | 154,318,5 | ||
Достоверность отличий от здоровых новорожденных р 0,01, р 0,05
При герпесвирусно-хламидийной инфекции концентрация лактоферрина был выше (р 0,01), чем при герпесвирусной в начале и в разгаре заболевания, однако при реконвалесценции на фоне нормализации клинических данных у больных с герпесвирусно-хламидийной пневмонией она осталась достоверно выше нормы.
Концентрация лактоферрина находилась в зависимости от длительности ИВЛ (таблица 4).
Таблица 3.
Динамика концентрации лактоферрина в сыворотке крови у
больных неонатальной пневмонией при различных видах смешанной инфекции
| | Лактоферрин (нг/мл) | |
| Период заболевания | ВПГ+ЦМВ n=23 | ВПГ+ЦМВ+Хл n=38 |
| начальный | 189,819,4 | 303,818,4 |
| разгара | 539,717,8 | 767,018,3 |
| Реконвалесценции | 141,315,2 | 209,419,2 |
| Здоровые новорожденные | 154,318,5 | |
Достоверность различий между группами ВПГ+ЦМВ и ВПГ+ЦМВ+Хл
р 0,01, р 0,05; отличие от здоровых новорожденных: р 0,05
Согласно данным таблицы 4, концентрация лактоферрина в сыворотке крови в начальном периоде заболевания достоверно превышает норму у всех больных. У детей, находившихся на продленной ИВЛ, она была исходно выше, чем у детей без ИВЛ. В периоде разгара заболевания содержание лактоферрина было выше у детей, находившихся на продленной ИВЛ (в течение 6 дней и более). В периоде реконвалесценции концентрация лактоферрина понизилась, но во всех группах осталась выше нормы.
Таблица 4.
Динамика концентрации лактоферрина (нг/мл) в сыворотке крови при неонатальной пневмонии в зависимости от длительности ИВЛ
| Длительность искусственной вентиляции лёгких | ||||
| Период Заболевания | I n=38 | II n=40 | III n=29 | IV n=10 |
| Начальный | 327,021,2 | 353,920,1 | 385,218,7 | 412,519,3 |
| Разгара | 624,518,7 | 663,220,1 | 1115,221,4 | 1564,919,1 |
| реконвалесценции | 216,119,8 | 251,917,4 | 258,818,8 | 206,521,0 |
| Здоровые новор. | 154,318,5 | |||
