Дипломная работа
| Вид материала | Диплом |
СодержаниеГлава ii. материалы и методы исследования 2. Тест – "tail flick" 3. Фармакологическое воэдействие 4. Характеристика используемых фармокологических препаратов |
- Дипломная работа по истории, 400.74kb.
- Дипломная работа мгоу 2001 Арапов, 688.73kb.
- Методические указания по дипломному проектированию дипломная работа по учебной дисциплине, 620.15kb.
- Дипломная работа выполнена на тему: «Ресторанный комплекс при клубе знаменитых людей:, 638.16kb.
- Дипломная работа: выполнение и защита методические рекомендации, 248.83kb.
- Дипломная работа Антона Кондратова на тему «Интернет-коммуникации в деятельности предприятия, 1083.86kb.
- Итоги VII всероссийского конкурса «Лучшая студенческая дипломная работа в области маркетинга», 99.02kb.
- Выпускная квалификационная (дипломная) работа методические указания по подготовке,, 629.59kb.
- Дипломная Работа на тему Аспекты взаимодействия категорий Языковая одушевленность неодушевленность, 908.09kb.
- Дипломная работа тема: Анализ удовлетворенности потребителей на рынке стоматологических, 187.27kb.
ГЛАВА II. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
1. Объект исследования
Объектом для проведения исследования была выбрана белая лабораторная крыса (Rattus norvegicus), как наиболее распространенная модель для экспериментальных исследлваний.
Исследования проводились на белых беспородных крысах - самцах массой 180 - 200г. Животные в достатке обеспечивались пищей и водой и содержались в стандартных условиях вивария, с естественным световым режимом, при температуре 18 - 200С.
2. Тест – "tail flick"
Для определения болевого порога применяли тест - tail-flick. (D Amour and Smith, 1941; Никольская и Кандашевская, 2003; Осмакова,2003). Одновременно в опыте находилось 10 - 15 животных. Болевое раздражение наносили погружением хвоста в горячую воду температурой 560С на глубину 6 см. В данном тесте показателем болевой чувствительности животных служило изменение латентного периода (ЛП) реакции избавления от болевого раздражителя - ЛП одёргивания хвоста Реакцию считали выполненной в том случае, когда животное полностью выдёргивало хвост из сосуда с горячей водой. ЛП одёргивания хвоста - это временной показатель, измеряемый в секундах с помощью секундомера. Животных перед началом эксперимента предварительно адаптировали к условиям эксперимента, помещая их в индивидуальные иммобилизационные клетки, в которых онисохраняли естественную для них позу, каждый день на 3часа в течении двух недель. Так же непосредственно в день проведения эксперимента за 30 минут до его начала животных вновь помещали в индивидуальные иммобилизационные клетки, с целью их адаптации. Затем до введения препаратов определяли исходный уровень болевой чувствительности (ЛП0), которое вычисляли как среднее из 4-х измерений ЛП реакции одёргивания хвоста, зафиксированных с интервалом в 10 минут. Введение препарата осуществляли, не вынимая животных из индивидуальных иммобилизационных клетк. Далее в течение 1,5 - 2 часов после инъекции с интервалами в 10 минут вновь фиксировали ЛП реакции избавления от болевого раздражителя.
При обработке полученных результатов использовали показатель - изменение ЛП реакции одёргивания хвоста, свидетельствующие об изменении болевой чувствительности животных. Это показатель оценивали по формуле: ЛП=ЛПi - ЛП0 (ЛПi - латентный период реакции одёргивания хвоста в каждый момент измерения. ЛП0 - среднее фоновое значение латентного периода одёргивания хвоста до инъекции).
Оценку достоверности различий осуществляли по критерию Ван-дер-Вардена.
3. Фармакологическое воэдействие
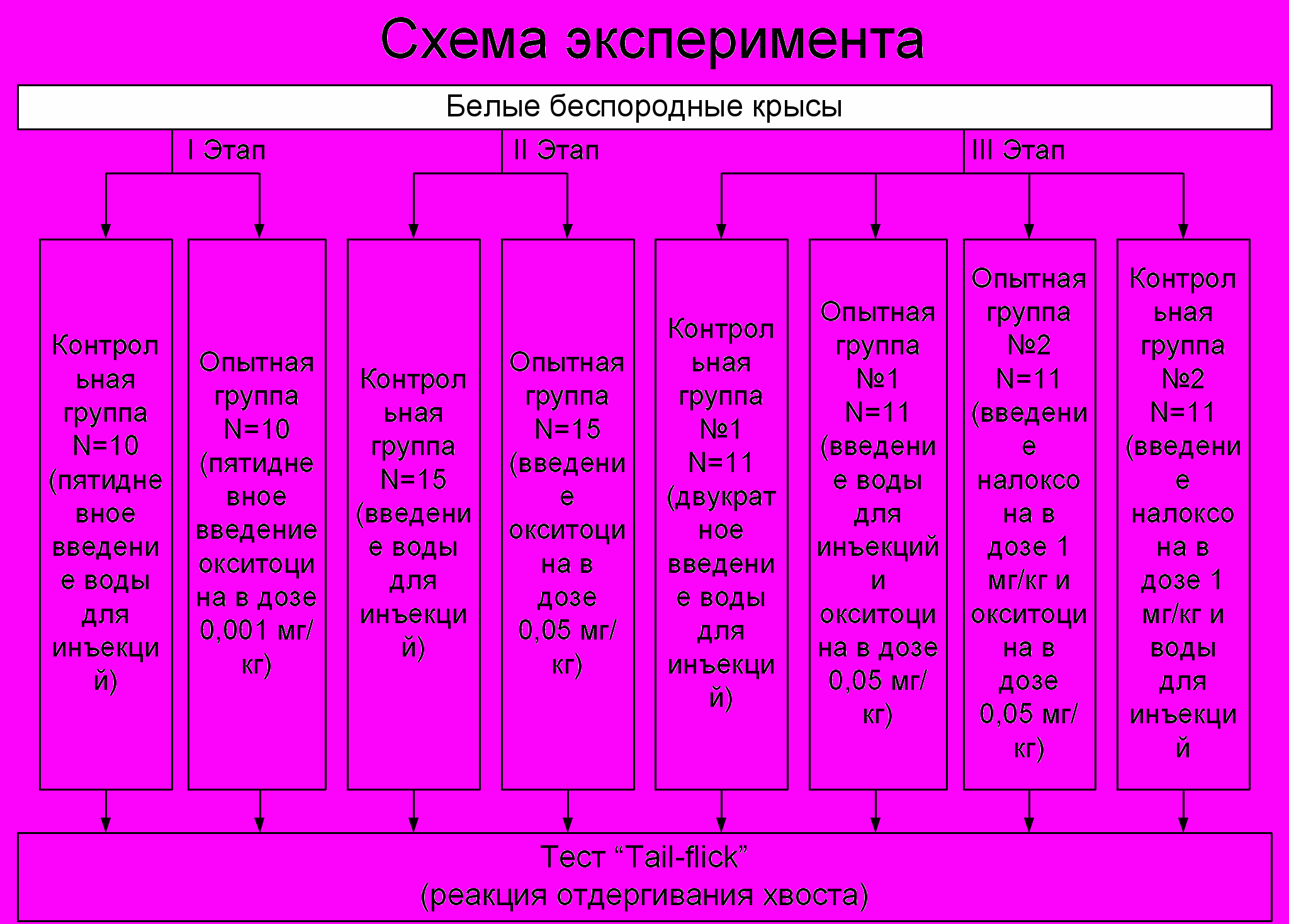
Исследования проводились в три этапа.
На первом этапе животных делили на две группы: контрольную и опытную. Опытной группе животных внутрибрюшинно вводили окситоцин в дозе 0,001мг/кг, а контрольной – воду для инъекций. Измерения проводили как в период 5-ти дневного введения, так и в течение 10-ти дней по окончанию фармакологического воздействия.
На втором этапе использовали однократное введение окситоцина в дозах 0,05 мг/кг. Животных также делили на две группы: контрольную и опытную. Опытной группе животных внутрибрюшинно вводили окситоцин в дозе 0,05 мг/кг, а контрольной – воду для инъекций.
На третьем этапе использовалось 4 группы животных: первой группе вводились вода для инъекций и окситоцин, второй – налоксон и окситоцин, третей – налоксон и вода для инъекций, четвёртой – контрольной двукратно вводилась вода для инъекций. Налоксон и вода вводились за 15 минут до инъекции пептида. Окситоцин вводили в дозе 0,05 мг/кг, налоксон в дозе 1 мг/кг (см. схему экспиремента).
Препараты вводили после определения исходного времени ЛП реакции одёргивания хвоста.
4. Характеристика используемых фармокологических препаратов
Окситоцин. Производитель "Гедеон Рихтер" Германия. Ампулы с прозрачной безцветной житкостью с концентрацией раствора 5 МЕ/мл. Растворителем для сухого вещества является вода для инъекций.
Применяют для вызывания и стимулирования родовой деятельности. Препарат наиболее эффективен при преждевременном отхождении околоплодных вод. Его назначают также при слабости родовой деятельности, связанной с атонией матки, и гипотонических маточных кровотечениях. Может применяться для искусственного вызывания родов (при осложнениях беременности).
Форма выпуска: в ампулах по 1 мл, содержащих по 5 МЕ окситоцина.
Налоксон Производитель Варшавский фармацевтический завод "Польфа" Польша. Ампулы с прозрачной безцветной житкостью с концентрацией раствора 0,4 мг/мл. Растворителем для сухого вещества является физиологический раствор.
Применяют налоксон главным образом при острой интоксикации наркотическими аналгетиками. Он эффективен также при алкогольной коме и различных видах шока, что связано, по-видимому, с активацией при шоке и некоторых формах стресса эндогенной опиодной системы, а также со способностью налоксона уменьшать гипотензию.
Форма выпуска: в ампулах по 1 мл, содержащих 0,4 мг налоксона гидро-хлорида.