Оптимизация диагностической и лечебной тактики у больных с ангиодисплазиями 14. 00. 44 сердечно-сосудистая хирургия 14. 00. 19 лучевая диагностика, лучевая терапия
| Вид материала | Автореферат |
- Комплексная лучевая диагностика в оценке репаративного процесса при лечении больных, 429.1kb.
- Лучевая терапия различными видами ионизирующего излучения в комплексном лечении больных, 785.18kb.
- Адъювантная лучевая терапия рака желудка. 14. 00. 14 онкология 14. 00. 19 лучевая диагностика,, 304.24kb.
- Ультразвуковая диагностика и малоинвазивные методы лечения осложнений после оперативных, 622.01kb.
- Селиверстов Павел Владимирович лучевая диагностика диспластически-дистрофического синдрома, 488.65kb.
- Селиверстов Павел Владимирович лучевая диагностика диспластически-дистрофического синдрома, 488.95kb.
- Структурно-денситометрический анализ ткани легких у больных хобл 14. 00. 43 пульмонология, 332.85kb.
- Рефлексотерапия в реабилитации больных поздними лучевыми повреждениями и паллиативной, 426.37kb.
- Радионуклидная диагностика воспалительных заболеваний опорно-двигательного аппарата, 543.39kb.
- Нейтронная и нейтронно-фотонная терапия злокачественных новообразований слюнных и щитовидной, 340.88kb.
ХИРУРГИЧЕСКОЕ И КОМБИНИРОВАННОЕ ЛЕЧЕНИЕ ПАЦИЕНТОВ С АРТЕРИОВЕНОЗНЫМИ ФОРМАМИ АНГИОДИСПЛАЗИЙ.
На сегодняшний день основой лечения пациентов с АВД является концепция органического сочетания возможностей стандартного хирургического вмешательства и рентгеноэндоваскулярных эмболизационных методов лечения. Именно эта позиция позволяет достичь максимальной радикальности при минимальной инвазивности.
Из 88 пациентов с АВД оперировано 86. В большинстве случаев у пациентов с АВД была избрана тактика лечения с использованием эндоваскулярных вмешательств (табл. 9).
Таблица 9.
Характер оперативных вмешательств у пациентов с АВД (n=86).
| Характер проведенных вмешательств | Количество пациентов |
| Рентгеноэндоваскулярная окклюзия Интраоперационная эмболизация | 26 2 |
| РЭО + удаление ангиоматозных тканей - радикальное - паллиативное | 3 12 |
| Удаление ангиоматозных тканей - радиальное - паллиативное | 5 15 |
| Удаление ангиоматозных тканей с последующими пластическими этапами (аутодермопластика, перемещенный кожный лоскут) | 5 |
| Разобщение артериовенозных свищей То же + резекция артериовенозных аневризм | 9 4 |
| Разобщение артериовенозных свищей + флебэктомия | 2 |
| Малая ампутация (экзартикуляция) | 2 |
| Ампутация | 1 |
| ИТОГО | 86 |
Только у 8 больных лечение носило радикальный характер, в остальных случаях оно было расценено как паллиативное, что было обусловлено инфильтративным характером поражения мягких тканей, удаление которых даже при ограниченных поражениях привело бы к нарушению функции конечности. Многоэтапность при лечении данной категории пациентов была обусловлена его палитивностью и дальнейшим прогрессированием заболевания.
Рентгеноэндоваскулярная окклюзия (РЭО) в большинстве случаев является паллиативным методом. Радикального результата можно достичь только в случаях единичных прямых артериовенозных свищей.
Варианты данного метода лечения предусматривали проведение: этапных эмболизаций у пациентов с диффузными и распространенными поражениями (n= 26); использование интраоперационной эмболизации (n=2); возможность проведения РЭО как этапа предоперационной подготовки. При этом варианте временной интервал между эмболизацией и последующим хирургическим вмешательством составлял 7-10 дней (n=15). Общее число проведенных лечебных эмболизаций составило 86. Их число колебалось от 1 до 6 процедур на одного пациента, составив в среднем 2,1 сеанса на пациента (табл. 10).
Таблица 10.
Локализация выполнявшихся РЭО.
| | Число больных | Кол-во этапных РЭО (последующие иссечения) |
| Артерии стопы | 3 | 8 (1) |
| Артерии голени | 10 | 18 (1) |
| Бедренно-подколенный сегмент | 8 | 24 (2) |
| Артерии таза | 3 | 3 (-) |
| Артерии предплечья | 5 | 5 (3) |
| Подключично-плечевой сегмент | 6 | 18 (3) |
| Бассейн НСА | 6 | 10 (4) |
| ИТОГО | 41 | 86 (15) |
Помимо уже длительное время использующихся для эмболизации калиброванных эмболов из гидрогеля, в 12 случаях для достижения постоянной окклюзии были применены цилиндрические эмболы из нелизирующегося полимерного материала поливинилалкоголя (PVA). Эмболы PVA (300-500 мк) вводились нами в виде взвеси в разбавленном контрастном веществе через просвет катетера в следующем соотношении: 1 часть контраста (14-15 мл) + 0,4 части изотонического раствора (5-6 мл) = 20 мл смеси на 1 флакон эмболов PVA. При этом, первоначально, для закрытия наиболее дистально расположенных отделов в зоне ангиодисплазии вводились сферические эмболы, заканчивалась эмболизация введением цилиндрических эмболов 0,5-0,7 мм, которые с их расположением в более проксимальных отделах сосудистого русла
С учетом высокой эффективности метода лечения при закрытии тех или иных афферентных артерий, нельзя забывать о возможности такого осложнения, как некроз тканей. В ряде случаев его возникновение сопряжено с недостаточным изучением архитектоники сосудистого русла, использовании неподходящего калибра эмболов. Такое осложнение отмечено в 3 (3,5 %) случаях. Особенности развития постэмболизационных некрозов таковы, что их появление может быть отмечено в сроки 2-3 недель после проведения РЭО на фоне постепенного ухудшения микроциркуляции в зоне вмешательства. Основные опасные зоны для этого осложнения - дистальные отделы кисти (n=1) и стопы (n=1). В одном случае возникновение некроза было связано с использованием 3 % этоксисклерола в процессе проведения комбинированной эмболизации на голени и недоучетом его распространения в кожные артериальные ветви.
В 2 (2,3 %) случаях данная лечебная процедура осложнилась развитием картины острого нарушения мозгового кровообращения, что было связано с миграцией эмболов из бассейна НСА с бассейн ВСА с возникновением очаговой неврологической симптоматики (т.н. “неконтролируемая эмболизация”). Оба осложнения потребовали проведения соответствующего лечения. При дальнейшем наблюдении за пациентами неврологический дефицит регрессировал.
Наилучшими возможностями наблюдения за результатами выполненной РЭО обладает дуплексное сканирование с оценкой показателей ОСК. Несмотря на хороший достигнутый результат по данным ангиографической картины в день исследования и тенденцию уменьшения степени артериовенозного сброса у большинства пациентов (за исключением распространенных форм с заинтересованностью большого количества афферентных сосудов), статистической достоверности этого снижения не отмечено (табл. 11).
В сроки 6-8 мес показатели ОСК при отсутствии каких-либо вмешательств (а это удаление ангиоматозных тканей) в проекции зоны патологического сброса приближаются к исходным значениям.
Таблица 11.
Показатели объемной скорости кровотока у пациентов с артериовенозными ангиодисплазиями конечностей до и после проведения сеансов РЭО в сроки 7-10 дней (n=11).
-
Исходная ОСК (мл/мин)
ОСК после РЭО (мл/мин)
A.femoralis
2517 + 1900
2350 + 1850
A.poplitea
786 + 540
662 +380
A.tibialis post.
178 + 120
158 + 110
A.tibialis ant.
167 + 150
117 + 60
Наиболее распространенным вмешательством явилось удаление ангиоматозных тканей. Радикальное вмешательство выполнено в 8 случаях при поверхностно расположенных поражениях. При этом возможно проведение подобных вмешательств как с предварительной РЭО (n=3), так и без нее (n=5).
Наилучшие условия для обширного удаления пораженных ангиоматозом тканей, включая мышцы, создаются при локализации поражения в проксимальных сегментах конечностей (бедро, ягодичная область, плечо, область плечевого сустава). При таких “проксимальных” локализациях меньше риск ухудшить функцию конечности и имеются возможности пластического закрытия раневой поверхности местными тканями или расщепленным кожным лоскутом.
Подобные вмешательства при распространенных формах инфильтративных поражений носили паллиативный характер, но даже такие вмешательства позволяли облегчить выраженность клинической симптоматики или улучшить центральную гемодинамику.
Разобщение артериовенозных свищей наиболее целесообразно выполнять при локальных формах поражения, особенно при наличии единичных прямых свищей, закрытие которых в силу локализации процесса, размера свищей, наличия соответствующих изменений магистральных вен в виде “артериализация” и формирования артериовенозных аневризм с использованием эндоваскулярных методик является проблематичным.
При наличии микрофистулезного поражения в 2 случаях проведено разобщение артериовенозных свищей путем выполнения скелетизации артерий (a.radialis и а.tibialis post. соответственно). Одномоментно в таком случае выполнялось лигирование перфорантных вен и удаление варикозно-расширенных поверхностных вен в зоне поражения. При макрофистулезных поражениях операции скелетизации мы не применяли ввиду отсутствия какого-либо гемодинамического эффекта.
При локализации артериовенозного сброса в самых дистальных отделах конечности (кисть, стопа) к радикальным операциям можно отнести и экономные ампутации. При этом, несмотря на органно-уносящий характер вмешательства, создаются наиболее благоприятные условия во время операции для удаления зоны ангиоматозного сброса.
ЛЕЧЕНИЕ ПАЦИЕНТОВ С ВЕНОЗНЫМИ ФОРМАМИ АНГИОДИСПЛАЗИЙ
Чрезвычайная вариабельность клинической симптоматики при этих формах поражения заставляет индивидуализировать в каждом конкретном случае лечебную тактику (табл. 12)
Таблица 12.
Схема лечебных мероприятий при венозных ангиодисплазиях (схематично).
| Форма венозной ангиодисплазии | Лечебные пособия |
| Трункулярные = стволовые (T) | |
| Дилатационные | Резекция с протезированием, Флебэктомия, Склеротерапия, Компрессия, Венотоники |
| Обструктивные | |
| Экстратрункулярные = нестволовые (ET) | |
| Диффузные | Радикальное удаление (?) Частичное удаление Склеротерапия, ЛК Компрессия, Венотоники |
| Ограниченные | Удаление ангиоматоза Склеротерапия, ЛК Компрессия, Венотоники (?) |
Из 110 пациентов оперировано 106 пациентов. В 3 случаях проведена изолированная склеротерапия. (табл. 13).
Венозные ангиодисплазии - стволовые - дилатационные (VM-T-D). Возможность проведения оперативных вмешательств при этих формах ангиодисплазий определяется протяженностью структурных врожденных изменений. При локальных поражениях (например, аневризма магистральной вены) можно рассматривать вопрос о резекции с последующим протезированием резецированного сегмента.
Таблица 13.
Характер проведенных оперативных вмешательств при венозных ангиодисплазиях (по числу пациентов).
| Вмешательства | Голова и шея | Верхние кон-ти | Нижние кон-ти | Туловище, ягодичн. область | Таз, НПО, сочетанные пораж. |
| Удаление ангиоматозных тканей | 12 | 22 | 39 | 4 | 10 |
| Флебэктомия (+ ЭДПВ) | - | - | 6 (1) | - | - |
| Протезирование вен | - | - | 1 | - | - |
| Лазерная коагуляция | 6 | - | 5 | 1 | - |
| Изолированная склеротерапия | 2 | 1 | - | - | |
| ИТОГО | 20 | 23 | 51 | 5 | 10 |
Венозные ангиодисплазии (мальформации) – стволовые - обструктивные (VM-T-O). Основным патогенетическим фактором при этом является клиническая картина хронической венозной недостаточности (ХВН) за счет нарушения оттока крови по глубоким венам.
Основой лечебной стратегии является консервативное лечение, базирующееся на компрессионной терапии и современных поливалентных венотониках. Оперативные вмешательства на глубоких венах, учитывая чаще встречающееся пролонгированное поражение, при таких поражениях не обеспечивают адекватной коррекции венозного оттока.
В случае появления и прогрессирования картины ХВН за счет перфорантного сброса для его устранения может быть применена над- или подфасциальная перевязка перфорантных вен. Эндоскопическая диссекция перфорантных вен голени выполнена в 2 случаях при аплазии магистральных вен (нижней полой вены – 1, бедренной вены – 1).
Экстратрункулярные = нестволовые (ET) ангиодисплазии (диффузные или ограниченные). Данные варианты венозных дисплазий по Гамбургской классификации являются наиболее распространенными. Различаясь только распространенностью процесса (диффузные или ограниченные), они имеют общие принципы лечения.
При венозных ангиодисплазиях мягких тканей с поражением кожных покровов приходится иссекать патологически измененные ткани вместе с пораженными участками кожи. Образовавшиеся дефекты следует закрывать с помощью местных тканей или свободной аутодермопластики.
Радикальное иссечение ангиоматозных тканей возможно лишь в случае ограниченной формы заболевания, при диффузном поражении возможно применение тактики многоэтапных оперативных вмешательств вплоть до полной ликвидации патологического процесса. При наличии кожных поражений (невус) в случае обширного поражения могут потребоваться этапные оперативные вмешательства с иссечением пораженных мягких тканей и последующим закрытием раневой поверхности с использованием различных вариантов пластики (свободная кожная пластика, дермотензия, кожно-фасциальные лоскуты на микро-сосудистых анастомозах).
Возможности пластической хирургии в комплексном лечении ангиодисплазий лица и шеи
При данной локализации различия между венозными и артериовенозными формами несколько стираются, учитывая особенности кровоснабжения данного региона и наибольшее влияние на жизненно-важные органы со стороны ангиоматоза вследствие давления извне.
В ряде случаев при локальных поражениях (как венозного, так и артериовенозного типа) удается выполнить радикальное удаление пораженных тканей с последующим закрытием раневой поверхности местными тканями после предварительно выполненной мобилизации.
Гораздо чаще в нашей клинической практике встречались ситуации, когда такой вариант пластики выполнить было невозможно. При значительных поражениях лица, когда невозможно использовать острое растяжение близлежащей неповрежденной кожи, применяется пластика перемещенным кожно-жировым лоскутом шеи.
В случае невозможности использования мобилизованного лоскута в отдаленном периоде (7-10 дней) может быть произведена аутодермопластика свободным перфорированным кожным лоскутом. Как правило, эта методика используется при закрытии раневой поверхности после удаления ангиоматозных тканей околоушной области и волосистой части головы.
Подобные вмешательства у всех пациентов носили этапный характер, что связано со стремлением закрыть операционную рану уже после удаления пораженных тканей и создания лучших условий приживления кожного трансплантата и меньшей вероятности его отторжения из-за отслойки.
Абляционные вмешательства в лечении больных с венозными ангиодисплазиями
С целью достижения облитерации венозных каверн при венозных диспалзиях нами предложена методика чрескожной лазерной коагуляции (ЧЛК). С этой целью использован отечественный компактный высокоэнергетический диодный лазер ЛАМИ, генерирующий луч в диапазоне 1030 нм с выходной мощностью до 25 Вт. Данная длина волны нами выбрана сознательно, учитывая тот факт, что пик поглощения лазерного излучения в крови приходится на диапазон 930-1050 нм Основным хромофором, наиболее сильно поглощающим лазерное излучение данной длины волны, является кровь. Именно этим определяется большой объем тепловыделения и нагревания тканей при использовании лазерного излучения с этой длиной волны.
Методика ЧЛК применена у 20 пациентов, средний возраст составил 26,3 + 7,8 лет. В 2 случаях диагностирована артериовенозная микрофистулезная форма ангиодисплазии, у 18 – венозная, в т.ч. с наличием венозно-кавернозного ангиоматоза - у 11. 13 пациентов ранее перенесли различные вмешательства по месту жительства и в нашем учреждении:
- удаление ангиоматозных тканей (10), в т.ч. в сочетании с РЭО – 2;
- склеротерапия – 2.
В общей сложности у 21 пациентов выполнено 30 вмешательств с применением лазерной коагуляции.
При артериовенозной форме коагуляции подвергались несостоятельный ствол МПВ и диспластические вены голени (n=3). Эти вмешательства выполнялись после завершения эндоваскулярного лечения с применением жидких склерозантов.
У 6 пациентов с венозной формой ангиодисплазии лазерная коагуляция применена как этап комбинированного хирургического вмешательства для устранения эмбриональных вен в области латеральной поверхности бедра и голени (вариант ЭВЛК). Обязательным этапом вмешательства считали тщательное изучение при ультразвуковом исследовании ангиоархитектоники и предоперационную маркировку диспластических вен, планируемых для ЛК. Эмбриональные вены на протяжении в/3 бедра, подвздошной области и голени с максимальным диаметром до 15 мм подвергались коагуляции после иссечения ангиоматоза бедра, лигирования атипичных перфорантных вен. При этом выбирались максимальные параметры энергетического воздействия (мощность воздействия 23-25 Вт). Несмотря на достаточно высокие параметры мощности (при методике ЭВЛК при лечении варикозной болезни используются 15-18 Вт), осложнений при этом не отмечено. При оценке ближайших результатов полная облитерация отмечена при проведении ЛК диспластических вен лишь на голени, на бедре уже в эти сроки отмечалось восстановление просвета венозных сосудов диаметром свыше 10 мм (срок наблюдения 10-12 мес).
При венозно-кавернозном ангиоматозе ЧЛК выполнена у 12 пациентов (21 лечебная процедура). Необходимость проведения повторных вмешательства возникала у пациентов с диффузным поражением нижних конечностей и лица.
Разброс выделенной энергии в нашей работе при проведении ЧЛК составил 0,57 – 10,83 кДж (среднее 4,6 + 2,8 кДж). При этом, если выделенная энергия при проведении вмешательств на лице варьировала от 0,57 до 7,5 кДж, то максимальные показатели были зарегистрированы при вмешательствах при ангиоматозах бедра – от 3 до 10,83 кДж. При расчете плотности выделенной энергии (на единицу площади ангиоматозных тканей) показатели отличались незначительно. Средний итоговый показатель составил 130,6 + 92 Дж/см2, что представляет достаточно высокую величину с учетом данных по энергетике, которые представлены в публикациях, посвященных ЭВЛК в лечении варикозной болезни (табл. 14).
Ни одного серьезного осложнения при выполнении данной методики нами не отмечено. Обязательное использование “гидравлической подушки” позволило избежать каких-либо трофических нарушений кожи в зоне вмешательства. При проведении ЧЛК на лице у всех пациентов был отмечен выраженный отек мягких тканей в зоне проведения коагуляции. Отек держался на протяжении 1-1,5 мес и не требовал каких-либо дополнительных назначений. По нашему мнению, этот факт не должен рассматриваться как осложнение ЧЛК.
Таблица 14.
Чрескожная лазерная коагуляция (ЧЛК) у пациентов с венозно-кавернозным ангиоматозом.
| Локализация | Количество пациентов | Число лечебных процедур | Площадь тканей, подвергнутых ЧЛК (см2) | Выделенная энергия (кДж) | Плотность энергии (Дж/см2) |
| Лицо и шея | 6 | 10 | 27,5 + 17,6 | 2,99 + 2,3 | 113,8 + 70,9 |
| Грудная стенка | 1 | 1 | 20 | 5,41 | 270 |
| Ягодица, бедро | 3 | 9 | 71,5 + 32,3 | 6,4 + 2,3 | 123,1 + 116,6 |
| Голень, стопа | 2 | 2 | 26 | 4,3 | 139,6 |
| ИТОГО | 12 | 21 | 43,5 + 32,7 | 4,6 + 2,8 | 130,6 + 92 |
В отдаленные сроки (от 6 до15 мес) проведена оценка у всех 21 пациентов. При проведении вмешательств на диспластических венах (n=9) положительный результат (полная окклюзия венозного сегмента) достигнут в 3, частичная окклюзия – в 2, реканализация отмечена в 4 случаях.
Наилучшие результаты в этой ситуации достигнуты при сочетании ЧЛК со стандартным хирургическим вмешательством, которое позволяет наиболее полно устранить механизм патологических рефлюксов и удалить наиболее измененные венозные сегменты. Наш небольшой опыт показывает, что использование методики лазерной коагуляции как метода облитерации диспластических вен должно выполняться при их диаметре, не превышающим 12 мм. При больших размерах мы должны склоняться в пользу хирургического удаления.
Оценка отдаленных результатов ЧЛК при венозно-кавернозном ангиоматозе (n=12), показывает, что стойкая окклюзия в зоне вмешательства сохраняется на протяжении всего срока наблюдения у большинства пациентов. У 5 пациентов для увеличения объема облитерации и последующего закрытия каверн выполнены повторные вмешательства в зоне первичного вмешательства или расположенных рядом областях. При повторных вмешательствах общая мощность излучения, как правило, повышалась.
Все пациенты на протяжении периода наблюдения отмечали значительное уменьшение болевого синдрома, отечности, напряжения тканей. Показатель субъективной оценки болевого синдрома (визуальная аналоговая шкала - ВАШ), составлявший до начала лечения 5,3 + 1,2 балла уменьшился до 3,2 + 0,9 ( p<0,05).
У 2 пациентов с диффузным поражением прекратились кровотечения в зоне ангиоматоза. При ДС при этом сохранялась картина частичной окклюзии в зоне вмешательства.
Таким образом, разработка и внедрение в клиническую практику методики эндовазальной лазерной коагуляции диспластических вен и ЧЛК при венозно-кавернозном ангиоматозе дало возможность за счет расширения спектра малоинвазивных вмешательств достигнуть определенного прогресса в достижении основной цели у этой категории пациентов – улучшении качества жизни.
Склеротерапия была использована у 16 пациентов с венозными дисплазиями различной локализации. Суммарно произведено 27 лечебных процедур. У 87,5 % пациентов склеротерапия сочеталась с оперативным вмешательством, в остальных случаях она явилась окончательным методом лечения. Для приготовления пенообразной консистенции препарата применялся 2 % раствор фибро-вейна или 3 % раствор этоксисклерола. Количество пены (приготовление за счет смешения жидкого склерозанта с воздухом в пропорции 1:4), применяемой за один сеанс, составило 4,5 + 1,1 [разброс 3-9] мл. Компрессионная терапия осуществлялась во всех случаях адгезивными бинтами с низкой степенью растяжимости.
Непосредственный успех процедуры расценен нами как 92,6 %. Высокая эффективность микропенной техники определяется возможностью вытеснения крови из просвета вены и более длительным контактом флебосклерозирующего препарата с эндотелием сосуда. Возможность значительного уменьшения количества используемого препарата за счет создания новой физической формы (пеноообразная) позволило повысить не только лечебный эффект склеротерапии, но и ее безопасность.
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ АНГИОДИСПЛАЗИЙ
Говоря о критериях оценки результатов проведенного лечения, стоит напомнить, что в нашей работе большинство клинических наблюдений при АВД было с диффузным и распространенным поражением. Это априорно делало невозможным радикальное удаление всего очага поражения вне зависимости от локализации или распространенности процесса без нарушения или утраты функции органа (конечности). Поэтому достаточно большая часть вмешательств носила паллиативный характер. Дальнейшее прогрессирование заболевания и возврат симптоматики (“рецидив”) были неизбежными процессами. Это требовало повторной госпитализации и проведения этапного лечения. В ряде случаев был необходим интервал между отдельными вмешательствами с целью адаптации нормальных тканей к возникшей ишемии и заживления послеоперационных ран. Поэтому у пациентов с АВД наиболее рациональным является оценка непосредственных и отдаленных результатов после каждой лечебной процедуры на данном этапе лечения. Такой подход дает и представление об эффективности различных способов лечения. Окончательная оценка отдаленных результатов выполнялась после завершения всех лечебных мероприятий.
Оценка отдаленных результатов нами проводилась на основании следующих критериев:
Хороший результат: полное устранение ранее имевшейся клинической симптоматики и функциональных расстройств или значительное уменьшение выраженности клинических симптомов при отсутствии или минимальной выраженности функциональных нарушении. Положительная динамика при ДС магистральных сосудов.
2. Удовлетворительный результат: симптомы и имевшиеся функциональные нарушения после операции с незначительной положительной динамикой. По данным ДС имелось снижение показателей ОСК в зоне выполнявшегося вмешательства.
3. Неудовлетворительный результат: прогрессирование клинических симптомов и функциональных нарушений, ухудшение показателей местной и центральной гемодинамики, ухудшение локального статуса в области поражения (некрозы). Отсутствие положительной динамики гемодинамических показателей в зоне поражения по данным ДС.
Отдаленные результаты лечения пациентов с АВД в сроки 12-60 мес оценены у 76 пациентов (табл. 15).
Таблица 15.
Отдаленные результаты лечения пациентов с артериовенозными ангиодисплазиями.
| Локализация | Число больных | Результаты лечения | ||
| Хорошие | Удовлетворительн. | Неудовлетворительн. | ||
| Голова и шея | 22 | 7 (31,8 %) | 11 (50 %) | 4 (18,2%) |
| Верхние конечности | 16 | 9 (56,2 %) | 4 (25 %) | 3 (18,8 %) |
| Нижние конечности | 34 | 14 (41,2 %) | 13 (38,2 %) | 7 (20,6 %) |
| Туловище | 1 | - | 1 | - |
| Таз и НПО | 1 | - | 1 | - |
| Смешанная локализация | 2 | - | 1 | 1 |
| ИТОГО | 76 | 30 (39,5 %) | 31 (40,7 %) | 15 (19,8%) |
Хорошие и удовлетворительные результаты при АВД после комбинированного достигнуты у 80,2 % пациентов.
В 19,8 % случаев отдаленные результаты признаны неудовлетворительными. Во всех этих случаях отмечалось диффузное и распространенное поражение, что не давало возможности устранить артериовенозный сброс при хирургическом вмешательстве. Эндоваскулярные вмешательства обеспечивали лишь временный гемодинамический эффект в сроки до 3-5 мес, далее отмечалось нарастание показателей ОСК, что свидетельствовало о нарастании объема патологического шунтирования. Поэтому такая категория пациентов нуждается в постоянном динамическом наблюдении и продолжении эндоваскулярного лечения – другой альтернативы без радикального хирургического устранения удаления ангиоматозных тканей не существует.
К удовлетворительным результатам нами отнесены и результаты “малых” ампутаций, т.к. их выполнение позволило полностью устранить артериовенозное шунтирование с ликвидацией трофических расстройств.
Ампутация бедра отнесена к неудовлетворительным результатам, хотя выполненное в дальнейшем протезирование и обеспечило хорошую социальную адаптацию пациента.
Наилучшие результаты при АВД с наличием трофических расстройств достигаются при комбинированном лечении, включающим в себя эндоваскулярное лечение с последующим удалением единым блоком пораженных тканей и проведением одного из вариантов пластики.
Одним из важных объективных критериев оценки проведенного лечения пациентов с АВД являются данные ультразвукового исследования, в первую очередь, ОСК. И если в случае диффузного поражения положительная динамика ОСК отсутствовала, то при ограниченном поражении было достигнуто значимое снижение данных показателей, регистрируемое на всех уровнях (рис. 8).
Отдаленные результаты лечения пациентов с венозными дисплазиями и лимфангиоматозом в сроки 12-28 мес оценены у 98 и 5 пациентов соответственно. Для оценки отдаленных результатов мы также использовали трехбальную систему (табл. 16). Помимо клинической картины из объективных методов оценки были использованы данные ДС магистральных вен и мягких тканей.
м
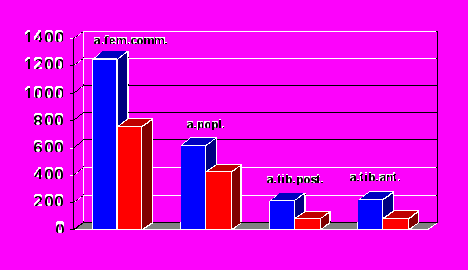 л/мин
л/мин
Исходные значения

Отдаленные результаты
Рис. 8. Динамика показателей ОСК по данным ДС в отдаленном периоде у пациентов с АВД нижних конечностей с ограниченным поражением (n=8, сроки наблюдения 12-20 мес).
Наименьшее количество хороших отдаленных результатов отмечены при проведении оперативных вмешательств на верхних и нижних конечностях (30 % и 40,4 % соответственно). На наш взгляд это связано с особенностями локализации поражения венозно-кавернозным ангиоматозом при этой локализации. Более частая встречаемость глубокого поражения с заинтересованностью мышц и межмышечных пространств, нервов, а также костных структур, делает невозможным радиальное удаление ангиоматоза без нарушения функции конечности. В случае ограниченных поражений любой локализации отдаленные результаты были расценены как хорошие.
Таблица 16.
Отдаленные результаты лечения пациентов с венозными дисплазиями и лимфангиоматозом.
| Локализация | Число больных | Результаты лечения | ||
| Хорошие | Удовлетворителн. | Неудовлетворительн. | ||
| Венозные дисплазии | ||||
| Голова и шея | 19 | 10 (52,6 %) | 8 (42,1 %) | 1 (5,3 %) |
| Верхние конечности | 20 | 6 (30 %) | 14 (70 %) | - |
| Нижние конечности | 47 | 19 (40,4 %) | 27 (57,4 %) | 1 (2,1 %) |
| Туловище | 4 | 4 (100 %) | - | - |
| Таз и НПО | 2 | - | 1 (50 %) | 1 (50 %) |
| Смешанная локализация | 6 | 2 (33,3 %) | 2 (33,3 %) | 2 (33,3 %) |
| ИТОГО | 98 | 43 (43,9 %) | 50 (51 %) | 5 (5,1 %) |
| Лимфангиоматоз | ||||
| Нижние конечности | 5 | 3 (60 %) | 2 (40 %) | - |
При выполнении ФПГ (n=12) в отдаленные сроки после операции (8-12 мес) отмечена положительная динамика показателей RT и Vo, хотя в отличие от пациентов с варикозной болезнью полной нормализации данных показателей даже после многоэтапного лечения мы не отметили. Время венозного возврата RT увеличилось c 7,4 + 1,3 сек до 15,8 + 1,4 сек (p=0,001), а выброс венозной помпы Vo – с 1,9 + 0,5 до 2,7 + 0,7 % (p=0,36) (рис. 9).
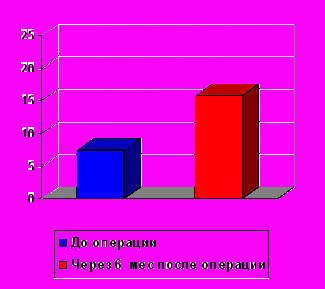






Норма


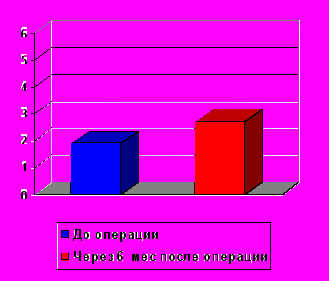
Рис. 9. Динамика RT (А) и Vo (Б) при оценке эффективности оперативных вмешательств при венозных дисплазиях (n = 12).
А) – по оси ординат – время венозного возврата RT ( в сек)
Б) – по оси ординат - венозный выброс Vo (в %)
Этот метод дополняет данные лучевых методов исследования и может быть использован для интегральной количественной оценки степени выраженности ХВН у пациентов с венозными ангиодисплазиями, позволяя оценить непосредственные и отдаленные результаты проведенных оперативных вмешательств.
Отдаленные результаты хирургического лечения лимфангиоматоза напрямую были связаны с глубиной и площадью поражения и, соответственно, возможностью радикального удаления при первичном вмешательстве. Но даже в случае наличия резидуальных тканей в клинической картине заболевания отмечалась положительная динамика в течение болевого синдрома, снижение выраженности лимфангоитов. Необходимым условием стабильности полученных результатов является постоянное динамическое наблюдение пациентов. Это позволяет объективно оценить клиническую ситуацию и поставить показания к проведению этапных операций.
ВЫВОДЫ
1. Комплексное ультразвуковое исследование на сегодняшний день является основным методом неинвазивной диагностики при всех формах ангиодисплазий, позволяющим предоставить качественную и количественную информацию о макродинамических характеристиках сосудистых пороков. При венозных формах это исследование может быть единственным для определения тактики лечения и объема операции или же дополняться другими неинвазивными методами исследования.
При артериовенозных формах дуплексное сканирование наряду с ангиографией играет важнейшую роль в диагностическом алгоритме, предоставляя возможность неинвазивного контроля результатов лечения.
2. Магнитно-резонансная томография является интегральным базовым методом в дополнении к ультразвуковому исследованию для точной топической диагностики ангиодисплазий, оценки объема поражения (интра- и экстракраниального компонента) и уточнения взаимоотношения питающих и коллатеральных сосудов. Режим Т1-взвешенного МР-изображения дает представление об объеме патологического процесса, а режим Т2-взвешенного МР-изображения дает информацию более качественную информацию о характере поражения. Степень изменения различных тканей наглядно демонстрируют МР-изображения в режимe STIR (с подавлением сигнала от жировой ткани).
3. Показатели диагностической чувствительности, специфичности и точности магнитно-резонансной томографии в диагностике локализации и величины поражения при ангиодисплазиях составляют 99 %, 98%, 98 %, поражения костных структур – 99 %, 96 % 97 %, оценки степени структурных изменений в тканях 99 %, 96 % и 97 % соответственно.
4. Методика лазерной доплеровской флоуметрии (ЛДФ) может быть использована для количественной оценки степени микроциркуляторных нарушений у больных с ангиодисплазиями и эффективности применения у этой группы пациентов консервативного лечения. Основными критериями оценки при этом явились показатели тонуса артериол, базального кровотока, амплитуды высоких колебаний AHF/CKO. При адекватной компрессии с использованием изделий III класса статистически значимо улучшались вышеописанные показатели микроциркуляции у пациентов как при венозных, так и при артериовенозных формах.
5. Наиболее оптимальным методом при артериовенозных ангиодисплазиях является комбинированное лечение, сочетающее возможности рентгеноэндоваскулярной окклюзии и стандартных вмешательств по удалению ангиоматозных тканей, а также многоэтапные РЭО для максимального устранения питающих артерий.
6. При венозных ангиодисплазиях наиболее радикальным являтся тактика этапных хирургических вмешательств (иссечение ангиоматозных тканей) в сочетании со склеротерапией и методиками термической абляции при наличии диффузного поражения. У пациентов с асимптомным и малосимптомным течением заболевания оправдано консервативное лечение и постоянное диспансерное наблюдение на базе специализированного учреждения. Несмотря на наличие общих тактических установок, наиболее предпочтительным в каждом конкретном случае является дифференцированный подход.
7. Предложенная малоинвазивная методика чрескожной лазерной коагуляции (ЧЛК) является эффективной для устранения патологической венозной емкости при венозных дисплазиях и носит более управляемый локализованный характер по сравнению с применявшейся ранее склеротерапией жидкими склерозантами. Сохраняется объективная необходимость тщательного изучения отдаленных результатов с оценкой полноты и длительности тромботической окклюзии, что должно ускорить внедрение данной методики в практическую медицину.
8. При лечении пациентов с ангиодисплазиями лица и шеи необходимо шире использовать принципы пластического закрытия раневых поверхностей с учетом адекватно выполненного гемостаза. Наилучшими возможностями в этом направлении имеет применение шейного кожно-жирового лоскута.
9. При артериовенозных формах ангиодисплазий с использованием комбинированных методов лечения при условии этапного лечения хороший и удовлетворительный результат достигается в 80,2 % случаев. Хорошие и удовлетворительные результаты хирургического лечения венозных дисплазий достигнуты в 43,9 % и 51 % случаев соответственно и напрямую связаны с глубиной и объемом поражения.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
На начальном этапе выявления ангиодисплазий вне зависимости от формы и локализации процесса целесообразно проведение комплексного ультразвукового исследования с использованием современных возможностей методики дуплексного сканирования для оценки гемодинамических характеристик.
- Рентгеноконтрастная ангиография должна выполняться при артериовенозных ангиодисплазиях только в тех случаях, когда последующим этапом планируется проведение лечебных пособий - хирургических или эндоваскулярных. Выполнение флебографии при венозных формах дисплазий должно быть сведено до минимума и ограничено диагностикой характера поражения глубоких вен.
- Компьютерную томографию и магнитно-резонансную томографию целесообразно выполнять как вспомогательные методы диагностики при необходимости дифференциации различных анатомических структур, оценки характера, структуры и протяженности. Учитывая более высокие показатели чувствительности, специфичности и точности магнитно-резонансной томографии при диагностике поражения костей, суставов при ангиодисплазиях, предпочтение в этих случаях необходимо отдавать данному методу исследования.
- С целью выявления афферентных артерий и дренирующих вен целесообразно проведение импульсных последовательностей спин-эхо без применения контрастных средств. Для уточнения ангиоархитектоники вышеуказанных сосудов, а также при наличии аневризматических расширений для улучшения качества изображения необходимо дополнять проведение стандартной методики исследования магнитно-резонасной ангиографией с применением контрастных препаратов.
- Для планирования объема оперативных вмешательств и отчетливой визуализации зоны поражения целесообразно проведение магнитно-резонансной ангиографии с проведением трехмерных реконструкций.
- Методики лазерной доплеровской флоуметрии и цифровой плетизмографии целесообразно использовать для характеристики микроциркуляторных нарушений и степени венозной недостаточности при локализации патологического процесса на нижних конечностях.
- С целью устранения венозных каверн и диспластических венозных сосудов в дистальных отделах конечностей целесообразно применение методики пенной (foam-form) склеротерапии.
- Для устранения патологической венозной емкости в глубине мышечного массива, особенно при отсутствии возможности адекватной компрессии, необходимо использовать методику лазерной коагуляции ангиоматозных тканей. Для достижения адекватной коагуляции и безопасности процедуры обязательными условиями являются создание “гидравлической подушки” и расчет выделяемой при этом энергии, которая должна достигать величины не менее 130 Дж/см2.
- Для контроля эффективности хирургического лечения пациентов с различными формами ангиодисплазий с наличием ангиоматоза целесообразно использовать в ближайшем и отдаленном послеоперационном периоде ультразвуковые методы и магнитно-резонансную томографию, при отсутствии ангиоматоза достаточным является применение ультразвуковых методов.
