Н. Н. Алипова, канд биол наук О. В. Левашова и канд биол наук М. С. Морозовой под редакцией акад. П. Г. Костюка москва «мир» 1996 ббк 28. 903 Ф50
| Вид материала | Документы |
- Приглашение и программа разнообразие почв и биоты северной и центральной азии, 521.14kb.
- М. А. Ляшко доц., канд физ мат наук; Т. Н. Смотрова доц., канд, 2299.13kb.
- Современные направления развития физической культуры, спорта и туризма, 4493.6kb.
- Отчет о проведении Международной научной конференции-семинара «Современные методы психологии», 97.76kb.
- Образовательная программа дошкольного образования Москва «Просвещение», 5670.3kb.
- Пособие для врачей и среднего медицинского персонала Минск, 5480.63kb.
- Ббк 63. 3(0) Н72, 4378.93kb.
- Тезисы докладов, 4290.75kb.
- Строительные нормы и правила нагрузки и воздействия сниП 01. 07-85* министерство строительства, 1162.86kb.
- Ббк 63. 3(0) Н72, 5546.58kb.
Часть V. КРОВЬ И СИСТЕМА КРОВООБРАЩЕНИЯ
Глава 18 ФУНКЦИИ КРОВИ.
X. Вайс, В. Елькманн
18.1. Основные положения
Кровь представляет собой непрозрачную красную жидкость, состоящую из бледно-желтой плазмы (плазма, лишенная фибрина, называется сывороткой) и взвешенных в ней клеток - красных кровяных телец (эритроцитов), белых кровяных телец (лейкоцитов) и кровяных пластинок (тромбоцитов). Исследование крови имеет большое значение в клинической диагностике, так как, с одной стороны, получить кровь несложно, а с другой стороны, при многих заболеваниях ее состав и свойства компонентов изменяются характерным образом.
Функции крови
Транспортная функция. Кровь-это прежде всего среда, осуществляющая транспорт различных веществ в пределах организма. Она переносит дыхательные газы-кислород и углекислый газ, как в физически растворенном, так и в химически связанном виде. Кислород переносится от легких к потребляющим его тканям, а углекислый газ-от тканей к легким. Кровь доставляет также питательные вещества от органов, где они всасываются или хранятся, к месту их потребления; образующиеся здесь метаболиты транспортируются к выделительным органам или к тем структурам, где может происходить их дальнейшее использование. Кровь осуществляет транспорт гормонов, витаминов и ферментов, образующихся в организме; эти вещества, поступая в кровь из органов, где они вырабатываются или хранятся, распределяются в сосудистом русле и доставляются к органам-мишеням. Благодаря высокой теплоемкости своей главной составной части-воды кровь обеспечивает распределение тепла, образующегося в процессе метаболизма, и его выделение во внешнюю среду через легкие, дыхательные пути и поверхность кожи.
Гомеостаз. Состав и физические свойства циркулирующей крови постоянно контролируются определенными органами и по мере надобности корректируются с целью обеспечения постоянства внутренней среды. Относительное постоянство концентраций растворенных веществ, температуры и рН-это важнейшее условие нормальной жизнедеятельности клеток организма.
Остановка кровотечения. Важная функция крови - ее участие в остановке кровотечения. Эта функция обусловлена способностью крови закрывать просвет мелких поврежденных сосудов и свертываться (разд. 18.7).
Обезвреживание чужеродных агентов. Организм обладает способностью обезвреживать чужеродные частицы и патогенные организмы, главным образом при участии фагоцитарных и антителообразующих клеток крови (с. 440).
Объем крови
На долю крови у взрослого человека приходится примерно 6-8% общей массы тела, а у детей в связи с более высоким содержанием в организме воды8-9%. У взрослого это соответствует 4-6 л крови (нормоволемия). Повышение общего объема крови называют гиперволемией, а снижение - гиповолемией. Способ измерения этой величины описан на с. 564, а распределение общего объема крови по различным отделам сосудистого русла - на с. 508
Гематокрит
Определение и нормальные пределы. Гематокритом называется часть объема крови, приходящаяся на долю эритроцитов. В норме у взрослого мужчины
ГЛАВА 18. ФУНКЦИЯ КРОВИ 415
гематокрит равен 0,44-0,46, а у женщины-0,41-0,43. В клинической практике гематокрит все еще иногда выражают в объемных процентах (мл клеток/дл крови). У здорового человека эта величина может претерпевать существенные и достаточно длительные изменения лишь при адаптации к большим высотам. У новорожденных гематокрит приблизительно на 20% выше, а у маленьких детей-примерно на 10% ниже, чем у женщин [6, 25].
Для определения гематокрита по методу Уинтроба кровь, предварительно лишенную способности свертываться, центрифугируют в течение 10 мин при 1000 g (g-ускорение свободного падения) в стандартной пробирке малого диаметра для определения гематокрита. Клетки крови, удельная масса которых выше, чем удельная масса плазмы, оседают на дно. Поскольку лейкоциты легче эритроцитов, они образуют тонкий беловатый слой между осевшими эритроцитами и плазмой. Значения гематокрита для крови, взятой из разных органов, а также для венозной, артериальной и капиллярной крови различаются из-за особых реологических свойств эритроцитов. Среднее значение гематокрита можно вычислить, умножив величину, полученную при определении гематокрита в крови локтевой вены по методу Уинтроба, на 0,9.
Гематокрит и вязкость крови. Если принять вязкость воды за 1, то средняя относительная вязкость крови у здорового взрослого человека составит 4,5 (3,5-5,4), а вязкость плазмы-2,2 (1,9-2,6). Увеличение гематокрита сопровождается более быстрым, чем при линейной зависимости, возрастанием вязкости крови (т.е. ее внутреннего трения) (см. рис. 20.3). Поскольку гидродинамическое сопротивление прямо пропорпионально вязкости, любое патологическое увеличение гематокрита приводит к повышению нагрузки на сердце, в результате чего кровообращение в некоторых органах может нарушиться.
18.2. Плазма крови
В 1 л плазмы человека содержится 900-910 г воды, 65-80 г белка и 20 г низкомолекулярных соединений. Удельная масса плазмы равна 1,025-1,029, а ее pH незначительно колеблется в пределах 7,37-7,43, составляя в среднем (в артериальной крови) около 7,4.
На рис. 18.1 схематически показаны три основных водных пространства организма - внутрисосудистое, интерстициальное (межклеточное) и внутриклеточное. Интерстициальная жидкость служит внешней средой для большинства клеток организма. Обмен веществами между плазмой крови и интерстициальной жидкостью происходит через обширную поверхность стенок капилляров, высокопроницаемых для воды и ионов. Обмен водой и небольшими молекулами между плазмой и интер-
 |
| Рис. 18.1. Схема жидкостных пространств организма Представлены округленные значения для человека массой 70 кг (по [8] с изменениями) |
стициальной жидкостью происходит очень быстро, поэтому состав последней, несмотря на существенные изменения в поглощении и выделении различных веществ клетками, колеблется незначительно. Так, в опытах с тяжелой водой D2O (меченной дейтерием) было показано, что более 70% всей жидкости плазмы обменивается с интерстициальным пространством за 1 мин.
Состав плазмы и интерстициалъной жидкости существенно различается лишь по концентрации белков, так как их крупные молекулы не могут свободно проходить через стенки капилляров.
Электролиты плазмы
Содержание электролитов. В табл. 18.1 и на рис. 18.2 приведены данные по ионному составу плазмы крови. К группе «органических кислот» относят молочную, лимонную и пировиноградную кислоты, а также аминокислоты.
Концентрации веществ удобнее выражать не в единицах отношения массы к объему (г/дл или мг/дл), а в молях на литр (молярность), эквивалентах на литр (нормальность, или эквивалентная концентрация) [экв/л = = моль/(валентность-л)]. В случае если частицы растворенного вещества занимают в растворе существенное пространство и необходимо учитывать уменьшение за счет этого объема раствора, его концентрацию часто выражают в молях на килограмм растворителя (моляльность) (см. табл. 18.1).
416 ЧАСТЬ V. КРОВЬ И СИСТЕМА КРОВООБРАЩЕНИЯ
| Таблица 18.1. Среднее содержание электролитов и неэлектролитов в плазме крови человека | |||
| | г/л | мэкв/л | ммоль/кг воды плазмы |
| Электролиты | | | |
| Катионы: | | | |
| натрий | 3,28 | 143 | 153 |
| калий | 0,18 | 5 | 5 |
| кальций | 0,10 | 5 | 3 |
| магний | 0,02 | 2 | 1 |
| Всего | | 155 | |
| Анионы: | | | |
| хлорид | 3,65 | 103 | 110 |
| бикарбонат | 0,61 | 27 | 28 |
| (Ьос(Ьат | 0,04 | 2 | 1 |
| сульфат | 0,02 | 1. | 1 |
| органические кислоты | | 6 | |
| белки | 65-80 | 16 | 1 |
| Всего | | 155 | |
| Неэлектролиты | | | |
| Глюкоза | 0,9-1,0 | | 5 |
| Мочевина | 0,40 | | 7 |
О
 смотическое давление. Концентрация растворенных в плазме веществ может быть выражена как осмотическое давление. Осмотическое давление плазмы крови в норме составляет 7,3 атм (5600 мм рт. ст., или 745 кПа), что соответствует температуре замерзания, равной — 0,54 °С. Растворы, осмотическое давление которых такое же, как у плазмы, называют изотоническими, растворы с большим осмотическим давлением -гипертоническими, а с меньшим -гипотоническими. Плазма изотонична по отношению к раствору неэлектролита, моляльность которого составляет всего 1/3. Около 96% осмотического давления крови обусловлено присутствием неорганических электролитов, в основном NaCl; давление, обусловленное данными веществами, называют кристаллоидно-осмотическим. Молекулярная масса NaCl низка, поэтому на единицу массы этого вещества приходится много молекул.
смотическое давление. Концентрация растворенных в плазме веществ может быть выражена как осмотическое давление. Осмотическое давление плазмы крови в норме составляет 7,3 атм (5600 мм рт. ст., или 745 кПа), что соответствует температуре замерзания, равной — 0,54 °С. Растворы, осмотическое давление которых такое же, как у плазмы, называют изотоническими, растворы с большим осмотическим давлением -гипертоническими, а с меньшим -гипотоническими. Плазма изотонична по отношению к раствору неэлектролита, моляльность которого составляет всего 1/3. Около 96% осмотического давления крови обусловлено присутствием неорганических электролитов, в основном NaCl; давление, обусловленное данными веществами, называют кристаллоидно-осмотическим. Молекулярная масса NaCl низка, поэтому на единицу массы этого вещества приходится много молекул.Регуляция осмотического давления плазмы имеет первостепенное значение для постоянства внутренней среды организма, или гомеостаза. Любое отклонение осмотического давления жидкостей внеклеточного пространства (плазмы крови и интерстициальной жидкости) от нормальных величин приводит к перераспределению воды между клетками и окружающей их средой. Если межклеточная жидкость становится гипотоничной, то вода входит в клетки и вызывает их набухание {клеточный
отек). Значительное увеличение объема клеток может привести к разрыву их мембран (см. осмотический гемолиз эритроцитов, с. 425).
В гипертонической среде, напротив, клетки теряют воду и сжимаются, что означает потерю тканями нормального тургора. В обоих случаях жизнедеятельность клеток в той или иной степени нарушается.
Функции электролитов плазмы. Изотоничность среды - одно из основных условий поддержания жизнедеятельности изолированной переживающей ткани. В то же время для сохранения клеточных функций этого условия недостаточно: необходимо также, чтобы различные ионы присутствовали в определенном соотношении. В табл. 18.2 приведены составы некоторых физиологических солевых растворов, успешно применяющихся в качестве сред для тканей in vitro. Хотя различные влияния тех или иных ионов известны давно, механизмы, лежащие в основе этих влияний, до конца не ясны.
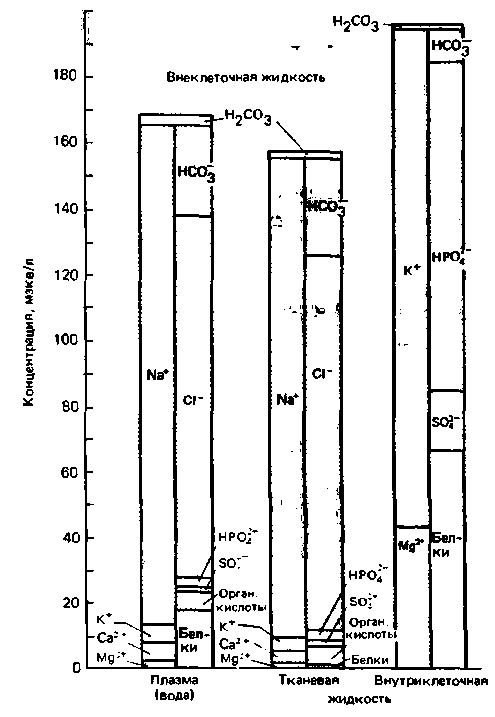 |
| Рис. 18.2. Электролитный состав плазмы, тканевой и внутриклеточной жидкостей (по [8] с изменениями) |
ГЛАВА 18. ФУНКЦИЯ КРОВИ 417
| Таблица 18.2. Состав наиболее распространенных физиологических растворов. Содержание различных ионов указано в мзкв/л | |||||
| Раствор Рингера | Раствор Тироде . для теплокроввых | ||||
| для холоднокровных | для теплокровных | | | ||
 | 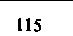 |  | 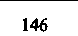 | 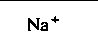 | 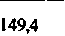 |
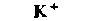 |  | 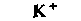 |  | 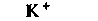 | 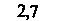 |
 | 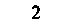 |  |  |  | 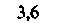 |
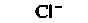 |  |  | 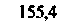 | 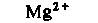 |  |
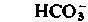 | 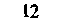 |  |  | 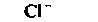 | 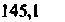 |
 |  |  |  |  | 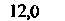 |
 |  |  |  |  |  |
| | | | | Глюкоза | 5,5 |
| | | | | (ммоль/л) | |
Б елки плазмы
елки плазмы
Общие свойства и функции. Высокая относительная вязкость плазмы (1,9-2,8 при относительной вязкости воды, равной 1) почти целиком обусловлена белками, содержание которых составляет 65-80 г/л. В связи с высокой молекулярной массой белков их моляльная концентрация весьма невелика - всего лишь около 1 ммоль/кг (см. табл. 18.1). Белковая фракция плазмы представляет собой смесь многих белков.
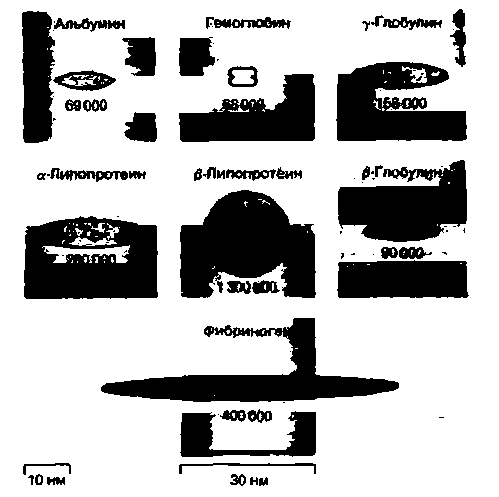 |
| Рис. 18.3. Молекулярные массы и схематические изображения формы некоторых белков плазмы и гемоглобина (по [19] с изменениями) |
Молекулярные массы белков плазмы варьируют от 44 000 до 1 300000. Частицы таких размеров относятся к коллоидам (рис. 18.3). Белки плазмы крови выполняют ряд функций.
- Питание. В организме взрослого человека содержится около 3 л плазмы, в которой растворено примерно 200 г белка. Это вполне достаточный запас питательных веществ. Обычно клетки поглощают не белки, а их компоненты-аминокислоты; однако некоторые клетки, в частности относящиеся к ретикулоэндотелиальной системе (РЭС), могут поглощать белки плазмы и расщеплять их при помощи собственных внутриклеточных ферментов. Высвобождающиеся при этом аминокислоты поступают в кровь, где сразу же могут использоваться другими клетками для синтеза новых белков.
- Транспорт. Многие небольшие молекулы в процессе переноса их от кишечника или депо к месту потребления связываются со специфическими белками плазмы (с. 421). Благодаря большой площади поверхности и наличию многочисленных гидрофильных и липофильных участков эти белки особенно пригодны для роли переносчиков. За счет связывания их липофильных групп с жироподобными нерастворимыми в воде соединениями белки могут удерживать такие вещества в растворе. Белки плазмы участвуют также в поддержании постоянного осмотического давления, так как способны связывать большое количество циркулирующих в крови низкомолекулярных соединений.
- Белки плазмы как неспецифические переносчики. Все белки плазмы связывают катионы крови, переводя их в недиффундирующую форму. Так, около 2/3 кальция плазмы неспецифически связано с белками. Этот связанный кальций находится в равновесии с физиологически активным кальцием, присутствующим в крови в виде свободных ионов. Связывание кальция белками зависит от pH: при повышении последнего (алкалоз; с. 621) связывание кальция усиливается.
- Роль белков в создании коллоидно-осмотического давления. Вследствие низкой молекулярной концентрации белков вклад их в общее осмотическое давление плазмы крови весьма невелик, но тем не менее создаваемое ими коллоидно-осмотическое (онкотическое) давление играет важную роль в регуляции распределения воды между плазмой и межклеточной жидкостью. В связи с тем что стенки капилляров в общем свободно пропускают небольшие молекулы, концентрация этих молекул и создаваемое ими осмотическое давление в плазме и в межклеточной жидкости примерно одинаковы. Что же касается белков плазмы, то их крупные моле-
418 ЧАСТЬ V. КРОВЬ И СИСТЕМА КРОВООБРАЩЕНИЯ
кулы лишь с большим трудом проходят через стенки капилляров (так, период полувыведения меченого альбумина из кровотока равен приблизительно 14 ч). Благодаря этой особенности, а также тому, что белки поглощаются клетками и переносятся лимфой, между плазмой и межклеточной жидкостью создается градиент концентрации белков: онкотическое давление плазмы равно примерно 25 мм. рт. ст. (3,3 кПа), а межклеточной жидкостипримерно 5 мм рт. ст. (0,7 кПа); разница между ними соответственно составляет около 20 мм рт. ст. (2,7 кПа).
Любое изменение осмотически эффективной концентрации белков плазмы крови приводит к нарушению обмена веществами и распределения воды между кровью и межклеточной жидкостью. Поскольку альбумин составляет самую большую фракцию белков плазмы (с. 419) (молекула альбумина относительно невелика, и его моляльная концентрация примерно в 6 раз больше, чем всех других белков плазмы), сдвиги в содержании альбумина особенно сильно влияют на коллоидно-осмотическое давление. Снижение концентрации альбумина в плазме часто приводит к задержке воды в межклеточном пространстве (интерстщиальный отек). В связи с этим искусственные кровезаменители, как правило, должны обладать тем же онкотическим (и кристаллоидно-осмотическим) давлением, что и плазма. В качестве коллоидов в таких растворах часто используют полисахариды (гидроксиэтилкрахмал, декстран) и полипептиды (желатину), так как получение в чистом виде белков плазмы крови человека-очень дорогостоящая процедура.
- Буферная функция. Поскольку белки - это амфотерные вещества (т.е. способные связывать в зависимости от pH среды и Н+, и ОН—), белки плазмы играют роль буферов, поддерживающих постоянство pH крови (с. 617).
- Предупреждение кровопотери. Свертывание крови, препятствующее кровотечению, частично обусловлено наличием в плазме фибриногена (с. 420). Процесс свертывания включает целую цепь реакций (в которых в качестве ферментов участвует ряд белков плазмы) и заканчивается превращением растворенного в плазме фибриногена в сеть из молекул фибрина, образующую сгусток (с. 432).
Разделение белков плазмы. Качественное и количественное определение белков плазмы крови широко вошло в повседневную практику (рис. 18.4). Электрофорез белков плазмы служит важным методом клинической диагностики, так как многие заболевания сопровождаются характерными изменениями в составе этих белков.
 |
| Рис. 18.4. Электрофореграмма сыворотки крови человека. Окрашенные полосы на бумажной ленте (Б) соответствуют зубцам на фотометрической кривой, отражающим указанное процентное содержание фракций разных белков. А. Схема прибора для электрофореза на бумаге |
Электрофорезом называется движение электрически заряженных частиц, находящихся во взвешенном состоянии или растворенных в жидкой среде, по градиенту напряжения. Молекулы белков построены из аминокислотных остатков, соединенных пептидными связями. Электролитические свойства этих молекул частично обусловлены ионизацией аминогрупп (—NH2) и карбоксильных (—СООН) групп, особенно тех, что расположены на концах боковых цепей. Такие группы электрически заряжены в соответствии с pH раствора (—NH3 или —СОО—). Для буферной функции белков еще важнее pH-зависимые имидазолъные группы остатка гистидина - одного из главных компонентов молекулы гемоглобина.
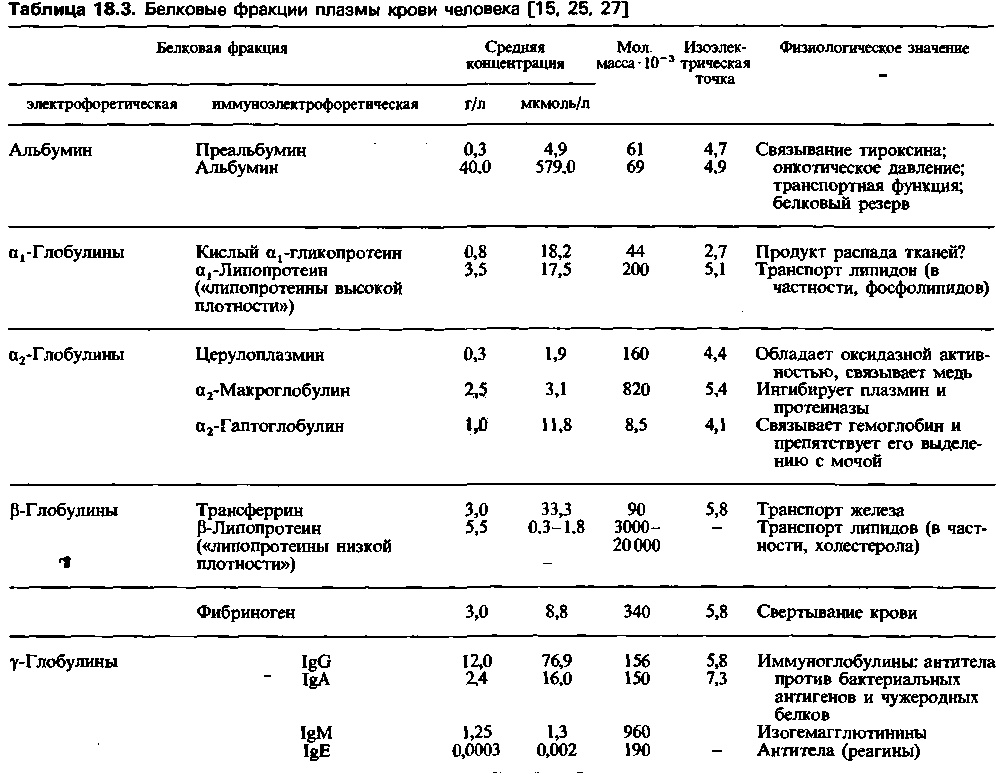
Электрофоретнческая подвижность белка зависит в основном от приложенного напряжения, размеров и формы молекулы и ее электрического заряда, который в свою очередь определяется разницей между значениями изоэлектрической точки (ИТ) для данного белка и pH раствора. Как видно из табл. 18.3, ИТ различных белков плазмы на ту или иную величину ниже 7. Следовательно, в нейтральной или щелочной среде все эти белки будут
ГЛАВА 18. ФУНКЦИЯ КРОВИ 4Ш
 |
 передвигаться в одном направлении (к аноду), но с различной скоростью (рис. 18.4).
передвигаться в одном направлении (к аноду), но с различной скоростью (рис. 18.4).Для того чтобы не только разделить белки, но также определить их молекулярные массы, применяют метод ультрацентрифугирования. На ультрацентрифуге Сведберга можно получить ускорение от 100000 до 750000 g. При данном ускорении скорость оседания молекул зависит от их удельной массы и формы (рис. 18.3) и плотности среды. Особенно хорошо белковые компоненты в какой-либо смеси можно разделить методом центрифугирования в градиенте плотности, так как при этом каждый из компонентов занимает в пробирке определенный уровень.
Еще более тонким способом разделения белков служит электрофорез в сочетании с иммунопреципитацией (иммуноэлектрофорез). При этом исследовании злектрофоретически разделенные белковые фракции диффундируют в геле по направлению к капле внесенной в него сыворотки. Когда белковый антиген достигает сыворотки, происходит осаждение антител-в геле появляется беловатая полоса мутности. При помощи этого метода было показано, что электрофоретически однородные белковые фракции могут состоять из нескольких белков, различающихся по иммунологическим свойствам (табл. 18.3).
Свойства и функции отдельных белковых фракций. Поскольку чаще всего для разделения белков используют электрофорез, в дальнейшем будут обсуждаться лишь белковые фракции, выделяемые этим методом. На рис. 18.3 схематично показаны относительные размеры и форма основных белков плазмы.
Альбумин плазмы. Около 60% общего белка плазмы приходится на долю альбумина, содержание которого составляет 35-45 г/л. Молекулярная масса альбумина-одного из самых низкомолекулярных белков плазмы-равна 69000. Поскольку концентрация альбумина высока, а размеры его молекулы невелики, этот белок на 80% определяет коллоидно-осмотическое давление плазмы. Общая площадь поверхности множества мелких молекул альбумина очень велика, поэтому они особенно хорошо подходят для выполнения функции переносчиков многих транспортируемых кровью веществ. К веществам, связываемым альбумином, относятся: били-
420 ЧАСТЬ V. КРОВЬ И СИСТЕМА КРОВООБРАЩЕНИЯ
рубин, уробилин, жирные кислоты, соли желчных кислот и некоторые экзогенные вещества - пенициллин, сульфамиды, ртуть и т. д. Одна молекула альбумина может одновременно связать 25-50 молекул билирубина (мол. масса 500). При многих патологических состояниях, в частности воспалительных заболеваниях и поражениях печени и почек, содержание альбумина снижается.
Глобулины плазмы. Глобулинами называют группу белков, которые могут быть разделены электрофоретически. В порядке убывания электрофоретической подвижности различают a1-, a2-, ßи γ-глобулины (рис. 18.4). Однако даже эти субфракции неоднородны по составу белков: каждую из них можно разделить при помощи других методов, например иммуноэлектрофореза (табл. 18.3).
Фракция а1-глобулинов состоит из многих коньюгированных белков, простетической группой которых являются углеводы-преимущественно гексозы и гексозамины. Эти белки называют гликопротеинами. Около 2/3 всего количества глюкозы плазмы присутствует в связанной форме в составе гликопротеинов. Эту связанную глюкозу невозможно определить с помощью клинических проб на сахар в плазме, лишенной белков; она может быть измерена лишь после отделения от белков методом кислотного гидролиза (в этом случае ее концентрация составляет 0,8-1,65 г/л). К субфракции гликопротеинов относится еще одна группа углеводсодержащих белков -протеогликаны (мукопротеины), в состав которых входят мукополисахариды.
К другим белкам, выделяющимся вместе с α1-глобулинами, относятся тироксин-связывающий белок, (витамин В12)-связывающий глобулин (транскобаламин), билирубин-связывающий глобулин и кортизол-связывающий глобулин {транскортин).
Фракция α2-глобулинов включает гаптоглобин, относящийся по химическому строению к протеогликанам, и медьсодержащий белок церулоплазмин. На каждую молекулу последнего приходится 8 атомов меди, обусловливающих оксидазную активность этого белка. Церулоплазмин связывает около 90% всей меди, содержащейся в плазме (однако с током крови к клеткам переносится медь, связанная не церулоплазмином, а альбумином).
К ß-глобулинам относятся основные белковые переносчики липидов и полисахаридов. Важное значение липопротеинов состоит в том, что они удерживают в растворе нерастворимые в воде жиры и липоиды и обеспечивают тем самым их перенос кровью. Около 75% всех жиров и липоидов плазмы входят в состав липопротеинов. Небольшие количества липопротеинов обнаруживаются и во фракции a1-глобулинов, однако большинство относится к ß-глобулинам; главный из них - это ß-липопротеин, молекула которого на 77% состоит из липи-
дов. Исследование липопротеинов плазмы методом ультрацентрифугирования и электрофореза (электрофоретическая подвижность липопротеинов обусловлена их белковым компонентом) - это важное средство диагностики различных форм гиперлипопротеинемий (см. учебники биохимии). Кроме липопротеинов к ß-глобулинам относится группа металлсодержащих белков, один из которых - трансферрин- служит переносчиком меди и, что особенно важно, железа. Каждая молекула трансферрина содержит два атома трехвалентного железа; именно трансферрин обеспечивает транспорт этого элемента кровью. В норме трансферрин плазмы лишь на 30% насыщен железом, и содержание железа составляет 1 мг Fe3+ на 1 л плазмы.
К неоднородной группе γ-глобулинов относятся белки с самой низкой электрофоретической подвижностью: их изоэлектрические точки ближе к нейтральному значению pH, чем у других белков плазмы (табл. 18.3). Данная группа включает большинство защитных и обезвреживающих веществ крови (иммуноглобулинов). Поскольку потребности в белках, выполняющих такие специфические функции, бывают различны, размеры и состав фракции γ-глобулинов существенно варьируют. Почти при всех заболеваниях, особенно воспалительных, содержание γ-глобулинов в плазме повышается. При этом общее количество белков плазмы обычно остается приблизительно тем же, так как повышение содержания γ-глобулинов сопровождается примерно равным уменьшением фракции альбумина; в результате так называемый альбумин-глобулиновый коэффициент снижается. К γ-глобулинам относятся также агглютинины крови, называемые анти-А и анти-В.
Фибриноген выявляется в виде узкой отдельной полосы, расположенной между полосами β- и γ-глобулинов. Этот белок представляет собой растворимый предшественник фибрина; последний превращается в нерастворимую форму, обеспечивая образование сгустка крови (с. 432). Молекула фибриногена имеет удлиненную форму (соотношение длина/ширина равно 17:1). Высокая вязкость растворов фибриногена обусловлена тенденцией его молекул образовывать агрегаты в виде «ниток бус».
Характерные изменения фракции фибриногена обнаруживаются лишь при некоторых редких заболеваниях, поэтому электрофоретически выявляемые сдвиги в содержании этого белка не имеют большого диагностического значения. Кроме того, при электрофорезе на бумаге подвижность удлиненной молекулы фибриногена в большей степени зависит от свойств бумаги, чем подвижность других белков плазмы. Из этих соображений при электрофорезе белков крови на бумаге, применяемом в клиниках, обычно используют не плазму, а сыворотку, в результате чего на типичной электрофореграмме полоса фибриногена отсутствует (рис. 18.4).
ГЛАВА 18. ФУНКЦИЯ КРОВИ 421
Синтез и оборот белков плазмы. При нормальном питании в организме человека за сутки вырабатывается около 17 г альбумина и 5 г глобулина. Период полураспада альбумина у человека равен 10-15 сут, а глобулина-примерно 5 сут; это означает, что за такой срок 50% общего количества белка сменяется новосинтезированным.
Вещества, транспортируемые плазмой крови
Как было показано в предыдущих разделах, неорганические электролиты и белки плазмы уже самим своим присутствием оказывают огромное влияние на ее важнейшие функции. В этом смысле данные вещества можно считать функциональными элементами плазмы.
Существует и другая группа компонентов плазмы-вещества, которые просто переносятся плазмой и в физиологических концентрациях мало влияют на ее свойства. Для таких веществ плазма служит прежде всего переносчиком. Эта неоднородная группа включает: а) питательные вещества, витамины и микроэлементы; б) промежуточные продукты обмена; в) гормоны и ферменты; г) вещества, подлежащие выведению.
Питательные вещества, витамины и микроэлементы. Самая крупная (по массе) фракция питательных веществ, транспортируемых плазмой,- это липиды (липидами называют все соединения, растворимые в эфире: жиры, липоиды и стероиды), однако содержание этих веществ в плазме варьирует в широких пределах (табл. 18.4).
После приема жирной пищи содержание липидов в крови может достигать 20 г/л, и плазма в этом случае приобретает молочно-белый цвет (липемия). Около 80% всех жирных кислот (глицериды, фосфолипиды и эфиры холестерола) образуют липопротеиновые комплексы, связываясь с глобулинами. Неэтерифицированные жирные кислоты соединяются преимущественно с альбумином. В отличие от липидов, содержание которых в плазме варьирует в зависимости от особенностей обмена веществ в данный момент, концентрация важнейшего из углеводов-глюкозы поддерживается на относительно постоянном уровне 0,8-1,2 г/л (4-7 ммоль/л), хотя скорости ее поглощения клетками и утилизации подвержены значительным колебаниям. К питательным веществам, переносящимся кровью, относятся также аминокислоты, среднее содержание которых в плазме составляет около 0,04 г/л. Источником аминокислот служат прежде всего белки пищи.
В плазме крови постоянно присутствуют все витамины (с. 730) и важные питательные вещества, обладающие свойствами витаминов (например, холин). Концентрация этих веществ в плазме варьирует, причем зависит не только от содержания их в пище и синтеза кишечной флорой, а для ряда витаминов определяется, кроме того, особыми факторами, облегчающими их всасывание. Так, всасывание витамина В12 зависит от «внутреннего фактора» Кастла. Многие витамины свободно циркулируют в плазме, однако некоторые из них, особенно жирорастворимые и ряд водорастворимых (например, витамин В12), связываются белками.
| Таблица 18.4. Содержание небелкового азота и липидов в плазме крови человека, г/л [27] | ||
| Азотсодержащее вещество | Среднее значение | Границы нормы |
| Мочевина | 0,14 | 0,1-0,2 |
| Аминокислоты | 0,05 | 0,03-0,07 |
| Мочевая кислота | 0,017 | 0,01-0,023 |
| Креатинин | 0,005 | 0,004-0,005 |
| Аммоний | 0,002 | 0,001-0,002 |
| Общий небелковый азот | 0,25 | 0,22-0,30 |
| Жиры | | |
| Нейтральный жир | | 0-4,5 |
| Жирные кислоты | | 2-4,5 |
| Стероиды | | |
| Холестерол | | 1,2-3,5 |
| Свободный холестерол | | 0,4-0,7 |
| Желчные кислоты | | 0,002-0,03 |
| Соли желчных кислот | | 0,05-0,12 |
| Фосфолипиды, общее | | 1,5-2,5 |
| содержание | | |
| Лецитин | | 1,0-2,0 |
| Кефалин | | 0-0,3 |
| Сфингомиелин | | 0,1-0,3 |
| Общее содержание эфирорастворимых веществ | 3,8-6,8 | |
М
 икроэлементами называют элементы, необходимые для построения структурных молекул, гормонов и т.п. Один из важнейших микроэлементов-это железо. Оно всасывается в кишечнике в виде белкового комплексамукозального трансферрина [33], причем скорость всасывания зависит не от снабжения, а от потребности в нем организма.
икроэлементами называют элементы, необходимые для построения структурных молекул, гормонов и т.п. Один из важнейших микроэлементов-это железо. Оно всасывается в кишечнике в виде белкового комплексамукозального трансферрина [33], причем скорость всасывания зависит не от снабжения, а от потребности в нем организма.Большая часть других металлов, относящихся к микроэлементам, циркулирует в плазме в составе металлсодержащих белков (металлопротеинов). Так, 90% меди связано с белком церулоплазмином (см. с. 420). Кобальт является важным компонентом витамина В12 (кобаламина). Практически весь иод присутствует в составе комплекса с так называемым тироксин-связывающим белком (с. 420).
Промежуточные продукты метаболизма. Из всех интермедиатов в наибольшем количестве в плазме присутствует молочная кислота. Содержание ее увеличивается при недостатке кислорода и интенсивной мышечной нагрузке. К органическим кислотам, постоянно присутствующим в крови, относится и пировиноградная кислота. Она образуется в результате метаболизма аминокислот и углеводов и поэтому играет ключевую роль в энергетическом обмене.
Гормоны и ферменты. Соединения этой группы представлены белками, полипептидами, аминами, амидами и стероидами.
Конечные продукты обмена (шлаки), которые не могут быть использованы и подлежат удалению из организма. Важнейшие из них-это диоксид углерода, мочевина, мочевая кислота, креатинин, билирубин и аммиак. Все эти вещества, за исключением диоксида углерода, содержат азот и выводятся почками. При нарушении функции по-
422 ЧАСТЬ V. КРОВЬ И СИСТЕМА КРОВООБРАЩЕНИЯ
чек уровень азотсодержащих продуктов обмена в крови увеличивается. Этот уровень измеряют по методу Кьельдаля, позволяющему определить содержание азота в плазме после осаждения из нее белков. Данный параметр используется при диагностике заболеваний почек. Для практических целей считают, что уровень небелкового азота (НБА), определяемый по методу Кьельдаля, соответствует содержанию азота в шлаках, однако около 1/5 общего НБА приходится на долю аминокислот, не являющихся шлаками. В табл. 18.4 перечислены основные компоненты плазмы, содержащие НБА.
