Способ формирования арефлюксного пищеводно-желудочного соустья при рефлюкс-эзофагитах ( экспериментальное исследование) 14. 00. 27 -хирургия
| Вид материала | Исследование |
- Сравнительная оценка методов формирования межкишечного соустья в хирургии толстой кишки, 363.47kb.
- Функционально адекватные анастомозы при гастрэктомии и резекции желудка (клинико-экспериментальное, 547.42kb.
- Обоснование способов хирургической коррекции нарушений углеводного обмена (клинико-экспериментальное, 502.51kb.
- Система комплексной интраоперационной профилактики спаечной болезни брюшины (клинико-экспериментальное, 626.28kb.
- Бандин Артем Александрович Владимир Васильевич Макарчук Содержание курсовой работы:, 28.4kb.
- Лазерная фотодинамическая терапия ожоговых ран (экспериментальное исследование) 14., 295.89kb.
- Экспериментальное обоснование применения нейропептидов в комплексной терапии острого, 259.86kb.
- И с нормальным психическим развитием (2-5 класс) Научный Е. В. Глазанова Работа представляет, 6.48kb.
- 1. При рефлюкс-эзофагите применяют: а нитроглицерин; б мотилиум; в но-шпу; г де-нол;, 467.53kb.
- Экспериментальное обоснование применения электропунктурной рефлексотерапии при лечении, 225.16kb.
На правах рукописи
БЕЮНОК АЛЕКСАНДР ЕНИЕВИЧ
СПОСОБ ФОРМИРОВАНИЯ
АРЕФЛЮКСНОГО ПИЩЕВОДНО-ЖЕЛУДОЧНОГО СОУСТЬЯ ПРИ РЕФЛЮКС-ЭЗОФАГИТАХ
( экспериментальное исследование)
14.00.27 -хирургия
Автореферат
диссертация на соискание ученой степени кандидата
медицинских наук
ТОМСК-2005
Работа выполнена в ГОУ ВПО Сибирский государственный медицинский университет Федерального агенства по здравоохранению и социальному развитию
Научный руководитель:
Доктор медицинских наук, профессор,
Член-корреспондент РАМН Дамбаев Георгий Цыренович
Официальные оппоненты:
Доктор медицинских наук, профессор, Жерлов Георгий Кириллович
Заслуженный деятель науки РФ
Доктор медицинских наук Гибадулин Наиль Валерианович
Ведущая организация:
ГОУ ВПО Новосибирская государственная медицинская академия Росздрава
Защита диссертации состоится «__»_______ 2005 года в ___ час. на заседании диссертационного совета Д 208.096.01 при Сибирском государственном медицинском университете по адресу: г. Томск, Московский тракт,2
С диссертацией можно ознакомиться в научно-медицинской библиотеке Сибирского государственного медицинского университета (634050, г.Томск,
пр.Ленина,107 )
Автореферат разослан «__ »____________ 2005 года
Ученый секретарь
диссертационного совета Суханова Г.А.
ОБЩАЯ ХАРАКТЕРИСТИКА ДИССЕРТАЦИИ
Актуальность проблемы. Хирургия пищевода – один из самых трудных и сложных разделов лечения заболеваний пищеварительного тракта. В вопросе о выборе метода лечения больных с грыжей пищеводного отверстия диафрагмы и рефлюкс-зофагита единого мнения нет.
Ряд авторов [ Skinner et al., Brantigan P.L. et al., Hamelman J. et al.1969 ] ставят показания достаточно широко, другие [ Ranfael R.et al., Fraser C.X.et al., Hill M. et al., 1973 ], отмечая значительное число рецидивов, настаивают на более строгом отборе больных. Б.В. Петровский и Н.Н. Каншин (1977) весьма четко определили показания к хирургическому лечению при данном заболевании: вопрос о хирургическом вмешательстве необходимо ставить лишь при неэффективности консервативного лечения, а также при наличии резко выраженных симптомов рефлюкс-эзофагита и при ряде тяжелых осложнений. Рефлюкс-эзофагит - самое распространенное заболевание пищевода, поэтому проблема профилактики и его осложнений до настоящего времени остается актуальной.Частота рефлюкс-эзофагита среди всех заболеваний пищевода составляет 5,8-75% [ Березов Ю.Е. и соавт., 1973,Уткин В.В., 1973,Шептулин А.А.,1995 ].
Рефлюкс-эзофагит характеризуется развитием тяжелых осложнений- язв, пептических стриктур, кровотечений, цилиндрической метаплазией слизистой оболочки пищевода (пищевод Баррета), потенциально опасных для жизни пациентов. При тщательном обследовании симптомы гастро-эзофагеальной рефлюксной болезни выявляются у 20-40% взрослой популяции [ Nebell R., 1976, Loff G., 1993 ], признаки рефлюкс-эзофагита у 2-10%, подвергшихся эндоскопическому исследованию [ Peterson K.,1995], наличие язв, стриктур, кровотечений, пищевода Баррета у 20% больных с рефлюкс-эзофагитом [ Speehler V., 1992 ].
До сих пор не решен вопрос о том, что является первопричиной рефлюкс-эзофагита: высокая кислотность продукции желудка и экспозиция ее в пищеводе или же напротив первичным звеном является нарушение моторики, декомпенсация запирательной функции нижнего пищеводного сфинктера, расстройства клиренса пищевода, замедление эвакуации содержимого желудка. Несмотря на определенные успехи, достигнутые в изучении проблемы рефлюкс-эзофагита, вопросы этиологии патогенеза, диагностики и лечения являются предметом дискуссии.
Клиницист стоит перед проблемой выбора: использовать ли в лечении рефлюкс-эзофагита консервативные методы или выставить показания к оперативному лечению. Резекция проксимального отдела желудка предполагает создание пищеводно-желудочного анастомоза взамен удаленной кардии, регулирующей поступление пищи из пищевода в желудок и предотвращающей попадание кислого желудочного содержимого на слизистую пищевода.До настоящего времени несостоятельность швов пищеводно-желудочных анастомозов является ведущей причиной летальности в раннем послеоперационном периоде.Частота данного осложнения по данным различных авторов составляет 1,9-33.4%. [ Березов Ю.Е., 1961, Бондарь Г. В. и соавт., 1993, 1994, Петерсон Б.Е., 1962, Черноусов А.Ф., 1990, 1995, Inberg T. et al., 1981, Lortat-Jacob J.,1975 ].В отдаленном п/о периоде состояние больных усугубляется развитием рефлюкс-эзофагита, рубцового стеноза пищевода.
По литературным данным рефлюкс-эзофагит после проксимальной резекции желудка и гастрэктомии наблюдается в 13-73% случаев. [Черный В.А., Щепотин И.В., 1983 ].Стеноз анастомоза в отдаленном п/о периоде наблюдается от единичных случаев до 50-60% [ Казанский В.И.,1965, Петерсон В.Е., 1972, Щепотин И.Б., 1988, Beker D.,1964, 1950, Nakajama Y.,1956, Pacellif R.et al.,1999 ].
Таким образом, несостоятельность швов пищеводно-желудочных анастомозов, рефлюкс-эзофагит, рубцовый стеноз соустья довольно часто сопровождают проксимальную резекцию желудка, а существующие методы не всегда предупреждают их возникновение.
Поэтому проблема разработки такой методики формирования пищеводно-желудочного анастомоза, которая позволит избежать или уменьшить число осложнений раннего и отдаленного послеоперационного периодов, является актуальной.
ЦЕЛЬ РАБОТЫ: Разработать новый способ формирования арефлюксного пищеводно-желудочного соустья при рефлюкс-эзофагитах.
ЗАДАЧИ ИССЛЕДОВАНИЯ:
1. Изучить в эксперименте макроскопическую картину сформированных мышечного «жома» и клапана из слизистого и подслизистого слоев пищевода, погруженных в желудок (в различные сроки).
2. Изучить в эксперименте морфологическую картину состояния слизистого и подслизистого слоев пищевода, погруженных в желудок (в различные сроки).
3. Изучить состояние мышечного «жома» по данным морфологических исследований.
4. Оценить функциональную активность сформированного «жома и клапана» в отдаленные сроки.
НАУЧНАЯ НОВИЗНА:
Разработана в эксперименте новая методика формирования арефлюксного «жомно-клапанного» соустья конец в конец с созданием искусственного жома в виде манжетки и инвагинационного клапана из слизисто-подслизистого слоя пищевода. Показано, что «жом и клапан» пищеводно-желудочного соустья сохраняют свою форму и тканевую структуру в ранние и отдаленные сроки после операции. Новизна и оригинальность этих исследований и разработанной новой технологии антирефлюксной операции при гастроэзофагеальной рефлюксной болезни подтверждена патентом Российской Федерации на изобретение ( Патент РФ «Способ формирования арефлюксного пищеводно-желудочного анастомоза» № 2235510).
ПРАКТИЧЕСКАЯ ЗНАЧИМОСТЬ РАБОТЫ:
На основании экспериментальных исследований показано, что применение арефлюксного пищеводно-желудочного соустья позволяет улучшить ближайшие и отдаленные результаты хирургического лечения больных при рефлюкс-эзофагитах. Профилактика рефлюкс-эзофагита достигается формированием «жома» из мышечной оболочки пищевода и эластичного «клапана» из слизисто-подслизистого слоев пищевода. Надежность пищеводно-желудочного соустья, обеспечивающая минимальный риск операции, значительные арефлюксные свойства позволяют расширить показания к радикальному хирургическому лечению лиц с сопутствующей патологией.
ОСНОВНЫЕ ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ:
1. Разработанная методика арефлюксного пищеводно-желудочного соустья надежна в отношении ранних специфических послеоперационных осложнений.
2. Сформированные «жом и клапан» пищеводно-желудочного соустья сохраняют свою форму, структуру и функциональную полноценность в ближайшие и отдаленные сроки после операции.
3. Искусственный «клапан», функционируя как единый механизм с искусственным «жомом», выполняет функцию дополнительного препятствия ретроградному забросу желудочного содержимого в пищевод, предупреждая развитие рефлюкс-эзофагита.
ВНЕДРЕНИЕ И АПРОБАЦИЯ РАБОТЫ
Рекомендации по предложенному экспериментальному способу формирования пищеводно-желудочного соустья при рефлюкс-эзофагитах используются в учебном процессе при чтении лекций на кафедре госпитальной хирургии с курсом онкологии Сибирского государственного медицинского университета.Основные положения работы доложены и обсуждены на заседании Томского областного общества хирургов (2003), на конференции, посвященной «10-летнему внедрению эндоскопической службы в Юргинском районе Кемеровской области» (2004),на заседании кафедры госпитальной хирургии СибГМУ, на апробационной комиссии о хирургии.
Публикации
По материалам диссертации опубликовано 4 статьи, получен 1патент Р.Ф. на изобретение.
Объем и структура работы
Диссертация изложена на 147 страницах машинописи и состоит из введения, 3 глав, заключения и выводов. Диссертация иллюстрирована 58 рисунками.
Список литературы включает 261 источник, в том числе 217 отечественный и 44 иностранных авторов.
Материалы и методы исследования
Экспериментальная часть работы выполнена на базе экспериментального отдела госпитальной хирургии с курсом онкологии клиники имени А.Г. Савиных и в Центральной научно-исследовательской лаборатории при Сибирском государственном медицинском университете в отделе экспериментальной хирургии и патофизиологии животных.
Гистологические исследования выполнены на базе областного бюро судебно-медицинской экспертизы г. Кемерово и патологоанатомического отделения МУЗ ЦГБ г. Юрга Кемеровской области (Главный внештатный патологоанатом, заведующий ПАО железнодорожной больницы г. Кемерово, кандидат медицинских наук Шрайбер А.А.).
Рентгенологические, эндоскопические исследования проводились сотрудниками рентгенологического кабинета и эндоскопического отделения клиники им. А.Г. Савиных.
С целью разработки методики формирования арефлюксного «жомно-клапанного» пищеводно-желудочного соустья и изучения морфофункционального состояния искусственного «жома и клапана» были поставлены эксперименты на 50 белых крысах различного возраста и веса (250 – 400 гр.) и 10 беспородных собаках обоего пола, массой тела 8- 20кг.
В соответствии с «правилами проведения работ с использованием экспериментальных животных», утвержденными Приказом МЗ СССР №755 от 12.08.1977г., все эксперименты и выведение животных из опытов осуществлялись под общей анестезией.
На крысах разрабатывалась методика формирования арефлюксного пищеводно-желудочного соустья, так как анатомические особенности ЖКТ этих животных позволяют беспрепятственно моделировать различные варианты оперативного вмешательства на пищеводе.
Прооперированных крыс выводили из опыта для проведения пневмопрессии и забора гистологического материала в сроки 1, 3, 7, 10, 14, 21, 30, 60, 90 суток,6 мес.,12 мес. после операции. Изучали особенности сформированных соустьев:
- Возможность формирования жомно-клапанного соустья;
- Проходимость соустья;
- Механическая прочность швов;
- Морфогенез зоны анастомоза в сроки от 1суток до 12 месяцев.
Для собак подготовка к операции, анестезиологическое пособие и ведение послеоперационного периода были однотипными.
Описание методики операции
При выполнении операции придерживались следующих правил:
- операция проводится чрезбрюшинным доступом.
- соблюдение асептичности и атравматичности.
- строгое послойное рассечение и сшивание анастомозируемых органов.
- создание мышечного «жома» на дистальном отделе пищевода высотой 15-20 мм. и искусственного «клапана» из слизисто-подслизистого слоев пищевода.
- не выполняется пилоропластика.
Верхне-средне-срединным доступом вскрывали брюшную полость. Выполняли мобилизацию левой доли печени по Кохеру. Пищевод обходили инструментом или пальцем брали на тесьму, или резиновую держалку, вытягивали в брюшную полость. Отступив 10 мм от кардиального жома циркулярно рассекали мышечные слои пищевода и заворачивали кверху на ширину 15-20 мм, свободный край подшивали к мышечному слою пищевода ( Рис. 1 ).
Выше края среза сосуды подслизистого слоя по всей окружности прошиваются узловыми кетгутовыми швами, причем не пересекаются стволы блуждающего нерва. Формирование пищеводно-желудочного соустья производилось в следующей последовательности. Накладывали 4-5 рядов швов на заднюю полуокружность соустья: на пищеводе берется нижний край сформированного жома с захватыванием подслизистого слоя; на дне желудка берется серозно-мышечная оболочка. Захватывание подслизистой основы пищевода при наложении ряда швов является важным моментом, предупреждающим их прорезывание. После наложения 4-5 швов при натягивании нитей сдвигается дно желудка к пищеводу, швы поочередно завязываются ( Рис. 2 ).
Затем накладывается ряд швов на переднюю полуокружность соустья: на дне желудка берется серозно-мышечная оболочка; на пищеводе берется нижний край сформированного «жома» с захватыванием подслизистого слоя передней стенки пищевода. Наложение швов чередуем (справа, слева), последний шов накладывается на середине соустья. После наложения 4-5 швов нити натягиваются, диссектором избыток слизисто-подслизистой основы погружается в просвет желудка, т.е. формируется «клапан» ( Рис. 2 ).

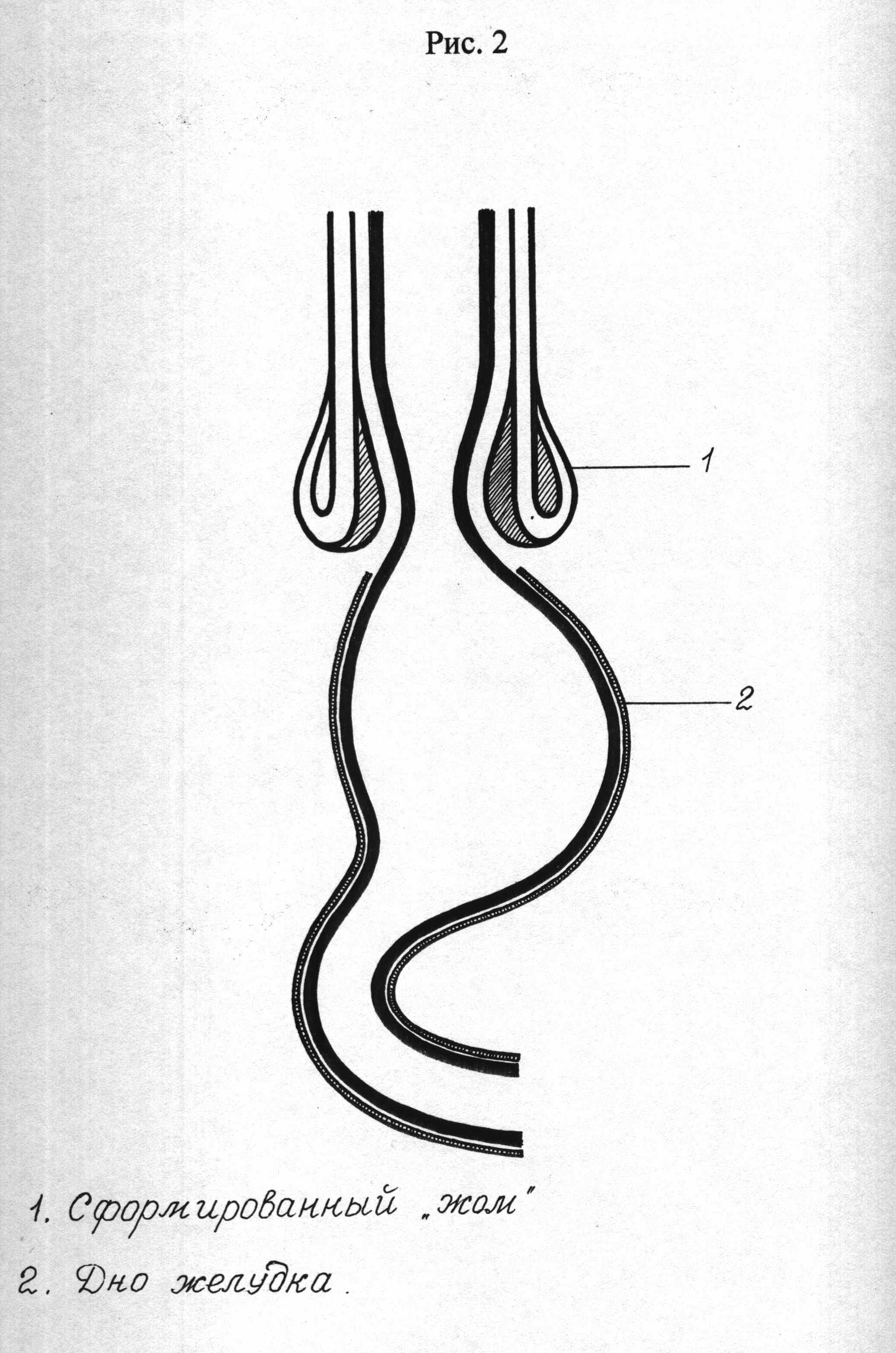
Рис. 1 Формирование мышечного «жома»
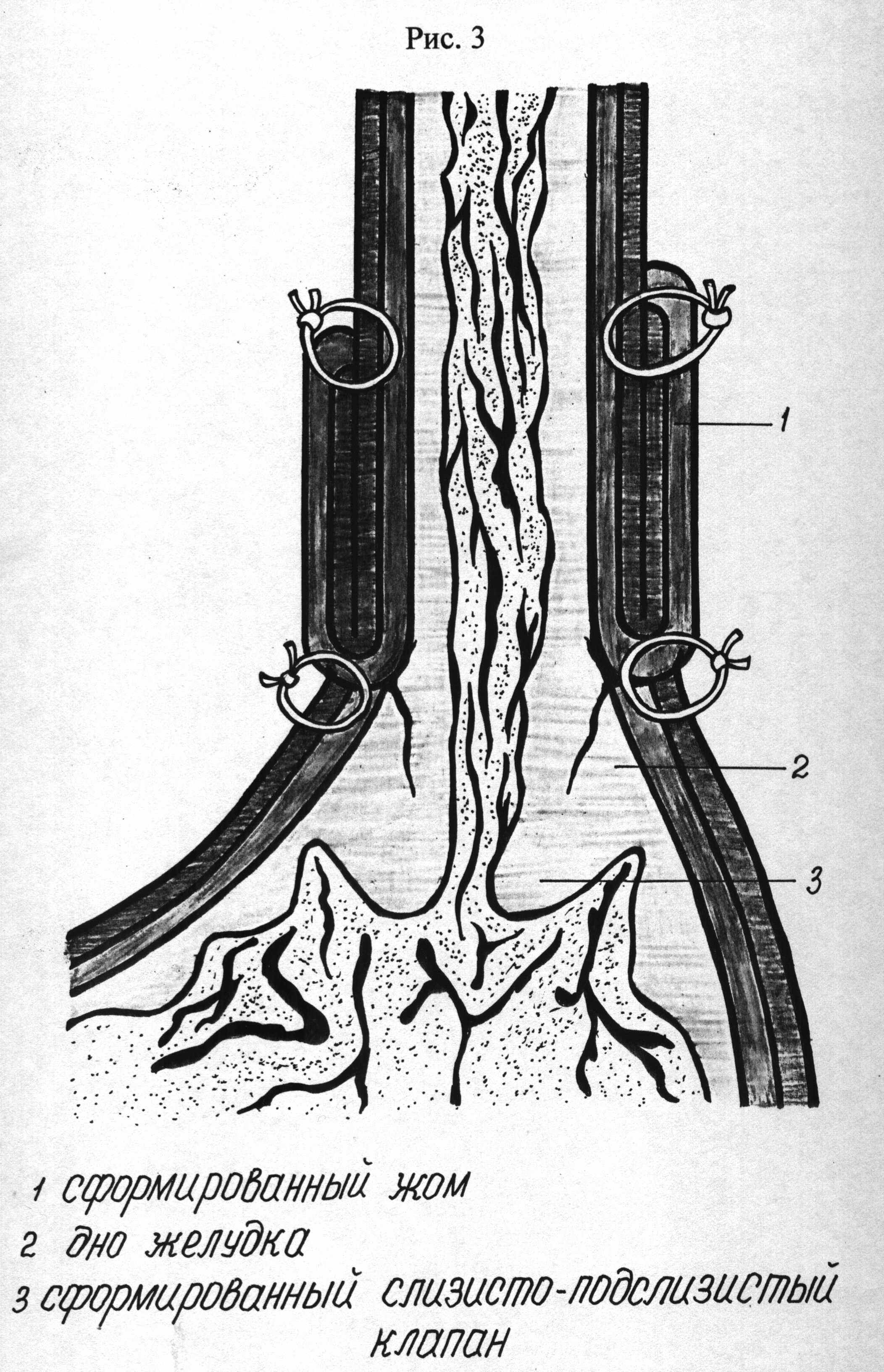
Рис. 2 Формирование «жома» и слизисто-подслизистого «клапана»
1) сформированный искусственный «жом»
2) дно желудка
3) инвагинированный «клапан» из слизисто-подслизистого слоев
Результаты исследований
Исследование механической прочности шва пищеводно-желудочного соустья проводили путем пневмопрессии. Для этого использовали ртутный медицинский манометр, позволяющий измерять давление в пределах от 10 до 260 мм рт. ст.
Измерение выполняли следующим образом: иссекали описанный выше комплекс органов, в просвет пищевода вводили силиконовую трубку, соединенную с манометром, пищевод над трубкой стягивали прочной лигатурой. Срез желудка герметично перевязывали. Препарат помещали под воду и затем медленно нагнетали воздух, контролируя показания манометра.
Пределом механической прочности соустья считалось давление, при котором в воде над швом соустья появлялись пузырьки воздуха. Если при достижении максимального давления манометра пузырьки воздуха не появлялись, то считали, что соустье сохраняет герметичность при давлении в 260 мм. рт. ст. Таким образом определена механическая прочность шва в 30 препаратах.
В контрольные сроки путем проведения эфирного наркоза крысы выводились из опыта. Визуально оценивали выраженность спаечного процесса в брюшной полости, внешний вид сформированного соустья; пальпаторно определяли кольцо сформированного жома пищевода, клапан через стенки дна желудка. Выделяли органокомплекс (средняя и нижняя трети пищевода, желудок).
Исследования препаратов проводили при увеличении в 100, 200, 400, 600 раз. При оценке морфологической картины обращалось внимание на сосудистые реакции, характер клеточных и волокнистых структур, степень восстановления эпителиального покрова.
3 сутки. При вскрытии брюшной полости выпота не обнаружено, брюшина гладкая, блестящая, спаечного процесса не выявлено, отека нет. Серозная оболочка желудка гладкая, блестящая, пальпаторно инфильтраций не выявлено. Со стороны просвета желудка отмечается значительный отек «хоботка». Верхушка «хоботка» темно-красного цвета, отечная, участков черного цвета нет, при надавливании пинцетом не секвестрируется. Слизистая желудка обычного цвета, блестящая.
7 сутки В брюшной полости выпота нет, умеренный спаечный процесс в области операционной раны. Желудочное соустье чистое, отека нет. Сероза гладкая, блестящая, налета фибрина нет. Пищевод не расширен. Со стороны просвета желудка отмечено, что «хоботок» вывернулся на 1/2 своей высоты, его края эластичны, сохраняется незначительный отек, застой в самой дистальной части.
21 сутки При вскрытии брюшной полости умеренный спаечный процесс в области операционной раны. Серозная оболочка желудка блестящая, гладкая. Линии швов не видно. Со стороны просвета желудка отмечено, что «хоботок» остается несколько полнокровным, хотя слизистая ровная, гладкая, сохраняется незначительный отек. Высота «хоботка» 8-9 мм. Пальпаторно «хоботок» эластичен, на расстоянии 1,5-2 мм от основания «хоботка» образовался вал слизистой желудка высотой 2 мм. При рассматривании сверху картина напоминает чернильницу-непроливашку
30 сутки. При вскрытии брюшной полости незначительный спаечный процесс в области послеоперационного раны, сероза гладкая, чистая, линия швов не видна. При вскрытии просвета желудка обнаружено, что «хоботок» розового цвета, поверхность гладкая, высота «хоботка» 7-8 мм, определяется валик из слизистой желудка вокруг «хоботка»
Три месяца В брюшной полости спаечного процесса не обнаружено. Зона соустья свободна, отека нет.Пальпаторно четко определяется в толще пищевода сформированный гладкомышечный «жом» в виде эластичного тяжа шириной 9-10 мм. При вскрытии желудка «хоботок» без воспаления, эластичен, несколько вытянут в продольном направлении. Высота «хоботка» 8 мм, вокруг «хоботка» валик слизистой желудка высотой 2 мм. При продольном рассечении пищевода в зоне соустья ясно виден гладкомышечный жом шириной 9 мм
Шесть месяцев В брюшной полости спаечного процесса не выявлено, сероза чистая, блестящая. Линия швов не видна. Четко определяется искусственный «жом» пищевода, пальпаторно определяется «хоботок» в просвете желудка. Со стороны слизистой «хоботок» без признаков воспаления, высота его составляет 8-9 мм, вокруг «хоботка» определяется валик слизистой желудка
Один год. В брюшной полости спаечного процесса нет, линия швов не видна. Сероза чистая, блестящая. Четко определяется сформированный «жом». Зона соустья свободная, отека нет. Со стороны слизистой «хоботок» высотой 8 мм, эластичный, находится в сомкнутом состоянии, вокруг «хоботка» определяется валик слизистой желудка.
У экспериментальных крыс в различные сроки после операции изучена морфологическая картина слизистой оболочки и подслизистой основы пищевода, погруженных в просвет желудка, состояние сформированного мышечного «жома» и прилегающих к соустью участков пищевода и желудка.
3 сутки. Зона соустья умеренно инфильтрирована сегментоядерными лейкоцитами, присутствуют зоны микронекрозов. Слизистая, подслизистая основа пищевода, погруженная в просвет желудка, характеризуется одинаковым утолщением в различных отделах, и особенно это касается ворсинок, которые не только утолщены, но и деформированы, в отдельных участках лишены покровного эпителия. Собственная пластинка слизистой характеризуется несколько паретичными сосудами, отдельные из них обильно заполнены форменными элементами. Окружающая сосуды ткань и проходящие здесь мышечные волокна слабо различимы. У основания ворсинок нередко видны скопления эритроцитов, лимфо-и гранулоцитов. Элементы мышечной пластинки слизистой при окраске по Ван-Гизону четко различимы, при чем это касается не только формы миоцитов, но и сократительного аппарата.
За пределами сосудов в некоторых участках подслизистой основы имеет место обильное скопление форменных элементов,превалируют эритроциты. Слизистая желудка в зоне соустья сохранена, хотя эпителий нередко разрушен, эпителиоциты набухшие, мышечный слой представлен хорошо выявляющимися миоцитами, цитоплазма которых умеренно окрашена эозином и пикриновой кислотой при окраске по Ван-Гизону.
Сформированный пищеводный мышечный «жом» представлен удовлетворительно выявляющимися гладкими миоцитами, идущими в неодинаковом направлении Миофибриллярный аппарат либо не виден, либо слабо окрашивается гематоксилином. В прослойках рыхлой неоформленной соединительной ткани между мышечными слоями «жома» видны многочисленные кровеносные сосуды и явления слабо выраженного периваскулярного отека, имеет место незначительное скопление форменных элементов среди мышечных клеток «жома».
7 сутки. В области соустья сохраняется экссудация сегментоядерными лейкоцитами. Язвенный дефект заполнен фибрином с шовным материалом, вокруг шовного материала встречается формирующаяся грануляционная ткань. Молодая грануляционная ткань заполняет дефекты между слизистыми, а по грануляционной ткани располагается клеточный инфильтрат, на этот клеточный пласт надвигается регенирирующий клеточный инфильтрат, появляется цилиндрический эпителий с базофильной цитоплазмой, единичными бокаловидными клетками, секретирующими слизь В основании мышечного «жома» сосуды расширены, заполнены форменными элементами, между продольными и циркулярными слоями очаги кровоизлияния. Миоциты продольного и циркулярного слоев в большинстве своем имеют обычный вид, участками между ними определяются скопления фибропластов и сегментоядерных клеток. По свободному краю «жома» также встречаются лейкоциты, часть из них находится в состоянии распада. В подслизистых слоях «клапана» имеется расширение артериол и капилляров, миграция лейкоцитов и свободных макрофагов. По всей площади соприкосновения подслизистых слоев определяется созревающая грануляционная ткань, богатая кровеносными сосудами, в которой четко прослеживается формирование коллагеновых волокон .
21 сутки. В зоне соустья серозный слой и слизистая оболочка восстанавливаются, отека нет, определяется умеренная инфильтрация тканей преимущественно плазматическими, лимфоидными клетками и гистиоцитами Эпителизация слизистой лишь частична. Подслизистая представлена формирующейся соединительной тканью. Вокруг шовного материала наблюдаются участки гранулематозного воспаления.В зоне «клапана» слизистая и подслизистая оболочки типичного строения, признаки отека и воспаления практически отсутствуют. На всемпротяжении участки некрозов замещаются фиброзной тканью по типу «гармошки» Некоторые мышечные волокна спазмированы, при этом структура миоцитов близка к типичной.
30 сутки. При гистологическом исследовании отмечается полная эпителизация по краю соустья. Щель стыка соустья представлена в виде узкой полоски зрелой соединительной ткани, богатой волокнистыми структурами. Мышечные слои «жома» представлены отчетливо выявляющимися элементами гладкой мускулатуры пищевода, цитоплазма мышечных клеток окрашивается эозином равномерно, кровеносные сосуды не расширены. Между подслизистыми слоями пищевода и дна желудка в области «клапана» определяется узкая полоска зрелой соединительной ткани Слизистая оболочка пищевода покрыта многослойным плоским эпителием и хорошо выраженным базальным слоем, отмечается незначительный отек собственной пластинки.
В подслизистой основе имеется умеренный отек, хорошо выявляются секреторные отделы собственных желез пищевода. В отдельных случаях можно увидеть увеличение диаметра просвета кровеносных сосудов и гомогенизацию коллагеновых волокон соединительной ткани. При изучении места контакта серозно-мышечной оболочки дна желудка с основанием мышечного «жома» пищевода выявляется узкая полоска зрелой соединительной ткани, покрытой снаружи слоем мезотелия.
В соединительной ткани собственной пластинки множество лимфоцитов, желудочные ямки более глубокие, в эпителии желудка единичные лейкоциты, гиперплазия однослойного цилиндрического эпителия.
Три месяца. При гистологическом исследовании в области «клапана» хорошо выявляются слизистые и подслизистые слои пищевода и дна желудка. В слизистой пищевода дифференцируется многослойный плоский эпителий, собственная пластинка, мышечная пластинка слизистой. Сосуды подслизистого слоя не расширены, отека нет, хорошо выделяются собственные железы подслизистой основы. Со стороны слизистой оболочки желудка четко выявляется покровный эпителий, желудочные ямки, но слабо выявляются секреторные клетки фундальных желез. В области «жома» хорошо определяются циркулярные и продольные слои пищевода. Отчетливо выявляются элементы не исчерченной мускулатуры, их цитоплазма равномерно окрашивается красителем, отмечается некоторое истончение мышечных слоев «жома». Артериальные и венозные сосуды по своему строению не отличаются от контроля. Эпителий слизистой оболочки пищевода и желудка сохранен, как сохранены и собственная пластинка, мышечный слой слизистой и подслизистая основа.
Шесть месяцев. Морфологическая картина напоминает картину в срок 3 месяца. «Жом и клапан» соустья полностью сохраняют свою структуру В воспалительных инфильтратах, локализующихся в основном в дистальном отделе «клапана», преобладают лимфо-гистиоцитарные клеточные элементы, плазматические клетки. Изучение динамики гистологической картины инвагинационного «клапана» в сроки до 6 месяцев свидетельствуют об отсутствии выраженных дистрофических и дегенеративных изменений в структуре «клапана», постепенной нормализации морфологии слизистой, с явной тенденцией к полному восстановлению характерных для нее структурных элементов.
Один год. При морфологическом исследовании в участке искусственного «жома» выявляются четко два выраженных пласта мышечной ткани, в которых гладкие миоциты идут в различных направлениях и соответственно принадлежат циркулярному и продольному слоям. Неисчерченные мышечные клетки на всех уровнях «жома» имеют обычный вид, равномерно окрашиваются красителями. Собственная пластинка слизистой представлена рыхлой волокнистой неоформленной соединительной тканью, сосочки которой врезаются в соединительную ткань. В соединительной ткани собственной пластинки множество лимфоцитов, желудочные ямки более глубокие, в эпителии желудка единичные лейкоциты, гиперплазия однослойного цилиндрического эпителия. Кровеносные сосуды не расширены, периваскулярного отека нет. В подслизистых слоях пищевода и дна желудка в области «клапана» хорошо выявляются кровеносные сосуды, которые имеют обычный диаметр просвета, лишь определяется небольшой периваскулярный отек. Между подслизистыми слоями видна узкая полоска зрелой соединительной ткани. Желудочная слизистая «клапана» сохранена, отмечается невыраженный отек и увеличение просвета. Стенка пищевода проксимальной вершины «клапана» на 3-4 см по своему строению близка от обычного строения.
Для объективной оценки арефлюксных свойств пищеводно-желудочного соустья в сроки от 1 месяца до года после операции проводилось эндоскопическое исследование, проба с пневмопрессией. Извлеченные в контрольные сроки макропрепараты исследовались с проведением пневмопрессии. Эндоскопическое исследование проводилось фиброгастроскопом фирмы «Olympus» с диаметром аппарата 9-11 мм.
Исследованию было подвергнуто 5 животных:
через 1 месяц – 1 собака, через 3 месяца – 1 собака, через 6 месяцев – 1 собака, и через 1 год – 2 собаки.
Данных за стеноз, рефлюкс-эзофагит не было выявлено ни в одном случае. У всех животных пищевод был свободен от слизи и желудочного содержимого. Слизистая оболочка пищевода была бледно-розового цвета, складки продольные, не расширены. Пищеводно-желудочное соустье во всех случаях было сомкнуто, при введении воздуха оно раскрывалось до 11-14 мм, приобретая округлую или овальную форму.
Тубус эндоскопа диаметром 11мм свободно проходил через пищеводно-желудочное соустье во всех случаях.
В желудке определялась слизь, в 2 случаях остатки пищи; желчи в желудке не определялось. При ретроградном осмотре «клапан» выглядел в виде выбухающей в просвет желудка эластичной манжеты с округлыми стенками, облегающей тубус эндоскопа, высота его -10-11 мм. При удалении эндоскопа из желудка створки «клапана» смыкались.
С целью объективной оценки арефлюксной функции пищеводно-желудочного соустья использован метод ретроградной пневмопрессии извлеченного желудочно-пищеводного комплекса.
Для этого в желудок через двенадцатиперстную кишку вводили резиновую трубку, вокруг которой на уровне пилорического отдела плотно завязывалась лигатура. К другому концу трубки присоединялся пружинный манометр аппарата Рива-Роччи для регистрации создаваемого внутрижелудочного давления.
При раздувании препаратов желудка животных они приобретали яйцевидную форму. Продолжающееся нагнетание воздуха сопровождалось периодическим сбросом в пищевод, регистрируемое при этом внутрижелудочное давление составляло 15-24 мм. рт. ст.
Проведенные исследования позволяют сказать, что благодаря формируемому «жому и клапану», пищеводно-желудочное соустье обладает значительными арефлюксными свойствами.
Для определения функционального состояния сформированного пищеводно-желудочного соустья пяти собакам в послеоперационном периоде были выполнены рентгенологические исследования. Исследования выполняли с помощью аппарата RUM-20 на рентгеновской пленке РМ-2, формата 24х32 см. Для проведения исследования животное вводили в наркоз инъекцией кетамина в дозе 5мг/кг. Через желудочный зонд в желудок вводили водную взвесь сернокислого бария. После удаления зонда оценивалось состояние тонуса пищевода, желудка, перистальтика, ритм эвакуации, время пассажа по кишечному тракту. Особое внимание обращалось на состояние пищеводно-желудочного соустья, периодичность и ритмичность его раскрытия, форму и размеры «клапана». В оптимальных проекциях выполняли обзорные и прицельные рентгенограммы желудка, зоны соустья.
После этого собака переводилась в положение Тренделенбурга для исследования замыкательной функции пищеводно-желудочного соустья. Наличие рефлюкса изучалось по регистрации заброса бариевой взвеси из желудка в пищевод выше сформированного «клапана и жома» .
ВЫВОДЫ
1. У экспериментальных животных методом расслоения стенки нижней трети пищевода разработана методика формирования искусственного «жома» из мышечной и адвентициальной оболочки и «клапана» из слизисто-подслизистой основы пищевода.
2. Формируемый в области соустья слизисто-подслизистый «клапан» не подвергается деструктивным изменениям и атрофии, на протяжении всего срока наблюдения сохраняет свою форму и тканевую структуру.
3. Макро- и микроскопические методы изучения различных участков искусственно сформированного «жома» из мышечной оболочки пищевода свидетельствуют об отсутствии в его структурах рубцовых и деструктивных изменений.
4. Искусственно созданные слизисто-подслизистый «клапан» и мышечный «жом» в области пищеводно-желудочного соустья надежно препятствуют рефлюксу содержимого из нижлежащих отделов в пищевод.
Практические рекомендации :
1. .Отдаленные результаты макроскопических и морфологических исследований искусственного « жома и клапана » дают основание рекомендовать предложенную методику в качестве альтернативного метода формирования арефлюксного пищеводно-желудочного соустья.
2.При формировании пищеводно-желудочного соустья необходимо четко придерживаться прецизионной техники.
3.Надежность пищеводно-желудочного соустья, обеспечивающая минимальный риск операции, значительные арефлюксные свойства позволяют расширить показания к радикальному хирургическому лечению лиц с сопутствующей патологией.
Список опубликованных работ по теме диссертации:
- Беюнок А.Е. Способ формирования арефлюксного пищеводно-желудочного соустья при рефлюкс-эзофагитах /А.Е.Беюнок, Г.Ц.Дамбаев// Журнал « Медицина в Кузбассе». Кемерово,2004-№2. С45-46
2. Беюнок А.Е. Морфологическое обоснование эффективности формирования арефлюксного пищеводно-желудочного соустья при рефлюкс-эзофагитах / А.Е. Беюнок // Юбилейный сборник научных трудов, посвященный 100-летию со дня рождения Г.Е.Островерхова.-Москва, 2004. С. 61.
- Беюнок А.Е. Особенности при формировании арефлюксного пищеводно-желудочного соустья при рефлюкс-эзофагитах / А.Е.Беюнок, Г.Ц.Дамбаев // Вопросы реконструктивной и пластической хирургии НИИ Микрохирургии ТНЦ СО РАМН.-Томск, 2005-№2.-С21-22.
- Беюнок А.Е. Способ формирования пищеводно-желудочного анастомоза / А.Е.Беюнок, Г.Ц.Дамбаев // Официальный бюллетень федеральной службы по интеллектуальной собственности, патентам и товарным знакам РФ- Москва,2004-№25.-С.354-355.
Патент:
1. Способ формирования пищеводно-желудочного анастомоза: Пат. 2235510, Россия: МКИ 7А61 В 17/00 / А.Е.Беюнок, Г.Ц.Дамбаев.Приоритет от 22.04.2002. Опубл.10.09.2004. Бюл.№25
Список сокращений
ПЖС - пищеводно-желудочное соустье
Р-Ф - рефлюкс-эзофагит
ГПОД - Грыжа пищеводного отверстия диафрагмы
пжк – пищеводно-желудочный комплекс
