Петрищева Светлана Николаевна учитель математики моу «сош №4» г. Называевска Омской области Тема урок
| Вид материала | Урок |
- Урок русского языка ( 2 класс ) Тема: правописание непроверяемых, 195.36kb.
- Организационно-педагогические условия функционирования педагогической технологии исследования, 304.79kb.
- Классен Светлана Викторовна, учитель математики высшей категории моу «Красногвардейская, 226.21kb.
- Урок геометрии и информатики. Тема урока по учебному плану: Построение правильных многоугольников, 131.04kb.
- Гусева Татьяна Валентиновна, учитель истории моу черногубовская оош калининского района, 120.19kb.
- Алтынник Антонина Николаевна учитель изобразительного искусства моу вейделевская сош, 39kb.
- Змановская Надежда Николаевна, Учитель литературы, моу: сош п. Горноправдинск урок, 121.81kb.
- Рогозина Светлана Яковлевна, учитель информатики моу сош №12 мо г-к Анапа, педагогический, 147.99kb.
- Самойлова Надежда Николаевна, учитель русского языка и литературы моу «Черлакская сош», 293.17kb.
- Чинькова Елена Николаевна Учитель математики первой категории моу томинской сош конспект, 22.98kb.
Петрищева С. Н., 218-972-053
Петрищева Светлана Николаевна
учитель математики
МОУ «СОШ №4» г.Называевска
Омской области
Тема урока: Решение химических задач с помощью пропорций. (8 класс)
Форма урока: Интегрированный урок (математика+химия)
Цель: развитие умений применения пропорций для решении химических задач
Задачи урока:
- образовательная: обобщить и систематизировать знания обучающихся по теме «Пропорция» и «Массовая доля вещества в растворе»;
- развивающая: развивать вычислительные навыки, умения применять знания на практике;
- воспитательная: воспитывать интерес к предмету и чувство взаимопомощи.
Сопровождение к уроку – компьютерная презентация (Приложение 1)
Ход урока:
- Организационный момент.
- Историческая справка
Пропорции в Древней Греции.
Слово «пропорция» латинского происхождения «proportio», означающее вообще соразмерность, определённое соотношение частей между собой. В древности учение о пропорциях было в большом почёте у пифогорейцев. С пропорциями они связывали мысли о порядке и красоте в природе, о созвучных аккордах в музыке и гармонии во вселенной. Некоторые виды пропорций они поэтому и называли «музыкальными», «гармоничными».
В ІV веке до н.э. общая теория пропорций для любых величин (соизмеримых и несоизмеримых) была создана трудами древнегреческих учёных, среди которых выдающееся место занимали Теэтет и Евдокс. Эта теория подробно изложена в книгах «Начала» Евклида. Пропорциями пользовались для решения разных задач и в древности, и в средние века, и сейчас.
Пропорции применяются не только в математике, но и в архитектуре, искусстве.
Заслуженное место заняла теория пропорций при решении задач по химии.
- Повторение материала.
а) Учитель математики:
- Что называют пропорцией?
2. Прочитайте равенства, записанные на доске:
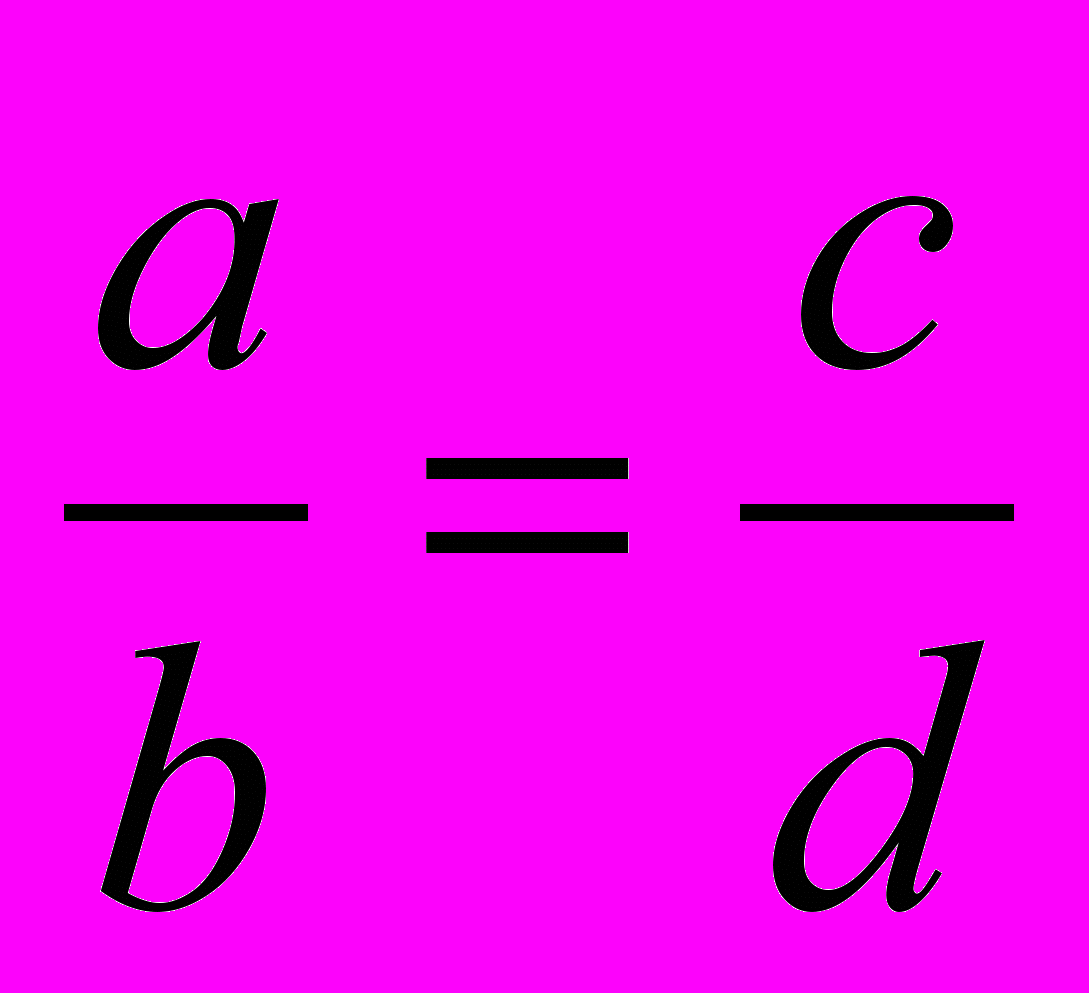 ;
;  ; 0,2:0,3=40:60;
; 0,2:0,3=40:60;3. Назовите крайние и средние члены пропорции;
4. Сформулируйте основное свойство пропорции;
5. Найдите неизвестные члены пропорций:
 ;
; 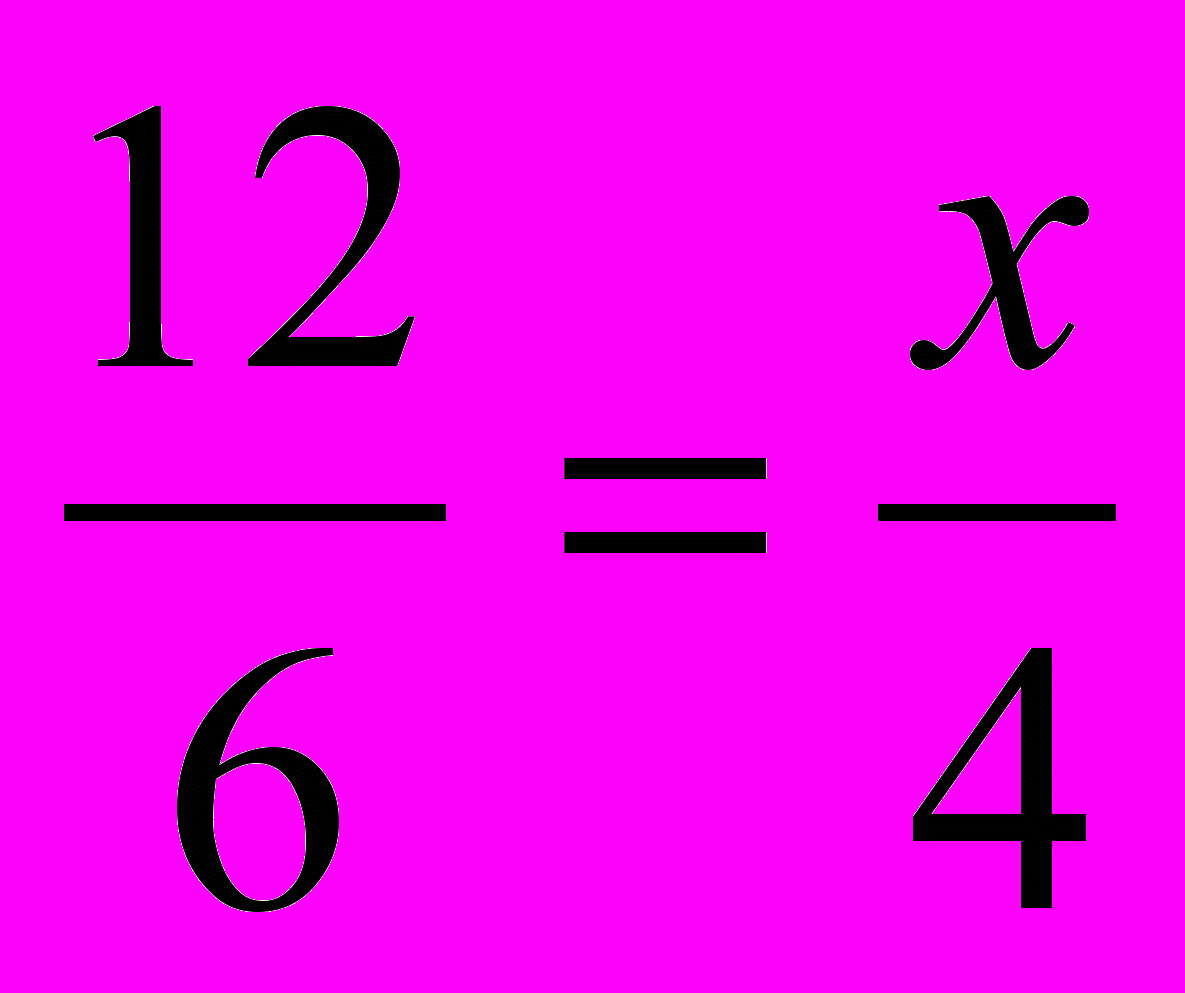 ; 3:y=2:5.
; 3:y=2:5.б) Учитель химии:
- Что называют растворами?
- Какие бывают растворы?
- Что такое процентная концентрация?
- Что показывает процентная концентрация?
- Из чего состоит любой раствор?
Запишем обозначение: mв- масса вещества;
mH2O- масса воды;
mp=mв+mH2O – масса раствора;
mp=100%
ω% - процентное содержание вещества в
растворах.
- Применение знаний для решения задач.
Задача 1. Приготовить 100г раствора соли CuSO4 1% концентрации.
Учитель химии:
- Что такое концентрация?
- Что необходимо знать для приготовления раствора соли?
- Назовите формулу массы раствора?
Учитель математики:
- Вычислим массу вещества и массу воды с помощью пропорции. Для этого запишем краткое условие задачи:
mp=100г – 100%
mв= ? - 1%
mH2O= ?
- Составим пропорцию:
 ;
;- Выразим неизвестную величину:
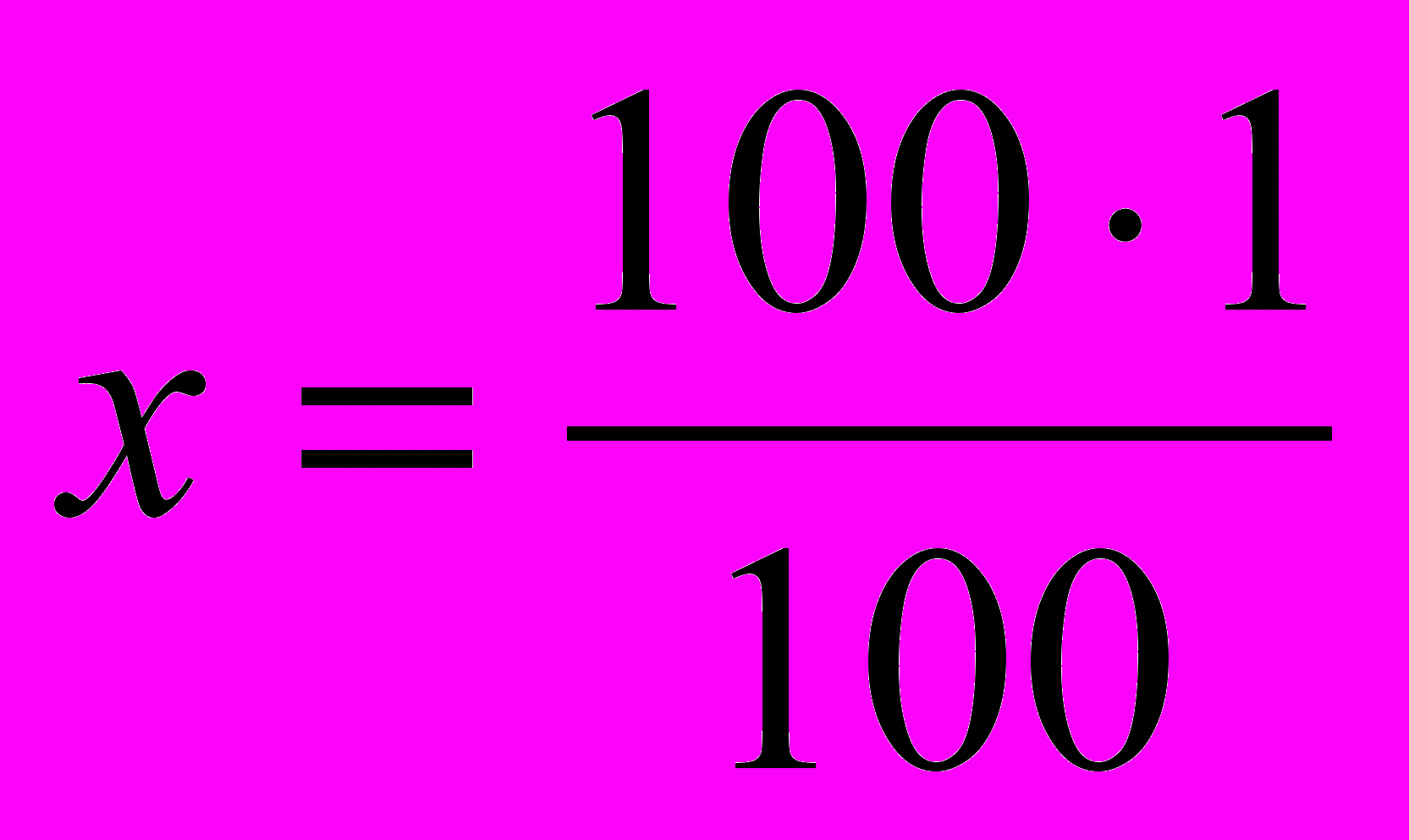
Вывод: получили 1г соли, т.е. mв=1г.
mp= mв+ mH2O
mH2O=mр- mв
mH2O=100-1=99 (г)
Ответ: mв=1г, mH2O=99г.
По данным задачи учитель химии демонстрирует опыт по получению раствора соли CuSO4 1% концентрации. Для этого взвешивает 1г соли CuSO4 и 99г воды, соединяет, получает раствор массой 100г.
Задача 2. Приготовить 150г раствора с массовой долей хлорида натрия 5%?
Учитель химии:
- Что такое массовая доля?
- Чему она равна по условию задачи?
- Что необходимо знать для приготовления раствора?
Учитель математики:
- Вычислим массу вещества и массу воды аналогично решению первой задачи.
- Известно, что масса раствора составляет 150г, что принимаем за 100%. Составим таблицу по условию задачи.
| Условие задачи: | Составление пропорции: | Решение пропорции: | Ответ задачи: |
| mр=150г – 100% mв= xг – 5% |  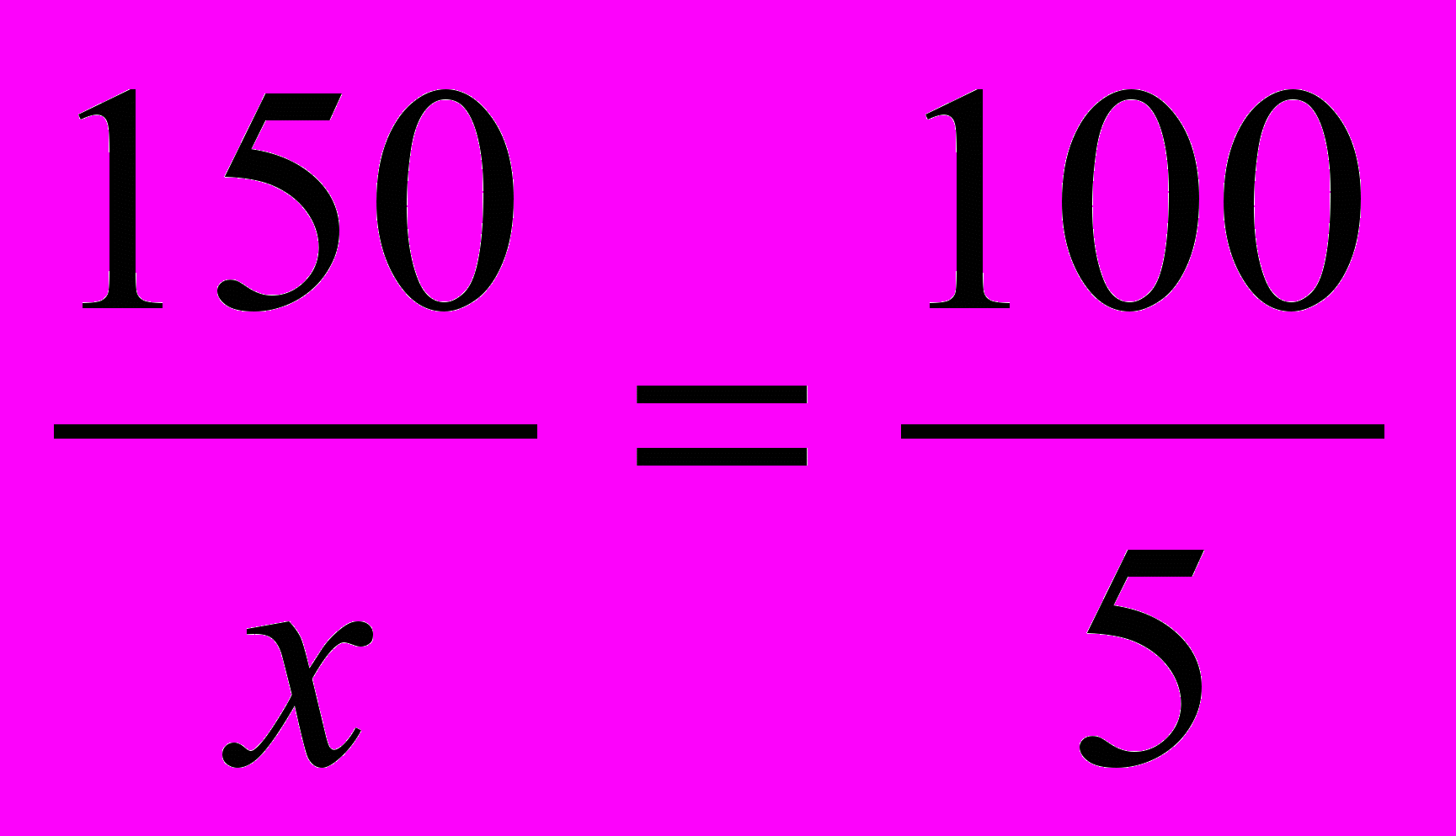 |  (г) (г) | mв=7,5 г mH2O=142,5 г |
| | mH2O= mр - mв | mH2O=150 – 7,5 =142,5(г) | |
Учитель химии: демонстрация опыта по получению данного раствора.
Вывод: При решении задач использовались пропорции, связывающие величины mв, mр, ω%.

- Выразите из этой пропорции mв.

Задача 3. Какова процентная концентрация раствора, полученного растворением 5г поваренной соли в 45 г воды?
Ученик у доски оформляет решение задачи.
mв=5г – х%
mH2O=45 г
mp= ? – 100%
- mp= mв+ mH2O
mp= 5 + 45= 50 (г)
50 г – 100 %
5 г - x %
2)
 ;
;  %
%Ответ: 10% концентрация раствора поваренной соли.
5. Самостоятельная работа (проводится в парах или группах)
Задача 4. Рассчитайте массу вещества и воды для приготовления раствора (120г) с массовой долей соли 8%.
(решения внести в таблицы)
| Условие задачи: | Составление пропорции: | Решение пропорции: | Ответ задачи: |
| mp=100г – 100% mв= ? - 8 % mH2O= ? | | | mв=9,6г |
| mp= mв+ mH2O | mH2O= | mH2O= | mH2O=110,4г |
Задача 5. Сколько грамм соли получает организм при внутривенном вливании 100г физиологического раствора? ( физиологический раствор – это 0,85% раствор поваренной соли)
| Условие задачи: | Составление пропорции: | Решение пропорции: | Ответ задачи: |
| mp= 100г – 100% mв= ? - 0,85 % mH2O= ? | | | mв= 0,85г |
| mp= | | | |
Ответ: 0,85г соли.
Задача 6. Содержание солей в морской воде достигает 3,5%. Сколько граммов соли останется после выпаривания 10кг морской воды?
| Условие задачи: | Составление пропорции: | Решение пропорции: | Ответ задачи: |
| mp= mв= | | | |
| | | | |
Ответ: 0,35кг соли = 350г в 10кг воды.
6. Контроль решения задач.
Учитель математики:
- Проверим правильность решения задач.
7. Подведение итогов.
Учитель математики:
- Назовите пропорцию, связывающую величины mp, mв, ω%.
(
 )
)- Выразите из этой формулы величины: mp, mв, ω%.
8.Домашнее задание.
Составить таблицу изученных формул.
