Теоретические и экспериментальные аспекты создания лекарственных средств на основе сырья природного происхождения 15. 00. 01 технология лекарств и организация фармацевтического дела
| Вид материала | Автореферат диссертации |
- Методические подходы к разработке учебных средств на основе информационных технологий, 380.75kb.
- Методология аналитических исследований фармацевтического рынка 15. 00. 01 технология, 668.16kb.
- Институциональные и методические основы лекарственного обеспечения больных социально, 1173.2kb.
- Краткая программа курса фармакогнозии для студентов медицинского факультета рудн, обучающихся, 91.24kb.
- Исследование организационно-правовых особенностей и разработка путей оптимизации обеспечения, 305.97kb.
- Курсовая работа по технологии лекарств тема: «Законодательные основы нормирования производства, 628.18kb.
- 11 экзаменационные вопросы по фармацевтической технологии для студентов очно/заочного, 244.55kb.
- Теоретические и экспериментальные исследования закономерностей формирования сырных, 733.87kb.
- Разработка трансдермальных лекарственных форм флаволигнанов 14. 04. 01 «Технология, 297.22kb.
- Производство и применение биологических средств защиты растений на основе энтомофагов,, 37.05kb.
Результаты исследований используются в учебном процессе:
- на кафедре фармацевтической технологии ГОУ ВПО «ПГФА Федерального агентства по здравоохранению и социальному развитию» при изучении теоретического и практического материала на 3 курсе очного факультета, на занятиях интернов, слушателей факультета дополнительного профессионального образования (Акт от 06.10.08).
Апробация работы. Основные положения диссертации представлены на: Межвузовской научно-практической конференции, посвященной 85-летию высшего образования на Урале (Пермь, 2001); Третьей международной научно-практической конференции «Здоровье и образование в XXI веке» (Москва, 2002); IX Российском национальном конгрессе «Человек и лекарство» (Москва, 2002); VI Международном съезде «Актуальные проблемы создания препаратов природного происхождения» (С.- Петербург, 2002); Областной научной конференции молодых ученых, аспирантов и студентов «Молодежная наука Прикамья – 2002» (Пермь, 2002); IV Международном конгрессе молодых ученых «Науки о человеке» (Томск, 2003); Межвузовской научно-практической конференции профессорско-преподавательского состава «Актуальные проблемы фармацевтической науки и образования: итоги и перспективы» (Пермь, 2003); Российской научно-практической конференции «Рациональное использование лекарств» (Пермь, 2004); XI Российском национальном конгрессе «Человек и лекарство» (Москва, 2004); XII Российском национальном конгрессе «Человек и лекарство» (Москва, 2005); XIII Российском национальном конгрессе «Человек и лекарство» (Москва, 2006); Научно-практической конференции «Разработка, исследование и маркетинг новой фармацевтической продукции» (Пятигорск, 2007); на ежегодных конференциях профессорско-преподавательского состава ПГФА (Пермь, 2001-2007 гг.), на научно-практической конференции «Актуальные вопросы образования, науки и производства в фармации» (Ташкент, 2008).
Публикации. По материалам диссертационной работы опубликовано 53 печатных работы, из них 3 патента РФ на изобретение, 1 рационализаторское предложение, 1 ФСП, 8 статей в изданиях, рекомендованных ВАК РФ, 6 статей в материалах съездов и конференций, 34 тезисов.
Связь задач исследования с проблемным планом фармацевтических наук. Диссертационная работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Пермская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию» в соответствии с планом научно-исследовательских работ (№ государственной регистрации 01.9.50 007426).
На защиту выносятся:
- методологические подходы и основные принципы создания научно-обоснованных составов, технологии и анализа лекарственных форм на основе сырья природного происхождения;
- результаты теоретических и экспериментальных исследований по обоснованию состава и изучению сбора «Нормофит», по разработке технологии и показателей качества ФЭС, НЭС, научно-обоснованных составов, технологии и показателей качества ПЛ на основе ФЭС, НЭС, препарата медицинской пиявки и гранул ФЭС;
- результаты фармакологического изучения разработанных субстанций и лекарственных форм.
Объем и структура диссертации.
Диссертационная работа изложена на страницах машинописного текста, иллюстрирована ___ рисунками, ___ таблицами и состоит из введения, обзора литературы, шести глав, посвященных экспериментальным исследованиям, выводов, списка литературы и приложения. Библиографический указатель включает ___ источников, в том числе ___ на иностранных языках.
В Приложение включена нормативная документация – ФСП, проекты ФСП, лабораторные и опытно-промышленный регламенты, проекты ОФС, Методические указания, акты внедрения и апробации.
Основное содержание работы
Обзор литературы (глава I) содержит теоретическое обоснование технологии получения и разработки показателей качества экстракционных препаратов. Показана целесообразность использования изучаемых видов сырья для создания лекарственных препаратов. Особое внимание уделено перспективности лекарственной формы – пленки лекарственные.
Во второй главе охарактеризованы объекты исследования и приведены методики, использованные при выполнении работы. При постановке и проведении экспериментов применяли методы математического планирования эксперимента. Статистическую обработку результатов проводили по общепринятым методикам ГФ ХI изд. При оценке степени достоверности различий средних данных использовали t-критерий Стьюдента.
Методологические подходы к разработке лекарственных средств на основе сырья природного происхождения
Предлагаемая методология базируется на проведении комплекса теоретических, технологических, физико-химических, биофармацевтических и фармакологических исследований, обеспечивающих получение современных, качественных, эффективных и безопасных лекарственных средств (рис.1). Она включает три этапа, каждый из которых завершается получением промежуточного продукта, обеспечивающего постановку задач для каждого последующего этапа.
Первый этап включает проведение поиска литературных данных с целью выявление сырья растительного и животного происхождения, воздействующего на основные симптомы воспалительных заболеваний пародонта. Известно, что при возникновении воспаления расширяются ссылка скрыта, вследствие чего увеличивается кровоснабжение, происходит замедление кровотока и как следствие, покраснение, местное повышение температуры, затем увеличение проницаемости стенки ссылка скрыта ведёт к выходу ссылка скрыта, ссылка скрыта из жидкой части ссылка скрыта (ссылка скрыта) в место повреждения - отёк, который, в свою очередь, сдавливая ссылка скрыта окончания, вызывает боль. В повреждённой ткани усиливаются процессы образования ссылка скрыта.
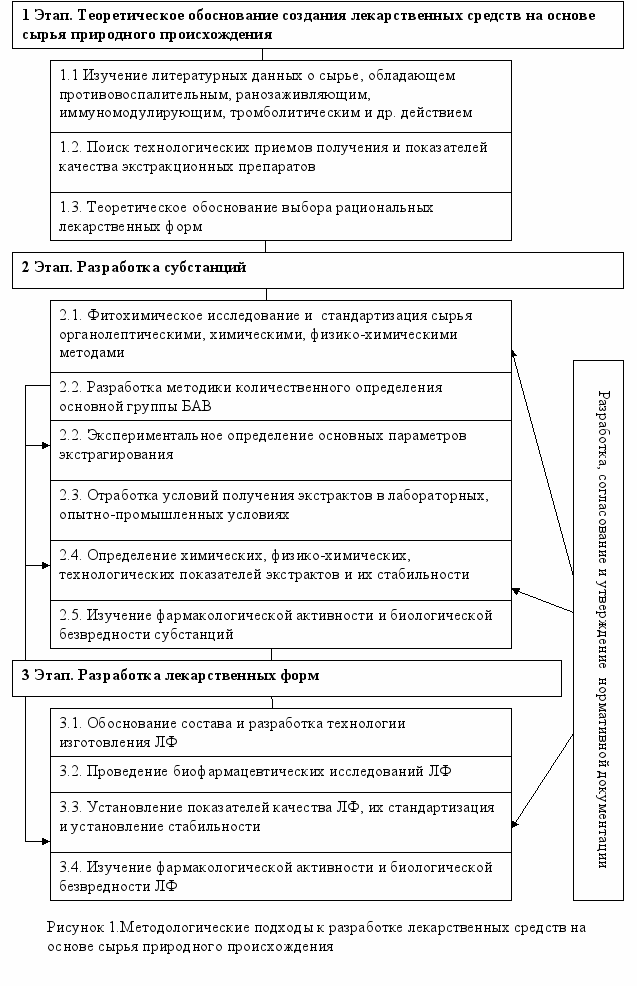
Обычно для устранения воспаления требуется применение нескольких препаратов, воздействующих на различные звенья патологического процесса. Использование растительного сырья обеспечивает широкий спектр фармакологического действия. Следующим слагаемым первого этапа исследования является поиск рациональных приемов экстрагирования ЛРС, позволяющих извлечь необходимое количество и спектр БАВ, изучение показателей стандартизации экстрактов.
Заключительной стадией первого этапа является выбор перспективных лекарственных форм. Применение в терапевтической практике лекарственных средств для профилактики и местного лечения инфекционно-воспалительных поражений слизистых оболочек в виде растворов, мазевых аппликаций характеризуются неточностью дозирования, слабыми адгезивными свойствами, незначительной глубиной проникновения лекарственного вещества в ткани, кратковременной терапевтической эффективностью, быстрым снижением концентрации препарата из-за разбавления слюной, необходимостью многократного введения вещества, большими затратами времени врача и пациента для лечения, а также необходимостью использования дополнительных средств для удержания тампонов. Создание ПЛ на основе субстанций природного происхождения обеспечивает максимальную биологическую доступность БАВ, точное и непрерывное дозирование в течение длительного промежутка времени, устранение биодеструкции ферментами ЖКТ. Гранулирование сухих экстрактов позволяет улучшить их технологические свойства и расширить область практического применения.
Разработка состава сбора и технологии получения сухих экстрактов
Главными составляющими при подборе лекарственного растительного сырья для формирования сбора, являлись следующие: данные о составе биологически активных веществ растений, опыте их использования в традиционной и официальной медицине для лечения воспалительных заболеваний.
В состав разрабатываемых композиций вводили и дублирующие по действию растительные компоненты, исходя из того, что усложнение комплекса биологически активных веществ, приводит к потенцированию фармакологических эффектов за счет того, что компоненты одноименного действия имеют различные точки воздействия и повышают надежность ожидаемого лечебного эффекта. При этом обеспечивается поливалентность действия и снижается возможность побочных эффектов.
При составлении сборов для лечения воспалительных заболеваний учитывали необходимость введения растений, обладающих противовоспалительным, антимикробным, регенеративным, кровоостанавливающим, обезболивающим, иммуномодулирующим и противоотечным действием, что позволило отобрать 13 видов лекарственного растительного сырья. Немаловажным при проведении поиска являлось изучение противопоказаний и предостережений при применении лекарственных растений, что позволило сократить количество лекарственных растений до 6 наименований.
Наличие растительных компонентов, содержащих различные группы БАВ, позволяет достичь потенцирования эффектов и поливалентного фармакологического действия. Все выбранные растения обладают противовоспалительной, антимикробной и регенеративной активностью. Поскольку в патогенезе воспалительных заболеваний наблюдается расширение капилляров и кровоточивость, в сбор введена трава очанки, обладающая также кровоостанавливающим и антиоксидантным действием, присутствие травы манжетки предполагает усиление обезболивающего действия сбора.
Процентное соотношение компонентов в сборе обосновывали теоретически с учетом вклада каждого компонента в оказание конечного лечебного эффекта и экспериментально (табл. 1).
Таблица 1
Составы сборов полифункционального действия
| Наименование сырья | Состав, % | |||
| №1 | №2 | №3 | №4 | |
| Трава фиалки | 20 | 25 | 25 | 25 |
| Листья земляники | 20 | 25 | 20 | 20 |
| Цветки ромашки | 20 | 20 | 20 | 15 |
| Цветки ноготков | 20 | 20 | 20 | 20 |
| Трава манжетки | 10 | 5 | 10 | 10 |
| Трава очанки | 10 | 5 | 5 | 10 |
Таким образом, по результатам исследований нами разработана оптимальная пропись сбора (№1), названного «Нормофит».
Разработанный сбор включает несколько растительных компонентов, что делает целесообразным постановку вопроса его стандартизации по комплексу доминирующих биологически активных соединений. С поликомпонентностью состава связаны трудности выбора группы БАВ, позволяющей репрезентативно стандартизировать сбор. Решение этой проблемы невозможно без детального изучения химического состава сбора и выбора приоритетных и специфических маркеров, по которым бы планировалось в дальнейшем проведение стандартизации.
Качественными реакциями и методами хроматографического анализа на бумаге и в тонком слое сорбента выделены и идентифицированы в сборе «Нормофит» индивидуальные фенольные соединения, такие как флавоноиды (рутин и кверцетин).

| 1,0 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 |
Рисунок 2. Схема тонкослойной хроматографии извлечения из сбора в системе БУВ (4:1:5).
При проведении одномерной бумажной хроматографии и ТСХ лучшее разделение флавоноидных соединений происходит в системе н-бутанол-уксусная кислота-вода (4:1:5), а при использовании двумерной бумажной хроматографии - в системе БУВ и 15%-ной уксусной кислоты. На рисунке 2 показано наличие не менее 18 веществ фенольной природы. По расположению пятен и их окраске до и после проявления парами аммиака можно сделать вывод, что в сборе присутствуют, как агликоны, так и гликозиды флавоноидов.
В результате определения спектральной характеристики извлечения из сбора установлено, что максимум находится в области от 405 до 415 нм (рис. 3).
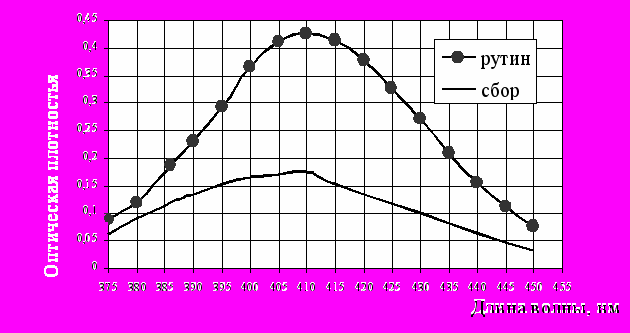
Рисунок 3. Спектральная характеристика ГСО рутина и извлечения из сбора.
Спектр поглощения сбора имеет максимум близкий к спектру рутина, поэтому он выбран в качестве доминирующего в сумме, на который в дальнейшем вели пересчет. В основу разрабатываемой методики количественного определения легла спектрофотометрия с комплексообразующей добавкой, аналитические параметры которой позволяют использовать ее для определения содержания флавоноидов в растительных объектах, содержащих неидентичный набор флавоноидов, а, следовательно, приемлемый и для сбора. В качестве аналитической принята длина волна 410 нм, а экстрагента – 70% спирт этиловый.
Далее подобраны оптимальные условия проведения количественного определения флавоноидов в сборе (табл. 2).
Таблица 2
Оптимальные условия количественного определения флавоноидов в сборе
| Экстрагент (спирт этиловый) | 70% |
| Измельченность сырья | 2-3 мм |
| Соотношение сырье – экстрагент | 1:100 |
| Время и кратность экстракции | Трехкратная экстракция по 30 мин |
| Длина волны | 410 нм |
| Концентрация комплексообразователя | 2% спиртовый раствор AlCl3 |
| Количество добавляемого комплексообразователя | 2 мл |
| Время комплексообразования | 40 мин и комплекс стабилен в течение 1 часа |
Метрологическая характеристика содержания суммы флавоноидов в сборе, в пересчете на рутин, представлена в таблице 3.
Таблица 3
Метрологическая характеристика методики количественного
определения суммы флавоноидов в сборе «Нормофит»
| Хср | S2 | Sx | E | E |
| 2,44 | 0,005 | 0,03 | 0,09 | 3,69% |
Относительная ошибка единичного определения с доверительной вероятностью 0,95 составляет 5,23%. Опыты с добавками ГСО рутина показали отсутствие систематической ошибки предлагаемой методики. Результаты проведенных исследований подтверждают ее воспроизводимость.
С помощью этой методики проанализировано пять серий сбора. Исходя из полученных данных, для включения в проект ФСП рекомендуется содержание суммы флавоноидов в сборе в пересчете на рутин не менее 2%.
В процессе фитохимических исследований сбора с использованием качественных реакций обнаружены другие группы БАВ: фенолкарбоновые кислоты, дубильные вещества, аскорбиновая кислота, свободные органические кислоты, полисахариды и определено их количественное содержание с помощью методов гравиметрии, титриметрии и спектрофотометрии. Содержание полисахаридов находится в пределах от 7,10 до 7,92%, дубильных веществ – 11,40 – 11,86%, аскорбиновой кислоты – 0,21-0,43, свободных органических кислот – 2,3-2,8, фенолкарбоновых кислот – 0,24-0,29.
Установлен качественный и количественный аминокислотный состав сбора «Нормофит» на аминокислотном анализаторе ААА-339 (ЧССР) (табл. 4).
Полученные данные позволили установить присутствие 14 аминокислот, из которых восемь незаменимых, среди которых преобладают аминокислоты – пролин, глицин, валин, цистеин и аргинин.
Таблица 4
Содержание свободных аминокислот в сборе «Нормофит»
| Наименование аминокислот | Содержание аминокислот, % |
| Лизин* | 0,111±0,004 |
| Метионин* | 0,154±0,006 |
| Цистеин | 0,58±0,01 |
| Гистидин* | 0,071±0,001 |
| Аргинин | 0,70±0,02 |
| Треонин* | 0,34±0,01 |
| Серин | 0,54±0,01 |
| Пролин | 1,52±0,08 |
| Глицин | 0,91±0,05 |
| Валин* | 0,72±0,03 |
| Изолейцин* | 0,26±0,01 |
| Лейцин* | 0,021±0,001 |
| Тирозин | 0,20±0,01 |
| Фенилаланин* | 0,42±0,02 |
Примечание: * - незаменимые аминокислоты
Методом атомно-абсорбционной спектрометрии с помощью дифракционного спектрографа ДФС-13-1 проведено определение макро- и микроэлементов в сборе «Нормофит», поскольку они играют важную роль в формировании систем организма, пластических процессах, проявляют фармакологическую активность, влияют на обмен веществ, активизируют ферментные системы, потенцируют действие витаминов С, Р, В2, В12 и др. (табл.5).
Таблица 5
Результаты изучения микроэлементного состава сбора «Нормофит»
| № п/п | Элемент | мг/кг сырья | |
| 1 | Ni | Никель | 7,51 |
| 2 | Co | Кобальт | 0,64 |
| 3 | Cr | Хром | 5,78 |
| 4 | Mn | Марганец | 352 |
| 5 | V | Ванадий | 1,20 |
| 6 | Ti | Титан | 110 |
| 7 | Sc | Скандий | 0,52 |
| 8 | Ge | Германий | 0 |
| 9 | Cu | Медь | 10,15 |
| 10 | Zn | Цинк | 11,2 |
| 11 | Pb | Свинец | 0 |
| 12 | Ag | Серебро | 0,055 |
| 13 | As | Мышьяк | 0 |
| 14 | Sb | Сурьма | 0 |
| 15 | Cd | Кадмий | 0 |
| 16 | Bi | Висмут | 0 |
| 17 | Mo | Молибден | 0,224 |
| 18 | Ba | Барий | 112 |
| 19 | Sr | Стронций | 46,5 |
| 20 | W | Вольфрам | 0 |
| 21 | Sn | Олово | 0 |
| 22 | Be | Бериллий | 0,14 |
| 23 | Zr | Цирконий | 11,5 |
| 24 | Ga | Галлий | 0,74 |
| 25 | Y | Иттрий | 1,10 |
| 26 | Yb | Иттербий | 0,17 |
| 27 | Li | Литий | 0 |
| 28 | Nb | Ниобий | 1,00 |
В тоже время, наличие и относительно высокое содержание некоторых микроэлементов (Zn, Mn, Cu), расширяет диапазон применения сбора для профилактики и лечения воспалительных заболеваний пародонта.
Таким образом, проведено подробное изучение химического состава сбора «Нормофит» и определено количественное содержание различных групп биологически активных веществ.
Результаты проведенных товароведческих, морфолого-анатомических и фитохимических исследований включены в проект ФСП «Сбор «Нормофит» (таблица 6).
Таблица 6
Результаты стандартизации сбора «Нормофит»
| Наименование показателей | Требования проекта ФСП | Фактические данные |
| Внешние признаки | Смесь неоднородных частиц листьев, стеблей, цельных или частично осыпавшихся корзинок со слабым, ароматным запахом. Вкус горьковатый. Цвет желто - зеленый с фиолетовыми и оранжево - коричневыми включениями. | Соответствует |
| Подлинность |
| Соответствует Соответствует Соответствует |
| Содержание суммы флавоноидов (в пересчете на рутин), %, не менее | 2 | 2,44+0,08 |
| Экстрактивных веществ, %, не менее | 25 | 35,86+1,53 |
| Золы общей, %, не более | 12 | 9,76+0,55 |
| Золы нерастворимой в 10% растворе HCl, %, не более | 5 | 4,6+0,30 |
| Частиц, не проходящих сквозь сито с отверстиями 3мм, %, не более | 10 | 1,9+0,08 |
| Потеря в массе при высушивании, %, не более | 10 | 4,37+0,14 |
| Органическая примесь, не более, % | 0,5 | 0,10+0,03 |
| Минеральная примесь, не более, % | 0,5 | 0,05+0,01 |
| Микробиологическая чистота | Категория 4а | Соответствует |
Срок годности сбора составил 2 года при хранении в бумажных пакетах, уложенных в пачки из бумаги или картона, в помещении с относительной влажностью воздуха 60+50С. При этом содержание действующих веществ оставалось на уровне, удовлетворяющем требованиям проекта ФСП.
Разработка технологии получения Фиалки экстракта сухого и
«Нормофит» экстракта сухого
Основными факторами, влияющими на скорость и полноту высвобождения действующих веществ, являются: тип экстрагента, температура, степень измельченности сырья, продолжительность экстрагирования и гидродинамические условия.
Установлено, что оптимальным экстрагентом является вода очищенная, в связи с этим предложено проводить экстракцию горячей водой. Далее нами изучена зависимость выхода БАВ (флавоноидов) при экстракции горячей водой в различных соотношениях к количеству сырья
Анализ экспериментальных данных свидетельствует о том, что оптимальным является соотношение сырья и экстрагента от 1:10 до 1:15. Дальнейшее увеличение объема экстрагента нецелесообразно, т.к. выход извлекаемых веществ не повышается.
Следующим важным фактором, влияющим на процесс экстрагирования флавоноидов, является степень измельчения сырья. Вместо разнотипного по величине частиц и механическим свойствам использовали вальцованное растительное сырье, измельченное до частиц менее 1 мм.
Для интенсификации процесса изучены условия перемешивания и рекомендовано проводить экстракцию при 70-800С и периодическом перемешивании в течение не менее 10 минут. При этом возрастала скорость экстракции, что позволило сократить время настаивания на каждой ступени на 30 минут.
С целью определения продолжительности и кратности экстракции изучено время наступления равновесной концентрации в системе «сырье - экстрагент» при 1, 2 и 3 контактах фаз. Установлено, что равновесное состояние в системе достигается через 1 час при первом контакте и через 30 минут при втором и третьем. Таким образом, трехкратная экстракция обеспечивает полное истощение сырья.
Все установленные факторы экстракции заложены в режим экстрагирования травы фиалки и сбора «Нормофит»: экстрагент − вода очищенная, соотношение сырья и экстрагента − 1:10-1:15, температурный режим − 75˚±5˚, размер частиц – 1-2 мм, трехкратная экстракция (первая - 30 мин, вторая и третья - 15 мин).
При изучении влияния способа сушки на содержание биологически активных веществ, физико-химические и технологические свойства экстрактов, исследованы процессы сушки в вакуум-сушильном шкафу (ВСШ), распылительным (РС) и сублимационным (СС) способами. В результате исследования усыновлено (табл. 7), что оптимальными показателями обладают экстракты, полученные распылительной сушкой. Установлено также, что экстракты, высушенные в вакуум-сушильном шкафу, требуют дополнительного измельчения, а сублимационной сушкой – более гигроскопичны (4,57%).
На базе ФГУП «Межбольничная аптека» УД Президента РФ отработаны опытно-промышленные регламенты и составлены технологические схемы получения Фиалки экстракта сухого и «Нормофит» экстракта сухого.
Для экстракции использована комплектная опытно-промышленная установка, включающая дозатор сырья, экстрактор, фильтрационную установку, вакуум-выпарной аппарат, сепаратор и сушилку.
Таблица 7
Результаты изучения влияния способа сушки на показатели качества ФЭС (1) и «Нормофит» экстракта сухого (2)
| № п/п | Показатели качества | Способ сушки | |||||
| ВСШ | РС | СС | |||||
| 1 | 2 | 1 | 2 | 1 | 2 | ||
| | Сыпучесть, г/сек | 1,42 | 2,40 | 1,46 | 1,80 | 1,84 | 2,73 |
| | Насыпная плотность, кг/м³ | 0,60 | 0,62 | 0,64 | 0,68 | 0,73 | 0,74 |
| | Угол естественного откоса, град | 37,0 | 35,0 | 45,0 | 42,0 | 40,0 | 36,0 |
| | Потеря в массе при высушивании, % | 4,13 | 3,22 | 4,22 | 3,16 | 4,56 | 4,55 |
| | Содержание суммы флавоноидов в пересчете на рутин, % | 4,02 | 4,75 | 4,12 | 4,98 | 3,98 | 4,52 |
Экстрагирование сырья проводили водой очищенной в экстракторе из нержавеющей стали с ложным дном вместимостью 200 л, снабженном якорной мешалкой, паровой рубашкой и гильзой для термометра. На дно экстрактора помещали серошинельное сукно и два слоя бязи, при сливе извлечение одновременно фильтровалось. Очистку объединенных водных извлечений осуществляли фильтрацией и сепарированием. Для упаривания извлечений применяли вакуум-выпарной аппарат Simax (ЧССР), который обладает высокой производительностью и мягкими условиями упарки. Сушку экстракта проводили на распылительной сушилке Niro Atomazer (Дания). Экспериментально при загрузках установлена оптимальная температура воздуха на входе 150-1800С, на выходе 70-800С, производительность сушилки составила 2,0-2,5 л/ч по испаренной влаге. Концентрация исходного извлечения для сушки должна быть не ниже 15%.
На всех стадиях технологического производства проводили контроль технологический (Кт), химический (Кх) и микробиологический (Км) сырья, концентрированного экстракта, осадка после сепарирования, шрота и конечного продукта производства - субстанции (рис. 4).
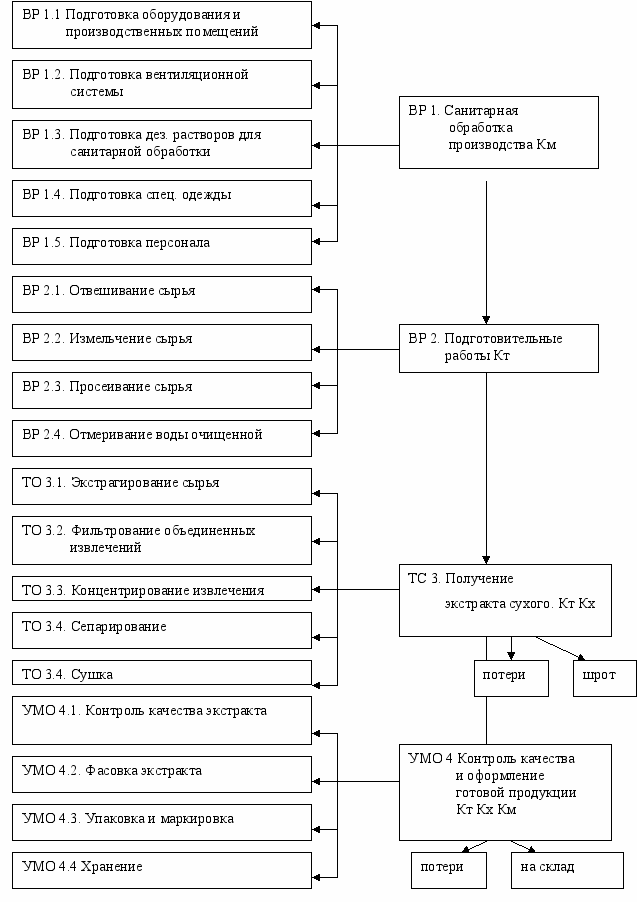 Рисунок. 4. Технологическая схема получения ФЭС
Рисунок. 4. Технологическая схема получения ФЭССтандартизация Фиалки экстракта сухого
Регламентируемые действующей ГФ показатели качества, указывают на необходимость разработки современных, точных, избирательных и воспроизводимых методик анализа. Изучение литературных данных, отечественных и ведущих зарубежных фармакопей позволило сформулировать общие требования, предъявляемые к указанной лекарственной форме, использованные при разработке проекта ОФС «Экстракты сухие»: внешний вид (описание), подлинность, содержание действующих веществ (количественное определение), потеря в массе при высушивании, содержание тяжелых металлов, микробиологическая чистота.
Стандартизацию ФЭС проводили на 5 сериях, полученных в опытно - промышленных условиях (табл. 9). Внешний вид, цвет и запах ФЭС определяли на основании визуальных наблюдений.
Для подтверждения подлинности использовали спектральную характеристику, проведение качественных реакций и хроматографию в тонком слое сорбента.
УФ-спектр. Ультрафиолетовый спектр поглощения раствора Б, приготовленного для количественного определения, в области от 380 до 470 нм имеет максимум при длине волны (405 ± 5) нм (рис.5).
Рис. 5. Спектр поглощения комплекса флавоноидов ФЭС с алюминия хлоридом и ГСО рутина
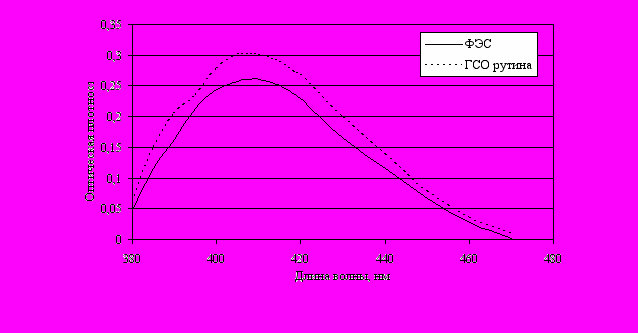
Качественные реакции. К 1 мл раствора, приготовленного для количественного определения, прибавляют 2 мл 2 % раствора алюминия хлорида в спирте этиловом 95%, раствор окрашивается в зеленовато-желтый цвет (флавоноиды).
Хроматография. На стартовую линию пластинки «Sorbfil» (ПТСХ-АФ-А-УФ) наносят 0,04 мл 10 % раствора фиалки экстракта сухого, рядом наносят по 0,005 мл 0,05 % растворов ГСО рутина и ГСО кверцетина (раздел «Количественное определение»). Пластинку помещают в камеру с системой растворителей н-бутанол-уксусная кислота-вода (4:1:5) и хроматографируют восходящим способом (смесь растворителей готовят и заливают в камеру непосредственно перед хроматографированием). Когда фронт растворителя пройдет 13 см, пластинку вынимают из камеры, высушивают в вытяжном шкафу в течение нескольких минут и просматривают в УФ свете при длине волны 254 нм. После обработки 1% раствором алюминия хлорида на хроматограмме должны быть видны 4 основные зоны: две ярко-желтого цвета (одна на уровне ГСО рутина, другая на уровне ГСО кверцетина), имеющие в УФ - свете зеленую флюоресценцию, остальные - с Rs около 0,57, Rs около 0,88, имеющие темную флуоресценцию (рис. 6). Допускается наличие 2-5 дополнительных зон.
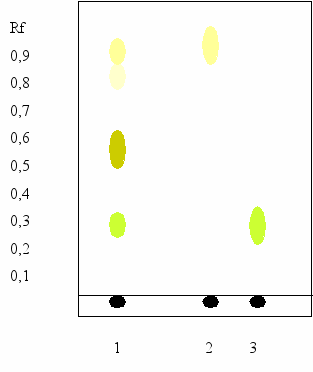
Рисунок 6. Схема хроматограммы ФЭС в системе н-бутанол-уксусная кислота-вода (4:1:5) методом ТСХ.
Количественное определение суммы флавоноидов проводили спектрофотометрическим методом после реакции с 2 % спиртовым раствором алюминия хлорида. Оптическую плотность раствора измеряли при длине волны 410 нм в кювете с толщиной 10 мм. Параллельно измеряли оптическую плотность стандартного образца рутина (ГСО).
Для количественного определения антоцианов разработана унифицированная методика спектрофотометрического определения в пересчете на цианидин-3,5-диглюкозид, которая апробирована на трех образцах сырья и ФЭС (табл. 8).
Таблица 8
Результаты количественного определения антоцианов в траве фиалки и ФЭС
| № п/п | Образец сырья | Содержание антоцианов, % | Еα | Е,% |
| | Трава фиалки | 0,115 | 0,005 | 4,26 |
| | Трава фиалки | 0,135 | 0,004 | 2,67 |
| | Трава фиалки | 0,127 | 0,005 | 4,02 |
| | Фиалки экстракт сухой | 0,122 | 0,004 | 2,38 |
| | Фиалки экстракт сухой | 0,115 | 0,003 | 2,02 |
| | Фиалки экстракт сухой | 0,158 | 0,006 | 4,51 |
Из таблицы следует, что относительная ошибка определения при доверительной вероятности 0,95 не превышает +4,51%.
Таблица 9
