V. свойства органических соединений
| Вид материала | Документы |
- Программа элективного курса по химии «строение и свойства кислородсодержащих органических, 667.3kb.
- Kirgizistan-tüRKİye manas üNİversitesi ders biLGİ formu, 147.19kb.
- Тематический план лекций модуля 1 с органической химии для студентов 2 курса фармацевтического, 25.24kb.
- Календарно-тематический план лекций по биоорганической химии 1 курс (2 семестр) специальность, 65.41kb.
- Лекция Классификация и изомерия органических соединений, 296.86kb.
- Тематический план лекций и самостоятельной работы по органической химии (осенний семестр), 91.46kb.
- 10 класс. Тема урока: «Причины многообразия органических соединений» Тип урока, 145.21kb.
- Дробот Светлана Сергеевна конспект, 69.15kb.
- Дробот Светлана Сергеевна конспект, 57.86kb.
- План лекций по биоорганической химии для студентов 1 курса медицинского факультета, 26.83kb.
5.10. Высокомолекулярные соединения
Высокомолекулярные соединения, или полимеры – продукты реакций полимеризации, представляют собой вещества, состоящие из макромолекул, в которых число соединенных между собой исходных молекул мономера достигает от нескольких тысяч до миллионов. В зависимости от природы мономера, степени полимеризации (число структурных звеньев в макромолекуле), геометрической формы макромолекулы получают полимеры с самыми различными свойствами. К полимерам относятся: полиэтилен, каучук, фенолформальдегидные смолы, органическое стекло, капрон и многие др. материалы. Полимеры природного происхождения называют биополимерами.
Реакция образования макромолекул полимера из молекул мономера (исходного низкомолекулярного вещества) называется полимеризацией. В зависимости от числа исходных веществ различают гомополимеризацию (участвует один вид мономера) и сополимеризацию (два и более различных видов мономера). Эти реакции широко используется для получения высокомолекулярных веществ и материалов (пластмассы, волокна, каучуки, клеи и т.д.).
Реакция полимеризации, протекающая с образованием высокомолекулярного вещества и побочного низкомолекулярного продукта (чаще всего воды) называется поликонденсацией. Примером реакции поликонденсации могут служить образование полипептидов из аминокислот, фенолформальдегидных смол из фенола и формальдегида.
Рассмотрим названия, строение и применение важнейших синтетических полимеров.
Полиакрилаты – полимеры на основе акриловой кислоты или ее производных. Например, полиметилметакрилат – это органическое стекло.
Полиакрилонитрил – [-СН2-СН(СN)-]n, продукт полимеризации акрилонитрила. Применяют для получения синтетических волокон, в том числе нитрона.
Полиамиды – полимеры, содержащие в макромолекулах амидные группы (-СО-NH-). Применяют в производстве синтетических волокон типа капрон, найлон, анид, перлон и др.
Полибутадиен – [-СН2-СН=СН-СН2-]n, синтетическое каучукоподобное вещество, впервые полученное в промышленных масштабах полимеризацией бутадиена-1,3 под руководством академика С.В. Лебедева в 1932 г. Сырье для получения резины.
Поливинилхлорид (полихлорвинил) – [-СН2-С(Cl)Н-]n, термопластичный полимер, при нагревании свыше 120 °С разлагается с выделением хлороводорода. Получают полимеризацией хлорвинила. Является основным компонентом при изготовлении искусственной кожи, клеенок, непромокаемых тканей и т.д.
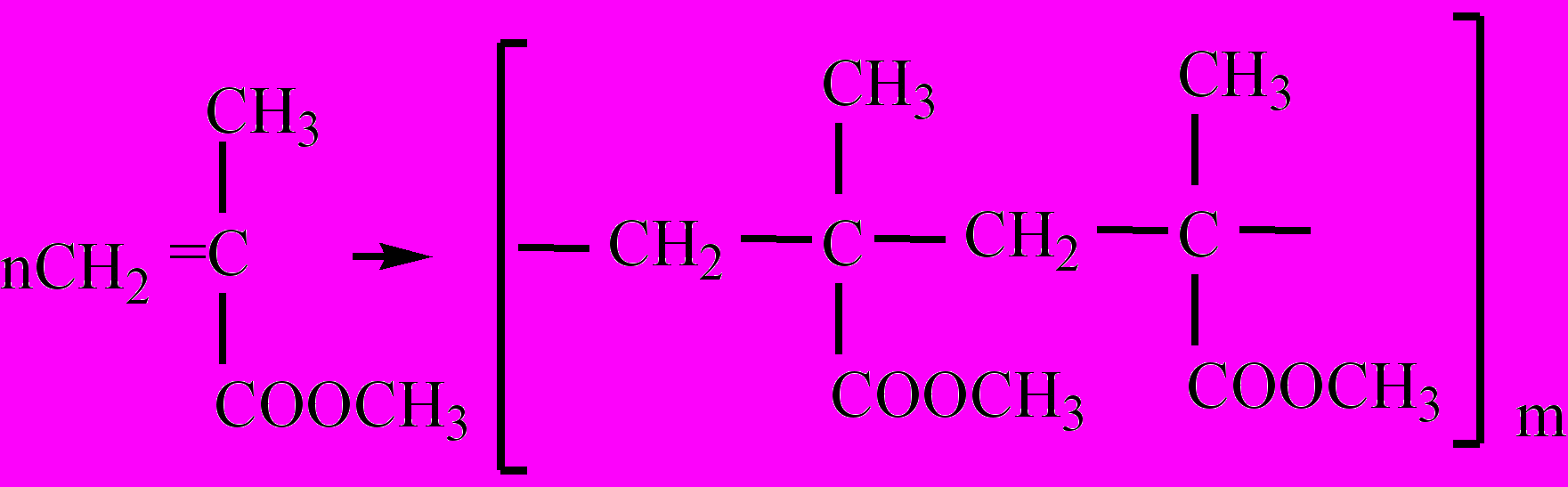
Полиметилметакрилат – полимер, образующийся в результате реакции полимеризации метилового эфира метакриловой кислоты. Полиметилмет-акрилат – твердое, бесцветное прозрачное и светостойкое вещество, вследствие чего получил название "органическое стекло". Применяется для остекления транспортных средств, для производства линз и других изделий.
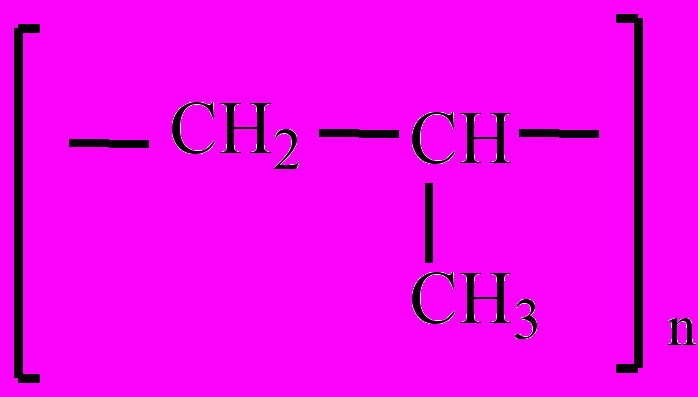
Полипропилен – продукт полимеризации пропилена. Твердый, жирный на ощупь, термопластичный материал, темп. пл. 160-176 оС. Используется для изготовления изоляционных материалов, труб, деталей, химической аппаратуры; выдерживает более высокие температуры (до 140 оС), чем полиэтилен.
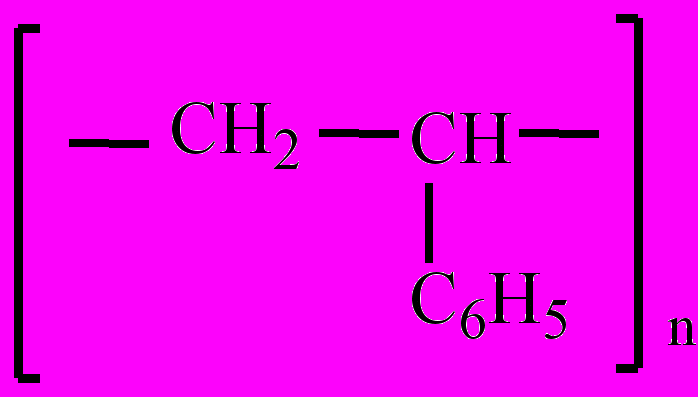
Полистирол – продукт полимеризации стирола. Термопластичный, стойкий по отношению к щелочам и кислотам (кроме азотной кислоты) материал, температура размягчения около 90 оС. Используется для производства корпусов электро- и радиоаппаратуры, посуды, игрушек и других изделий промышленно-бытового назначения. На основе полистирола получают пенопласты.
Политетрафторэтилен (фторопласт, тефлон) – (-CF2-CF2-)n, продукт полимеризации тетрафторэтилена. Отличается от других пластмасс более высокими температурами размягчения и разложения (415 оС), высокой химической стойкостью и прочностью. Находит широкое применение как конструкционный материал в технике, медицине, в быту.
Полиформальдегид (полиоксиметилен) – [-CH2O-]n, синтетический полимер, продукт полимеризации формальдегида; твердое вещество белого цвета. Отличается большой жесткостью, износо- и влагостойкостью, прочностью, малой усадкой при переработке, устойчивостью к щелочам, растворителям. Применяется главным образом вместо цветных металлов и сплавов в производстве конструкционных деталей, а также для изготовления пленки и технического волокна.
Полиэтилен – [-СН2- СН2-]n, продукт полимеризации этилена. В зависимости от условий полимеризации получают полиэтилен высокого давления с молярной массой до нескольких сот тысяч и более прочный полиэтилен низкого давления с молярной массой до 3 млн. Твердый, белого цвета, термопластичный, жирный на ощупь материал. Горит голубоватым пламенем. Химически стоек по отношению к растворам щелочей и кислот (исключение HNO3). Применяется в производстве изоляционных, упаковочных, пленочных, химически стойких материалов, а также предметов бытового назначения.
Полимеры, макромолекулы которых имеют разветвленную или сетчатую структуру, называются полимерами разветвленного строения. По своим свойствам отличаются повышенной прочностью, не термопластичны, плохо растворимые в органических растворителях.
Полимеры, в макромолекулах которых структурные звенья имеют строго определенное повторяющееся по всей цепи строение и расположение в пространстве, называются полимерами стереорегулярного строения. Примером такого полимера может служить изопреновый каучук, в макромолекулах которого все метиленовые группы в структурных звеньях находятся в цис-положении. В макромолекулах дивинилового каучука структурные звенья также находятся в цис-положении, что обусловливает его высокую эластичность. Полимеры стереорегулярного строения обладают чаще всего лучшими потребительскими свойствами и качествами по сравнению с полимерами, не имеющими стереорегулярное строение.
Опыты с синтетическими полимерами. При исследовании свойств полимеров прежде всего рассматриваются их отношение к нагреванию, характер горения, газообразные и твердые продукты горения, отношение к кислотам, щелочам и органическим растворителям.
а) Возьмите полиэтиленовую пробку, или другое ненужное изделие из полиэтилена и осторожно нагрейте его над пламенем до размягчения (не допускайте возгорания) измените форму материала и остудите. Новая форма при этом сохраняется. Сделайте вывод о термопластичности полиэтилена.
б) Сверните небольшой кусочек полиэтиленовой пленки в плотный рулончик и нагрейте более сильно. Полиэтилен плавится, если его поджечь он сгорает голубоватым пламенем (осторожно, расплавленные капли!) без копоти. Задуйте пламя, и осторожно понюхайте белый дымок. Пахнет, как горящая свеча (почему?).
в) Сложите небольшой листок полиэтиленовой пленки пополам, чтобы края двух половинок совпадали. Накройте листы бумагой и проведите по бумаге (по краям пленки) нагретым паяльником или ребром утюга. Пленка прочно «сварится», и вы получите пакет.
г) Образец поливинилхлорида внесите в пламя горелки. В отличие от полиэтилена полимер не плавится, а разлагается. Поднесите к газообразным продуктам разложения влажную фиолетовую лакмусовую бумажку. Лакмус краснеет, так как вследствие разложения полимера выделяется хлороводород.
д) Обломок изделия из полистирола, например от авторучки, слегка нагрейте над пламенем до размягчения. Изогните горячий образец и остудите его. Убедитесь, что полистирол относится к термопластичным пластмассам. Еще раз нагрейте образец до плавления (осторожно – горячие капли!), прикоснитесь карандашом к расплавленному участку и отведите карандаш в сторону. За ним потянется тонкая, застывающая на воздухе нить. Подожгите образец. Он горит коптящим пламенем с характерным запахом стирола, который образуется при разложении полимера.
е) Поместите в одну пробирку кусочек каучука, в другую – кусочек резины, залейте бензином и закройте пробкой. Через 2-3 дня наблюдайте растворение каучука и набухание резины.
ж) Клей для склеивания резины («резиновый» клей) представляет собой раствор каучука в органических растворителях. Налейте в пробирку немного бензина, добавьте каплю иодной настойки и несколько капель клея. Встряхните смесь и убедитесь в непредельности каучука.
з) Налейте клей в виде тонкой длинной нити на дно сухой чистой фарфоровой чашки и несильно нагрейте на песчаной бане до испарения растворителя. После испарения испытайте каучуковую нить на эластичность, разрыв, размягчение при нагревании и растворимость в бензине и воде.
и) Обнаружение серы в резине. Приготовьте резиновую крошку или нарежьте немного резины в виде маленьких кусочков, поместите их в вертикально укрепленную в штативе пробирку, заткните ее отверстие ваткой, смоченной раствором нитрата свинца (II) и нагрейте. Одним из продуктов разложения резины является сероводород, реагирующий с солями свинца с образованием черного сульфида свинца (II).
Получение фенолформальдегидной смолы. В небольшую колбу поместите 15 г фенола и 25 мл концентрированного раствора формалина и нагревайте (под тягой!) на горелке, периодически встряхивая содержимое колбы. Добавьте 1–2 мл соляной кислоты и продолжайте нагревание. Вначале реакция идет бурно и смесь в колбе становится однородной. Через некоторое время на дне колбы образуется смолистый осадок. Верхний слой жидкости слейте и быстро извлеките смолу, которая на воздухе густеет и постепенно затвердевает.
Свойства оргстекла. Кусочек органического стекла (полиметил-метакрилат) осторожно нагрейте над пламенем горелки. Образец размягчается, измените его форму и охладите. Сделайте вывод о термопластичности полимера. Подожгите кусочек оргстекла. Оно горит с характерным потрескиванием голубым некоптящим пламенем с выделением метилового эфира метакриловой кислоты, что обнаруживается по специфичному запаху эфира.
Получение искусственного шелка. Эксперимент по получению искусственного шелка требует много времени, поэтому его проводят на занятиях кружка, а на уроке демонстрируют отдельные его этапы и конечный процесс. Около 20 г гидроксокарбоната меди растворите в 25 %-ном растворе аммиака путем его постепенного добавления к соли и при постоянном помешивании. В полученный медноаммиачный раствор внесите медицинскую вату небольшими порциями и перемешивайте до полного растворения клетчатки и получения вязкой массы. Растворение ваты идет медленно, поэтому опыт можно отложить на 1–3 дня. Для получения нитей искусственного волокна медноаммиачный раствор клетчатки наберите в медицинский шприц и выдавливайте через иглу, погруженную в осадительный раствор, представляющий собой 10–15%-ный раствор серной или соляной кислоты.
Обнаружение хлора в исследуемом образце. Прокалите конец тонкой медной проволоки в пламени спиртовки, коснитесь им (в горячем виде) исследуемого образца (линолеум, изделие из искусственной кожи, раствор хлороформа и т.д.), затем вновь внесите проволоку в пламя. Появление красивой изумрудной окраски пламени укажет на наличие хлора (в составе соединений) в анализируемых пробах.
Идентификация твердых полимеров. Определение полимеров возможно на основании их внешнего вида и с помощью ряда последовательных опытов. а) Прежде всего, внимательно осмотрите образец и подробно опишите его внешние признаки (цвет, твердость, эластичность, тактильные ощущения и т.д.).
б) Далее поместите образец в сосуд с водой и определите его относительную плотность по сравнению с водой.
Таблица по определению твердых полимеров
| Наименование полимера Свойства образца полимера | Амино-пласты | Фено- пласты | Поли-мета- крилат | Поли- этилен | Поли- стирол | Поли-винил- хлорид |
| Внешние признаки: -твердый, хрупкий -можно деформировать -жирный на ощупь -легче воды -тяжелее воды При нагревании: -размягчается -не размягчается При внесении в пламя -загорается легко -загорается с трудом Характеристика пламени -светящееся -коптящее -несветящееся -зеленоватое -желтое голубовато Особенности горения -потрескивание -разбрасывание частиц -вздувание изделия -обугливани Запах продуктов горения -хлороводорода -горящей свечи -цветочный, сладковатый -фруктовый, сладковатый -фенола и формальдегида -аммиака, формальдегида с селедочным запахом Проба на хлор | + + + + + + + + + | + + + + + + + + + | + + + + + + + + | + + + + + + + + | + + + + + + + + | + + + + + + + + + |
в) Для определения отношения к нагреванию кусочек полимера поместите в стаканчик и медленно нагревайте на песчаной бане. Одновременно поставьте рядом стаканчик с водой. С помощью стеклянной палочки контролируйте начало размягчения полимера. Отметьте при этом, произошло ли размягчение до начала закипания воды (до 100 оС), в момент закипания (100 оС) или после него (выше 100 оС). Учтите также, что многие полимеры не размягчаются при нагревании, а разлагаются с выделением газообразных продуктов.
г) Далее проведите тест (в вытяжном шкафу) на поведение полимера в пламени. Для пробы возьмите пинцетом небольшой образец вещества и внесите в верхнюю зону пламени (осторожно!) горелки так, чтобы пламя охватило небольшой участок полимера (соблюдайте правила пожарной безопасности!). Отметьте следующие явления: плавится ли образец с образованием капель, горит ли полимер только в пламени или также вне его, каков характер горения (яркость, копоть, потрескивание, цвет пламени).
д) Погасите пламя резким движением руки, или сильным дуновением. Отметьте свойства продуктов разложения (выделяется ли дымок, легче он воздуха или опускается вниз, каков его запах (осторожно!) и цвет).
е) Обязательно проведите пробу на хлор.
При определении наименования полимера на основе эксперимента следует помнить, что в состав полимерных изделий, кроме самого полимера входят различные добавки – наполнители, красители, пластификаторы и т.д.
Свойства этих компонентов могут существенно влиять на ход эксперимента и исказить его результаты, так как описанные признаки соответствуют чистым полимерам.
Результаты исследования сравните с данными таблицы по определению твердых полимеров и сделайте соответствующие выводы.
Идентификация волокон. Для определения разновидности волокна, его с помощью пинцета вносят пламя (можно в фарфоровой чашечке на несгораемой подставке поджечь немного этанола; сухое горючее использовать не рекомендуется, так как оно при горении выделяет запах). Во время опыта нужно соблюдать правила пожарной безопасности и внимательно наблюдать за скоростью сгорания, выделением запаха (осторожно!) и внешним видом продуктов сгорания.
Таблица по определению волокон
| №№ | Вид волокна | Характер сгорания | Запах | Продукты сгорания |
| 1 | Ацетатное | Сгорает быстро | | Темный твердый шарик |
| 2 | Хлопчатобумажное | Сгорает быстро | Запах жженной бумаги | Зола серого цвета |
| 3 | Вискозное | Сгорает быстро | Запах жженной бумаги | Зола серого цвета |
| 4 | Шерсть; шелк | Сгорает медленно | Запах жженных перьев | Темный хрупкий шарик |
| 5 | Лавсан | Горит коптящим пламенем | | Темный блестящий шарик |
| 6 | Нитрон | Сгорает медленно | | Темный рыхлый неблестящий шарик |
| 7 | Капрон | Плавится | Неприятный запах | Темный твердый блестящий шарик |
| 8 | Хлорин | Горит небольшим коптящим пламенем. Вне пламени не горит | | Черный хрупкий шарик |
Рассмотрите выданные вам образцы волокон и проведите их идентификацию. Результаты исследования сравните с данными таблицы по определению волокон и сделайте соответствующие выводы.
Вопросы и задания
1. В обиходе всегда найдется немало ненужных и поломанных изделий из полимеров. Соберите побольше подобных вещей, определите из каких полимеров они изготовлены и оформите красочную коллекцию "Полимеры в быту". Сколько видов твердых полимеров в вашей коллекции?
2. Аналогично, соберите набор различных тканей, ниток и волокон, проведите их идентификацию и оформите коллекцию "Волокна и ткани в быту". Сколько видов тканей и волокон набралось в вашей коллекции?
3. С целью увеличения срока использования таблиц и рисунков или предохранения их от загрязнения и порчи на бумажную поверхность наносят растворы полимеров. Для приготовления таких растворов 5–10 г измельченного полимера (оргстекло, полистирол) растворите в 100 мл подходящего органического растворителя (ксилол, толуол, четырех-хлористый углерод, этилацетат и др.). Раствор нанесите несколько раз, каждый раз дожидаясь, чтобы предыдущий слой полностью высох. Проведите инвентаризацию дидактических таблиц в вашем химическом кабинете, и самые нужные для учебного процесса защитите от преждевременного износа.
Примечание. Покрытие обязательно должно проводиться на открытом воздухе или в вытяжном шкафу во избежание отравления летучими растворителями.
