Координационная химия и реакционная способность смешанных ацидопорфириновых комплексов марганца в растворах 02. 00. 01 неорганическая химия 02. 00. 04 физическая химия
| Вид материала | Автореферат |
- Рабочая программа дисциплины (модуля) «математический анализ», 424.74kb.
- Рабочая программа дисциплины (модуля) «Уравнения математической физики», 266.58kb.
- Рабочая программа дисциплины (модуля) «Линейная алгебра и аналитическая геометрия», 275.82kb.
- Координационные свойства комплексов меди и марганца с β-октаалкилпорфиринами и их мезо-фенильными, 305.31kb.
- Алкилиденанилины: структура и реакционная способность в гидрировании 02. 00. 03 органическая, 495.9kb.
- Утверждаю, 65.11kb.
- «Неорганическая химия», 1345.55kb.
- Рабочая программа дисциплина ‹‹Неорганическая химия›› опд. Ф. 02 Специальность 020101, 343.5kb.
- Химия и химическое образование на рубеже веков: смена целей, методов и поколений, 258.11kb.
- Конспект лекций по курсу «Неорганическая и аналитическая химия», 18.21kb.
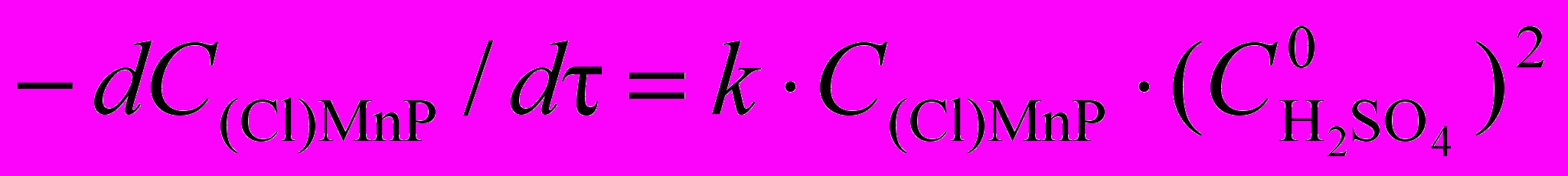 (12)
(12)Записав схему реакций и уравнение скорости лимитирующей стадии аналогично (6 – 9) и (10) соответственно и выразив
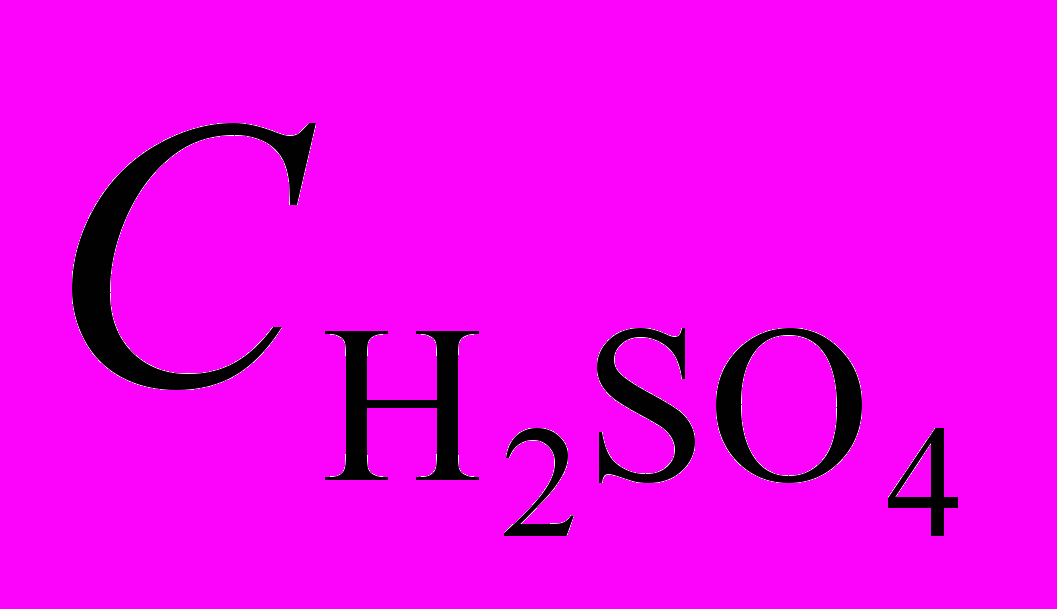 из уравнения для константы равновесия (6), получим кинетическое уравнение процесса в целом (уравнение 13).
из уравнения для константы равновесия (6), получим кинетическое уравнение процесса в целом (уравнение 13).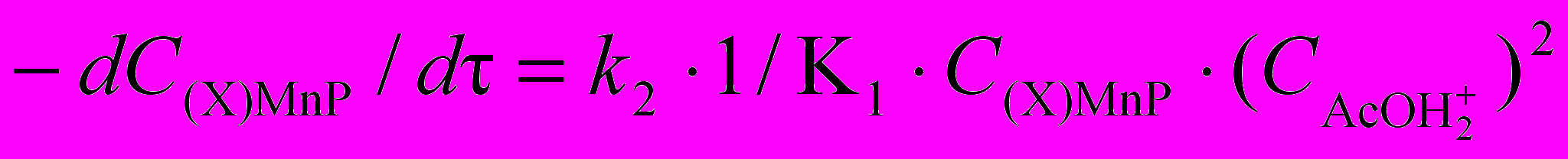 (13)
(13)При низких концентрациях H2SO4 в AcOH (10-4 – 10-2 моль/л) равновесие (6) практически нацело смещено вправо, что позволяет констатировать приближенное равенство концентрации
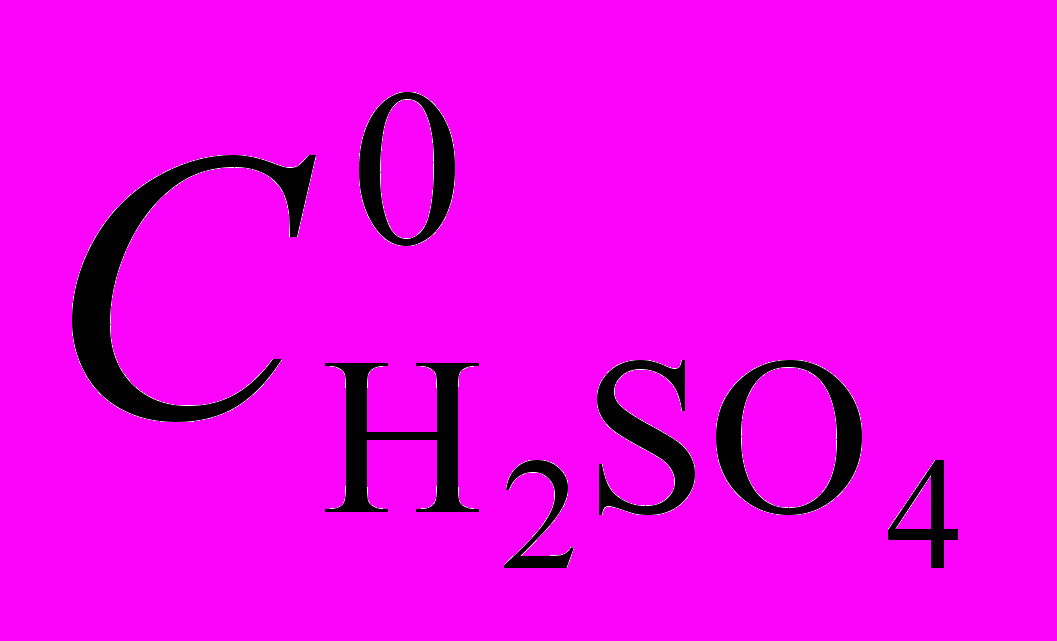 и равновесной концентрации AcOH2+. Т. о., уравнение (13) тождественно экспериментальному уравнению скорости (12), а константа k в уравнении (12) равна k2.1/K1.
и равновесной концентрации AcOH2+. Т. о., уравнение (13) тождественно экспериментальному уравнению скорости (12), а константа k в уравнении (12) равна k2.1/K1.Реакция диссоциации (X)MnOEP, а также моно- и дифенил-производных ((Cl)MnMPOEP, (Cl)Mn5,10DPOEP, (Cl)Mn5,15DPOEP) протекает при более высокой концентрации H2SO4 (табл. 4). Показано, что в кинетическое уравнение диссоциации этих комплексов входит общая кислотность h0 (уравнение 14), и механизм их диссоциации аналогичен рассмотренному выше (уравнения 6 – 9).
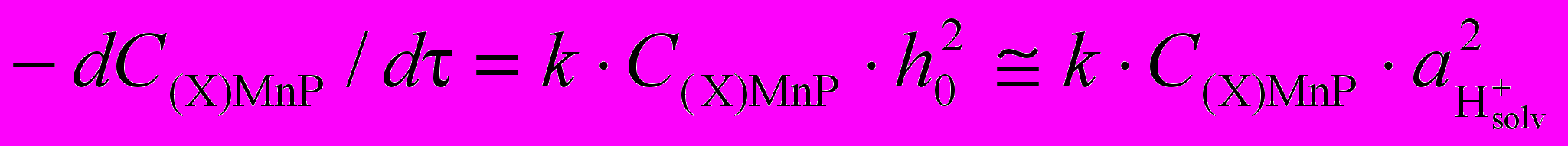 (14)
(14)Таблица 4. Кинетические параметры диссоциации марганец(III)октаэтилпорфиринов
в смешанных растворителях AcOH - H2SO4
| Комплекс |  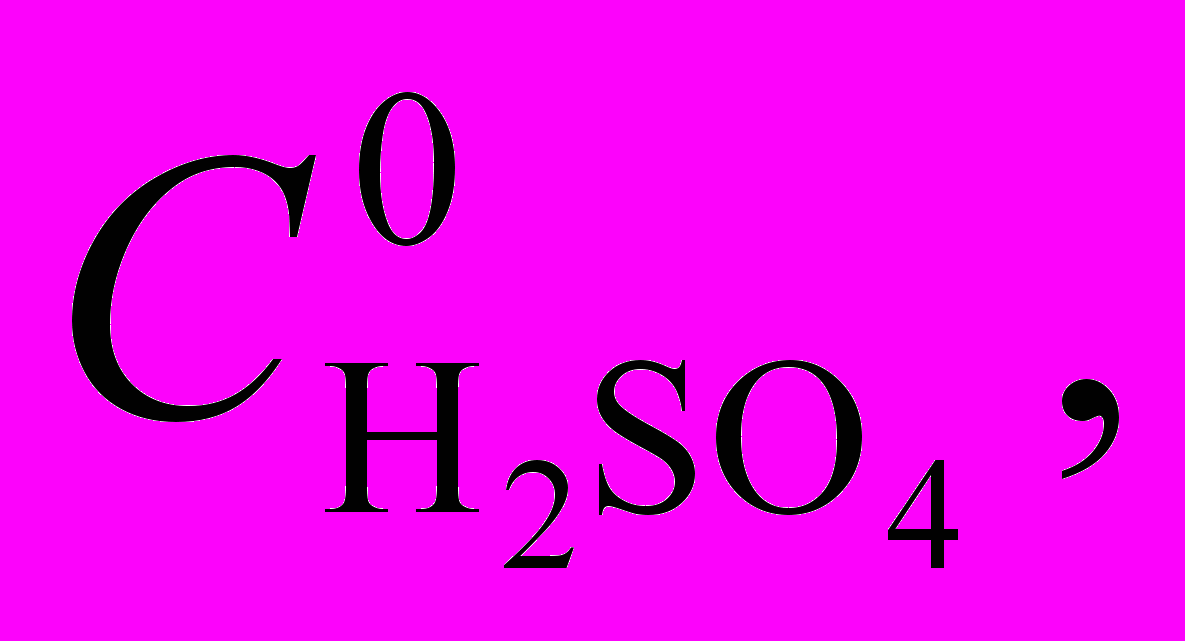 моль/л моль/л | k298, л2.моль-2.с-1 | Е, кДж/моль | ΔS≠, Дж/моль.K |
(Cl)MnTriPOEP | 0,019 0,070 | 0,55 0,03 | 61 3 | -53 10 |
(Cl)MnTetPOEP | 0,0018 0,0042 | 69,0 0,6 | 48 1 | -56 3 |
| (Cl)MnOEP | 5,16 ¸ 6,44 | (1,6 ± 0,2).10-17 | | |
| (AcO)MnOEP | 5,52 ¸ 6,57 | (4,75± 0,5).10-17 | | |
| (SCN)MnOEP | 5,57 ¸ 7,21 | (1,3 ± 0,2).10-17 | | |
| (Cl)MnMPOEP | 4,73 ¸ 6,05 | (2,5± 0,6).10-14 | | |
| (Cl)Mn5,10DPOEP | 2,62 ¸ 4,26 | (2,7± 0,5).10-10 | | |
| (Cl)Mn5,15DPOEP | 0,66 ¸ 1,97 | (2,5± 0,3).10-12 | | |
