Учебное пособие Рекомендовано научно-методическим советом
| Вид материала | Учебное пособие |
- Бизнес-планирование предприятия учебное пособие Рекомендовано учебно-методическим советом, 1729.98kb.
- Учебное пособие Рекомендовано учебно-методическим советом угаэс уфа-2005 удк 330., 1365.17kb.
- Учебное пособие Рекомендовано учебно-методическим советом угаэс уфа-2006, 1339.31kb.
- Учебное пособие Рекомендовано учебно-методическим советом угаэс уфа-2009, 2459.47kb.
- Учебное пособие Рекомендовано учебно-методическим советом угаэс уфа-2008, 3188.71kb.
- Учебное пособие Часть 1 Рекомендовано учебно-методическим советом угаэс уфа 2006, 1359.55kb.
- Учебное пособие Изд. 2-е, перераб и доп. Петрозаводск Издательство Петргу 2006, 1457.49kb.
- Учебное пособие для вузов Составитель Т. А. Тернова, 241.22kb.
- Учебное пособие для вузов Составитель Т. А. Тернова, 241.72kb.
- Учебно-методическое пособие, 281.65kb.
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
Воронежский государственный архитектурно-строительный университет
О.Р. Сергуткина, О.В. Артамонова, О.Б. Кукина
РАБОЧАЯ ТЕТРАДЬ ПО ХИМИИ
Учебное пособие
Рекомендовано научно-методическим советом
Воронежского государственного архитектурно-строительного университета в качестве учебного пособия для студентов всех специальностей, обучающихся дистанционно по направлению 270100 «Строительство»
Воронеж 2010
УДК 54.00
ББК 24.00
Рецензенты:
Сергуткина, О.Р. Рабочая тетрадь по химии : учебн. пособие / О.Р. Сергуткина, О.В. Артамонова, О.Б. Кукина ; Воронеж. гос. арх.-строит. ун-т. − Воронеж, 2010. 98 с.
Даны рабочие задания по общей, неорганической, аналитической, физической химии и химии высокомолекулярных соединений, содержащие краткие теоретические сведения, необходимые для выполнения заданий. Описаны экспериментальные опыты, которые студент должен уяснить, написать соответствующие химические реакции и сделать выводы.
Приводимые в каждом задании примеры позволяют понять значение излагаемого материала, а выполняемые самостоятельно упражнения − закрепить его, что очень важно при дистанционном обучении.
Учебное пособие предназначено для студентов всех специальностей, обучающихся дистанционно по направлению 270100 «Строительство».
Ил. 42. Табл. 26. Библиограф.: 2 назв.
УДК 54.00
ББК 24.00
Печатается по решению научно-методического совета Воронежского
государственного архитектурно-строительного университета
Оглавление
| Введение | 4 | |
| Задание 1. | Строение вещества 1.1. Строение атома и периодическая система 1.2. Химическая связь | 5 5 10 |
| Задание 2. | Классы неорганических соединений | 15 |
| Задание 3. | Общие закономерности химических процессов 3.1. Основы химической термодинамики 3.2. Химическая кинетика 3.3. Химическое равновесие | 26 26 29 35 |
| Задание 4. | Свойства растворов 4.1. Общие свойства растворов 4.2. Равновесия в растворах электролитов | 40 40 44 |
| Задание 5. | Окислительно-восстановительные и электрохимические процессы 5.1. Окислительно-восстановительные реакции 5.2. Гальванический элемент 5.3. Электролиз 5.4. Коррозия металлов | 57 57 61 66 71 |
| Задание 6. | Аналитическая химия 6.1. Качественный химический анализ 6.2. Количественный химический анализ 6.3. Физико-химические и физические методы анализа | 76 76 79 81 |
| Задание 7. | Высокомолекулярные соединения 7.1. Общие сведения и методы получения полимеров 7.2. Строение и свойства полимеров 7.3. Природные полимеры | 87 87 93 96 |
| Заключение | 98 | |
| Библиографический список | 98 | |
ВВЕДЕНИЕ
Рабочая тетрадь служит как для описания химического эксперимента, так и для самоконтроля усвоенного материала, что очень важно в дистанционном обучении.
Тетрадь содержит 7 заданий по четырём блокам (дидактическим единицам) рабочей программы, т.е. изучается полный курс дисциплины «Химия». Для выполнения каждого задания следует изучить и усвоить относящийся к данному заданию материал по источникам, указанным в разделе «Подготовка к выполнению задания».
Краткие теоретические сведения рабочих заданий являются основой для понимания описываемых экспериментов и приводимых примеров. Упражнения предназначены для самостоятельного выполнения и являются методом самоконтроля усвоения учебного материала.
При изучении экспериментальной части раздела «Выполнение задания» в соответствующих местах рабочей тетради составляется уравнения реакций описанных опытов, формулируются и записываются выводы.
Рабочие задания сопровождается типовыми контрольными упражнениями, аналогичными заданиям экзаменационного тестирования.
Разделы «Выполнение задания» выделены в отдельный файл «Выполнение заданий. Самостоятельная работа», который студент заполняет: набирает уравнения реакций, записывает выводы, выполняет упражнения на месте пропечатанных свободных линий. Допускается выполнение рабочих заданий «от руки» в скопированном файле.
На проверку выполненные задания присылаются по электронной почте в деканат факультета дистанционного обучения или предоставляются лично методисту данной специальности. Зачтённые разделы «Выполнение задания» рабочей тетради являются допуском к экзамену.
Задание 1. СТРОЕНИЕ ВЕЩЕСТВА
1.1. СТРОЕНИЕ АТОМА И ПЕРИОДИЧЕСКАЯ СИСТЕМА
ПОДГОТОВКА К ВЫПОЛНЕНИЮ ЗАДАНИЯ
Изучить и усвоить:
· лекцию «Строение атома и периодическая система» [Часть 2 УМК, раздел 1.1]
Цель выполнения задания
∙ Установить связь между положением элементов в периодической системе, строением их электронных оболочек и свойствами.
∙ Выяснить причины и закономерности периодического изменения свойств элементов и их соединений.
Теоретические сведения
Атом химического элемента представляет собой сложную квантово-механическую систему. Охарактеризовать состояние электрона в атоме можно с помощью квантовых чисел: главного, орбитального, магнитного, спинового. В квантово-механической модели строения атома используют вероятностный подход. Область пространства, в котором наиболее вероятно нахождение электрона, называется атомной орбиталью.
Атомные орбитали, разрешённые на первых четырёх энергетических уровнях и соответствующие им состояния электронов представлены в табл. 1.1.
Таблица 1.1
Значения квантовых чисел и состояния электронов
| Главное квантовое число | n = 1 | n = 2 | n = 3 | n = 4 |
| Орбитальное квантовое число и типы АО | s (l=0) | s (l=0), p(l=1) | s(l=0), p(l=1), d(l=2) | s(l=0), p(l=1), d(l=2), f(l=3) |
| Состояние электрона | 1s | 2s, 2p | 3s, 3p, 3d | 4s, 4p, 4d, 4f |
Электронное строение атома может быть представлено в виде электронных формул или энергетических (квантовых) ячеек. При распределении электронов в атоме учитывают:
∙ принцип минимальной энергии,
∙ правило Клечковского;
∙ принцип (запрет) Паули;
∙ правило Гунда.
Электроны в атоме в первую очередь заполняют атомные орбитали с минимальной энергией. Последовательность заполнения атомных орбиталей:
l s < 2 s < 2р < 3 s < 3р < 4 s < 3d < 4р < 5 s ≈ 4 d < 5р < 6 s ≈ 5 d ≈ 4f …. (1.1)
В соответствии с принципом Паули на одной орбитали максимально может быть только два электрона.
Порядок написания электронных формул следующий:
1) по таблице Д.И. Менделеева находят символ элемента и записывают его;
2) слева внизу от символа ставят порядковый номер элемента, который указывает общее количество электронов в атоме;
3) после символа – номер энергетического уровня: 1, 2, 3, 4, …, значение которого численно совпадает с главным квантовым числом;
4) затем − тип орбитали (s, p, d, f). Сверху справа над типом орбитали записывают количество электронов.
Электронное строение атома определяет положение элемента в периодической системе. Номер периода совпадает с максимальным значением главного квантового числа. Количество неспаренных электронов определяет валентность, номер группы совпадает с максимальной степенью окисления элемента.
С ростом заряда ядра периодически меняется электронная конфигурация атомов, поэтому периодически меняются различные характеристики атомов, например, их размеры, энергия ионизации, сродство к электрону, относительная электроотрицательность, валентность, степень окисления и другие, определяющие окислительно-восстановительную способность и кислотно-основную характеристику элементов.
Тенденции изменения энергии ионизации, сродства к электрону и электроотрицательности для элементов главных подгрупп II − IV периодов периодической системы представлены на рис. 1.1.
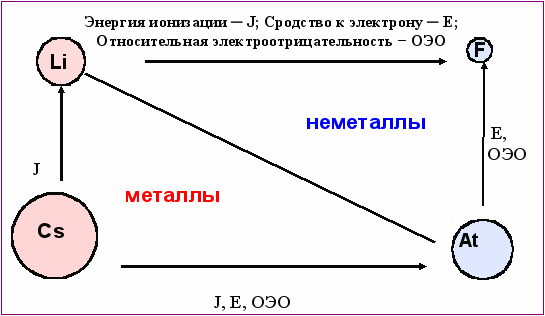
Рис. 1.1. Изменение энергии ионизации, сродства к электрону и относительной
электроотрицательности в главных подгруппах периодической системы элементов
В одних и тех же группах и в одних и тех же подгруппах расположены элементы с одинаковым строением внешних электронных оболочек (электронные аналоги), которые оказывают наибольшее влияние на химические свойства элементов. Поэтому можно сказать, что в одних и тех же группах и подгруппах находятся элементы со сходными свойствами, что находит своё выражение в составе высших оксидов, гидроксидов и летучих водородных соединений (табл. 1.2)
Таблица 1.2
Формулы некоторых соединений в зависимости от положения
элементов в периодической системе
| Главные подгруппы периодической системы | ||||||
| I | II | III | IV | V | VI | VII |
| Число электронов на внешнем электронном уровне | ||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Формулы высших оксидов | ||||||
| Э2О | ЭО | Э2О3 | ЭО2 | Э2О5 | ЭО3 | Э2О7 |
| Формулы газообразных водородных соединений | ||||||
| | | | ЭН4 | ЭН3 | Н2Э | НЭ |
| Формулы высших гидроксидов | ||||||
| ЭОН | Э(ОН)2 | Э(ОН)3 | Н2ЭО3 | НЭО3 | Н2ЭО4 | НЭО4 |
ВЫПОЛНЕНИЕ ЗАДАНИЯ
Если перед номерами ответов стоят значки «□», то правильный ответ не один.
Пример 1.1. Максимальное число электронов на орбитали n = 2, l = 1 равно …
1) 4 2) 6 3) 8 4) 2
Решение. В соответствии с табл. 1.1, значению n = 2, l = 1 соответствуют атомные орбитали 2р, которых максимально может быть три. В соответствии с принципом Паули на одной орбитали максимально может быть только два электрона, а на трёх − 6.
Правильный ответ 2.
Упражнение 1.1. Максимальное число электронов на орбитали n = 3, l = 2 равно …
1) 4 2) 6 3) 10 4) 2
______________________________________________________________________________
Пример 1.2. Относительная величина электроотрицательности элементов уменьшается в ряду … □ 1) Se, S, O □ 2) B, C, N □ 3) Cl, Br, J □ 4) P, Si, Al
Решение. Относительная величина электроотрицательности элементов уменьшается в периодах слева направо (ответ 4) и в главных подгруппах сверху вниз (ответ 3).
Упражнение 1.2. Относительная величина электроотрицательности элементов увеличивается в ряду …
□ 1) As, P, N □ 2) Al, Si, P □ 3) O, S, Se □ 4) P, Al, Si
_____________________________________________________________________________
Пример 1.3. Порядковый номер элемента, валентные электроны атома которого расположены на орбиталях 4s24p4, равен 1) 22 2) 32 3) 34 4) 24
Решение. В соответствии со строением внешнего энергетического уровня 4s24p4 данный элемент расположен в четвёртом периоде (заполняются четыре квантовых слоя, n = 4). На АО внешнего энергетического уровня 6 электронов, следовательно, это элемент 6 группы главной подгруппы, т.к. валентные электроны находятся в состоянии «s» и «p». В периодической системе этот элемент селен, него порядковый номер 34, Для подтверждения правильности ответа напишем электронную формулу селена
34 Se 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4.
Упражнение 1.3. У атома элемента с электронной конфигурацией 1s22s22p63s23p64s13d5 число заполненных электронных уровней и максимальная степень окисления равны…
1) 3 и 3 2) 5 и 4 3) 6 и 3 4) 6 и 4
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Пример 1.4. Хлорид-иону соответствует электронная конфигурация…
1) 1s22s22p63s23d6 2) 1s22s22p63s23p6 3) 1s22s22p63s23p4 4) 1s22s22p63s23d5
Решение. Электронная формула хлора 17Cl 1s22s22p63s23p5
Хлорид-ион Cl¯ имеет на один электрон больше: 1s22s22p63s23p6
Упражнение 1.4. Иону О2ˉ соответствует электронная конфигурация…
1) 1s22s22p3 2) 1s22s22p6 3) 1s22s22p0 4) 1s22s22p5
__________________________________________________________________
Пример 1.5. Частицы, обладающие одинаковым строением внешнего энергети-
ческого уровня, расположены в ряду …
1) Ar, Clˉ, Ca2+ 2) O2-, Mg2+, Ar 3) Ne, Al3+,S2- 4) Ne, Clˉ , Ca2+
Решение.
Электронная формула аргона 18 Ar 1s22s22p63s23p6
Электронная формула хлора 17Cl 1s22s22p63s23p5
Электронная формула хлорид-иона Clˉ 1s22s22p63s23p6
Электронная формула кальция 20Са 1s22s22p63s23p64s2
Электронная формула иона кальция Са2+ 1s22s22p63s23p6
Правильный ответ 1.
Упражнение 1.5. Частицы, обладающие одинаковым строением внешнего энергетического уровня, расположены в ряду …
1) Ar, Cl, Ca2+ 2) O2-, Mg2+, Ne 3) Ne, Al3+, S2- 4) Ne, Clˉ , Ca2+
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Пример 1.6. Число неспаренных электронов в атоме брома в основном состоянии равно … 1) 7 2) 1 3) 3 4) 5
Решение. Электронная формула атома брома 35 Br 1s22s22p63s23p63d104s24p5. Состоянию электронов 4р соответствует три АО, на которых максимально может быть шесть электронов. Атом брома имеет в состоянии 4р пять электронов, следовательно, у него один неспаренный электрон:
Упражнение 1.6. Число неподеленных электронных пар на валентном энергетическом уровне атома азота в основном состоянии равно … 1) 0 2) 3 3) 2 4) 1
_____________________________________________________________________________
Пример 1.7. Формула высшего оксида элемента, электронная конфигурация атома которого 1s22s22p63s23p64s13d5, имеет вид … 1) Э2О 2) Э2О3 3) Э2О5 4) ЭО3
Решение. По числу электронов порядковый номер данного элемента «24». Данный элемент хром, расположенный в шестой группе., поэтому максимальная степень окисления равна «+6» и формула высшего оксида CrO3 (ЭО3).
Упражнение 1.7. Формула водородного соединения элемента с электронной конфигурацией атома в основном состоянии 1s22s22p63s23p4 имеет вид …
1) ЭН 2) ЭН4 3) ЭН3 4) ЭН2
__________________________________________________________________________________________________________________________________________________________
Пример 1.8. Число завершенных энергетических уровней и максимальная степень окисления элемента с электронной конфигурацией 1s22s22p63s23p63d104s24р1
соответственно равно … 1) 2 и 6 2) 2 и 5 3) 3 и 3 4) 3 и 1
Решение. Порядковый номер элемента «31», это галлий, расположенный в четвёртом периоде, третьей группе, главной подгруппе. Полностью завершены у него три энергетических уровня: 1-й − 1s2, 2-й − 2s22p6, 3-й − 3s23p63d10. На внешнем уровне галлий имеет три электрона, которые может отдать, вступая в химическую связь, следовательно, максимальная степень окисления элемента равна трём. Правильный ответ «3».
Упражнение 1.8. Число завершенных энергетических уровней и максимальная степень окисления элемента с электронной конфигурацией 1s22s22p63s23p64s13d5
соответственно равно … 1) 2 и 6 2) 2 и 5 3) 3 и 3 4) 3 и 5
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ТИПОВЫЕ КОНТРОЛЬНЫЕ УПРАЖНЕНИЯ
Отметьте правильные ответы. Если перед номерами ответов стоят значки «□», то правильный ответ не один.
1. Квантовое число l характеризует…
1) форму электронной орбитали 2) собственный магнитный момент
3) ориентацию электронной орбитали 4) энергию электронной орбитали
2. В состоянии 5p максимально может находиться ____ электронов
1) 6 2) 10 3) 2 4) 14
3. Число завершенных энергетических уровней и максимальная степень окисления элемента с электронной конфигурацией 1s22s22p63s23p64s23d5
соответственно равно … 1) 2 и 7 2) 2 и 5 3) 3 и 5 4) 3 и 7
4. Иону Fˉ соответствует электронная конфигурация…
1) 1s22s22p3 2) 1s22s22p6 3) 1s22s22p0 4) 1s22s22p5
5. Порядковый номер элемента, валентные электроны атома которого расположены на орбиталях 4s24p2, равен … 1) 22 2) 32 3) 34 4) 24
6. Формула водородного соединения элемента с электронной конфигурацией атома в основном состоянии 1s22s22p63s23p3 имеет вид … 1) ЭН 2) ЭН4 3) ЭН3 4) ЭН2
7. Формула высшего оксида элемента, электронная конфигурация атома которого 1s22s22p63s23p64s23d5, имеет вид … 1) Э2О 2) Э2О7 3) Э2О5 4) ЭО3
8. Относительная величина электроотрицательности элементов уменьшается в ряду … □ 1) Se, S, O □ 2) B, C, N □ 3) Cl, Br, J □ 4) P, Si, Al
1. 2. ХИМИЧЕСКАЯ СВЯЗЬ
ПОДГОТОВКА К ВЫПОЛНЕНИЮ ЗАДАНИЯ
Изучить и усвоить:
· лекцию «Химическая связь» [Часть 2 УМК, раздел 1.2]
Цель выполнения задания
· Ознакомиться с квантово-механическими представлениями об основных типах химической связи.
· Рассмотреть механизм образования ковалентной и ионной связи.
· Научиться устанавливать тип химической связи и описывать основные химические свойства веществ.
Теоретические сведения
Химическая связь возникает при взаимодействии электронных оболочек и ядер атомов, в результате которого понижается полная энергия системы и образуются молекулы и кристаллические вещества. Различают три основных вида химической связи: ковалентная, ионная, металлическая.
Согласно методу валентных связей (МВС) ковалентная связь образуется двумя атомами за счёт двух электронов с антипараллельными спинами, т.е. она локализована между двумя атомами. Общая электронная пара может образоваться в результате взаимодействия двух атомов, имеющих непарные электроны с антипараллельными спинами (обменный механизм) или одного атома, имеющего неподелённую электронную пару и другого атома, имеющего свободную атомную орбиталь (донорно-акцепторный механизм).
В зависимости от положения области перекрывания электронных облаков различают ковалентную связь полярную и неполярную. Если эта область расположена симметрично относительно ядер атомов и принадлежит им в равной степени, то такая связь называется ковалентной неполярной. Этот вид связи наблюдается, обычно, в молекулах, образованных атомами с одинаковой электроотрицательностью. Например, Н2, Сl2, F2, N2, О2 и т.д.
В молекулах, атомы которых различаются по электроотрицательности, общая электронная пара смещена с атому с большей электроотрицательностью (ЭО). Такая ковалентная связь называется ковалентной полярной. Чем больше разница ЭО, тем более полярной будет химическая связь. Электроотрицательность элементов главных подгрупп 1–7 групп первых пяти периодов периодической системы приведена в табл. 1.3.
Таблица 1.3
Электроотрицательность атомов (по Полингу)
-
Период
Группы
1
2
3
4
5
6
7
I
H
2,10
II
Li
0,98
Be
1,50
B
2,00
C
2,50
N
3,07
O
3,50
F
4,00
III
Na
0,93
Mg
1,20
Al
1,60
Si
1,80
P
2,20
S
2,60
Cl
3,00
IV
K
0,91
Ca
1,04
Ga
1,80
Ge
1,80
As
2,10
Se
2,50
Br
2,80
V
Rb
0,89
Sr
0,99
In
1,50
Sn
1,80
Sb
1,80
Te
2,10
J
2,60
Большинство химических соединений можно представить образованными по ковалентному полярному типу химической связи. Вследствие смещения электронной плотности к более ЭО атому и направленности в пространстве ковалентной химической связи молекулы, как правило, представляют собой диполи. Однако имеются молекулы, построенные по полярному типу связи, но не являющиеся диполями, например, СО2, СН4 (см. ниже).
При образовании химической связи электронные облака претерпевают гибридизацию (изменение формы) и располагаются в пространстве таким образом, чтобы быть равноудалёнными друг от друга (рис 1.2).
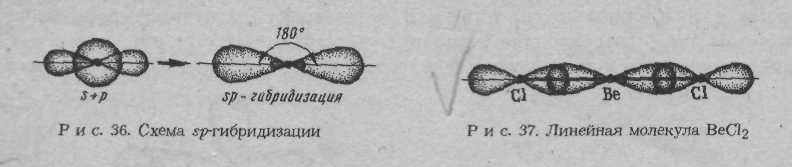
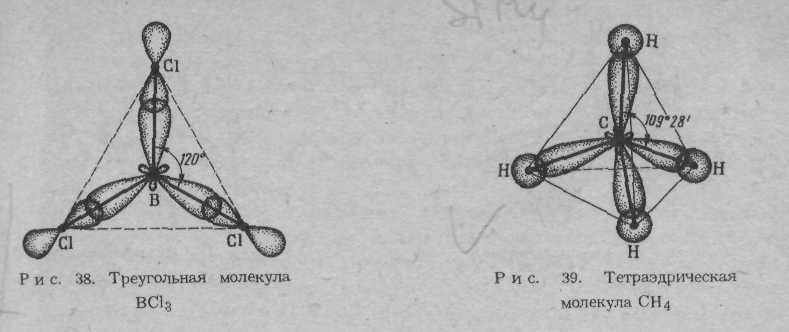
sp2 − гибридизация sp3 − гибридизация
Рис. 1.2. Схема пространственной конфигурации молекул: линейная (при sp − гибридизации), треугольная (при sp2 − гибридизации), тетраэдрическая (при sp3 − гибридизации)
В соответствии с sp- гибридизацией молекула BeCl2 (аналогично и СО2) линейна, т.к. смещение электронных облаков от бериллия к хлору и от углерода к кислороду направлено под углом 180 0 в противоположную сторону и молекула будет неполярной при наличии полярной связи.
Также неполярны молекулы при sp3- гибридизации ( в нашем случае CCl4), т.к. геометрическое сложение векторов химических связей С − Cl, направленных к вершинам пространственного тетраэдра, приводит к нулевому результату.
Пространственная конфигурация молекул определяется числом атомов в молекуле и направленностью химической связи. Если в молекуле больше двух атомов, то в зависимости от типа гибридизации АО центрального атома, угол под которым направлены химические связи к другим атомам принимает величину близкую к значениям, указанным в табл. 1.4. Если одна или несколько гибридных орбиталей заняты неподелёнными парами электронов, то пространственная конфигурация молекул может меняться.
Таблица 1.4
Пространственная конфигурация некоторых соединений
| Тип гибридизации центрального атома | Угол между связями, град | Наличие несвязывающих электронных пар | Конфигурация молекулы | Примеры соединений |
| sp | 180 | − | Линейная | ZnCl2, CaCl2, BeCl2, CO2, С2Н2 |
| sp2 | 120 | − | Треугольная | BCl3, CO32‾, AlF3, С2Н4 |
| sp3 | ~ 109 | нет | тетраэдрическая | CH4, СCl4 |
| sp3 | 108 | 1 пара | пирамидальная | NH3, PCl3 |
| sp3 | 104,5 | 2 пары | угловая | H2O |
При очень большой разности ЭО у взаимодействующих атомов электронное облако химической связи максимально смещается в сторону атома с бóльшей ЭО. Электрон почти полностью переходит от одного атома к другому, в результате чего атомы превращаются в ионы. Ионная связь – результат электростатического взаимодействия противоположно заряженных ионов, она является предельным случаем ковалентной полярной связи.
Способностью наиболее легко отдавать электроны обладают атомы элементов, имеющих наименьшую энергию ионизации, а принимать электроны ─ имеющих наибольшее сродство к электрону (рис.1.1).
Наименьшей энергией ионизации обладают атомы щелочных и щелочноземельных металлов, при образовании ионной связи они будут образовывать положительно заряженные ионы, отдавая электроны. Атомы галогенов имеют наибольшее сродство к электрону, и они будут принимать электроны, образуя отрицательно заряженные ионы. Типично ионные соединения образуются при взаимодействии щелочных и щелочноземельных металлов с галогенами, например, NaCl, KF и т.п. Большинству солей присущ ионный тип связи.
Современные методы экспериментальных исследований показывают, что в кристаллах таких соединений сохраняется некоторая доля ковалентности, т.к. электроны не переходят полностью от одних атомов к другим. Поэтому принято говорить об определённой степени ионности связи в зависимости от разности в электроотрицательности взаимодействующих атомов.
ВЫПОЛНЕНИЕ ЗАДАНИЯ
Пример 1.9. Суть обменного механизма образования ковалентной химической связи состоит …
1) в перекрывании двух свободных орбиталей двух атомов
2) в перекрывании одноэлектронных орбиталей взаимодействующих атомов
3) в перекрывании любых электронных орбиталей
4) в перекрывании двухэлектронной орбитали одного атома и свободной орбитали дру-
гого атома
Решение. Ковалентная химическая связь двухэлектронная и двухцентровая. Согласно обменному механизму общая пара электронов (двухэлектронная) образуется двумя атомами (двухцентровая), имеющими по одному непарному электрону с антипараллельными спинами. Правильный ответ 2.
Например, так можно представить образование молекулы водорода (рис. 1.3).
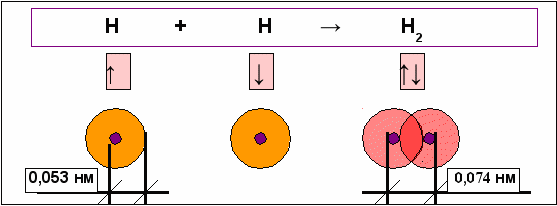
Рис. 1.3. Схема перекрывания электронных облаков
при образовании молекулы водорода
Пример 1.10. Суть донорно-акцепторного механизма образования ковалентной химической связи состоит …
1) в перекрывании двух свободных орбиталей двух атомов
2) в перекрывании одноэлектронных орбиталей взаимодействующих атомов
3) в перекрывании любых электронных орбиталей
4) в перекрывании двухэлектронной орбитали одного атома и свободной орбитали дру-
гого атома
Решение. В этом случае один атом (донор) предоставляет пару электронов, а второй атом (акцептор) − свободную атомную орбиталь. Правильный ответ 4.
Типичным представителем соединения, образовавшегося по донорно-акцепторному механизму. является ион [NH4]+ (рис. 1.4).
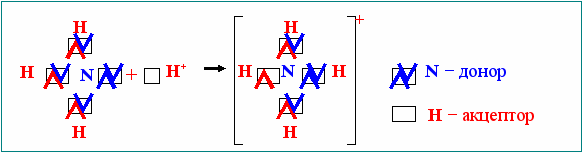
Рис. 1.4. Донорно-акцепторный механизм образования ковалентной связи
в ионе [NH4]+
Упражнение 1.9. Укажите соединение, в котором реализуется связь, образованная по донорно-акцепторному механизму …
1) хлорида аммония 2) молекула хлороводорода 3) аммиака 4) молекула азота
____________________________________________________________________________________________________________________________________________________________
Упражнение 1.10. Частицей, которая может являться акцептором электронной пары, является … 1) Fˉ 2) H+ 3) S2ˉ 4) NH3
____________________________________________________________________________________________________________________________________________________________
Пример 1.11. Только полярные молекулы представлены в ряду …
1) CO2, SO3, NH3 2) NH3, SO2, H2O 3) CCl4, NO, NO2 4) BF3, CO2, SO2
Решение. Среди приведённых молекул СО2 и CCl4 являются неполярными (см. рис. 1.2). Правильный ответ 2.
Упражнение 1.11. Валентный угол равен соответственно 180 ° и 120 ° в соединениях … (табл. 1.4)
1) NH3 и C2H4 2) C2H2 и CH4 3) ZnCl2 и C2H4 4) CH4 H2O
______________________________________________________________________________
Упражнение 1.12. Молекулы PCl3 и NF3 имеют _______ пространственную конфигурацию...
1) угловую 2) треугольную 3) пирамидальную 4) линейную
______________________________________________________________________________
Пример 1.12. Наибольшим дипольным моментом обладает молекула …
1) H2Se 2) H2O 3) H2Te 4) H2S
Решение. Все приведённые молекулы построены однотипно и имеют угловую форму с несколько отличающимся углом связи между водородом и соответствующим элементом. В целом молекулы представляют собой диполи. В ряду сходно построенных молекул дипольный момент увеличивается по мере увеличения разности ЭО атомов. В ряду элементов Te →Se → S → O электроотрицательность увеличивается, в этом же направлении увеличивается полярность молекул.
Правильный ответ 2.
Упражнение 1.13. Наибольшим дипольным моментом обладает молекула …
1) HCl 2) HF 3) HJ 4) HBr
______________________________________________________________________________
Упражнение1.14. Наибольшей степенью ионности характеризуется химическая связь в соединении…
1) BN 2) NH3 3) NO2 4) Li3N
Для объяснения используйте представления о механизме образования ковалентной полярной связи и относительные электроотрицательности элементов.
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Задание 2. КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
ПОДГОТОВКА К ВЫПОЛНЕНИЮ ЗАДАНИЯ
Изучить и усвоить видеозапись лабораторной работы «Основные классы неорганических соединений [Приложение к УМК: диск 2, работа 2].
Цель выполнения задания
· Познакомиться с методами получения и химическими свойствами оксидов и гидроксидов.
· Научиться составлять уравнения реакций получения солей.
· Усвоить принцип кислотно-основного взаимодействия.
Теоретические сведения
Оксиды – сложные вещества, состоящие из двух элементов, один из которых – кислород. Общая формула оксидов: ЭХОУ, где х – число атомов элемента, у – число атомов кислорода.
Оксиды бывают несолеобразующие (SiO, CO, N2O, NO) и солеобразующие. Последние в свою очередь делятся на оснóвные, кислотные и амфотерные. Химический характер оксидов, образуемых различными элементами, можно определить в соответствии с табл. 2.1.
Таблица 2.1
Зависимость свойств оксидов от химической природы элементов
и степени окисления металла или неметалла
| Элементы | Металлы | Неметаллы | ||
| Степень окисления атомов элементов, образующих оксиды | +1, +2 | +3, +4 | +5, +6, +7 | |
| Свойства | оснóвные | амфотерные | кислотные | |
| Примеры | Na2O, CaO (кроме ZnO, BeO, SnO…) | Al2O3, SnO2 (а также ZnO, BeO, SnO…) | CrO3, Mn2O7 | CO2, SO3 |
К гидроксидам относятся основания (основные гидроксиды), кислоты (кислотные гидроксиды) и амфотерные гидроксиды.
Основания – сложные вещества, молекулы которых состоят из атомов металлов и одной или нескольких гидроксильных групп OН‾. Например: NaOH, Ca(OH)2, Fe(OH)2.
Кислоты – сложные вещества, молекулы которых состоят из атомов водорода и кислотного остатка. Например: НCl, H2SO4, H2CO3. Существуют также бескислородные кислоты, которые не являютя гидратами оксидов, например: HCl, HBr, H2S.
Соли – сложные вещества, состоящие из кислотного и основного остатков. Например: NaCl, CaSO4, FeCO3. Кислотный остаток – группа атомов, которая получается, если от кислоты мысленно отнять один или несколько атомов водорода. Оснóвный остаток – часть молекулы основания, которая остаётся при мысленном отрыве от неё одной или нескольких гидроксильных групп.
ВЫПОЛНЕНИЕ ЗАДАНИЯ
