Дипломная работа
| Вид материала | Диплом |
- Дипломная работа по истории, 400.74kb.
- Дипломная работа мгоу 2001 Арапов, 688.73kb.
- Методические указания по дипломному проектированию дипломная работа по учебной дисциплине, 620.15kb.
- Дипломная работа выполнена на тему: «Ресторанный комплекс при клубе знаменитых людей:, 638.16kb.
- Дипломная работа: выполнение и защита методические рекомендации, 248.83kb.
- Дипломная работа Антона Кондратова на тему «Интернет-коммуникации в деятельности предприятия, 1083.86kb.
- Итоги VII всероссийского конкурса «Лучшая студенческая дипломная работа в области маркетинга», 99.02kb.
- Выпускная квалификационная (дипломная) работа методические указания по подготовке,, 629.59kb.
- Дипломная Работа на тему Аспекты взаимодействия категорий Языковая одушевленность неодушевленность, 908.09kb.
- Дипломная работа тема: Анализ удовлетворенности потребителей на рынке стоматологических, 187.27kb.
материалы и методы исследования
2.1. Характеристика исследуемых элементов
В настоящее время известно около 50 минеральных элементов, которые постоянно находятся в организме. Предполагают, что некоторые элементы, присутствующие в тканях и жидкостях организма не выполняют существенной функции в обмене веществ. Наличие их в организме обусловливается случайным поступлением с пищей. Такие заявления не всегда оправданы, так как в последние годы из числа считавшихся случайными выявлен ряд элементов, необходимых для жизнедеятельности организма (хром, олово, кремний, никель, ванадий, свинец, литий и др.). Ошибка такого рода возникла в результате того, что при дефиците этих элементов не было зафиксировано симптомов минеральной недостаточности (Кальницкий, 1985).
В данной работе проводили масс-спектрометрические исследования. С помощью этого метода определяли содержание Na, K, Ca, Fe, Mn, Pb в тканях головного мозга. Кратко охарактеризуем данные химические элементы:
2.1.1. Na (натрий)
Во организме человека Na является очень важным элементом. Он находится в виде хлорида Na в плазме крови в концентрации 0,9 %, поддерживая осмотическое давление на постоянном уровне (Власюк, 1997).
Na – основной катион, участвующий в поддержании кислотно-щелочного равновесия. От выведения или удержания Na в организме зависит регуляция объема внеклеточной жидкости и плазмы крови, так как одна молекула Na осмотически связывает 400 молекул воды. Na играет важнейшую роль в ионном балансе внутренней среды живого организма. Задерживая воду в тканях, он обцславливает способность биологически важных коллоидов тканей к набуханию. Вместе с калием Na участвует в возникновении нервного импульса, играя основную роль в механизме кратковременной памяти. Ионы Na подавляют активность ферментов мышц и поэтому необходимы для сокращения мышц.
То есть Na влияет на состояние мышечной и сердечно-сосудистой систем. Считают, что он опосредует развитие гипертонической болезни за счет как увеличения объема внеклеточной жидкости, так и повышения тонуса артериол, капилляров и прекапилляров.
По действию на сердечную мышцу Na является антагонистом К, поскольку натрий расслабляет ее, а калий, наоборот, сокращает.
Суточное потребление Na человеком, как правило, значительно превышает физиологическую потребность и составляет в среднем 3-6 г. в день. Практически в таком же количестве Na выводится из организма. Всасывание полученного с пищей Na начинается в желудке и происходит в тонкой кишке. Большая часть Na в организме находится в динамическом состоянии, обмениваясь между разными частями клетки, между клеткой и внеклеточной жидкостью и смешиваясь с Na, получаемым с пищей. По системе воротной вены всосавшийся Na поступает в печень, оттуда в небольших количествах в кровь и распределяется по всему внеклеточному пространству.
Ионы Na, вместе с ионами K распределены по всему организму человека, причем первые входят в состав межклеточных жидкостей в качестве наиболее распространенных катионов, тогда как вторые встречаются главным образом внутри клеток (Уильямс Д., 1998).
В клетках существует механизм, обеспечивающий выведение ионов Na+ и поглощение ионов K+ - натриевый насос или Na+-K+ - активизируемая аденозинтрифосфатаза. Работа этого насоса приводит к появлению на мембране клетки градиента концентрации ионов и как следствие – к возникновению электрического потенциала (Anderson, 1997).
Равновесие Na в организме регулируется почками. Основное количество Na выводится из организма с мочой, некоторое количество – с потом и немного – с калом. В норме с мочой выделяется около 95 % Na, поступившего с пищей. Натриевая недостаточность у человека не наблюдается, так как суточная потребность в этом элементе полностью и даже с избытком покрывается за счет поваренной соли и продуктов питания, особенно животного происхождения. При избытке Na+ повышается хрупкость сосудов, нарушается водный баланс в организме (Власюк, 1997).
При недостатке na в организме уменьшается количество воды. У животных нарушается аппетит, появляется вялость и стремление лизать различные предметы, а при более значительной недостаточности шерсть теряет блеск и взъерошивается, заболевают суставы, ухудшается усвоение корма, уменьшается продуктивность животных (Власюк, 1997).
В опытах на изолированном сердце кролика по Лангендорфу измерены показатели Na/Ca-обмена в условиях 65 минут ишемии и реперфузии. Уровень Na увеличивался при ишемии и уменьшался при перфузии препарата раствором, не содержащим калия (Anderson, 1997).
2.1.2 К (калий)
В кровяных клетках и в тканях организма содержатся высокие концентрации ионов К+, тогда как в омывающих эти клетки и ткани жидкостях имеет место обратная ситуация. Такое резко неравновесное распределение ионов щелочных металлов кажется удивительным, если учесть их способность диффундировать сквозь клеточные мембраны. Na диффундирует преимущественно внутри клеток, а К – наружу.
В организме животных и человека около 98 % всего калия находятся внутри клеток. В организме человека содержание К составляет 160-250 г или около 4000-9000 МЭКВ . Содержание К меняется в зависимости от возраста, пола, конституции, причем эти сдвиги связаны с изменением клеточной массы тела. Суточная потребность в калии для взрослого человека составляет 2-3 г или 50-75 МЭКВ , для ребенка 16-30 мг/кг веса. Потребленный с пищей калий всасывается из кишечника в кровь и поступает в воротную вену печени, затем постепенно распределяется в периферический кровоток. Большая часть калия выводится через почки, в гораздо меньшей степени – пищеварительным трактом и совсем незначительно – потовыми железами. Процесс выведения калия складывается из следующих этапов: фильтрация из плазмы в клубочках, затем практически полная реабсорбция в проксимальных канальцах и, наконец, активная секреция клетками дистального сегмента нефрона, основанная на обмене между ионами К+ и H+ ,К+ и Na+.
Калий участвует в осуществлении важнейших жизненных функций организма. Он влияет на состояние мышечной и сердечно-сосудистой систем, участвует в возникновении и передаче нервного импульса. При каждом мышечном сокращении ионы К выходят из мышечного волокна, а при стадии покоя возвращаются обратно. Калий необходим для фосфорилирования адениловой кислоты в аденозинтрифосфорную, которая является поставщиком энергии для биохомических процессов, а также принимает участие в поддержании ионного равновесия в организме (Власюк, 1997). Калий участвует в реализации эндогенных и экзогенных импульсов, воспринимаемых клетками периферической и центральной нервной системы, калий обеспечивает тем самым координационные и трофические процессы в организме и связь организма с внешней средой. Калий участвует в поддержании осмотического давления, кислотно-основного состояния, а также в процессах обмена в клетке.
С участием ионов К+, содержащихся в эритроцитах, происходит перенос кислорода гемоглобином (Москалев, 1998).
По физиологическому действию на организм К является антагонистом Ca.
Шок при тяжелых ожогах обусловлен потерей ионов К из клеток (Уильямс, 1998).
При недостатке К у животных ухудшается аппетит, замедляется рост, понижается возбудимость нервной системы, появляется болезненность в суставах, а в тяжелых случаях наступает истощение, а затем паралич сердца (Власюк, 1997).
То есть гипокалиемия может приводить к нарушению деятельности сердечной мышцы, желудочно-кишечной проводимости, сократительной способности скелетной мускулатуры. Гипокалиемия развивается при надостаточном поступлении К с пищей, а также при применении некоторых лекарственных средств, особенно диуретиков группы тиазидов, сердечных гликозидов и др. Применяют препараты калия для предупреждения и лечения гипокалиемии, при интоксикации препаратами наперстянка, а также аритмиях различного происхождения.
Показано, что гипокалиемия и гипокальциемия, вызванные гипомагниемией у человека сопровождаются выраженным изменением электролитного состава и кислотно-щелочного равновесия биологических сред организма (Elisaf Moses, Milionis Kanalampos, Siampopoulos kostas 1997).
2.1.3. Са (кальций)
Са относится к щелочноземельным металлам, обладает высокой биологической активностью, является основным структурным компонентом костей скелета и зубов животных и человека, а также важным компонентом системы свертывания крови.
Основное количество Са (99 %) сконцентрировано в костях, на построение которых он расходуется. Он также входит в состав протоплазмы, ядер клеток и межклеточных веществ.
Потребность в Са зависит от возраста, физиологического состояния организма, патологических процессов и др. (Афонский, 1997)
Са относится к трудноусвояемым элементам. Попадающие с пищей в организм человека соединения Са практически нерастворимы в воде. Под влиянием кислого содержимого желудка они частично переходят в растворимые соединения, но ввиду незначительной всасываемости Са в желудке этот переход существенного значения не имеет.
Щелочная среда тонкого кишечника способствует образованию трудноусвояемых соединений Са, и лишь воздействие на них желчных кислот позволяет перевести Са в усвояемое состояние. Наиболее интенсивно Са всасывается в двенадцатиперстной и тощей кишках. Значительная часть Са выделяется с калом. Выделение Са зависит от характера питания (Власюк, 1997).
В сложном процессе регуляции Са обмена важная роль принадлежит печени. С желчью выделяются неорганические соединения Са. Почки выполняют важную функцию в обмене Са. Роль почек определяется, прежде всего, их участием в выделении с мочой ионизированного Са и его диффундирующих соединений. Вместе с тем образование соединений Са с белками и др. высокомолекулярными органическими соединениями препятствуют его свободной диффузии через мембранный барьер почечных клубочков. В связи с этим большая часть Са выводится из организма не с мочой.
Регуляция обмена Са ПТГ (паратиреоидином-гормон паращитовидной железы – паратгормон) и КТ (кальцитонин-гормон щитовидной железы) связана с действием гормонов гипофиза, коры надпочечников и щитовидной железы. На обмен Са существенное влияние оказывают также глюкокортикоиды и минералкортикоиды.
С обменом Са тесно связано функционирование многочисленных белков и ферментов, а также синергидные и антагонистические отношения с микроэлементами. Был обнаружен новый класс кальцийзависимых фосфолипид - связывающих белков копинов у всех органоидов начиная с растений и заканчивая человеком. Копины содержат два фосфолипид-связывающих домена и один металл-связывающий домен. Конкурентные взаимоотношения между различными металлами (Zn, Hg, Cu, Cd) и Ca могут определять различные биологические эффекты и в конечном счете определять судьбу неврологических процессов (Уильямс, 1998).
Кальций играет многочисленную роль в жизнедеятельности организма: участвует в передаче первых импульсов, выполняет важную пластическую роль при формировании тканевых структур и влияет на многие физиологические и биохимические процессы, постоянно протекающие в организме человека и животных, благодаря тому, что он способен образовывать прочные соединения с белками, фосфолипидами, органическими кислотами. Са понижает клеточную проницаемость в электрогенезе нервной, мышечной и железистой тканей, в процессах сипантической передачи, участвует в секреции и действии гормонов. В механизме мышечного сокращения Са пренадлежит особая роль. Сокращение мышечного волокна происходит в результате взаимодействия двух основных мышечных белков – миозина и актина. Фактором, разрешающим сокращение, служат ионы Са2+, при повышении их концентрации в миоплазме происходит присоединение Са к регуляторному белку, в результате чего актин становится способным взаимодействовать с миозином. Соединяясь, эти два белка образуют актомиозин и мышца сокращается. Са понижает возбудимость нервной системы (Афонский,1997).
Ионам Са2+ принадлежит исключительная роль в регуляции тонуса симпатической и парасимпатической нервной системы. Са повышает рефлекторную возбудимость спинного мозга и центра слюноотделения. Са уменьшает способность тканевых коллоидов связывать воду, возбуждает деятельность сердца (Власюк, 1997).
Большую роль играет Са в образовании и сохранении целостности костной ткани. Межклеточное костное вещество содержит большое количество солей Са, которым вместе с белками обеспечивают твердость и эластичность кости.
Са способствует свертыванию крови, замедляет действие токсинов, снижает температуру тела, повышает устойчивость организма к инфекциям.
Содержания Са в организме взрослого человека составляет около 20 г. на 1 кг. тела; у новорожденного около 9 г. на 1 кг. Основная часть Са содержится в костной и хрящевой тканях и в зубах.
В сутки взрослый человек должен получать с пищей от 800 до 1100 мг. Са. В большом количестве Са нуждаются дети, беременные женщины и кормящие матери.
Повышение концентрации Са оказывает стабилизирующее влияние на мембрану нервных клеток. Избыток Са в организме может приводить к дифициту Zn и P, в то же время Са препятствует накоплению Pb в костной ткани. (Скальный, 1999)
Большой избыток Са вреден. При нем у животных снижается аппетит, замедляется рост, исчезает блеск волосяного покрова, появляется расстройство нервной системы. (Власюк, 1997)
Повышение содержания Са в мозге может возникать при синдроме злокачественной гипертеримии, семейном гипокалиемическом периодическом параличе, мышечной дистрофии, периодической мигрени, спинно-мозжечковой атаксии, некоторых формах эпилепсии, расстройствах слухового, зрительного и вестибулярного аппаратов.
Гипокальциемия может развиваться при дифиците витамина D, длительном приеме глюкокортикоидов, нарушении гормонального статуса. Уменьшение содержания ионов Са в плазме крови и тканях обуславливает развитие различных патологических процессов. Острая гипокальциемия приводит к тетании, хроническая – может сопровождаться расстройствами скелетной и гладкой мускулатуры, сердечнососудистой системы, нарушением свертывания крови. Недостаток Са в плазме крови вызывает мышечные судороги и даже конвульсии (Уильямс, 1998)
При недостатки Са у молодняка развивается рахит, а взрослые животные страдают остеомаляцией и остепорозом, при котором происходит не нарушение окостенения хрящевой ткани, а рассаывание солей Са и Р из костной ткани, кости постепенно размягчаются, становятся пористыми и под тяжестью тела искривляются и даже ломаются. (Власюк, 1997)
Острый инфаркт миокарда вызывали в эксперименте окклюзией коронарной артерии. Содержание Са2+ в митохондриальной фракции (Мх) увеличивалось в 0,5 ч. после возникновения ишемии и продолжало расти через 1 и 3 ч. Набухание Мх через 0,5 ч. было обратимым, а в сроки 1 и 3 ч. ишемии приводило к некрозу Мх. Активность мембранной Са2+ - АФТ-азы в Мх постепенно уменьшалось после ишемии, что могло быть одной из причин перегруженности Мх Са2+ (Zhon Lin, Zhany Yuanhui, 1996).
2.1.4. Fe (железо)
В настоящее время Fe делят на функционирующее, транспортное и Fe депо (Ноздрюхина, 1989).
К функционирующему (78 %) относится Fe, содержащееся в гемоглобине и осуществляющее транспорт О2, Fe мышц и Fe, входящее в состав ферментов и осуществляющее окислительную функцию дыхательных ферментов – каталазы, пероксидазы, цитохрома С.
К депонированному или запасному Fe относятся ферритин и гемосидерин – широко распространенные в тканях. Их наиболее высокие концентрации имеются, как правило, в печени, селезенке и костном мозгу (Ноздрюхина Л.Р., 1998).
Fe, обнаруживаемое в плазме крови является транспортной формой Fe, которое связано с белком трансферрином, представляющим собой -глобулины и, возможно, -глобулины и альбулины.
Концентрация Fe в плазме крови зависит от возраста: у новорожденных она равна 175 мкг %, у детей в возрасте 1 года – 73 мкг %; затем концентрация Fe вновь увеличивается до 110-115 мкг % и до 13 лет существенно не меняется.
Обмен Fe в организме во многом зависит от нормального функционирования печени. При паренксиматозных поражениях печени нарушается ее функция по депонированию Fe, т.к. пораженный или погибающий гепатоцит отдает Fe в кровь. Вместе с тем из-за утраты гепатоцитами способности ассимилировать Fe разрушающихся эритроцитов происходит его накопление в сыворотке крови. При анемических состояниях лечебное применение Fe обусловлено его участием в процессе гемоглобинообразования, совершающемся в эритробластах костного мозга (Уильямс, 1998).
Всасыванию лекарственного Fe в пищеварительном тракте способствуют следующие факторы: наличие свободной соляной кислоты, необходимой для диссоциации соединений Fe, поступающих в желудок, наличие восстановителей, необходимых для превращения трехвалентного Fe в более усвояемую форму – II-валентного Fe, которое меньше раздражает слизистую оболочку желудочно-кишечного тракта; наличие веществ, способных связывать Fe, образуя с ним усвояемые компоненты; такими веществами в желудке является специфический гликопротеид, в кишечнике – белок апоферритин, а также некоторые аминокислоты. Дальнейшее поступление как лекарственного, так и пищевого Fe в кровеносное русло и в конечном итоге в костный мозг зависит от достаточного содержания в крови свободного (ненасыщенного) трансферрина (Ноздрюхина, 1989).
Резкие нарушения в соотношении минеральных компонентов рациона может существенно влиять на усвоение Fe. Очень высокий уровень фосфатов, а также поступление больших количеств Zn, Cd, Mn снижает усвоение Fe.
Fe выступает в качестве центрального атома при переносе О2 гемоглобином от легких к тканям и при хранении кислорода миоглобином в скелетных мышцах (Ершов, Второва, 1991).
Fe участвует в следующих биохимических превращениях:
- Транспорт электронов (цитохромы,железосеропротеиды)
- Транспорт и дипонирование О2 (миоглобин, гемоглобин)
- Участие в формировании активных центров окислительно-восстановительных ферментов (оксидазы, гидролазы, СОД)
- Транспорт и депонирование Fe (трансферрин, ферритин, гемосидерин, сидерохромы, лактоферрин).
Дисбаланс или недостаточность Fe в организме способствует повышенному накоплению токсичных металлов в нервной системе (Mg, Cu, Cd, Al и др.)
Недостаток Fe может привести к анемиям. У беременных женщин наблюдается недостаток Fe как из-за большой потребности в нем плода, так и вследствие увеличения объема крови в последние месяцы перед родами (Уильямс, 1998).
2.1.5. Mn (марганец).
Mn входит в состав многих тканей животных: общее количество его составляет не более 0.05 мг %; больше всего Mn обнаружено в печени (Афонский С.И., 1998).
Mn необходим для эритропоэза и образования гемоглобина; Mn стимулирует синтез холестерина и жирных кислот, проявляя тем самым лиотропное действие.
Кроме влияния на процессы кроветворения Mn влияет на антителогенез, ускоряя образование антител.
Mn является важным кофактором формирования межклеточных контактов с участием интегринов, что важно в процессах клеточного роста (Saito, 1991). Влияя на железы внутренней секреции, Mn противодействует отложению жиров в печени, стимулирует рост организма (Власюк, 1997).
Ежедневное поступление Mn с пищей составляет 2-9 мл. Однако его биодоступность составляет менее 5 %. Mn наиболее богаты органы, которые содержат значительное количество митохондрий: мозг, печень, почки, поджелудочная железа, кишечник.
Полупериод его биологической жизни в организме человека составляет 37 дней. Основной путь экскреции – желчь. Основными мишенями токсического действия Mn является ЦНС и бронхолегочный эпителий. Mn приникает через гематоэнцефалический барьер, обладает четким тропизмом к подкорковым структурам головного мозга. Особенно легко Mn проникает в мозг новорожденного (Takeda et al, 1999).
Неблагоприятное воздействие Mn на здоровье человеческой популяции связана с широким использованием органических и неорганических соединений. Некоторые исследования показали, что значительное повышение содержания Mn в загрязненном воздухе увеличивает риск развития Паркинсонизма (Lober, 1999).
Избыточное поступление Mn в организм животных ведет к повышению его концентрации в костях и появлению в них изменений, идентичных изменениям в костях при рахите.
Кости, печень, почки, поджелудочная железа и гипофиз взрослых людей содержит обычно более высокие концентрации Mn, чем другие органы (Афонский, 1998).
При марганцевой недостаточности у животных задерживается рост и окостенение скелета, связано это с нарушением фосфатно-кальциевого обмена, которые зависит от недостатка Mn.
Недостаточность Mn у человека не обнаружена, но хроническое отравление горняков, занятых на добыче марганцевых руд, подробно освещено (Takeda, 1999).
2.1.6. Pb (свинец).
Pb и его соединения, особенно свинец, органические соединения жирного ряда, обладают высокой токсичностью и представляют значительную профессиональную вредность для работающих в контакте с ним. Кроме того, полагают, что Pb является мутагеном.
Pb относится к ядам, действующим преимущественно на нервную систему, сосудистую и непосредственно на кровь. Pb депонируется в основном (до 90 %) в скелете, выделяется преимущественно с мочой и калом, в условиях высокого поступления Pb в организм, он выделяется, главным образом, с мочой. Pb обнаруживается в слюне, желудочном соке, желчи, грудном молоке. Обладая способностью проникать через плацентарный барьер, Pb может накапливаться в организме плода и оказывать неблагоприятное влияние на течение беременности и родов.
До 10 % Pb, попавшего с пищей и водой в организм всасывается в кишечнике, при вдыхании паров и аэрозолей Pb его усвоение организмом в 10-20 раз выше, то есть в этом случае Pb может поглощаться почти полностью.
Роль Pb в организме неясна. По-видимому Pb не является биогенным микроэлементом (Авцын с соавт., 1991).
В тоже время присутствие обычных количеств Pb, обусловленных естественным фоном, очевидно, безвредно для организма.
Результаты исследований указывают на возможное участие Pb в обменных процессах как у больных с ишемической болезнью сердца, так и при поражении органов пищеварения.
2.2. Влияние совместного действия магния и витамина В6
на организм (препарат магне-В6).
Значительная часть наиболее употребляемых лекарственных препаратов склонна к реакциям комплексообразования с металлами MЭ in vitro (Калетина, Подымов, 1981).
Микроэлементы не только сами обладают определенным физиологическим действием, но могут даже проявлять синергизм по отношению к целому ряду веществ. Установлено, что Mn и Mo потенциируют действие сердечных гликозидов. Mn усиливает действие аскорбиновой кислоты (Палладин, 1965).
Синергистов в усвоении Mg принимает участие витамин В6. Согласно исследованиям Ю.Ф. Крылова (2001) и Эрл Миндела (2000), присутствие Mg активирует ферменты, содержащие (в качестве коэнзимов) витамины группы В.
Для восполнения дефицита Mg и витамина В6 применяется пищевая добавка MgB6.
Фармакологическое действие: уменьшает возбудимость нейронов и замедляет нейромышечную передачу (Mg2+),
Нормализует многие ферментативные реакции. Применяется при лечении и прифилактике расстройств, связанных с физическими и нервными перегрузками. Витамин В6 увеличивает концентрацию Mg в плазме и эритроцитах, снижает экскрецию Mg с мочой. Mg в печени стимулирует превращения витамина В6 в его активные метаболиты. Витамин В6 участвует в транспорте Mg внутрь клетки, увеличивая его внутриклеточное содержание (Судаков, 1996).
В составе препарата оптимальное сочетание Mg и витамина В6 (Судаков, 2000).
Форма выпуска: 1 таблетка, покрытая оболочкой, содержит магния лактата 500 мг (в том числе Mg 48 мг) и пиридоксина гидрохлорида 125 мг; в блистере 10 шт.; в коробке 5 блистеров.
Одна ампула с 10 мл раствора для приема внутрь – 250 и 62,5 мг активных веществ соответственно; в коробке 10 шт. (Крылов, 2001).
Показания к применению: Дефицит Mg в организме, ассоциированная кальциевая недостаточность, спазмофилия (Крылов, 2001). Пищеварительная система: спазмы, функциональные кишечные расстройства. Мышечная система: мышечные судороги. Нервная система: парастезии, головокружения (Судаков, 1996).
Побочные действия: Диарея, боли в животе, парастезия, периферическая нейропатия.
Способ применения и дозы: внутрь по 2 таблетки или по 1 ампуле, запивая стаканом воды, 2-3 раза в день. Рекомендуется принимать при длительном голодании, несбалансированном питании, определенных формах алкоголизма, детям в период интенсивного роста, беременным женщинам, спортсменам (Судаков, 1996).
Методы предосторожности: При ассоциированной кальциевой недостаточности до начала кальциетерапии рекомендуется насыщение организма магнием (Крылов, 2001).
Конаневич Е.В., Дудкой С.В. (1997) и другими были приведены результаты применения препарата Магне-В6 для лечения невынашивания во втором триместре беременности у 49 женщин. У 42 пациенток получен положительный эффект. Они выписаны с прогрессирующей беременностью. Авторы рекомендуют Магне-В6 для широкого применения в клинической практике (Конаневич, Дудка, Геревич, Суханова, Коноплянко, Суменко, 1997).
Изучение потребности в микроэлементах – актуальнейшая проблема, так как совершенно ясно, что сбалансированность рационов в отношении микроэлементов не менее важна, чем баланс других пищевых веществ.
До сих пор сведения о потребности в отдельных микроэлементах не всегда детально обоснованы, в связи с чем имеются значительные расхождения в рекомендованных величинах. Изучая потребность в одном микроэлементе, следует учитывать наличие коррелятивных взаимоотношений как с другими микроэлементами, так и с другими пищевыми веществами (Смоляр, 1989).
2.3. Пищевой рацион крыс.
Главными составными частями рациона крыс в виварии служат корнеплоды, зерно и сено или зеленая трава. В качестве основного зернового корма можно рекомендовать овес и пшеницу как более полноценный корм по сравнению с ячменем. Полезно чередовать сорта или давать смесь(Башенина, 1975).
Дополнительным высококалорийным белковым кормом служат горох, подсолнечник, желуди хлеб. Их следует давать 1-2 раза в неделю. В хлебе содержатся витамины группы В, поэтому полезно включать его в рацион.
В качестве сочного корма дают корне- и клубнеплоды, которые в неволе служат для грызунов основным источником углеводов, некоторых витаминов и МЭ, а также воды.
Наиболее полноценным кормом является морковь, богатая каротином и другими питательными веществами. На втором месте по ценности стоят столовая и сахарная свекла и капуста. При отсутствии других кормов можно давать картофель.
В качестве животного корма можно давать вареное мясо, крутые яйца, колбасу, молоко (Башенина, 1975).
Для обеспечения полноценного витаминного питания следует прежде всего разнообразить рацион кормами, богатыми теми или иными витаминами. Всем грызунам весьма полезно давать в свежем виде самые разнообразные ягоды и фрукты. Особенно полезны яблоки, сушеные фрукты (Палладин, 1965).
Полезно включать в рацион дрожжи, которые по количеству необходимых аминокислот, витаминов и МЭ превосходят все остальные продукты (Башенина, 1975).
Суточная потребность взрослой белой крысы (весом около 200 г) в пищевых веществах составляет для основных компонентов: белки – 4 г, углеводы – 25 г, жиры – 2 г, витамин А – 0,9 мг, Е – 0,6 мг, К – 2 мг, пиридоксин – 10 мг и другие витамины; минеральные вещества: Са – 40-50 мг, Mg – 4 мг/кг, Fe – 0,25 мг, Na – 0,5 мг % рациона, К – 12 мг, Mn – 0,5-0,8 мг и другие (Гамбарян, 1955).
А.В. Палладин (1965) указывает следующие соотношения пищевых веществ в оптимальном для роста белой крысы рационе: казеин – 35 г, зерновая смесь – 37 г, свиное сало – 15 г, масло – 9 г, минеральные соли – 4 г, при этом ежедневно 0,2-0,6 г дрожжей и 20-30 г свежего салата или другой зелени.
Также для крыс разработаны рецепты брикетированных кормов («кексы»), в которых содержатся все необходимые для них вещества (Башенина, 1975).
2.4. Методика проведения эксперимента.
Исследования влияния введения MgB6 на ионный состав тканей головного мозга проводилось на 18 беспородных крысах массой 182 9,3 г, которые содержались в изолированных клетках по 6 особей в каждой на стандартном рационе при свободном доступе воды.
Схема эксперимента представлена на рис. 1
Все животные были разделены на три группы. Одна группа: интактные животные – не получали никаких фармакологических веществ. Вторая группа – контрольные животные. Они в течение 10 дней получали дистиллированную воду 5 мл/кг внутрижелудочно. Третья группа – экспериментальные животные – получали в течение 10 дней Магне-В6 внутрижелудочно 5 мл/кг. Рекомендуемая доза для MgB6: 2 таблетки или одна ампула 2-3 раза в день. Одна ампула содержит 10 мл раствора (Судаков, 1996). То есть норма для MgB6 0,5 мл/кг. Из этого видно, что крысы получали избыточное количество MgB6 по сравнению с нормой. Введение растворов производили per os. Набирали в шприц раствор. Фиксировали рукой крысу вертикально. На канюлю шприца надевали гибкий пластиковый катетер длиной 8-9 см. И, используя естественное положение головы крысы, вводили его в полость желудка, осторожно продвигая его по задней стенке глотки в пищевод на глубину 5-7 см; и вводили раствор.
На 11 день эксперимента соответственно животные получали нембуталовый наркоз, подвергались декапитации и по стандартной методике извлекали головной мозг. Его помещали в чашки Петри, после чего брали срезы кусочков ткани мозга толщиной 1-1,5 см из областей: ГТ, ОП, центральная извилина ЛДК.
Гипоталамус – высший вегетативный центр, который регулирует деятельность внутренних органов.
ЛДК – регулирует все функции, в том числе и над гипоталамусом.
Эти образцы помещали в пластиковые пробирки, замораживались при t18-20C для дальнейшего исследования на спектрофотометре, на базе лаборатории криминалистики УВД г. Москвы, где проводили масс-спектрометрические исследования. С помощью этого метода определили содержание Na, K, Ca, Fe, Mn, Pb в тканях головного мозга.
Полученные результаты подвергались статистической обработке с целью установления достоверности наблюдаемых результатов. Статистическую обработку проводили с помощью пакета программы Microsoft Excel с определением средней ошибки полученных данных. Достоверность данных оценивали с помощью Т-критерия Стьюдента.
Белые крысы n = 18
Группа I
интактные животные
n = 6
Группа II контрольные дживотные n = 6 получали внутрижелудочно в течение 10 дней дистиллированную воду в дозе 5 мл на 1 кг массы тела
Группа III экспериментальные животные n = 6 получали внутрижелудочно в течение 10 дней MgB6 в дозе 5 мл на кг массы тела



Введение нембутала (40-50 мг/кг)
с последующим забоем крыс

| Лобная доля коры больших полушарий | гипоталамус | Обонятельные луковицы |


-
И сследование элементов
сследование элементов



-
Na
K
Ca
Fe
Mn
Pb
Рис. 1. Схема эксперимента.
2.5. Методика определения ионного состава
головного мозга белых крыс.
После проведения опытов каждая группа крыс получала нембуталовый наркоз (внутрибрюшно 40-50 мг/кг).
Наркозированные животные подвергались декапитации и затем, путем вскрытия черепной коробки извлекался головной мозг, его помещали в чашку Петри, после чего брали срезы кусочков тканей мозга толщиной 1,0-1,5 см.
Материалы отправляли в Москву, где определяли содержание ионов в образцах биообъектов методом хромато-масс-спектрометрии.
Для исследования микроэлементного состава головного мозга использовался аппарат для хромато-масс-спектрометрической диагностики, который состоит из хромато-масс-спектрометра НКВ-2091 (Швеция), системы обработки данных 2КВ-2130 (Швеция), содержащей компьютер РДР 113Н (США), дисплей (Tektornix) и графопостроитель (Verstabea), а также блока обработки биопроб, устройства для термосорбции и ввода проб собственного изготовления. Масс-спектральный анализ с предварительными хромографическими разделениями соединений и непрямой обработкой результатов на ЭВМ обеспечивает достоверную идентификацию индивидуальных компонентов, которая достигается как четким разделение анализируемых веществ, так и получением однозначной характеристики каждого из них. Преимущества этого метода характеризуются высокой чувствительностью, возможностью селективного детектирования и одновременно получения необходимой информации о структуре компонентов, и позволяет успешно проводить количественное определение несмотря на то, что детектирующее устройство обладает высокой пороговой чувствительностью, достигающей 0,05-5 Кг. Надежно зафиксировать необходимые соединения с высокой точностью путем ввода в прибор малых биопроб затруднительно. Прямой ввод биопроб в хромато-масспектрометр не всегда целесообразно из-за низкой концентрации определяемых компонентов, присутствия легко разлагающихся веществ, возможность загрязнения газохроматографической колонки нелетучим остатком, вследствие чего необходимо отделять определенные летучие соединения от биосубстратов. Извлечение анализируемых проб из концентратора с сорбентом проводят термической десорбцией концентрированных органических веществ при 250-300С в охлажденном жидким азотом металлическом капилляре. При последующем нагревании с помощью источника постоянного тока Б5-21 проба с током газа носителя поступала в хроматографическую колонку для разделения веществ. Разделение проводили на стеклянной капиллярной колонке с неподвижной жидкой фазой S - 30 размером 0.3 мл х 50м в изотермическом режиме в течение первых пяти минут и последующим программированием нагрева со скоростью 5С/мин до 150.
Пройдя газохроматографическую колонку разделенные индивидуальные компоненты поступают в масс-спектрометр, в нем для каждого из веществ образуется комплекс ионов с различными массами.
При составлении с размерами физико-химическими параметрами веществ можно сделать вывод, что масспектрометр является строго специфической характеристикой соединений. Такой метод позволяет за короткое время получить значительный объем данных, характеризующих исследуемую биопробу и представлять их в виде графиков и таблиц.
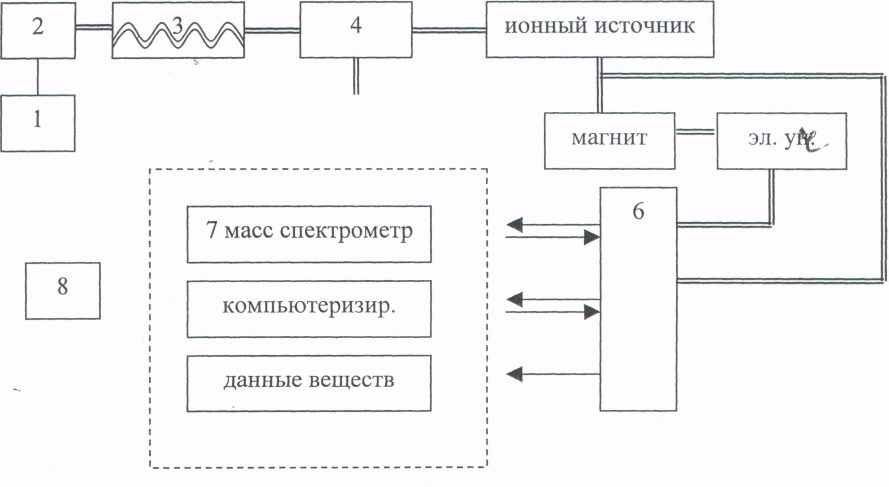
Схема строения хромато-масс-спектрометра.
1 – блок ввода и обработки биопроб
2 – устройство для термодесорбции
3 – газовый хроматограф
4 – молекулярный сепаратор
5 – масс-спектрометр
6 – ЭВМ
7 – дисплей
8 - графопостроитель
(Малышев, 1984)
2.6. Методика статистической обработки результатов.
Статистическую обработку результатов исследования проводили с помощью Т-критерия Стьюдента. Закон Т-распределения служит основой так называемой теории малой выборки, которая характеризует распределение выборочных средних в нормально распределяющейся совокупности в зависимости от объема выборки. Т-распределение зависит только от числа степеней свободы К=n-1, причем с увеличением объема выборки, Т-распределение быстро приближается к нормальному с параметрами μ = 1 и = 1 и уже при n 30 не отличается от него. Т-распределение симметрично и отражает специфику распределения средней арифметической (х ) в случае малой выборки в зависимости от ее объема (n).
Для выборок, объем которых не \превышает 30 единиц, величина Т-распределения нормальна и не зависит от числа наблюдений. Если же n 30, характер Т-распределения зависит от числа наблюдений. Для практического использования Т-распределения составлена специальная таблица (табл. 5 приложений Лакин, 1990), в которой содержаться критические точки (t st) для разных уровней значимости l и числа степеней свободы К.
Для определения достоверности различий между показателями микроэлементов опытной и контрольной групп вычисляли следующие величины:
хк – средняя арифметическая контрольной группы;
хо – средняя арифметическая опытной группы;
Sхк, Sхо - ошибки средних арифметических .
Фактическое значение Т-кретерия Стьюдента вычисляли по формуле:
Tф = d/Sd, где (1)
d – разность средних арифметических
Sd – ошибка разности средних арифметических
tst находят по таблице «критические точки Т-критерия Стьюдента» при различных уровнях значимости L для К = n-1, где К – число степеней свободы, а n – объем выборки.Если tф tst, то Но – принимается и различия между выборочными средними являются недостоверными, p 0.05 (0,001 или 0,01). tф tst, то Но отвергается, различия считаются достоверными, p 0.05 (0,001 или 0,01).
