На правах рукописи
| Вид материала | Документы |
- Печатная или на правах рукописи, 21.09kb.
- Удк 796/799: 378 , 770.24kb.
- На правах рукописи, 399.58kb.
- На правах рукописи, 726.26kb.
- На правах рукописи, 1025.8kb.
- На правах рукописи, 321.8kb.
- На правах рукописи, 552.92kb.
- На правах рукописи, 514.74kb.
- На правах рукописи, 670.06kb.
- На правах рукописи, 637.26kb.
^ 4. Влияние сердечной ресинхронизирующей терапии на динамику ХСН, качество жизни и летальность у больных с хронической сердечной недостаточностью.
Группа пациентов, которым проводилась сердечная ресинхронизирующая терапия состояла из 40 пациентов с ХСН III-IV ФК, резистентных к проводимой адекватной современной терапии ХСН. Группа была представлена мужчинами, средний возраст 66,7+11,9 лет. В 12 случаях (30,0%) у больных с постоянной фибрилляцией предсердий был использован режим бивентрикулярной электрокардиостимуляции типа VVIDBiV, у оставшихся 28 человек (70,0%) – типа DDDBiV. Сердечная ресинхронизирующая терапия сочеталась с современной медикаментозной терапией ХСН.
Эффективность проводимой СРТ мы сравнивали с медикаментозной терапией в целом и с медикаментозной терапией у пациентов с электрическим асинхронизмом (широкий комплекс QRS)..
^ 4.1. Сравнительная характеристика влияния медикаментозной и сердечной ресинхронизирующей терапии на внутрисердечный асинхронизм
У больных ХСН, которым проводилась СРТ, имелось увеличение средних значений показателей внутри- и межжелудочкового асинхронизма. Нами был проведен анализ этих значений и оценены их показатели за 3 года наблюдения. Было проведено сравнение показателей асинхронизма у лиц, получающих только медикаментозную и сердечную ресинхронную терапию. Полученные данные представлены в таблице 7 и 8.
^ Таблица 7
Влияние медикаментозной терапии на показатели асинхронизма
| | Исходно 1 | Через 12 мес 2 | Через 36 мес 3 |
| QRS, мс | 137,2±6,4 | 126,2±4,3* | 138,1±5,6 |
| ВЖМЗЗС-МЖП | 113,4±20,5 | 112,5±21,7 | 115,4±22,1 |
| МЖМЗ, мс | 65,2±7,2 | 72,2±5,7** | 76,4±7,5** |
| МЖМЗТДМ, мс | 68,7±6,6 | 70,2±5,7 | 76,1±6,4** |
Примечание: значимые различия между группами 1-2 и 1-3 * – p<0,05; **– p<0,01.
^ Таблица 8
Влияние СРТ на показатели асинхронизма
| | Исходно 1 | Через 12 мес 2 | Через 36 мес 3 |
| QRS, мс | 152,2±4,3 | 114,1±4,6* | 118,2±4,7* |
| ВЖМЗЗС-МЖП | 128,5±21,7 | 86,4±22,1* | 92,6±23,4* |
| МЖМЗ, мс | 76,6±8,2 | 46,4±7,5** | 41,3±7,8* |
| МЖМЗТДМ, мс | 92,8±6,5 | 47,1±6,4* | 46,8±6,8* |
Примечание: значимые различия между группами 1-2 и 1-3 * – p<0,05; **– p<0,01.
Данные таблиц 7 и 8 показывают, что среди пациентов, получающих медикаментозную терапию исходно величина комплекса QRS составляла 137,2±6,4 мс, на фоне терапии через 12 месяцев - 126,2±4,3 мс, а через 36 месяцев - 138,1±5,6 мс. Медикаментозная терапия в целом по группе достоверно не влияла на величину комплекса QRS, прослеживалась лишь тенденция к его уменьшению, так через 12 месяцев эта разница составила 11 мс, а через 36 месяцев произошло увеличение на 0,9 мс по сравнению с исходным значением.
При использовании КРСУ отмечалось позитивное влияние на величину комплекса QRS в целом по группе, так спустя 12 месяцев этот показатель снизился на 38,1±0,3мс (p<0,05), а через 36 месяцев он был меньше исходного на 34,0±0,4 мс (p<0,05).
В группе пациентов с установленным КРСУ отмечалось отчетливое уменьшение внутри- и межжелудочкового асинхронизма. Так спустя 12 месяцев величина внутрижелудочкового асинхронизма уменьшилась до 86,4±22,1 мс, а через 36 месяцев эта величина составляла 92,6±23,4 мс. Что было достоверно ниже исходного значения 128,5±21,7 мс (p<0,05). Аналогичная картина просматривалась и в показателях межжелудочкового асинхронизма. При оценке межжелудочкового асинхронизма методом импульсной допплерографии через 12 месяцев эта величина составляла 46,4±7,5 мс, через 36 месяцев - 41,3±7,8 мс. По сравнению с исходным значением 76,6±8,2 мс имеет место достоверное снижение показателя (p<0,05). Оценка межжелудочкового асинхронизма проводилась, кроме того, с использованием тканевой импульсно-волновой допплерографии миокарда. Данная методика подтвердила полученные результаты и ее показатели соответственно составили 47,1±6,4 мс через 12 месяцев и 46,8±6,8 мс – через 36 месяцев, исходное значение - 92,8±6,5. Разница между показателями была так же достоверной (p<0,05).
Использование медикаментозной терапии не оказывало существенного влияния на показатели внутрисердечного асинхронизма. Однако, через 36 месяцев отмечалось достоверное увеличение механической межжелудочковой задержки, определяемой как при традиционной эхокардиографии, так и при использовании тканевой допплерографии. Так данные межжелудочковой задержки через три года составляли МЖМЗ - 76,4±7,5 мс, МЖМЗТДМ - 76,1±6,4 мс, при исходных значениях МЖМЗ- 65,2±7,2 мс и МЖМЗТДМ- 68,7±6,6мс.
^ 4.2 Сравнительная характеристика тяжести ХСН среди пациентов получающих только медикаментозную терапию и кардиоресинхронную терапию.
Восстановление внутрижелудочкового синхронизма при использовании кардиоресинхронной электростимуляции приводило к улучшению клинического течения и тяжести ХСН по сравнению с группой, получающей только медикаментозную терапию. На фоне установки кардиоресинхронного устройства (КРСУ) происходило достоверное снижение функционального класса ХСН, так через 3 года среднее значение ФК составило 2,3±0,4, в группе медикаментозной терапии 2,8±0,3 (р <0,01). Данные клинического состояния (в баллах) с использованием ШОКС так же достоверно снизились и составили в группе больных с КРСУ – 7,2 ±0,5, а в группе больных с медикаментозной терапией - 8,6±0,8 (р <0,05). Тест 6-ти минутной ходьбы был достоверно выше в подгруппе с установленным кардиоресинхронизирующим электрокардиостимулятором и составляет 382 ±24 м по сравнению с другой группой 315 3,4±52 м.
Группа пациентов с широким комплексом QRS является наиболее прогностически неблагоприятной в течении ХСН и развитии осложнений. Поэтому становится целесообразным сравнить показатели тяжести ХСН в подгруппе больных с QRS > 120 мс на фоне медикаментозной терапии с группой больных, где проводилась сердечная ресинхронизирующая терапия. На фоне проводимой терапии с использованием КРСУ отмечалось достоверное снижение функционального класса ХСН до 2,4±0,4 (p<0,05) по сравнению с 3,0±0,3 в подгруппе с широким комплексом QRS, где проводилась только медикаментозная терапия. Достоверно ниже и количество баллов по шкале ШОКС в группе с установленным КРСУ 7,2±0,5 по сравнению с 11,2±0,8 (p<0,05) в группе с широким комплексом QRS. Тест 6-ти минутной ходьбы показывал достоверное увеличение переносимости физической нагрузки так через 3 года после установки КРСУ проходимое расстояние увеличилось до 356 ±24 м по сравнению с группой, получающей только медикаментозную терапию, где эта дистанция составляла 204±22 м (p<0,05).
На фоне СРТ было отмечено достоверное улучшение функционального класса ХСН, толерантности к физической нагрузке по результатам теста 6-ти минутной ходьбы и балльной оценки по шкале клинического состояния. Наблюдалось уменьшение выраженности таких симптомов сердечной недостаточности как, периферические отеки, влажные хрипы в легких, гепатомегалия (т.е. прежде всего, связанных с застоем жидкости в организме). Очевидно, что установка кардиоресинхронизирующего устройства приводила к достоверно лучшему течению хронической сердечной недостаточности по сравнению с использованием только медикаментозной терапии как в целом по группе, так и в подгруппе пациентов с широким комплексом QRS. Причем достоверность различий отмечалась уже спустя 1 год после начатого лечения.
Следует отметить, что более выраженное улучшение гемодинамических параметров у больных с сердечной ресинхронизирующей терапией отмечалось у пациентов с более широким комплексом QRS и более выраженным внутри- и межжелудочковым асинхронизмом до кардиостимуляции.
Мы проанализировали частоту госпитализаций, частоту амбулаторных обращений и частоту вызова неотложной помощи у пациентов с установленным КРСУ в течение первого года наблюдения, причинами которых стало прогрессирование ХСН. Затем сравнили эти показатели с данными группы пациентов в целом, получающих только медикаментозную терапию, и имеющих широкий комплекс QRS и получающих только медикаментозную терапию.
Число госпитализаций в группе с установленным КРСУ стало меньше на 36,4% по сравнению с общей группой, получавшей медикаментозную терапию. По сравнению с подгруппой, лечившейся медикаментозно и имеющей широкий комплекс QRS, это снижение составило 46,2%. Число амбулаторных обращений снизилось на 35,5% по сравнению с общей группой использующих в своем лечении только медикаментозную терапию и на 46,6% по сравнению с подгруппой с широким комплексом QRS.
Число вызовов неотложной помощи в подгруппе с КРСУ снизилось на 68,3% по сравнению с группой получающей медикаментозную терапию и на 74,2% среди пациентов с электрическим асинхронизмом.
Использование бивентрикулярной стимуляции, приводящее к восстановлению внутрижелудочкового синхронизма сопровождается снижением частоты обращаемости за медицинской помощью по сравнению с медикаментозной терапией как в целом по группе, так и среди пациентов с электрически асинхронизмом.
При проведении сердечной ресинхронизирующей терапии с использованием бивентрикулярной стимуляции, восстановление внутрисердечного синхронизма сопровождалось улучшением систолической и диастолической функции миокарда. Так совокупный показатель систолической функции ФВ достоверно был выше через год в группе с установленным КРСУ, составляя 43,4% по сравнению с 30,3% в группе пациентов с широким комплексом QRS, получающих только медикаментозную терапию. Индекс сферичности (ИС) как маркер ремоделирования, также на фоне СРТ претерпевал обратное развитие, составляя 0,720,15 по сравнению с исходным значением 0.810,1. В группе больных с широким комплексом QRS через год ИС увеличился до 0,890,1 по сравнению с исходным значением – 0,760,15, это свидетельствует о том, что форма ЛЖ приближалась к форме шара. Показатель соотношения скорости раннего пика (Е) диастолического трансмитрального потока и скорости диастолического движения фиброзного кольца митрального клапана (em) E/em на прямую отражает конечно диастолическое давление в левом желудочке и является маркером диастолической функции ЛЖ. При использовании СРТ этот показатель снижается, достигая через год 8,81,4, по сравнению с исходным значением 13,81,2. В группе пациентов с широким комплексом QRS, получающих медикаментозную терапию значение этого показателя остается высоким 10,71,1, исходно его величина составляла 12,31,6.
^ 4.3. Качество жизни больных с ХСН с установленным кардиоресинхронным устройством
Через два месяца после установки кардиоресинхронизирующего устройства у пациентов достоверно увеличились показатели параметров качества жизни во всех шкалах, соответствующих как физическим, так и эмоциональным компонентам качества жизни (p<0,01).
Через 12 месяцев показатели качества жизни снизились по всем шкалам, характеризующих как физическое, так и эмоциональное состояние больных, но были достоверно выше как исходных показателей (p<0,05), так и показателей, полученных спустя 2- месяца после установки кардиоресинхронизирующего устройства. Через 36 месяцев (3 года), показатели качества жизни оставались достоверно более высокими по сравнению с исходными значениями.
^ 4.4 Корреляционный анализ гемодинамических показателей и внутрисердечного асинхронизма при использовании СРТ у больных ХСН.
Для определения дополнительных критериев при отборе пациентов для проведения СРТ мы провели корреляционный анализ гемодинамических показателей и показателей внутрисердечного асинхронизма у больных ХСН, которым в качестве метода лечения проводилась сердечная ресинхронизирующая терапия.
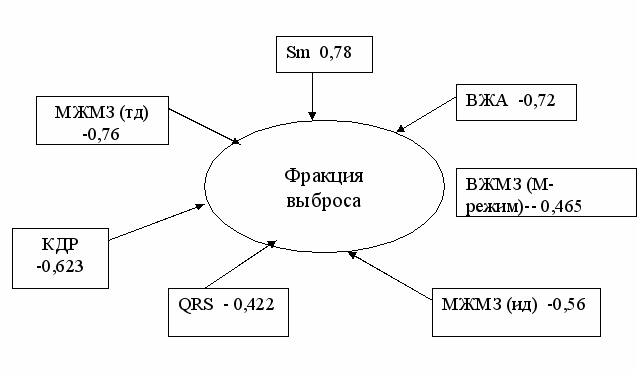
^ Рис. 1 Корреляционные связи фракции выброса ЛЖ и показателей асинхронизма
Основным показателем, отражающим состояние гемодинамики, мы выбрали величину фракции выброса, рассчитанную методом Симпсона. Снижение фракции выброса имло сильную отрицательную связь с коэффициентом более 0,7 с такими показателями асинхронизма как межжелудочковая механическая задержка (метод тканевой допплерографии), внутрижелудочковая диссинхрония (метод тканевой допплерографии), а так же сильную положительную связь с показателем, отражающим систолическую скорость движения продольных волокон миокарда левого желудочка (метод тканевой допплерографии).
Средняя, устойчивая отрицательная связь показателя фракции выброса с коэффициентом корреляции больше 0,5 отмечена с показателями межжелудочковой механической задержки, определяемыми при обычной импульсной допплерографии, а так же величиной конечно-диастолического размера ЛЖ.
Средняя отрицательная связь выявлена с межжелудочковой механической задержкой (М-режим ЭхоКг) - коэффициент 0,465 и комплексом QRS - коэффициент 0,422.
Корреляционный анализ – это всего лишь математическая модель. Выявляемые при его проведении связи между показателями формальны и интерпретация полученных результатов носит дискуссионный характер. Тем не менее, этот метод статистической обработки позволил нам предположить относительную силу этих взаимоотношений.
Так при проведении анализа полученные данные могут свидетельствовать о важности оценки указанных показателей внутрисердечного асинхронизма для отбора больных ХСН на СРТ. Причем совершенно очевидно, что приоритет следует отдать параметрам, которые определяются с использованием тканевой допплерографии.
Выполненный дискриминантный анализ зависимости прироста ФВЛЖ у больных ХСН на фоне КРСУ от исходных значений внутрисердечного асинхронизма позволил уточнить показатели асинхронизма и их значения, при которых целесообразна коррекция с помощью бивентрикулярной электрокардиостимуляции.
С этой целью пациенты были классифицированы на 2 группы: с более высоким увеличением сократимости ЛЖ и с менее высоким (p<0,01). В результате были получены критические значения для каждого из показателей: межжелудочковая механическая задержка по разнице потоков в легочной артерии и аорте – 40 мс, межжелудочковая механическая задержка по сумме систолических скоростей движения миокарда базальных сегментов правого и левого желудочков – более 100 мс.
4.4. Выбор режима и определение параметров ресинхронизирующей электрокардиостимуляции у больных хронической сердечной недостаточностью с помощью эхокардиографических методик.
В процессе наблюдения за больными с имплантированными электрокардиостимуляторами необходим подбор оптимальных параметров стимуляции.
Современные устройства для кардиоресинхронной терапии позволяют подбирать предсердно-желудочковую и межжелудочковую задержки. В первом случае создают оптимальные условия для диастолического наполнения ЛЖ, а во втором – для сердечного выброса. Неадекватный подбор параметров стимуляции может привести к прогрессированию как СДЛЖ, так и ДДЛЖ, что будет сопровождаться нарастанием явлений ХСН.
При оптимизации АВ-задержки мы стремились достичь временных параметров, позволяющих максимально наполнить левый желудочек, обеспечить сокращение желудочков сразу после сокращения предсердий. Подбор АВ-задержки осуществлялся с использованием формулы Риттера, оценки трансмитрального потока и определению времени наполнения левого желудочка. Оптимальной считалась АВ-задержка при которой соотношение пиков трансмитрального потока приближалось к физиологическому, а время наполнения левого желудочка не превышало 40% от всего сердечного цикла. Подбор AV-задержки позволил увеличить ФВЛЖ на 15,2%, а диастолическую скорость движения фиброзного кольца МК (Em) на 37,2%. Проведенное исследование доказывает тот факт, что оптимизация АВ-задержки в большей степени влияет на диастолическую дисфункцию, чем на систолическую. Проведенный нами корреляционный анализ позволил выявить связи оптимальной предсердно-желудочковой задержки, определенной по методу Риттера, с другими ультразвуковыми показателями. Сильные прямые связи с коэффициентом корреляции 0,84 были выявлены с интегралом линейной скорости трансмитрального потока (VTI ТМК) и диастолической скоростью движения продольных волокон миокарда левого желудочка Em с коэффициентом – 0,74. Систолические показатели не обладали значимыми корреляционными связями с оптимальной AV задержкой.
Подбор межжелудочковой задержки осуществлялся методом вычисления разницы интервалов от начала комплекса QRS до начала потока в аорте и легочной артерии – не более 40 мс и задержки движения латеральной стенки левого желудочка относительно межжелудочковой перегородки - не более 40 мс.
Оптимизация VV-задержки позволила увеличить ФВЛЖ на 20,8%, а систолическую скорость движения волокон миокарда ЛЖ Sm на 47,3%. Корреляционные связи оптимальной межжелудочковой задержки с другими ультразвуковыми показателями выглядили следующим образом: сильная связь с систолической скоростью движения продольных волокон миокарда левого желудочка (Sm) и ФВ левого желудочка, коэффициент корреляции 0,78 и 0,76 соответственно. Связь с диастолической скоростью движения продольных волокон миокарда левого желудочка Em слабая , коэффициент корреляции 0,26.
Показатели корреляционного анализа могут свидетельствовать о возможности применения показателей VTI ТМК и Em для оптимизации AV задержки, а Sm и ФВЛЖ – для оптимизации VV задержки.
У пациентов с хронической формой фибрилляции предсердий подбор АВ-задержки невозможен. Подбор межжелудочковой ресинхронизации не отличается от такового в группе пациентов с синусовым ритмом.
^ 4.5 Летальность в группе пациентов с сердечной ресинхронизирующей терапией.
Предложенный нами отбор пациентов для проведения сердечной ресинхронизирующей терапии и подбор оптимальных параметров стимуляции привел к тому, что за 3 года наблюдения летальность составила 10,0%. За время наблюдения в группе больных с установленным КРСУ умерло 4 человека (10%). Смерти произошли через 1, 4, 5 и 11 месяцев после имплантации кардиостимулятора. У трех пациентов была выявлена фибрилляция желудочков (ФЖ) и смерть расценивалась как внезапная. У 1 пациента развился повторный крупноочаговый инфаркт миокарда. По данным многоцентровых исследований годичная выживаемость составляет 70,0-75,0%.
Использование сердечной ресинхронизирующей терапии с помощью бивентрикулярной электрокардиостимуляции, в дополнение к медикаментозной терапии, положительно влияет на клинику, течение и прогноз хронической сердечной недостаточности за счет комплексного воздействия на внутрисердечный асинхронизм, систолическую и диастолическую функции левого желудочка. Она расширяет возможности современного лечения больных ХСН.
ВЫВОДЫ
У больных хронической сердечной недостаточностью, с установленными показаниями для имплантации искусственного водителя ритма, возможна установка только физиологического двухкамерного электрокардиостимулятора. Использование однокамерной желудочковой стимуляции приводит к прогрессированию ХСН уже через год после имплантации. Эффективность медикаментозной терпи достоверно выше, чем данный режим стимуляции.
- Использование стресс-эхокардиографии с последовательным увеличением частоты стимуляции установленного электрокардиостимулятора для подбора параметров стимуляции приводит к улучшению динамики ХСН. Это сопровождается улучшением качества жизни, уменьшением частоты госпитализаций, обращаемости за медицинской помощью и потребности перепрограммировании ЭКС, снижением смертность от сердечно-сосудистых причин и увеличением выживаемости не зависимо от режима стимуляции.
- У больных с ИБС после имплантации искусственного водителя ритма изменяется клиническое проявление болезни, типичный болевой синдром встречается в 22,7% случаев. Использование стресс-эхокардиографии позволяет на ранних этапах выявить прогрессирование коронарной недостаточности, подобрать адекватный режим стимуляции и терапии. У пациентов с синдромом ЭКС в 38% случаев за клинической картиной синдрома скрывается прогрессирование и развитие ИБС..
- Наличие внутрисердечного асинхронизма у больных с ХСН приводит к прогрессированию заболевания, снижению качества жизни и выживаемости.
- Выявление увеличения внутрижелудочковой механической задержки свыше 100 мс в М-режиме при транторакальной эхокардиографии в покое является показанием к проведению тканевой допплерографии миокарда для своевременного выявления внутрисердечного асинхронизма.
- Сердечная ресинхронизирующая терапия с использованием бивентрикулярной электрокардиостимуляции по сравнению с медикаментозным лечением восстанавливает внутрижелудочковый синхронизм, что сопровождается длительной (в течение 3 лет) положительной динамикой ХСН, снижением частоты госпитализаций и обращаемости за медицинской помощью, улучшением качества жизни, и повышением выживаемости.
- Использование сердечной ресинхронизирующей терапии приводит к улучшению и/или восстановлению параметров внутрисердечного асинхронизма. Параметры электромеханического внутрисердечного асинхронизма, определяемые с использованием эхокардиографии такие как механическая межжелудочковая задержка (по данным импульсной и тканевой допплерографии) и индекс внутрижелудочкового асинхронизма в большей степени связаны с эффективностью ресинхронизирующей терапии, чем ширина комплекса QRS.
- Использование импульсной и тканевой допплерографии миокарда с оценкой скоростных и временных показателей трансмитрального, трансаортального потока и движения фиброзного кольца митрального клапана позволяет подобрать оптимальные параметры стимуляции при проведении сердечной ресинхронизирующей терапии.
