Хронические перикардиты как проявление универсальной иммуно-воспалительной реакции: диагностика и прогнозирование клинико-морфологических вариантов 14. 00. 06 кардиология
| Вид материала | Автореферат |
- Лекция «Синдром легочного инфильтрата. Тактика ведения больных с внебольничной и нозокомиальной, 95.95kb.
- Нежелательные лекарственные реакции у детей как проявление мутации генов, кодирующих, 405.53kb.
- Синдром системной воспалительной реакции и метаболическая функция легких, 493.51kb.
- Обучающая программа Конгресса Школы для практикующих врачей по специальностям Кардиология, 109.72kb.
- Современные проблемы аллергодиагностики, 181.67kb.
- Томского Научного Центра со рамн автореферат, 725.4kb.
- Тематический план лекций по внутренним болезням и сестринскому делу в терапии для студентов, 52.51kb.
- Расписание занятий по курсу госпитальной терапии, 138.36kb.
- Тема 7 «Диагностика системы менеджмента организации», 397.43kb.
- Пособие для студентов IV,V,VI курсов, интернов, клинических ординаторов и врачей, 718.65kb.
Взаимосвязь этиологии и характера течения перикардита
Проведенное исследование является репрезентативным по этиологическому признаку, так как в нем представлены все основные этиологические формы (табл.3), входящие в Маргбургский регистр перикардитов (Европейские рекомендации по диагностике и лечению заболеваний перикарда, 2004).
Таблица 3
Сравнение этиологии перикардита по данным Маргбургского регистра
и изучаемой группы
| Этиология | Данные Маргбургского регистра, % | Данные изучаемой группы, % |
| I Инфекционные перикардиты 1. Вирусный 2. Бактериальный (в т.ч. туберкулезный) 3. Грибковые и паразитарные Всего: | 30-50 5-10 Низкая заболев 35-60 | 21,0 20,0 1 42,0 |
| II Неинфекционные перикардиты | | |
| 1. Метаболические - мекседема - уремия - беременность 2. Перикардиты при системных и аутоиммунных заболеваниях - ревматоидный артрит - СКВ - анкилозирующий спондилоартрит 3. При аутоиммунных процессах второго типа - постперикардиотомный - постинфарктный - при лекарственной и сывороточной болезни - аутореактивный 4. Травматический перикардит - при прямом повреждении - при непрямом повреждении - после облучения средостения 5. Опухолевые перикардиты - первичные опухоли перикарда - метастатические опухоли перикарда - при лейкемии и лимфоме - паранеопластический перикардит Всего: | Высок. заболев. 23,1 Низкая заболев. 35 Низкая заболев. Высокая забол. Высокая забол. 58,10 | 2,1 14,4 8,7 34,4 |
| III Идиопатический перикардит | 3,5-50 | 23,6 |
В
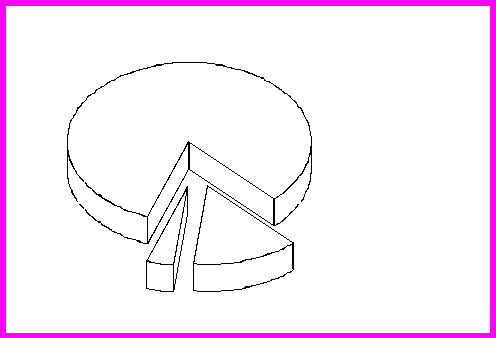
 ходе анализа этиологической структуры перикардитов выявлена зависимость характера течения перикардита от причин заболевания (рис. 2). Острые перикардиты имели достоверное преобладание инфекционных причин (46 наблюдений) над неинфекционными (8 наблюдений) и идиопатическими (2 случая). Хронические перикардиты формировались преимущественно под влиянием неинфекционных (59 – 42,4%) факторов или носили идиопатический характер (44 – 31,7%), реже имели инфекционный генез (36 – 25,9%).
ходе анализа этиологической структуры перикардитов выявлена зависимость характера течения перикардита от причин заболевания (рис. 2). Острые перикардиты имели достоверное преобладание инфекционных причин (46 наблюдений) над неинфекционными (8 наблюдений) и идиопатическими (2 случая). Хронические перикардиты формировались преимущественно под влиянием неинфекционных (59 – 42,4%) факторов или носили идиопатический характер (44 – 31,7%), реже имели инфекционный генез (36 – 25,9%).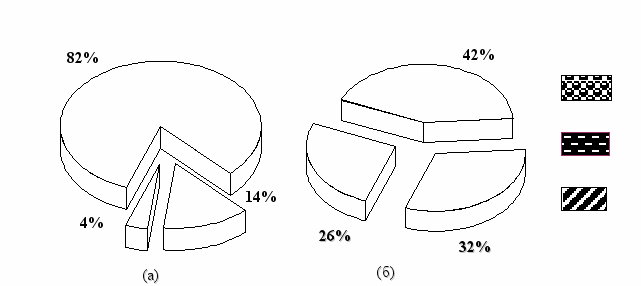
–
– инфекционные
–
– не инфекционные
–
– идиопатические
Рис. 2. Взаимосвязь этиологии и течения перикардитов
(а) – острое течение; (б) – хроническое течение
В группе неинфекционных перикардитов выявлено достоверное преобладание хронических форм (р<0,001), также как и в группе идиопатических (р<0,001).
Среди этиологических факторов, входящих в группу неинфеционных перикардитов, можно отметить превалирование заболеваний, протекающих с участием аутоиммунных механизмов. Нозологические формы, имеющие в своей основе аутоиммунные механизмы, вошли в подгруппы: аутоиммунных и системных заболеваний (ревматоидный артрит, СКВ, анкилозирующий спондилоартрит), аутоиммунных процессов второго типа (постперикардиотомный и постинфарктный синдромы, лекарственная и сывороточная болезнь, аутореактивный перикардит), травматических перикардитов, а также паранеопластических в составе опухолевых перикардитов. Таким образом, результаты проведенного исследования показали достоверное преобладание хронических перикардитов в этиологических группах, включающих заболевания, патогенез которых обусловлен аутоиммунными процессами.
Изучение клинико-морфологических вариантов острых и хронических заболеваний сердечной сорочки, показало, что экссудативные перикардиты чаще наблюдались при острых формах заболевания (р<0,001), а адгезивные (р<0,001) и констриктивные (р<0,01) – при хронических. Таким образом, продуктивное воспаление являлось определяющим при хронических перикардитах.
Течение острых и хронических перикардитов осложнилось констрикцией камер сердца в 84 наблюдениях (43,1%): острых перикардитов – в 20 случаях (35,7%), хронических – в 64 (46%), разница по числу осложнений не достоверна (p<0,2). По характеру констрикции при остром и хроническом процессах выявлено достоверное отличие (р<0,001): эластическая форма встречалась только при острых перикардитах, ригидная и смешанная – при хронических.
Изучение этиологии перикардита показало, что любой из инфекционных и неинфекционных факторов мог служить причиной как острого перикардита, так и хронического. Результаты нашего наблюдения совпадают с данными литературы о том, что при перикардитах этиология играет роль лишь запускающего фактора, в последствии заболевание приобретает течение, не зависящее от его первопричины (Амосова Е.Н., 2005). Это положение было подтверждено фрагментом нашей работы, посвященной проблеме перикардитов, вызываемых ассоциацией этиологических факторов. В группу перикардитов с многофакторным поражением перикарда вошли 48 (24,6%) наблюдений.
А
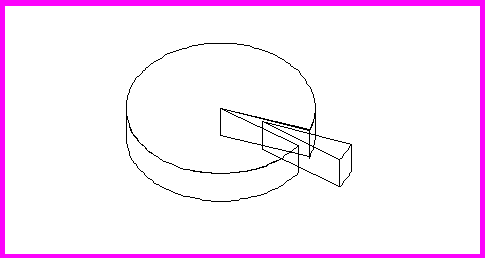 ссоциация этиологических факторов послужила причиной острого перикардита в двух случаях, что составило 3,6% острого воспаления сердечной сорочки (рис. 3). Остальные 46 наблюдений относились к хроническому воспалению серозной оболочки сердца и представили 33,1% от всей группы хронических перикардитов. Хронические перикардиты формировались при участии ассоциации этиологических факторов достоверно чаще, чем острые (p<0,001).
ссоциация этиологических факторов послужила причиной острого перикардита в двух случаях, что составило 3,6% острого воспаления сердечной сорочки (рис. 3). Остальные 46 наблюдений относились к хроническому воспалению серозной оболочки сердца и представили 33,1% от всей группы хронических перикардитов. Хронические перикардиты формировались при участии ассоциации этиологических факторов достоверно чаще, чем острые (p<0,001).96% - хроническое
4% - острое
Рис. 3. Течение перикардита при многофакторном поражении
В результате анализа структуры причин перикардита в группе с многофакторным поражением серозной оболочки сердца выявлено 8 запускающих и 6 провоцирующих этиологических факторов (табл. 4). В роли запускающих этиологических факторов инфекционные и неинфекционные выступали одинаково часто: в 22 (45,8%) наблюдениях первопричиной служили инфекционные, а в 26 (54,2%) - неинфекционные. В структуре запускающих факторов наибольшее значение имел туберкулез среди инфекционных причин (68,2%) и травма перикарда - среди неинфекционных (50%), что отражает особенности этиологической структуры перикардитов в проведенном исследовании. В группу больных с многофакторным поражением перикарда вошли пациенты, страдавшие в анамнезе туберкулезным перикардитом, то есть токсико-аллергическим поражением серозной оболочки сердца. Таким образом, среди инфекционных и неинфекционных первопричин преобладали заболевания, протекавшие на фоне измененного иммунного ответа.
Таблица 4.
Значения этиологических факторов при многофакторном поражении перикарда
| Этиологические факторы | Запускающие | Разрешающие |
| Туберкулез | 34% | – |
| Травма | 25% | 10% |
| Вирусная инфекция | 15% | 68% |
| Лекарственная болезнь | 8% | 10% |
| Лейкемия | 10% | – |
| Инфаркт миокарда | 2% | 4% |
| Уремия | 2% | – |
| Системные заболевания | 4% | – |
| Бактериальная инфекция | – | 2% |
| Микседема | – | 6% |
| Итого: | 100% | 100% |
В структуре провоцирующих факторов превалировали инфекционные – в 32 (66,7%) случаях, неинфекционные встретились в 16 (33,3%) наблюдениях (p<0,002). Причем наибольшее значение в рецидивировании хронических перикардитов имела вирусная инфекция (p<0,005). Среди неинфекционных разрешающих факторов достоверного преобладания какого-либо из них не выявлено.
В проведенном исследовании чаще наблюдалось сочетание инфекционных и неинфекционных причин — в 31 (66,7%), ассоциация двух инфекционных факторов встретилась в 10 (22,9%) случаях, неинфекционных – в 5(10,4%). Запускающие этиологические факторы объединяет измененный иммунный ответ, который может иметь значение при повторном воздействии уже другого этиологического фактора. Варианты сочетаний этиологических показаны на рис. 4.
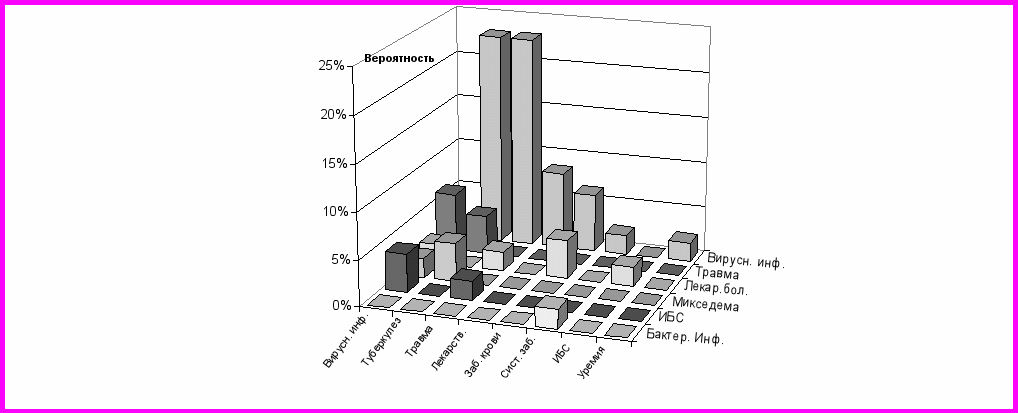
Разрешающие
Запускающие
Рис. 4. Варианты сочетаний этиологических факторов
Результаты изучения перикардитов с многофакторным поражением перикарда важных не только для понимания патогенеза хронического перикардита, имеют большое практическое значение. Перикардиты, вызванные ассоциацией этиологических факторов резистентны к стандартным схемам лечения. Уточнение причин обострения хронического перикардита позволяет выбрать адекватную лечебную тактику и определить поддерживающую терапию.
Обращаясь к роли этиологических факторов в формировании хронического воспаления листков перикарда, необходимо учитывать специфику региональной этиологической структуры перикардитов. Результаты проведенного исследования свидетельствуют об особенностях этиологической структуры перикардитов у жителей Свердловской области в сравнении с данными Маргбургского регистра перикардитов. По данным Маргбургского регистра в структуре инфекционных перикардитов туберкулезные совместно с другими бактериальными поражениями перикарда составили 5-10%, тогда как в изучаемой группе на долю туберкулезного поражения перикардитов пришлось 16,4% всех случаев заболевания и 39% инфекционных перикардитов. Существенное влияние туберкулезной инфекции на этиологическую структуру перикардитов у жителей Свердловской области вызвано неблагоприятной эпидемической обстановкой.
Другой многочисленной этиологической группой, обусловившей особенности этиологической структуры перикардитов у жителей Свердловской области, явились травматические перикардиты – 28 наблюдений, на долю которых пришлось 14,4% от всей изучаемой группы и 41,8% от общего числа неинфекционных поражений перикарда. Травма перикарда закончилась формированием хронического перикардита в 23 (82,1%) случаях травматических поражений перикарда. Травматические хронические перикардиты протекали в двух вариантах: в виде отдаленной перикардиальной реакции на травму, имеющей черты аутоиммунного процесса, – 14 наблюдений и в виде субклинически протекающего адгезивного перикардита с исходом в констриктивный процесс – 9 наблюдений.
Названные этиологические формы перикардитов имели как самостоятельное значение в развитии хронических перикардитов, так и играли определяющую роль в формировании перикардитов сочетанной этиологии.
Характеристика хронических перикардитов по лабораторным
показателям, данным гистоморфологии и результатам
инструментальных методов исследования
Значение и роль этиологических факторов в формировании хронического воспаления серозной оболочки сердца, а также преобладание продуктивного воспаления при хронических перикардитах позволили предположить определяющую роль иммунной системы как в формировании хронического перикардита, так и в возникновении рецидивов заболевания. Для характеристики иммунного ответа исследованы иммунограмма (табл. 5) и показатели цитокиновой системы у больных с различным течением перикардита.
Таблица 5
Показатели иммунного статуса у больных перикардитом
| Показатель (единицы измерения) | Больные перикардитом М ± m, n=195 | Контрольная группа М ± m, n=50 | Значимость |
| Т-лимфоциты, (%) В-лимфоциты, (%) НСТ спонтанный, % НСТ стимулированный, % Индекс стимуляции ИГ А, г/л ИГ М, г/л ИГ G, г/л ЦИК, усл.ед. Антитела к ДНК, усл. ед. | 62,89 ± 0,98 13,38 ± 0,53 28,00 ± 1,57 35,79 ± 1,42 1,49 ± 0,07 2,28 ± 0,14 1,44 ± 0,07 10,76 ± 0,45 110,47± 7,01 0,33 ± 0,004 | 56,34 ± 1,27 8,05 ± 0,98 16,27 ± 3,36 47,36 ± 6,2 4,1 ± 1,2 1,9 ± 0,15 0,89 ± 0,07 10,75 ± 0,37 48,4 ± 3,64 0,1 ± 0,001 | <0,005 <0,001 >0,05 >0,05 <0,001 >0,05 <0,005 >0,05 <0,001 <0,001 |
У больных перикардитом в сравнении с контрольной группой обнаружена тенденция к повышению уровней Т-лимфоцитов (p<0,005) и В-лимфоцитов (p<0,001) в пределах референтных интервалов, найдены достоверно более низкие показатели индекса стимуляции НСТ-теста (p<0,001). Указанные изменения показателей клеточного иммунитета у больных перикардитом можно объяснить «напряжением» клеточного иммунитета при снижении фагоцитарного резерва нейтрофилов. Средние значения иммуноглобулинов не отличались от таковых в контрольной группе, кроме ИГМ, показатели которого были выше, чем в контрольной группе (p<0,002). В сравнении с контрольной группой изменения иммунограммы у больных перикардитами включали достоверное повышение средних показателей ЦИК (p<0,001) и антител к ДНК (p<0,001). Что свидетельствовало об участии аутоиммунных механизма в патологии сердечной сорочки. В исследовании не выявлено достоверных различий показателей иммунного статуса у больных разных этиологических групп.
С целью оценки регуляции иммунитета исследованы показатели цитокиновой системы сыворотки крови 31 больного: 14 – инфекционным перикардитом, 6 – неинфекционным, 5 – идиопатическим, 6 – перикардитом сочетанной этиологии. В число изучаемых цитокинов вошли: провоспалительный интерлейкин ИЛ-1 альфа, противовоспалительные интерлейкины ИЛ-4 и РАИЛ-1альфа, а также ИНФ-гамма (табл. 6)..
Таблица 6
Показатели интерлейкинов у больных перикардитом
| Показатель (единицы измерения) | Больные перикардитом М ± m, n=31 | Контрольная группа М ± m, n=20 | Значимость |
| ИЛ-1 альфа, пг/мл ИЛ-4, пг/мл РАИЛ-1, пг/мл Интеферон-гамма, пг/мл | 0,98 ± 0,32 14,35 ± 1,97 420 ± 36,32 18,71 ± 11,87 | 5,53 ± 3,32 48,98 ± 6,47 680,39 ± 248,55 20,11 ± 6,52 | <0,001 <0,001 <0,001 <0,01 |
В группе больных перикардитом в сравнении с контрольной группой обнаружено достоверное снижение уровней противовоспалительных интерлейкинов ИЛ-4, РАИЛ-1 альфа и ИНФ-гамма. Выявленные особенности системы регуляции иммунитета у больных перикардитом объясняют формирование хронической формы воспаления при недостатке противовоспалительных интерлейкинов, а повышение концентрации ИНФ-гамма свидетельствует о стимуляции фагоцитарной активности, что соответствует изменениям клеточного звена иммунитета. Низкие концетрации провоспалительного цитокина ИЛ-1 альфа мы связываем с ингибированием ИЛ-альфа белками крови на фоне воспалительной реакции.
Сравнение показателей цитокиновой системы у больных с различным течением процесса показало достоверные отличия концентраций РАИЛ-1альфа в группах с тяжелым и субклиническим вариантами хронического процесса, а также с острым воспалением серозной оболочки сердца (табл. 7). Тяжелое течение хронического перикардита ассоциировалось с концентрациями РАИЛ-1 альфа 208± 17,8 пг/мл, в то время как нормальные его значения составляют 350-700 пг/мл. В наблюдениях с субклиническим течением хронического перикардита, средние показатели РАИЛ-1 имели нормальное значение - 444± 32,7 пг/мл. При остром течении перикардита зарегистрированы значения РАИЛ-1, близкие к верхней границе нормы. Полученные результаты позволяют рекомендовать использование показателей РАИЛ-1 для определения характера течения перикардита. Концентрации других цитокинов не имели достоверных отличий в группах больных с различным характером течения процесса.
Таблица 7
Показатели цитокинов сыворотки крови в группах больных острым
и хроническим перикардитом
| Интерлейкины, (пг/мл) | Хронический перикардит, тяжелое течение M±m, (n= 9) | Хронический перикардит, субклиническое течение M±m, (n= 17) | Острый перикардит M±m, (n= 5) | Значимоcть |
| ИЛ-1 альфа ИЛ-4 Интерферон-гамма РАИЛ-1 | 1,11±0,807 14,2± 3,58 42,2± 38,6 208± 17,8 | 0,706±0,361 13,2± 2,49 2,65± 2,65 444± 32,7 | 1,6±0,678 18,6± 6,74 31± 24,2 750± 67,1 | p12>0,05 p13>0,05 p23>0,05 p12>0,05 p13>0,05 p23>0,05 p12>0,05 p13>0,05 p23>0,05 p12<0,001 p13<0,001 p23<0,001 |
Оценка системного воспалительного ответа у больных перикардитом определялась с учетом содержания острофазовых реактантов: титра комплемента и С-РП. Выявлены значительные колебания показателей С-РП в крови больных перикардитом: от нормальных у больных с давним хроническим перикардиальным выпотом до высоких (768 мг/л) у пациентов с острыми формами заболевания. Средние показатели С-РП, определенные с использованием непараметрического критерия Манна – Уитни составили 42,48 ± 13,24 мг/л, имея достоверные отличия от контрольной группы (р<0,001). Активность системы комплемента незначительно варьировала у пациентов (от 29,2 до 64 усл. ед.), но средние показатели (47,01±0,64 усл.ед.) достоверно отличались от таковых в контрольной группе (p<0,001). Таким образом, выявлена высокая информативность показателей острофазовых реактантов в изучаемой группе для оценки воспалительного ответа, независимо от характера течения заболевания.
Доказательством того, что течение перикардита определяется не столько этиологией, хотя, безусловно, зависит от нее, сколько реактивностью организма, стало сравнение показателей иммунитета между группами больных, имевших проявления перикардита на фоне полисерозита (8 наблюдений), и с изолированным перикардитом (187 наблюдений).
Группа больных полисерозитом немногочисленна, но представлена, как и группа сравнения, инфекционными (туберкулезным и герпетическим) и неинфекционными (при ревматоидном артрите, системной красной волчанке, аутореактивный перикардит) поражениями перикарда. В ходе исследования выявлено, что все больные, имевшие признаки поражения перикарда на фоне полисерозита, имели существенные сдвиги показателей гуморального иммунитета и выраженное повышение уровня С-РП (табл. 8) в сравнении с аналогичными показателями в группе пациентов с изолированным перикардитом: ИГА – в 1,7 раза (р<0,05), ИГМ – в 2 раза (p<0,001), С-РП – в 22,4 раза (p<0,001), ЦИК – в 3,2 раза (p<0,001), антитела к ДНК – в 2,3 раза (p<0,05).
Таблица 8
Показатели С-РП и иммунитета в группах больных перикардитом, являющихся проявлением полисерозита, и изолированным перикардитом
| Показатели | Перикардит при полисерозите (M ± m), n=8 | Изолированный перикардит (M ± m), n=187 | Значимоcть |
| С-РП, мг/л НСТ СП, % НСТ СТ, % Индекс стимуляции ИГ А, г/л ИГ М, г/л ИГ G, г/л ЦИК, ед. АТ ДНК усл. ед. | 514± 93,1 38,1± 1,9 44,8± 2,4 1,17± 0,01 3,76± 0,71 2,68± 0,42 12,1± 0,42 302± 10,1 0,069± 0 | 23,1 ± 7,2 27,1 ± 1,7 35 ± 1,5 1,51± 1,1 2,18± 0,138 1,36±0 ,068 10,7 ± 0,48 95,3 ± 5,04 0,03±0 ,005 | p12<0,001 p12>0,05 p12>0,05 p12>0,05 p12<0,05 p12<0,001 p12>0,05 p12<0,001 p12<0,05 |
Следовательно, характер поражения серозных оболочек – ограниченный (изолированный перикардит) или генерализованный (полисерозит) – определялся не этиологическим фактором, а зависел от иммуно-воспалительного ответа на причину заболевания. В случаях полисерозита наблюдалась активная воспалительная реакция, характеризующаяся существенным возрастанием уровней С-РП, иммуноглобулинов классов А и М, ЦИК. Изолированное поражение перикарда сопровождалось более низкими концентрациями С-РП и иммуноглобулинов классов А, М и ЦИК в сравнении с изменениями этих показателей при полисерозите.
Таким образом, анализ изменений лабораторных показателей в группе больных перикардитом подтвердил, что течение перикардита в большей степени зависит от характера иммуно-воспалительной реакции, чем от этиологии.
С целью анализа зависимость воспалительных изменений перикарда от этиологии заболевания и выявления особенностей воспалительных изменений перикардиальных листков проведено исследование морфологического материала. Результаты морфологического анализа операционного материала показали, что в подавляющем большинстве случаев (в 25 из 27 – 92,6%) морфологическая картина при перикардите носила неспецифический характер и не зависела от этиологии заболевания (табл. 9). Только в двух наблюдениях при карциноматозе перикарда и аутореактивном перикардите морфологические изменения отличались по характеру клеточной инфильтрации, что позволило выделить их в особые формы перикардита.
Таблица 9.
Гистоморфология листков перикарда и прилежащих тканей
(операционный материал)
| Морфологическая картина | N, (%) | инфильтрация | сосудистая реакция | соединитель ная ткань |
| 1.Рецидивирующее воспаление 2.Затухающее воспаление 3.Исход воспаления 4.Особые формы перикардита | 14 (51,9%) 4 (14,8%) 7 (25,9%) 2 (7,4%) | полиморфно-клеточная (нейтрофилы, лимфоциты, плазмоциты, гистиоциты) мононуклеарная (лимфоциты, плазмоциты, моноциты) не выявлена | капиллярит с экссудативным компонентом продуктивный капиллярит артериоло-склероз | зрелая волокнистая с признаками гиалиноза и кальциноза в 9 наблюдениях зрелая с гиалинозом зрелая с признаками склероза, гиалиноза, кальциноз во всех препаратах |
| Итого | 27 (100%) | | | |
Суть неспецифических изменений определялась состоянием соединительной ткани, наличием клеточной инфильтрации, сосудистой реакцией и присутствием кальциноза. Сосудистая реакция и клеточная инфильтрация манифестировали воспалительный процесс в листках перикарда. Активная воспалительная реакция проявлялась лейкостазом, экссудативным компонентом и полиморфно-клеточной инфильтрацией, включавшей нейтрофилы, лимфоциты, плазмоциты, гистиоциты. При затихании воспаления инфильтрация была представлена мононуклеарными клетками: лимфоцитами, плазмоцитами, моноцитами. Сосудистая реакция наблюдалась при активном рецидивирующем и затухающем воспалении и проявлялась продуктивным капилляритом.
Результаты гистоморфологического исследования свидетельствовали, что констриктивный перикардит в 70,3% наблюдений протекал на фоне активного или стихающего воспаления в листках перикарда. В исследуемых фрагментах перикарда присутствовали признаки хронического воспаления и изменения, свойственные рецидиву воспалительного процесса.
Воспаление перикардиальных листков, проявлявшееся клеточной инфильтрацией, продуктивным капилляритом и отеком межуточкой ткани, не ограничивалось перикардиальными листками, а распространялись на жировую ткань, располагающуюся под эпикардом, и субэпикардиальные слои миокарда. Причем признаки продуктивного воспаления в жировой ткани выражены не менее, а в некоторых препаратах даже более чем в серозной оболочке сердца. Вовлечение в воспалительный процесс жировой клетчатки, прилежащей к серозной оболочке сердца, проявлялось интенсивной клеточной инфильтрацией и продуктивным капилляритом. Учитывая активную роль жировой ткани в воспалительном процессе (Гитель И.П., Гусев Д.Е., Пономарь Е.Г., 2006) обнаруженные изменения имеют значение в пролонгировании воспалительного процесса при перикардите. Продуктивный капиллярит, охватывающий концевые капилляры ацинозных долек приводит к гипоксии адипоцитов, которые способны продуцировать провоспалительный интерлейкин-6. Интерлейкин-6 регулирует ответ острой фазы воспаления, он является единственным цитокином, стимулирующим синтез всех белков острой фазы воспаления.
Морфологические изменения свидетельствовали о волнообразном течении воспаления в серозной оболочке сердца: одновременно в препаратах присутствовал кальциноз, как свидетельство завершенного воспаления, и морфологические признаки активного и затухающего воспаления перикарда и эпикарда, причем такое сочетание прослеживалось более чем в половине (56,3%) наблюдений.
В доступной нам литературе мы не обнаружили описания того, что воспаление перикардиальных листков вызывает грубые изменения их нервного аппарата (рецепторов и нервных проводников). Найденные изменения объясняют симптомы, возникающие при острых процессах – функциональные нарушения в работе сердца (постоянную, не связанную с нагрузкой тахикардию, изменения артериального давления) и устойчивый болевой синдром. При хронических перикардитах поражение нервно-рецепторного аппарата перикарда приводит к стойкому снижению адаптивной способности миокарда к нагрузкам в условиях адгезивного перикардита, даже если он не носит констриктивный характер. Поражение нервно-рецепторного аппарата перикарда можно рассматривать как одну из причин снижения качества жизни у больных хроническим перикардитом и лиц, перенесших острую форму заболевания.
Хронические формы патологии перикарда проявляются продуктивным воспалением, диагностика которого сложнее, чем экссудативного, независимо от применяемых методов визуализации сердца – ЭхоКГ, КТ, МРТ. Для оценки возможностей ЭхоКГ в диагностике продуктивного воспаления серозной оболочки сердца было проведено сопоставление данных гистоморфологии операционного материала и результатов дооперационных ЭхоКГ-исследований у 27 больных, подвергшихся перикардэктомии.
На основании изучения ультразвукового изображения неизмененных листков перикарда в контрольной группе, нами разработана методика измерения толщины перикардиальных листков, основанная на учете особенностей анатомии и физиологии серозной оболочки сердца. Предложенная методика рекомендует толщину перикарда измерять по передней поверхности сердца перед стенкой правого желудочка, учитывая особенности отражения ультразвука, а для определения утолщения эпикарда, обусловленного продуктивным воспалением и не связанного с морфологическими особенностями здорового эпикарда, мы предлагаем использовать измерение его в области задней стенки сердца, повышая информативность и чувствительность способа. Предложенный способ измерения толщины висцерального листка перикарда обусловлен анатомическими особенностями различных зон висцерального листка. По передней поверхности эпикарда в местах наибольшего контакта с плотными тканями грудины и рёберных хрящей (в области передней поверхности правого желудочка, правого предсердия и по краям правого ушка) в течение жизни формируются реактивные структуры в виде уплотнения поверхностного слоя серозной оболочки, получившие название «сухожильных» или «млечных» пятен (С.С. Михайлов, 1982). В силу описанных особенностей эпикарда передней стенки, при ЭхоКГ-оценке он может выглядеть более ярким и утолщенным, чем эпикард других участков сердца даже у здоровых пациентов.
Проведенные измерения толщин нормальных перикардиальных листков у пациентов с интактными листками сердечной сорочки показал, что перикард у них имеет толщину от 1,5 мм до 1,9 мм, эпикард задней стенки от 1,3 мм до 2,0 мм. Таким образом, толщина неизмененных перикардиальных листков не превышала 2 мм и разница между их толщинами не была достоверна (p<0,1).
По данным ЭхоКГ в группе больных констриктивным перикардитом как перикард, так и эпикард были статистически достоверно утолщены по сравнению с толщиной париетального (р<0,001) и висцерального (р<0,001) листков перикарда у здоровых пациентов. Толщина перикарда у разных больных колебалась от 3,5 мм до 13,1 мм, эпикарда – от 5,8 мм до 16,2 мм. Но во всех случаях толщина эпикарда каждого больного превышала толщину его перикарда. Разность толщин перикардиальных листков в группе больных колебалась от 1,2 мм до 3,1 мм, разница между толщинами перикарда и эпикарда в изучаемой группе и у здоровых пациентов достоверна (р<0,001)
Определяемое предложенным ЭхоКГ-методом утолщение перикардиальных листков свыше 3-4 мм свидетельствует об их продуктивном воспалении. Преобладающее утолщение эпикарда в сравнении с перикардом свойственно констриктивной форме адгезивного перикардита, причем диагностически значимая разница толщины эпикарда и перикарда составляет более 1,2 мм.
Проведенное ранее исследование (Кочмашева В.В., Рождественская Е.Д., 1995) показало, что разницу между толщиной перикарда, полученной путем измерения при проведении ЭхоКГ, и толщиной перикарда по данным морфологического исследования, можно определить с помощью уравнения регрессии:
Толщина перикарда = 0,812 × толщина перикарда (ЭхоКГ) + 0,47
Согласно приведенному уравнению, у больных перикардитом толщина перикарда, измеренная при ультразвуковом исследовании, превышает таковую по данным морфометрии (рис. 5). Анализ зависимости разностей морфометрической и эхокардиографической толщины перикарда (разность 1), с одной стороны, и разностей эхокардиографической толщины перикарда и эпикарда (разность 2), с другой, выявил, что по мере увеличения морфометрической толщины перикарда значения обеих разностей возрастают.
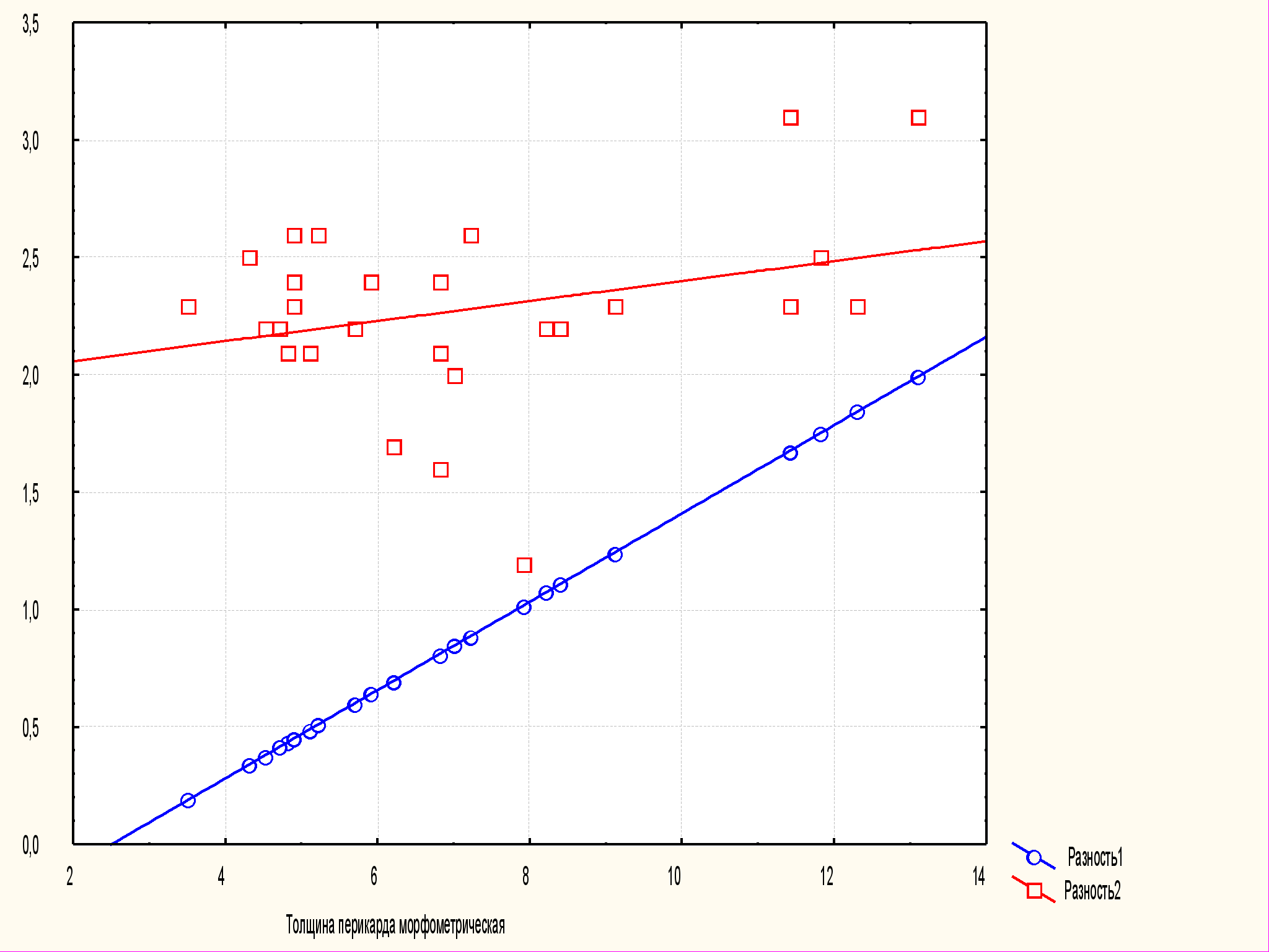
Разность 1 = 0,188×X–0,47
Разность 2 = 0,0426×X+1,9738
Рис. 5. График зависимости разностей толщины эпикарда и перикарда,
определенных с помощью ЭхоКГ, от морфометрической толщины перикарда
(X – морфометрическая толщина перикарда)
Сопоставление данных ЭхоКГ и гистоморфологии показало, что ультразвуковое отражение серозной оболочки сердца при продуктивном воспалении включает в себя не только серозную оболочку, но и слой прилежащих тканей, подвергшийся воспалительной инфильтрации. У больных констриктивным перикардитом слой субэпикардиальных инфильтрированных тканей превышает слой инфильтрированных тканей, прилежащих к перикарду.
Таким образом, проведенное сопоставление морфологических изменений при перикардите и данных ЭхоКГ показало, что ЭхоКГ-исследование позволяет не только выявить признаки продуктивного воспаления листков перикарда, но и диагностировать контриктивную форму хронического перикардита на ранних стадиях. Суть сопоставления заключается в том, что выявляемый при ЭхоКГ утолщенный эпикард, превышающий по толщине перикард, является не истинным эпикардом, а суммарным ультразвуковым отражением, состоящим из сложения отражений воспаленного эпикарда и вовлеченных в воспаление подлежащих тканей, и свидетельствует о выраженном продуктивном воспалении с распространением процесса на подэпикардиальную жировую ткань и эпикардиальные слои миокарда. Таким образом, диагностируемое при ЭхоКГ утолщение эпикарда, преобладающее над толщиной перикарда, является свидетельством отека и клеточной инфильтрации, распространяющихся с серозной оболочки сердца на соседние ткани.
На основе данных, полученных при анализе лабораторных и эхокардиографических показателей, при использовании метода пошагового дискриминантного анализа создана модель прогноза клинико-морфологических вариантов хронического перикардита.
Использование метода пошагового дискриминантного анализа позволило выделить из 128 рассматриваемых клинических, лабораторных и инструментальных признаков семь прогностически значимых (табл. 10). В число прогностически значимых вошли количественные и качественные признаки. Каждый из них имеет как самостоятельное значение в прогнозировании, так и виде сочетаний с другими признаками.
Таблица 10
Прогностические признаки
| Обозначение | Признак (единицы измерения) |
| Х1 Х2 Х3 Х4 Х5 Х6 Х7 | Фракция изгнания × толщина перикарда (мм) Перикардиальные спайки (баллы) × РНПВ (баллы) Объем экссудата (мл) НСТ-тест стимулированный (%) Объем экссудата (мл) × перикардиальные спайки (баллы) Общий белок крови (г/л) В-лимфоциты (× 109/л)× НСТ-тест стимулированный (%) |
Способ прогнозирования клинико-морфологического варианта хронического перикардита состоит в сравнении прогностических индексов, вычисленных для каждого из вариантов по формулам:
DI = X1×V1 + X2×V2+ X3×V3+ X4×V4 +X5×V5+ X6×V6+ X7×V7 – 29,9970
DII = X1×V1 + X2×V2+ X3×V3+ X4×V4 +X5×V5+ X6×V6+ X7×V7 – 15,4811
DIII = X1×V1 + X2×V2+ X3×V3+ X4×V4 +X5×V5+ X6×V6+ X7×V7 – 18,6546
где DI – прогностический индекс экссудативного перикардита, DII – адгезивного, DIII – констириктивного, значения Хn×Vn соответствуют прогностическим признакам, умноженным на прогностические коэффициенты. Наибольшее значение прогностического индекса соответствует прогнозируемому варианту.
Разработанный способ прогнозирования обладает при экссудативном перикардите чувствительностью 94,1%, специфичностью 74,4%; адгезивном – чувствительностью 81,8%, специфичностью 84,4%, констриктивном – чувствительностью 50%, специфичностью 80,2%.
Результаты прогнозирования имеют практическое значение, так как наиболее трудным для клинической практики и ультразвуковой диагностики является продуктивное воспаление перикарда, лежащее в основе адгезивного и констриктивного перикардита. С целью улучшения прогноза констриктивной формы хронического перикардита предложен способ ультразвуковой диагностики его ранней стадии по преобладающему утолщению эпикарда в сравнении с перикардом (Кочмашева В.В., Беликов Е.С., Дергунова М.А., 2008).
