Синдром системной воспалительной реакции и метаболическая функция легких
| Вид материала | Документы |
- Лекция «Синдром легочного инфильтрата. Тактика ведения больных с внебольничной и нозокомиальной, 95.95kb.
- План лекции: Понятие о сепсисе. Классификация. Этиология и патогенез сепсиса, 72.74kb.
- Пневмопати и, 57.44kb.
- Современные проблемы аллергодиагностики, 181.67kb.
- Ельный процесс легких, захватывающий респираторные отделы, вне зависимости от этиологии, 133.89kb.
- «Российская медицинская академия последипломного образования Росздрава», 280.78kb.
- Хронические перикардиты как проявление универсальной иммуно-воспалительной реакции:, 560.5kb.
- Теория и метод системной психологии, 951.46kb.
- S: Функция выявления закономерностей исторического развития это функция, 1125.29kb.
- Общие сведения и классификация легких бетонов, 252.54kb.
Синдром системной воспалительной реакции и метаболическая функция легких
Б.Д. Зислин, С.Н. Скорняков
МУ ГКБ №40, НИИ фтизиопульмонологии
Борис Давидович Зислин, доктор мед. наук, заместитель главного врача МУ ГКБ №40, г. Екатеринбург
Резюме
Многолетнее изучение состояния основных функций жизнеобеспечения в раннем периоде после операций на легких позволило увидеть много общих черт синдрома СВР и послеоперационного синдрома в хирургии легких. Обращало на себя внимание непосредственное участие расстройств метаболической функции легких в течении и прогнозе послеоперационного синдрома. Исследованию были подвергнуты 311 мужчин в возрасте 57.8±0.52 л, перенесших пневмонэктомию по поводу рака. Изменения регистрировались в основном в тех системах, которые отражают неспецифические метаболические реакции организма: смещение равновесия системы ПОЛ-АОА в сторону накопления продуктов пероксидации, гиперкоагуляция с начальными проявлениями синдрома ДВС, увеличение объема эритроцитов, угнетение Т-клеточного звена иммунитета, депрессия сердечного выброса, возрастание постнагрузки и систолического давления в легочной артерии. Наиболее выраженные, высоко достоверные изменения обнаруживались в содержании СМ. У больных с гладким послеоперационным течением перечисленные выше изменения были выражены умеренно и проявлялись преимущественно в виде тенденции на протяжении первых 3 суток. Причем, по большинству изучаемых параметров они достоверно отличались от группы больных с осложненным течением. Расстройства основных функциональных систем у последних прогрессировали до конца первой недели, а затем, в большинстве случаев, подвергались медленному регрессу. Также авторами была проведена оценка эффективности двух методов экстракорпоральной гемокоррекции с позиций возможного протезирования метаболической функции легких: карбогемосорбции (ГС) и внутривенного лазерного облучения крови (ВЛОК).
В последнее время пристальное внимание патофизиологов, реаниматологов и специалистов по интенсивной терапии критических состояний обращается на изучение синдрома системной воспалительной реакции (СВР).
Установлена неспецифичность его проявления, фазовость течения, ведущая роль в формировании полиорганной недостаточности, существенное участие биологически активных аминов в генезе его возникновения и прогрессирования [1, 2].
Многолетнее изучение состояния основных функций жизнеобеспечения в раннем периоде после операций на легких позволило нам увидеть много общих черт синдрома СВР и послеоперационного синдрома в хирургии легких. Обращало на себя внимание непосредственное участие расстройств метаболической функции легких в течении и прогнозе послеоперационного синдрома.
Вопросу об участии легких в генезе СВР посвящена обширная литература. Однако основное внимание исследователей обращалось на расстройства газообменной функции (острое повреждение легких, респираторный дистресс синдром). Нарушения метаболической функции исследованы существенно меньше. Это обстоятельство послужило основанием для проведения специального исследования, направленного на изучение роли и места метаболической дисфункции легких в возникновении и прогрессировании СВР в хирургии легких.
Материал и методы исследования
Моделью стрессовой ситуации, которая могла спровоцировать синдром системной воспалительной реакции, было избрано оперативное вмешательство. Исследованию подвергнуты 311 мужчин в возрасте 57.8±0.52 л, перенесших пневмонэктомию по поводу рака, разделенных на 2 группы: с неосложненным (241 - 77.5%) и осложненным (70 - 22.5%) послеоперационным периодом.
Изучение интегральных параметров основных систем жизнеобеспечения осуществлялось традиционными методами. Газообменную функцию легких оценивали по газовому составу, кислотно-основному состоянию артериальной и смешанной венозной крови, величине внутрилегочного шунтирования крови (Qs/Qt). Из параметров центральной гемодинамики регистрировали ударный (УИ), сердечный (СИ) объемы крови, периферическое сопротивление сосудов (ОПСС) и систолического давления в легочной артерии (ДЛА) неинвазивным методом. Состояние процессов перекисного окисления липидов и антиоксидантной защиты оценивали по содержанию коньюгированных диенов (КД) и общей антиокислительной активности (АОА). При исследовании системы гемостаза определяли коагуляционную активность крови (Тсв), содержание продуктов деградации фибрина (ПДФ), О реологических свойствах крови судили по величине вязкости и объему эритроцита (MCV) Выраженность эндогенной интоксикации оценивали по уровню среднемолекулярных олигопептидных фракций (СМ254), в артериальной и венозной крови. Оценку иммунного статуса осуществляли по основным показателям клеточного и гуморального иммунитета in vitro: абсолютному количеству Т- (Е-РОК), В- и "нулевых" лимфоцитов, а также по содержанию сывороточных иммуноглобулинов классов А, M, G. Интегральным показателем состояния метаболической функции легких считали артерио-венозный градиэнт СМ (a/v СМ),
Регистрацию перечисленных параметров проводили до операции (исходные данные) и на 1, 3, 7 и 14 сутки после вмешательства.
Обсуждение результатов исследования
Для того, чтобы достичь поставленной цели необходимо было предварительно разрешить два основных вопроса:
1. Корректно ли при отсутствии классических маркеров СВР (цитокинов, простагландинов, белков острой фазы и др.) судить о наличии системной воспалительной реакции?
2. Имеются ли в нашем распоряжении критерии, отражающие метаболические функции легких.
Для ответа на первый вопрос необходимо, хотя бы кратко, остановиться на патогенезе СВР. Этот вопрос изучен достаточно полно [1-7]
В развитии системной воспалительной реакции выделяют 3 стадии.
1 стадия характеризуется локальной продукцией цитокинов в ответ на повреждающий фактор. При продолжающемся воздействии инициирующего агента процесс переходит во 2 стадию.
Во 2 стадии отмечается выброс цитокинов в системный кровоток, что приводит к активизации макрофагов, тромбоцитов, гиперпродукции гормона роста. Под влиянием нарастающей концентрации цитокинов происходит активация комплемента С5, что сопровождается секвестрацией полинуклеаров, тромбоцитов, эндотелиоцитов с появлением в кровотоке активных форм кислорода. Эта фаза 2 стадии носит название "кислородный взрыв" и характеризуется появлением в кровотоке продуктов перекисного окисления липидов (перекиси, гидроперекиси, альдегиды, кетоны), медиаторных аминов (гистамин/серотонин, октопанин, кинины, норадреналин и др.) и эйкосаноидов (простагландины, простациклин, тромбоксан и др.).
Развивается острофазная реакция, следствием которой является прогрессирование цитокинемии, появление островазных протеинов (фибриноген В, фибронектин и др.) и дисфункция кишечника с появлением в кровотоке токсических продуктов (эндотоксемия). Нарастающий эндотоксикоз сопровождается периферическим ангиоспазмом, нарушением равновесия в системе ПОЛ-АОА, нарушением в системе гемостаза, реологическими расстройствами, мембранной дисфункцией, что, в свою очередь, способствует прогрессированию эндотоксикоза. Результатом этого порочного круга является тканевая гипоксия.
Острофазовая реакция контролируется провоспалительными и противовоспалительными медиаторами (смешанный антагонистический реактивный синдром - САРС [1]).
При нарушении равновесия между про- и противовоспалительными медиаторами процесс переходит в 3 стадию - полиорганную недостаточность. Преобладание провоспалительных факторов сопровождается анафилаксией, тотальным воспалением, некрозом. Преобладание противовоспалительных факторов приводит к ареативности, иммунодефициту.
Для характеристики системной воспалительной реакции мы располагаем, прежде всего, данными о системе ПОЛ-АОА, которая является маркером начальных фаз (фаза кислородного взрыва) 2 стадии СВР.
Мы располагаем также интегральным параметром эндотоксикоза - среднемолекулярными олигопептидами (СМ254). Пул СМ254 включает в себя простагландины, простациклин, тромбоксан, медиаторные амины (гистамин, норадреналин и др.), т.е. вещества, реализующие поздние фазы 2 стадии СВР.
Мы имеем данные о системе гемостаза, реологии крови, периферическом сосудистом сопротивлении, характеризующими еще более поздние фазы 2 стадии. И, наконец, мы обладаем данными о напряжении кислорода в смешанной венозной крови (PvO2), позволяющими получить некоторую информацию о тканевом газообмене, нарушения которого (гипоксия) характерны для финальной фазы 2 стадии СВР.
Таким образом, мы располагаем большинством основных критериев, характерных для системной воспалительной реакции, и, на вопрос о корректности суждения о СВР, имеем полные основания ответить положительно.
Метаболическая функция легких изучена также достаточно полно. Она реализуется преимущественно в эндотелии легочных сосудов. Известно 4 пути метоболизма биологически активных аминов в легких [8]:
- поглощение веществ с последующим их включением во внутриклеточный обмен (серотонин, норадреналин),
- ферментативный гидролиз (брадикинин, ангиотензин),
- смешанный путь, состоящий как из гидролиза, так и из внутриклеточного транспорта (АТФ, АДФ). Эти амины гидролизуются с образованием аденозиннуклеатида - вещества, принимающего активное участие в энергетических процессах,
- синтез новых веществ (простгландинов из арахидоновой кислоты).
Большинство из перечисленных биологически активных веществ составляют пул СМ254. Следовательно, по градиенту их концентрации в венозной (притекающей к легкому) и артериальной (оттекающей от легкого) крови можно, в какой-то степени, судить о состоянии метаболической функции легких.
Анализ динамики изучаемых параметров в обеих группах больных свидетельствовал об однотипных изменениях. Различия состояли лишь в степени выраженности расстройств соответствующих функциональных систем. Было установлено, что по всем основанным параметрам у больных с осложненным течением была зарегистрирована достоверно более выраженная динамика.
Данные о послеоперационной динамике некоторых интегральных показателей, определяющих состояние основных функциональных систем пациентов с осложненным послеоперационным периодом, представлены в таблице 1
Таблица 1
Состояние основных функциональных систем у больных с осложненным послеоперационным периодом
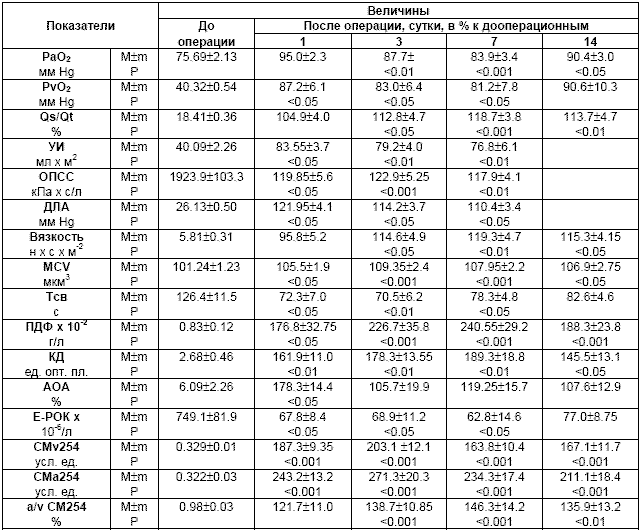
Из материалов таблицы 1 видно, что наиболее ранние (1 сутки) изменения регистрировались, в основном, в тех системах, которые отражают неспецифические метаболические реакции организма. Были отчетливо выражены: смещение равновесия системы ПОЛ-АОА в сторону накопления продуктов пероксидации, гиперкоагуляция с начальными проявлениями синдрома ДВС, увеличение объема эритроцитов, угнетение преимущественно Т-клеточного звена иммунитета,
Реакция гемодинамики характеризовалась депрессией сердечного выброса, преимущественно за счет ударного объема, существенным возрастанием постнагрузки и систолического давления в легочной артерии. Наиболее выраженные, высоко достоверные изменения обнаруживались в содержании СМ.
Обращал на себя внимание и тот факт, что в 1 сутки достоверно регистрировалась венозная гипоксемия при отсутствии достоверных различий в артериальном РО2, что свидетельствовало о преобладании метаболических расстройств.
Начиная с 3 суток наблюдалось прогрессирование перечисленных выше функциональных расстройств. Отмечалось достоверное возрастание артери-венознозного градиента по СМ, увеличение внутрилегочного шунта, артериальной гипоксемии, вязкости крови.
У больных с гладким послеоперационным течением перечисленные выше изменения были выражены умеренно и проявлялись преимущественно в виде тенденции на протяжении первых 3 суток. Причем, по большинству изучаемых параметров они достоверно отличались от группы больных с осложненным течением. Расстройства основных функциональных систем у последних прогрессировали до конца первой недели, а затем, в большинстве случаев, подвергались медленному регрессу.
Обращала на себя внимание динамика СМ (таб. 2). В обеих группах этот показатель достоверно возрастал, но его увеличение у группы больных с осложненным течением (группа Б) было достоверно большим. Однако, важно другое. Если у больных с неосложненным течением (группа А) венозно-артериальный градиент, будучи несколько увеличенным в 1 сутки после операции, уже к 3 суткам достигал исходных (дооперационных) величин, то у больных с осложненным течением он неуклонно возрастал и оставался высоким до конца второй недели.
Таблица 2
Динамика среднемолекулярных олигопептидов
| Показатели | Группа больных | Величины (M±m) | ||||
| До операции | После операции, сутки, в % к дооперационным | |||||
| 1 | 3 | 7 | 14 | |||
| СМv254 усл. ед. | А | 0,312±0,007 | 192,7±4,2* | 171,35±5,6* | 136,8±6,1* | 116,3±6,8* |
| Б | 0.329±0.01 | 187.3±9.35* | 203.1 ±12.1* | 163.8±10.4* | 167.1±11.7* | |
| p | | | <0.05 | <0.05 | <0.001 | |
| СМа254 усл. ед. | А | 0.292±0.019 | 236.9±9.2* | 203.8±13.9* | 152.4±12.5* | 119.6±14.2* |
| Б | 0.322±0.03 | 243.2±13.2* | 271.3±20.3* | 234.3±17.4* | 211.1±18.4* | |
| p | | | <0.01 | <0.001 | <0.001 | |
| a/v CM254 % | А | 0.94±0.02 | 119.1±9.2* | 112.0±8.2 | 107.4±13.1 | 103.1±8.2 |
| Б | 0.98±0.03 | 121.7±11.0* | 138.7±10.85* | 146.3±14.2* | 135.9±13.2* | |
| p | | | <0.05 | <0.05 | <0.05 | |
А - группа больных с неосложненным течением. Б - группа больных с осложнениями.
* - достоверные различия с исходными данными.
Таким образом, можно было констатировать, что у больных с неосложненным течением метаболическая дисфункция легких страдала существенно в меньшей степени и полностью восстанавливалась через трое суток после операции, в то время как при осложненном течении она неуклонно прогрессировала до окончания второй недели.послеоперационного периода. В свете полученных данных представлялось важным выяснить, влияет ли нарушение метаболической функции легких на состояние других систем жизнеобеспечения больного. Это можно было решить с помощью корреляционного анализа, установившего причинно-следственные связи СМ с другими изучаемыми параметрами (таб. 3).
Таблица 3
Коэффициенты корреляции (R) параметров эндотоксикоза*
| Параметры | СМ254 | v \ a градиент СМ254 | ||||
| 1 сутки | 3 сутки | 7 сутки | 1 сутки | 3 сутки | 7 сутки | |
| PaO2 (мм Hg) | -0.53 | -0.69 | -0.33 | -0.66 | -0.59 | -0.52 |
| PvO2 (мм Hg) | | | | -0.76 | -0.79 | -0.69 |
| Qs\Qt (%) | +0.59 | +0.71 | +0.58 | +0.71 | +0.78 | +0.70 |
| ОПСС (кПа х с/л) | +0.75 | +0.82 | +0.97 | +0.60 | +0.51 | +0.54 |
| ДЛА (мм Hg) | +0.64 | +0.64 | +0.61 | +0.66 | +0.59 | +0.67 |
| КД (ед. опт. Пл.) | +0.53 | +0.64 | +0.47 | +0.69 | +0.66 | +0.45 |
| АОА (%) | -0.28 | -0.74 | -0.76 | | | |
| Тсв (с) | | | | -0.73 | -0.68 | -0.53 |
| Вязкость (н х с х м-2) | +0.60 | +0.55 | +0.43 | | | |
| MCV (мкм3) | +0.41 | +0.54 | +0.58 | +0.51 | +0.59 | +0.62 |
| Е-рок (10-6/л) | -0.35 | -0.81 | -0.64 | -0.41 | -0.51 | -0.61 |
* Все коэффициенты корреляции достоверны - Р <0.05.
Из материалов таблицы 3 следует, что обнаруживается высокая теснота корреляционных связей почти со всеми изучаемыми параметрами, что является веским доводом в пользу концепции о ведущей роли метаболической дисфункции легких в генезе послеоперационных функциональных расстройств.
Если эта концепция верна, то применение методов протезирования метаболической функции легких должно было дать выраженный эффект.
Изучение этого вопроса было нами предпринято у 92 больных, к которым, начиная с 1 суток после пневмонэктомии на фоне традиционной терапии применялись два метода экстракорпоральной гемокоррекции (ЭКГК): карбогемосорбция (ГС) в 1 и 3 сутки после операции (64 больных) и внутривенное лазерное облучение крови (ВЛОК) в 1-5 сутки (28 больных). Контрольную группу составили 151 больной, которым проводилась только традиционная терапия. Сравнительные данные о динамике некоторых показателей представлены в таблице 4.
Таблица 4
Состояние некоторых параметров в зависимости от методов лечения
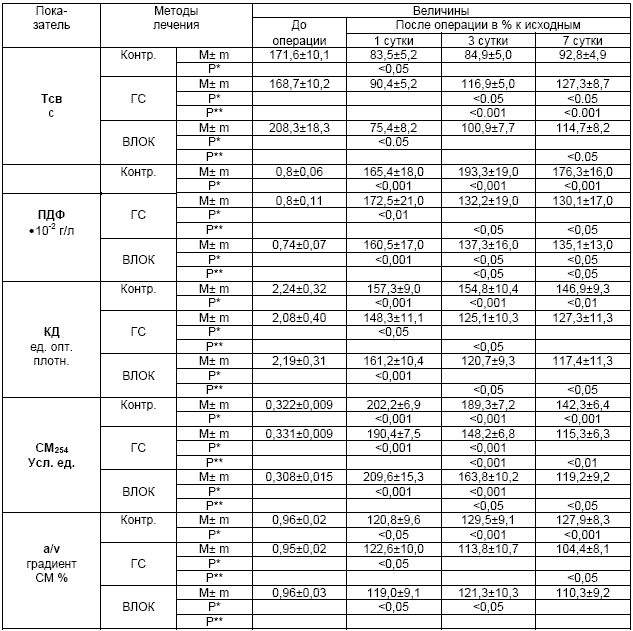
Р* - достоверность различий с исходными данным
Р** - достоверность различий с контрольной группой
Из материалов таблицы 4 следует, что применение методов ЭКГК, начиная с 3 суток послеоперационного периода (в 1 сутки они еще не могли оказать своего воздействия), существенно влияло на динамику изучаемых показателей.
Так, время свертывания крови (Тсв) при гемосорбции достоверно превышало исходные величины и значимо отличалось от аналогичного показателя контрольной группы. При применении ВЛОК этот показатель оставался на дооперационном уровне и на 7 сутки был достоверно выше, чем в контрольной группе. Содержание ПДФ у больных, получавших сеансы ВЛОК, было значимо меньше, а у получавших гемосорбцию -вообще не отличалось от исходных величин. Содержание КД, будучи в контрольной группе высоко достоверно выше исходных показателей, у больных, которым применялись методы ЭКГК, достоверно не отличались от исходных величин. Причем, у больных, получавших ВЛОК, темп снижения этого параметра даже несколько превышал таковой в группе с гемосорбцией, в связи с чем, на 3 и 7 сутки послеоперационного периода он был достоверно ниже, чем в контрольной группе.
Содержание СМ почти на всех сроках наблюдения у всех больных достоверно превышало дооперационный уровень, однако, у больных, получавших сеансы ЭКГК, это повышение было достоверно меньше, а к концу 1 недели уже не превышало дооперационного уровня.
Естественно было ожидать, что столь характерная динамика СМ не могла не отразиться на артерио-венозном градиенте СМ. Если у больных контрольной группы этот параметр на протяжении всей 1 недели после операции был достоверно выше исходных величин, то у больных, получавших ГС, он вообще достоверно не менялся, а у получавших ВЛОК, достигал дооперационного уровня уже к концу 1 недели.
Однако, наиболее веским доводом в пользу высокой эффективности методов ЭКГК в предупреждении прогрессирования синдрома системной воспалительной реакции являются непосредственные исходы операций.
Из 92 больных, которым проводилась интенсивная терапия с помощью ЭКГК, ни у одного не отмечено развития полиорганной недостаточности, в то время как в контрольной группе она развилась у 33 больных (21.8%) и сопровождалась летальностью 8,6% (13 человек). В группе оперированных, в которой проводилась гемокоррекция лишь один больной (1,1%) погиб от массивной тромбоэмболии легочной артерии на 2 сутки после операции, успевший получить только 1 сеанс ВЛОК.
Возникает существенный вопрос: каковы же механизмы столь благоприятных эффектов экстракорпоральной гемокоррекции?
В отношении карбогемосорбции можно полагать, что при ней ведущее значение имеет элиминация (истинное удаление) из кровотока биологически активных веществ и других продуктов метаболизма.
Что же касается ВЛОК, то, очевидно, что прямые элиминационные эффекты при его проведении отсутствуют. Тогда каковы же причины детоксикационных эффектов этого метода?
Работами последних лет [9,10] достаточно убедительно показано, что в качестве первичного фотоакцептора низкоинтенсивного лазерного излучения в живых системах можно рассматривать сложно организованные биологические жидкости, такие как плазма. Возникающие под воздействием облучения конформационные перестройки структурной матрицы сопровождаются изменением физико-химических свойств плазмы (реологии, диффузии, фазовой устойчивости и др.), что, в свою очередь вызывает изменение активности биохимических реакций, механических, транспортных, структурных и других свойств мембран и клеток. Эти факторы и определяют, в конечном итоге клеточные, органные и организменные эффекты лазерной "биостимуляции" [11]. Можно предполагать, что именно мембраностабилизирующие эффекты и выраженное нормализующее влияние на процессы, определяющие эффективность микроциркуляции (клеточной агрегации, транскапиллярного обмена), лежат в основе зарегистрированных у больных, получавших сеансы ВЛОК, отчетливых тенденций к снижению выраженности метаболических нарушений. Весьма вероятно, что в реализации воздействий ВЛОК на организм большое значение имеют процессы ПОЛ и антиоксидантной защиты. Уровень АОА у больных этой группы к моменту окончания курса ВЛОК и до конца периода наблюдения достоверно превышал не только соответствующую величину у пациентов контрольной группы, но и больных, получавших ГС. Все это не могло не сказаться на снижении продукции цитокинов и других биоактивных аминов с одной стороны, и большей сохранности метаболических функций легкого - с другой стороны.
Может возникнуть вопрос: правомочно ли заявлять, что ЭКГК являются методом, способным протезировать метаболические функции легких? Мы полагаем, что это правомерно.
Во-первых, потому, что оба изучаемых нами метода обладают отчетливой детоксикационной активностью и, следовательно, способны замещать одну из основных метаболических функций легких.
Во-вторых, они нивелируют гиперкоагуляцию, снижают активность процессов паракоагуляции и перекисного окисления липидов, являющихся "пусковым механизмом" синдрома неспецифического воспалительного ответа, в основе которого лежат, прежде всего, нарушения метаболических функций легких.
Следует только отметить, что, хотя оба метода экстракорпоральной гемокоррекции способны замещать метаболическую функцию легких, однако, механизмы реализации этой способности различны. Гемосорбция удаляет из кровотока токсические продукты, появившиеся в нем вследствие несостоятельности метаболических функций легких, и, в этом плане, ее можно рассматривать как метод, протезирующий эту функцию. ВЛОК, корригируя дисфункцию мембран и клеток, предупреждает возникновение эндотелиальной недостаточности и, тем самым, сохраняет, либо даже восстанавливает сниженный метаболический потенциал легких. В этом плане, весьма перспективным может выглядеть сочетанное применение обоих методов экстракорпоральной гемокоррекции для протезирования метаболических функций легких.
Библиография
Библиография 1. Bone R. Toward a theory regarding the pathogenesis of the systemic inflammatory response syndrome: what we do and do not know about cytokine regulation. Crit. Care Med.- 1996.- V.24- N.1- P.163-72.
2. Bone R. Toward a theory regarding the pathogenesis of the systemic inflammatory response : what we do and do not know about cytokine regulation. Critical Care Med. - 1996. - V.24. - P. 163 - 72
3. Bone R. Reevaluation of the role of cellular hypoxia and bioenergetic failure in sepsis. JAMA. - 1992. - V. 18. - P. 1503 - 1510.
4. Bone RC. Immunologic dissonance: a continuing evolution in our understanding of the systemic inflammatory response syndrome (SIRS) and the multiple organ dysfunction syndrome (MODS). Ann Intern Med. - 1996. - V. 125. - P. 680-687
5. Зильбер А.П. Респираторная медицина. "Этюды критической медицины". - Кн. 2. -Петрозаводск. -1996. -488 с.
6. Лейдерман И.Н., Руднов В.А., Клейн А.В., Николаев Э.К. Синдром гиперметаболизма - универсальное звено патогенеза критических состояний. Вестник интенсивной терапии - 1997.- №3.- С.17-23.
7. Медвинский И.Д., Зислин Б.Д., Юрченко Л.Н. Концепция развития полиорганной недостаточности на модели гестоза. Анест. Реаним.- 2000.-№3.-С.48-52
8. Сыромятникова Н.В.. Гончарова В.А., Котенко Т.В. Метаболическая активность легких.- Л., 1987. -168 с.
9. Илларионов В.Е. Основы лазерной терапии. М. 1992. -127 с.
10. Минц Р.И., Скопинов С.А.. Структурная альтерация биологических жидкостей и их моделей при информационных воздействиях. 1. Гелий-неоновый лазер. Действие электромагнитного излучения на биологические объекты и лазерная медицина. Владивосток: ДВО АН СССР.- 1989.- С.6-41.
11. Куртенок Л.Г., Титкова С.М., Зинякова М.В. Применение внутрисосудистого лазерного облучения в хирургии. Сов. медицина. -1992.- № 3. - C. 31-33.
От редакции
С позиций современного уровня знаний стало очевидным, что операция как любая механическая травма может инициировать формирование СВР различной степени тяжести. Авторы статьи известные в России специалисты в области анестезиологии и реаниматологии. В значительной мере их научные разработки были связаны с проблемами лёгочной хирургии. Анализ и обобщение накопленных фактов позволил им в итоге сформулировать оригинальную концепцию послеоперационного синдрома в хирургии лёгких.
Представляется логичным, что в дальнейшем авторы стали рассматривать послеоперационный синдром в качестве в одной из клинических форм СВР.
Особая роль лёгких и наличие широкого набора негазообменных функций справедливо послужили основанием для проведения специальных исследований, направленных на изучение роли и места метаболической дисфункции легких в возникновении и прогрессировании СВР в хирургии легких.
Прежде всего, хотелось бы отметить значительный объём работы, который был выполнен для разрешения поставленной задачи. В результате можно утверждать о существовании вклада нарушений ряда негазообменных функций лёгких в поддержание СВР. Получение новых данных о наличии взаимосвязи между СВР и ПОЛ, параметрами гемостаза, кислородного транспорта углубляет наши представления о реакции на операционную травму больных раком лёгкого. Между тем, ряд промежуточных заключений, некоторые методологические подходы и рекомендации нуждаются в обсуждении.
Наиболее важными из них представляются следующие:
1. Утверждая о эффективности ЭКГК авторы не приводят данные сопоставимости групп по индексам общей тяжести состояния(SAPS, APACHE и др.), сопутствующей патологии и что принципиально важно критериям по которым судили о развитии органной дисфункции(SOFA, LOD, J.Marshall, A. Baue et al.), не описан протокол стандартной терапии, не ясно каким был дизайн исследования(исторический контроль или проспективное нерандомизированное контролируемое исследование). Не ясно какой из методов ЭКГК оказался эффективным, поскольку при окончательном анализе пациенты с ВЛОК и ГС объединены.
2. Вызывает сомнение представление всех данных в относительных величинах: в процентах к исходному уровню в динамике (Табл. 1, 2, 4). Такой способ обработки и подачи материала не соответствует требованиям медицины, основанной на доказательствах [1].
3. C нашей точки зрения, в плане осмысления информационной значимости, было бы полезным соотнесение обнаруженных в послеоперационном периоде гомеостатических изменений с классическими критериями СВР.
В целом, приветствуя углублённый подход к анализу реакции на операционную травму больных раком лёгкого и оригинальную интерпретацию его результатов, мы полаем, что рекомендации по использованию ГС и ВЛОК нуждаются в более аргументированном обосновании с позиций современной методологии, предъявляемой к клиническим испытаниям [1-3].
Литература
1. Флетчер Р., Флетчер С., Вагнер Э. Клиническая эпидемиология. Основы доказательной медицины. Пер. с англ. М., Издательство Медиа Сфера, 1998, 352с.
2. Бащинский С.Е. Разработка клинических практических руководств с позиций доказательной медицины. М., Издательство Медиа Сфера, 2004, 135с.
3. Laupacis A., Sackett D. An assessment of critically useful measures of the consequences of treatment. NEJM 1988;318:1728-1733.
Сергей Алексеевич Шляпников
зав. кафедрой хирургических инфекций Санкт-Петербургской медицинской академи им. И.И. Мечникова