Н. Н. Алипова, канд биол наук О. В. Левашова и канд биол наук М. С. Морозовой под редакцией акад. П. Г. Костюка москва «мир» 1996 ббк 28. 903 Ф50
| Вид материала | Документы |
- Приглашение и программа разнообразие почв и биоты северной и центральной азии, 521.14kb.
- М. А. Ляшко доц., канд физ мат наук; Т. Н. Смотрова доц., канд, 2299.13kb.
- Современные направления развития физической культуры, спорта и туризма, 4493.6kb.
- Отчет о проведении Международной научной конференции-семинара «Современные методы психологии», 97.76kb.
- Образовательная программа дошкольного образования Москва «Просвещение», 5670.3kb.
- Пособие для врачей и среднего медицинского персонала Минск, 5480.63kb.
- Ббк 63. 3(0) Н72, 4378.93kb.
- Тезисы докладов, 4290.75kb.
- Строительные нормы и правила нагрузки и воздействия сниП 01. 07-85* министерство строительства, 1162.86kb.
- Ббк 63. 3(0) Н72, 5546.58kb.
22.2. Перенос кислорода кровью
Физическая растворимость газов
Парциальное давление (напряжение) газов в жидкости. Почти во всех жидкостях может содержаться некоторое количество физически растворенных газов. Содержание растворенного газа в жидкости зависит от его парциального давления. Если жидкость привести в состояние термодинамического равновесия с находящимся над ней газом (для этого необходимо, чтобы площадь соприкосновения и время контакта обеих фаз были достаточно велики), то в жидкости создается напряжение газа, равное его парциальному давлению в газовой фазе.
Содержание физически растворенных газов в крови. Содержание газа в жидкости в физически растворенном виде зависит от его напряжения Рг и коэффициента растворимости Бунзена а, отражающего свойство растворимости. Коэффициент Бунзена соответствует объему газа (в миллилитрах), физически растворяющемуся в 1 мл жидкости при напряжении газа, равном 1 атм (1 атм = 760 мм рт. ст. = 101 кПа). Зависимость содержания физически растворенного газа в жидкости от его напряжения и коэффициента растворимости называется законом Генри-Дальтона:
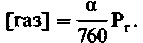 (3)
(3)В знаменателе этого выражения стоит число 760, так как при определении α в качестве единиц
используют атмосферы, а напряжение газа Рг обычно выражают в миллиметрах ртутного столба.
Величина коэффициента Бунзена зависит от природы растворенного газа, свойств растворителя и температуры. В табл. 22.1 приведены некоторые значения этого коэффициента для растворов атмосферных газов в воде и крови. Используя закон Генри-Дальтона [уравнение (3)], можно вычислить содержание физически растворенного газа в жидкости, исходя из его напряжения и величины а. Так, в артериальной крови (при РО2 = 95 мм рт. ст. и РСО2 = 40 мм рт. ст.) содержание физически растворенного О 2 составляет 0,003 мл О2 на 1 мл крови, а СО2-0,026 мл СО 2 на 1 мл крови. Несмотря на то что напряжение СО2 ниже, чем напряжение О2, количество физически растворенного СО2 в 9 раз больше. Это объясняется тем, что коэффициент растворимости для СО2 в 20 раз больше, чем для О2.
| Таблица 22.1. Коэффициент растворимости Бунзена α (мл газа-мл растворителя"1 ∙ атм -1) для О2, СО2 и Ν2 в воде и в крови | |||
| | 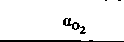 | 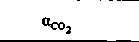 |  |
| Вода, 20 °С | 0,031 | 0,88 | 0,016 |
| Вода, 37 °С | 0,024 | 0,57 | 0,012 |
| Кровь, 37 °С | 0,024 | 0,49 | 0,012 |
Х
 отя содержание в крови О2 и СО2 в физически растворенной форме относительно невелико, эта их форма играет огромную роль в жизнедеятельности организма. Для того чтобы связаться с теми или иными веществами, дыхательные газы сначала должны быть доставлены к ним в физически растворенном виде. Таким образом, при диффузии в ткань или из нее каждая молекула О2 или СО2 в течение некоторого времени находится в растворенной форме.
отя содержание в крови О2 и СО2 в физически растворенной форме относительно невелико, эта их форма играет огромную роль в жизнедеятельности организма. Для того чтобы связаться с теми или иными веществами, дыхательные газы сначала должны быть доставлены к ним в физически растворенном виде. Таким образом, при диффузии в ткань или из нее каждая молекула О2 или СО2 в течение некоторого времени находится в растворенной форме.Связывание кислорода гемоглобином
Кислородная емкость крови. Большая часть кислорода переносится кровью в виде химического соединения с гемоглобином. Для того чтобы узнать, какое наибольшее количество О2 может быть связано гемоглобином, следует иметь в виду, что молекула последнего состоит из четырех субъединиц (рис. 22.3). Следовательно, реакцию оксигенации можно записать следующим образом:
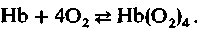 (4)
(4)Таким образом, 1 моль гемоглобина может связать до 4 моль О2. Поскольку объем 1 моль идеального газа составляет 22,4 л, 64 500 г гемоглобина связывают 4 · 22,4 л О2 , a 1 г гемоглобина - 1,39 мл О2. При анализе газового состава крови получают несколько меньшую величину (1,34 - 1,36 мл О2 на 1 г Hb). Это обусловлено тем, что
610 ЧАСТЬ VI. ДЫХАНИЕ
небольшая часть гемоглобина находится в неактивном состоянии [25]. Таким образом, ориентировочно можно считать, что in vivo 1г Hb связывает 1,34 мл О2 (так называемое число Хюфнера).
В последнее время стало принятым выражать молярную концентрацию гемоглобина в пересчете на его мономер (с. 845). В этом случае 1 моль Hb (= 16 100 г Hb) может связать до 1 моль О2 (= 22,4 л О2). Такой расчет дает в итоге ту же величину, что и расчет числа Хюфнера.
Исходя из числа Хюфнера, можно, зная содержание гемоглобина, вычислить кислородную емкость крови: [О2]макс = (1,34 мл О2 на 1 г Hb) (150 г Hb на 1 л крови) = 0,2 л О2 на I л крови. Однако такое содержание кислорода в крови может достигаться лишь в том случае, если кровь контактирует с газовой смесью, насыщенной кислородом (РО2 > 300 мм рт. ст.); при этом равновесие (4) значительно сдвинуто вправо. В естественных условиях эта реакция протекает при меньшем значении парциального давления О2, поэтому гемоглобин оксигенируется не полностью.
Кривая диссоциации оксигемоглобина. Реакция взаимодействия кислорода с гемоглобином (4) подчиняется закону действующих масс. Это означает, что соотношение между количествами гемоглобина и оксигемоглобина зависит от содержания физически растворенного О2 в крови; последнее же, согласно закону Генри-Дальтона, пропорционально напряжению О2. Процент оксигемоглобина от общего содержания гемоглобина называют кислородным насыщением (So ) гемоглобина:
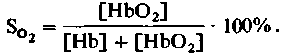 (5)
(5)Если гемоглобин полностью дезоксигенирован, то SО2 = 0%; если же весь гемоглобин превратился в оксигемоглобин, то SО2 = 100%. В соответствии с законом действующих масс насыщение гемоглобина кислородом зависит от напряжения О2. Графически эту зависимость отражает так называемая кривая диссоциации оксигемоглобина. Как видно из рис. 22.6, эта кривая имеет S-образную форму. Расположение кривой диссоциации оксигемоглобина зависит от ряда факторов (см. ниже). Наиболее простым показателем, характеризующим расположение этой кривой, служит так называемое напряжение полунасыщения Р50, т.е. такое напряжение О2, при котором насыщение гемоглобина кислородом составляет 50%. В норме (при pH 7,4 и t = 37°C) Ρ50 артериальной крови составляет около 26 мм рт. ст. (3,46 кПа) [9, 29].
Интерпретация кривой диссоциацив оксигемоглобина.
Причины S-образной формы кривой диссоциации оксигемоглобина до конца не ясны. Если бы каждая молекула гемоглобина присоединяла только одну молекулу О2, то
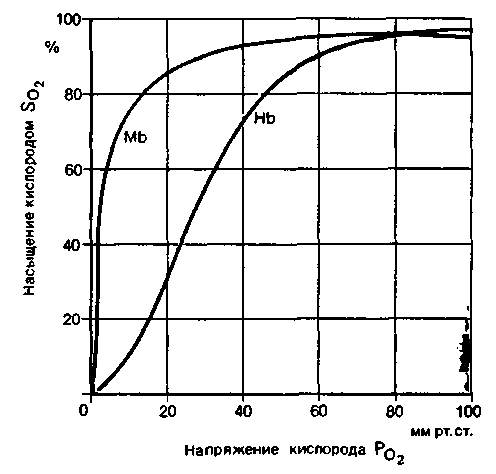 |
| Рис. 22.6. Кривые диссоциации оксигемоглобина (Hb) и оксимиоглобина (Mb) при pH 7,4 и t 37 oС |
кинетика этой реакции графически описывалась бы гиперболой [11]. Именно такая гиперболическая кривая диссоциации характерна, например, для реакции соединения кислорода с красным мышечным пигментом миоглобином (Mb), аналогичной реакции оксигенации гемоглобина [1]. Строение миоглобина сходно со структурой одной из четырех субъединиц гемоглобина, поэтому молекулярные массы этих двух веществ соотносятся как 1:4. Поскольку в состав миоглобина входит лишь одна пигментная группа, одна молекула миоглобина может присоединить только одну молекулу О2:
 (6)
(6)Гиперболическая кривая диссоциации для этой реакции приведена на рис. 22.6.
Исходя из вполне правдоподобного предположения о том, что S-образная форма кривой диссоциации НbО2 обусловлена связыванием одной молекулой гемоглобина четырех молекул О2 , Эдер выдвинул так называемую гипотезу промежуточных соединений. Согласно этой гипотезе, присоединение четырех молекул О2 к гемоглобину происходит в несколько стадий, причем каждая из этих стадий влияет на равновесие следующей реакции. Таким образом, реакция соединения кислорода с гемоглобином описывается четырьмя константами равновесия, что и объясняет сигмоидную форму кривой диссоциации оксигемоглобина.
В то же время возможно и другое объяснение, согласно которому существуют две формы гемоглобина - оксигенированная и дезоксигенированная, переходящие одна в другую в результате конформацнонных перестроек. Если предположить, что параметры равновесия реакций оксигенации для этих двух форм гемоглобина различны, то с позиции данной гипотезы можно объяснить S-образную форму кривой диссоциации НbО2 [11,14].
ГЛАВА 22. ТРАНСПОРТ ГАЗОВ КРОВИ 611
Биологический смысл формы кривой диссоциации оксигемоглобина. Конфигурация кривой диссоциации оксигемоглобина имеет важное значение с точки зрения переноса кислорода кровью. В процессе поглощения кислорода в легких напряжение О2 в крови (РO2 ) приближается к таковому в альвеолах (с. 590). У молодых людей РO2 артериальной крови составляет около 95 мм рт. ст. (12,6 кПа). Из рис. 22.6 видно, что при таком напряжении насыщение гемоглобина кислородом составляет примерно 97%. С возрастом (и в еще большей степени при заболеваниях легких) напряжение О2 в артериальной крови может значительно снижаться, однако, поскольку кривая диссоциации оксигемоглобина в правой ее части почти горизонтальна, насыщение крови кислородом уменьшается ненамного. Так, даже при падении РO2 в артериальной крови до 60 мм рт. ст. (8,0 кПа) насыщение гемоглобина кислородом равно 90%. Таким образом, благодаря тому что области высоких напряжений кислорода соответствует горизонтальный участок кривой диссоциации оксигемоглобина, предупреждается существенное снижение насыщения артериальной крови кислородом.
Крутой наклон среднего участка кривой диссоциации оксигемоглобина свидетельствует об очень благоприятных условиях для отдачи кислорода тканям. При изменении локальной потребности в кислороде он должен высвобождаться в достаточном количестве в отсутствие значительных сдвигов РO2 в артериальной крови. В состоянии покоя РO2 в области венозного конца капилляра равно приблизительно 40 мм рт. ст. (5,3 кПа), что соответствует примерно 73% насыщения. Если в результате увеличения потребления кислорода его напряжение в венозной крови падает лишь на 5 мм рт. ст. (0,7 кПа), то насыщение гемоглобина кислородом снижается не менее чем на 7%; высвобождающийся при этом О2 может быть сразу же использован для процессов метаболизма.
Содержание О2 в артериальной и венозной крови.
Количество химически связанного кислорода в крови зависит от насыщения им гемоглобина (
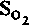 ).
).Зная величину SO2 , можно, исходя из числа Хюфнера, вычислить объемное содержание О2 в крови (в л О2 на 1 л крови):
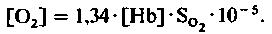 (7)
(7)где SO2 выражено в процентах, а [Hb] - в граммах на литр. Подставляя в это уравнение количественные значения кислородного насыщения, можно вычислить, что в артериальной крови (SO2 = 97%) содержание кислорода составляет около 0,20, а в венозной (SO2 =73%) оно равно 0,15. Таким образом, артериовенозная разница по концентрации кислорода (авРO2 ) составляет 0,05 (табл. 22.2). Это означает, что в норме при прохождении крови через тканевые капилляры используется лишь 25% общей кислородной емкости. Разумеется, разные органы существенно различаются по степени извлечения кислорода (см. рис. 23.2), так что величины для венозной крови, приведенные в табл. 22.2, представляют собой средние значения показателей, варьирующих в широких пределах. При интенсивной физической нагрузке артериовенозная разница по кислороду может превышать 0,1.
Факторы, влияющие на кривую диссоциации оксигемоглобина
Форма кривой диссоциации НbО2 обусловлена главным образом реакционноспособностью гемоглобина, однако сродство крови к кислороду может измениться под действием других факторов [2, 12, 14], как правило, приводящим к увеличению или уменьшению наклона кривой диссоциации без изменения ее S-образной формы. Такое влияние оказывают температура, pH, напряжение СО2 и некоторые другие факторы, роль которых возрастает при патологических состояниях.
Влияние температуры. Равновесие реакции оксигенации гемоглобина (как и большинства химических реакций вообще) зависит от температуры. При понижении температуры наклон кривой диссоциации оксигемоглобина увеличивается, а при ее повышении-снижается (рис. 22.7, А). У теплокровных
| Таблица 22.2. Параметры дыхательных газов и pH для артериальной и венозной крови у здоровых молодых людей в покое | ||||||||
| | PO2 | So2 % | [О2], л О2/л крови | Рсо2 | [СО2], ■ л СО2/л кров» | pH | ||
| | мм рт.ст. | кПа | мм рт. ст. | кПа | | |||
| Артериальная кровь | 95 | 12,6 | 97 | 0,20 | 40 | 5,3 | 0,48 | 7,40 |
| Венозная кровь | 40 | 5,3 | 73 | 0,15 | 46 | 6,1 | 0,52 | 7,37 |
| Артериовенозная разница | | | | 0.05 | | | 0.04 | |
612 ЧАСТЬ VI. ДЫХАНИЕ
 |
| Рис. 22.7. Влияние различных параметров крови на кривую диссоциации оксигемоглобина [9, 29]. А. Влияние температуры. Б. Влияние pH (эффект Бора). В. Влияние напряжения С02. Г. Влияние содержания 2,3-дифосфоглицерата (2,3-ДФГ) в эритроците. Красная кривая, соединяющая точки а (артериальная кровь) и β (венозная кровь), или так называемая эффективная кривая диссоциации оксигемоглобина, отражает фактический газообмен в состоянии покоя |
животных этот эффект проявляется только при гипотермии или лихорадочном состоянии (с. 683, 684).
Влияние pH и РO2 . Форма кривой диссоциации оксигемоглобина в значительной степени зависит от содержания в крови ионов Н+ (эта зависимость приведена на рис. 22.7, Б, где в качестве показателя концентрации ионов Н+ указаны значения pH). При снижении pH, т. е. подкислении крови, сродство гемоглобина к кислороду уменьшается и угол наклона кривой диссоциации оксигемоглобина уменьшается. На рис. 22.7, Б приведены значения pH плазмы, хотя для понимания механизмов влияния Н+ на
диссоциацию оксигемоглобина важнее знать влияние на кривую диссоциации pH внутри эритроцитов. Однако этот параметр измерить трудно, поэтому обычно ограничиваются определением pH плазмы. Влияние pH на характер кривой диссоциации оксигемоглобина (см. рис. 22.7, Б) называют эффектом Бора.
pH крови тесно связан с напряжением в ней СО2 (РO2 ): чем выше РO2 , тем ниже pH. На рис. 22.7, В приведено семейство кривых диссоциации оксигемоглобина при различных значениях РСO2 . Видно, что увеличение напряжения СО2 в крови сопровождается снижением сродства гемоглобина к кислороду и
ГЛАВА 22. ТРАНСПОРТ ГАЗОВ КРОВИ 613
уменьшением угла наклона кривой диссоциации НbО2. Эту зависимость называют также эффектом Бора, хотя при детальном количественном анализе было показано, что влияние СО2 на форму кривой диссоциации оксигемоглобина нельзя объяснить только изменением pH. Очевидно, сам диоксид углерода оказывает на диссоциацию оксигемоглобина специфическое действие [14].
Биологический смысл эффекта Бора. Эффект Бора имеет определенное значение как для поглощения кислорода в легких, так и для его высвобождения в тканях (хотя значение этого эффекта не следует преувеличивать). Рассмотрим сначала процессы, происходящие в легких. Поглощение О2 идет одновременно с выделением СО2, поэтому по мере насыщения гемоглобина кислородом кривая диссоциации оксигемоглобина сдвигается влево. На рис. 22.7, В этим изменениям соответствует красная кривая, которую иногда называют эффективной кривой диссоциации НЬО2. По мере того как венозная кровь (точка в; РO2 = 40 мм рт. ст., РCO2 = 46 мм рт. ст.), насыщаясь кислородом, превращается в артериальную (точка а; РO2 = 95 мм рт. ст., РCO2 = 40 мм рт. ст.), сродство гемоглобина к кислороду постоянно увеличивается. В результате, хотя перенос кислорода осуществляется путем диффузии, скорость этой диффузии несколько возрастает. Таким образом, эффект Бора способствует связыванию кислорода в легких.
Несколько большее значение эффект Бора имеет для переноса О2 из капилляров в ткани. Поскольку одновременно с выходом кислорода из крови в нее поступает СО2, кривая диссоциации оксигемоглобина смещается вправо. Все эти процессы соответствуют сдвигу на эффективной кривой диссоциации от точки а до точки в (красная кривая на рис. 22.7, В). Снижение сродства гемоглобина к кислороду приводит к еще большему падению содержания оксигемоглобина, и в результате кислород поступает в ткани при относительно высоком Ро в капилляре. Таким образом, и в данном случае эффект Бора способствует обмену кислорода.
Влияние патологических факторов. При ряде патологических состояний наблюдаются изменения в процессах переноса кислорода кровью. Так, сушествуют заболевания (например, некоторые виды анемий), которые сопровождаются сдвигами кривой диссоциации оксигемоглобина вправо (реже влево). Причины таких сдвигов окончательно не ясны. Известно, что на форму и угол наклона кривой диссоциации оксигемоглобина оказывают выраженное влияние некоторые фосфорсодержащие органические соединения, концентрация которых в эритроцитах при патологии может изменяться. Наибольший эффект среди таких соединений оказывает 2,3-Дифосфоглицерат-2,3-ДФГ (рис. 22.7, Г) [16, 22]. Сродство гемоглобина к кислороду зависит также от содержания в эритроцитах катионов. Необходимо отметить и влияние патологических сдвигов pH: при повышении pH {алкалозе) захват кислорода в легких благодаря эффекту Бора облегчается, но
его отдача в тканях затрудняется, а при снижении pH (ацидозе) наблюдается обратная картина. Наконец, значительный сдвиг кривой диссоциации оксигемоглобина влево имеет место при отравлении СО.
Особенности кривой диссоциации оксигемоглобина у плода. В плаценте, как и в любом другом органе, газообмен осуществляется путем диффузии. В то же время особое внимание следует обратить на различие в сродстве крови матери и плода к кислороду. При анализе в одинаковых условиях наклон кривой диссоциации оксигемоглобина в крови плода несколько брльше, чем в крови матери, однако in vivo эта разница почти целиком сводится на нет благодаря эффекту Бора (pH крови плода несколько ниже, чем pH материнской крови). В связи с этим разница в сродстве крови матери и плода к кислороду практически не отражается на газообмене в плаценте. Такая ситуация наиболее благоприятна для обмена газов, что становится очевидным, если учесть различия в концентрации гемоглобина в крови матери и плода [7, 21].
На рис. 22.8 приведены кривые диссоциации оксигемоглобина для крови матери и плода к мо-
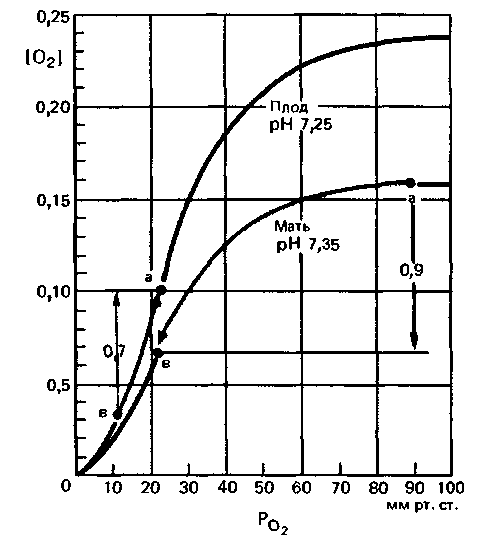 |
| Рис. 22.8. Зависимость концентрации кислорода [02] в крови от его напряжения (РО2) у матери и у плода к моменту рождения. В ходе плацентарного газообмена содержание 02 в крови матери падает от а (в артериальной крови) до β (в венозной крови), а в крови плода возрастает от в' (в пупочной артерии), до а' (в пупочной вене) |
614 ЧАСТЬ VI. ДЫХАНИЕ
менту рождения. При их построении использованы средние значения pH в области плаценты. Поскольку содержание гемоглобина в крови матери и плода различно (120 и 180 г/л соответственно), по оси ординат отложено не насыщение гемоглобина кислородом, а объемное содержание О2 в крови. Процессам дезоксигенации крови матери и оксигенации крови плода соответствует ход кривых в направлении стрелок между точками а и в (мать) и в' и а' (плод). Видно, что при одном и том же напряжении О2 кровь плода связывает значительно больше кислорода, чем кровь матери. Так, при РO2 = 25 мм рт. ст. (3,3 кПа) содержание О2 в крови матери составляет 0,08, а в крови плода-0,11.
Особую роль в плацентарном газообмене играет эффект Бора. В процессе диффузии газов сродство крови матери к кислороду в результате поступления СО2 снижается, а сродство крови плода повышается (на рис. 22.8 это не показано). Благодаря такому двойственному влиянию эффекта Бора скорость обмена кислорода увеличивается.
Связывание гемоглобина с оксидом углерода
Оксид углерода (угарный газ, СО) обладает гораздо большим сродством к гемоглобину, чем кислород. Даже при крайне низких парциальных давлениях СО гемоглобин превращается в карбоксигемоглобин:
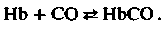 (8)
(8)Равновесие этой реакции значительно смещено вправо, поэтому кривая диссоциации карбоксигемоглобина имеет очень крутой наклон. Высокое сродство оксида углерода к гемоглобину обусловлено тем, что СО диссоциирует от Hb гораздо медленнее, чем О2 [3]. Максимально эффективная концентрация для СО (с. 720) составляет 30 ppm (частей на миллион), что соответствует FCO = 3-10~5 (0,003 об.%). В артериальной крови человека, пребывающего достаточно долго в среде с таким содержанием СО, на долю НbСО приходится около 5% общего содержания гемоглобина. Парциальные давления СО и О2, при которых содержание соответственно НbСО и НbО2 составляет по 5%, соотносятся как 1:350. Иными словами, в данных пределах парциальных давлений сродство Hb к СО примерно в 350 раз выше, чем к О2.
Токсичность оксида углерода обусловлена именно высоким сродством этого соединения к гемоглобину. СО представляет собой газ без цвета и запаха, образующийся при неполном сгорании органических веществ. Иногда он входит в состав бытового газа; кроме того, он выделяется при работе двигателей внутреннего сгорания. Даже при низких концентрациях СО вытесняет кислород из соединения с гемоглобином, при этом последний теряет способность к переносу О2. В норме на долю НbСО приходится лишь 1 % общего количества гемоглобина в крови; у курильщиков же к вечеру она достигает 20%. Об опасности, которую угарный газ представляет для автомобилистов, говорит тот факт, что на дорогах с особенно интенсивным движением содержание СО в воздухе достигает 3-10-4. При такой концентрации СО шахтерам положено надевать дыхательные аппараты.
Токсичность угарного газа обусловлена не только блокированием гемоглобина, но и другим эффектом. Когда часть гемоглобина превращается в НbСО, кривая диссоциации оксигемоглобина (для гемоглобина, еще не блокированного СО) сдвигается влево [3] и может в итоге приобретать форму гиперболы. В результате происходит еще большее снижение напряжения О2 в тканевых капиллярах.
При тяжелом отравлении угарным газом, отличительным признаком которого служит вишнево-красная окраска крови, жизнь пострадавшего можно спасти путем немедленного применения искусственного дыхания, по возможности с чистым кислородом. При этом напряжение кислорода в крови увеличивается, и О2 частично вытесняет СО из связи с гемоглобином. Рекомендуется также переливание большого количества крови, так как при этом в кровь пострадавшего поступает гемоглобин, способный переносить кислород.
