Номенклатура органических соединений. Номенклатура – совокупность правил составления химических названий
| Вид материала | Лекция |
- Номенклатура полимеров и сополимеров, 89.7kb.
- Лекция 1 систематическая номенклатура (ганча-видмана) моноциклических соединений. Номенклатура, 342.04kb.
- Порядок составления номенклатуры дел, 135.26kb.
- План занятия №1 Классификация, номенклатура и пространственное строение органических, 96.42kb.
- Тематический план лабораторно-практических занятий по курсу «Биоорганическая химия», 104.14kb.
- Тематический план лабораторно-практических занятий по курсу «Механизмы биоорганических, 111.47kb.
- Тематический план лекций и самостоятельной работы по органической химии (осенний семестр), 91.46kb.
- 1. Изомерия и номенклатура, 41.98kb.
- Рабочая программа дисциплины органическая химия I, II направление ооп 240700 биотехнология, 541.26kb.
- Разграфка и номенклатура карт разграфка карт, 55.1kb.
Лекция 1. Номенклатура органических соединений.
Номенклатура – совокупность правил составления химических названий веществ, классов, групп и др.
Первоначально, в период накопления фактических знаний, веществам давали названия, никак не указывающие на их строение. В названии отражали исходное сырье (лимонен), особо заметные свойства (флуоресцеин), способ получения (пирогаллол), имя ученого (реактив Иоцича), форму молекулы (кубан) и т.д. Эти тривиальные (традиционные) названия – историческая номенклатура – в большинстве своем сохранилась и используется по сей день. По мере развития и систематизации химических знаний веществам стали давать названия, указывающие на их сходство с другими веществами по строению (метиловый, этиловый, пропиловый спирт). Они составляют рациональную номенклатуру (от лат. ratio – разум). Рациональная номенклатура рассматривает все вещества определенного класса как производные главного и наиболее простого его представителя. Например, для предельных углеводородов таким веществом является метан, для непредельных – этилен и ацетилен.
СН3
/
СН3 – СН – СН3 триметилметан Н3С – СН=СН – С3Н7 метилпропилэтилен
Н3С – С≡С – С2Н5 метилэтилацетилен
Первое соединение можно рассматривать как метан, у которого три атома водорода замещены на три метильные группы. Второе соединение – как этилен, у которого два атома углерода замещены на два радикала - метил и пропил. Третье соединение – как ацетилен, у которого вместо двух атомов водорода находятся метильная и этильная группы. Рациональную номенклатуру используют для названия сравнительно небольших молекул.
Главное место занимает международная систематическая заместительная номенклатура (IUPAC – International Union of Pure and Applied Chemistry), разрабатываемая комиссией Международного союза теоретической и прикладной химии (ИЮПАК).
Согласно этой номенклатуре строение молекул органических веществ выражают при помощи сложных слов-названий. Различные части этих слов отражают особенности строения. Так например, у соединений насыщенного ряда (алканов) корень обозначает число углеродных атомов в главной цепи (самой длинной) или связанной с ней функциональной группе:
С -мет
С – С -эт
С – С – С -проп
С – С – С – С -бут
С – С – С – С – С -пент и далее корни греческих числительных.
Обозначения боковых заместителей (меньших по числу углеродных атомов) цепей, вводят в виде приставок к корню в алфавитном порядке. В названиях радикалов к обозначению числа углеродных атомов добавляют «ил» (метил, этил, пропил). Отсутствие или наличие двойной, тройной связи обозначают соответственно суффиксами «ан», «ен», «ин».
В сучае наличия повторяющихся заместителей используют умножающие приставки («ди», «три», «тетра» и т.д.) перед соответствующим элементом.
Местоположение заместителей указывают с помощью локантов – цифр или букв, для разделения которых применяют дефисы, запятые, скобки. При этом сумма локантов должна быть наименьшей.
Старшую характеристическую группу обозначают в последнем суффиксе. Если она расположена не у крайнего углеродного атома главной цепи (и возможны другие варианты расположения) – используют соответствующий локант.
Правильно составленному названию соответствует только одна формула.
Таким образом, согласно этой номенклатуре, в органическом соединении выделяется основа, в которую вместо одного или нескольких атомов водорода входят какие-то заместители. Для углеводородов, например, необходимо выбрать главную, т.е. наиболее длинную цепь, а затем пронумеровать атомы углерода в ней. При этом начало нумерации определяет близость к концу цепи кратной (непредельной) связи или большего числа простейших заместителей. Количество атомов углерода в основной цепи определяет корень названия этой основыв соответствии с названием предельного углеводорода, содержащего то же число атомов (эт-, бут-, гекс- и т.д.). Затем следует суффикс, определяющий наличие или отсутствие кратных связей (-ан – когда нет кратных связей; ен-1 двойная связь; диен -2 двойные связи; -ин – 1 тройная связь и т.п.). Заместители в соответствии с их качеством и количеством перечисляются в начале названия, при этом цифра перед названием заместителя указывает тот атом углерода в основной цепи, при котором он находится:
1 2 3 4 5 6 7
Н2С= С - СН = С – СН – СН - СН3
| | | |
СН3 Cl C2H5 СН3
2,6-диметил-4-хлор-5-этил-гептадиен-1,3
Цифры в конце названия указывают атомы углерода, после которых расположены кратные связи.
СН3
5 4 3| 2 1
Н2С = СН – С – С ≡ СН 3-метил-3-этилпентен-4-ин-1
|
C2H5
В циклических соединениях начало нумерации определяется по тем же принципам (наличию кратной связи или заместителя). Следует отметить, что для бензола при наличии двух и более заместителей, помимо цифровых обозначений, часто используют приставки: орто- (о), мета- (м), пара- (п). Если положение первого заместителя соответствует цифре 1, то другие положения называются соответственно: 2 и 6 – орто-положениями; 3 и 5 –мета-положениями; 4 – пара-положеним.
Для пространственных изомеров применяют стереохимическую номенклатуру. Оптические изомеры, вращающие плоскость поляризованного света вправо (правовращающие), обозначают знаком (+), левовращающие – знаком (-). Направление вращения определяется экспериментально.
Часто используемой и точной в обозначении изомеров является система Кана-Ингольда-Прелога (R-, S-). Она позволяет определить абсолютную конфигурацию атомов и групп вокруг каждого хирального центра. Для этого необходимо:
- Определить порядок старшинства групп, соединенных с асимметрическим атомом. Атом, имеющий наибольший атомный номер, считается старшим. Если в первом круге старшинство совпадает – сравнивают сумму порядковых номеров атомов второго круга. Кратные связи считают за две и три соответственно.
- Ориентировать хиральный центр в пространстве таким образом, чтобы младший заместитель оказался в максимально удаленном положении. При этом три старшие группы будут направлены на наблюдателя.
- Соединить воображаемой стрелкой старшие заместители последовательно от 1-го ко 2-му и к 3-му.
- Если старшинство убывает по часовой стрелке, то атому присваивают наименование R ( от латинского rectus – правый), если против часовой – S ( от латинского sinister – левый).
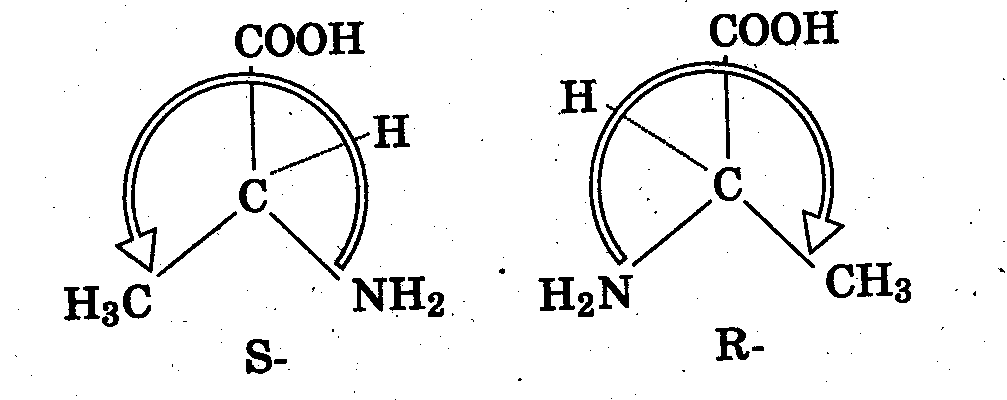
Обозначение изомеров в этом случае не имеет никакого отношения к направлению вращения и имеет историческое происхождение.
Для геометрических изомеров употребляют обозначения цис- или Z (одинаковые или родственные заместители расположены по одну сторону плоскости двойной связи или цикла) и транс- или Е (одинаковые или родственные заместители расположены по разные стороны плоскости двойной связи или цикла).
Специфичность частных случаев пространственной изомерии выделяет их номенклатуру в специальный раздел – стереохимическую номенклатуру.
Пример 1.
Назвать по систематической номенклатуре (IUPAC):

Решение.
- Определяем главную функциональную группу и выбираем для неё суффикс, обозначающий принадлежность к классу (табл.1). В данном случае функциональная группа отсутствует.
- Выбираем главную (самую длинную) цепь, определяющую корень в названии. Главная цепь содержит 7 атомов углерода – корень «гепт».
- Oпределяем степень насыщенности: соединение относится к предельным углеводородам – суффикс «ан».
- Устанавливаем характер имеющихся заместителей и располагаем их в алфавитном порядке в префиксной части названия: заместители одного вида – метил.
- Определяем умножающие приставки, имея в виду, что они не учитываются при алфавитном размещении префиксов.
- Проводим нумерацию главной цепи с учётом того, что сумма локантов (номеров, указывающих положения заместителей у атомов цепи) должна быть наименьшей. Цифры (локанты) ставят перед префиксами и после суффиксов, к которым они относятся: 2,2,3,5-тетраметил.
- Компонуем название, используя соответствующие разделительные знаки: 2,2,3.5-тетраметилгептан.
Пример 2.
Назвать следующее соединение: СН3-СНCl-СН(CH3)-СН=СCl-СН3
Решение.
- Функциональной группы, обозначаемой префиксом, нет.
- Главная цепь: шесть углеродных атомов «гекс».
- Cтепень ненасыщенности: двойная связь «ен».
- Заместители: «метил», «хлор».
- Умножающие приставки: два атома хлора «ди».
- Нумерация справа налево (двойная связь должна получить наименьший номер 2).
- Локанты заместителей 4,2,5.
- Название в целом: 4-метил-2,5-дихлоргексен-2
Таблица 1
Классы соединений и названия характеристических групп
| Класс | Формула* | Префикс | Суффикс |
| катионы | | онио | оний |
| карбоновые кислоты | -СООН | карбокси | карбоновая кислота |
| сульфоновые кислоты | -SO3H | сульфо | сульфокислота |
| амиды | -СОONH2 -C(O)NH2 | карбамоил - | карбоксамид амид |
| нитрилы | -С≡N | циано - | карбонитрил нитрил |
| альдегиды | -СНО | формил, оксо | карбальдегид, аль |
| кетоны | ›С(О) | оксо | он |
| спирты, фенолы | -ОН | гидрокси, окси | ол |
| тиолы | -SH | меркапто | тиол |
| амины | - NH2 | амино | амин |
| двойная связь | = | - | -ен |
| тройная связь | ≡ | - | -ин |
| эфиры (простые) | -OR | алкокси | - |
| галогенпроизводные | F, Cl, Br, I | фтор, хлор, бром, йод | фторид, хлорид, бромид, иодид |
| нитрозосоединения | -NO | нитрозо | - |
| нитросоединения | -NO2 | нитро | - |
| диазосоединения | -N2 | диазо | диазоний |
| азиды | -N3 | азидо | азид |
* - группа, стоящая выше, считается старшей
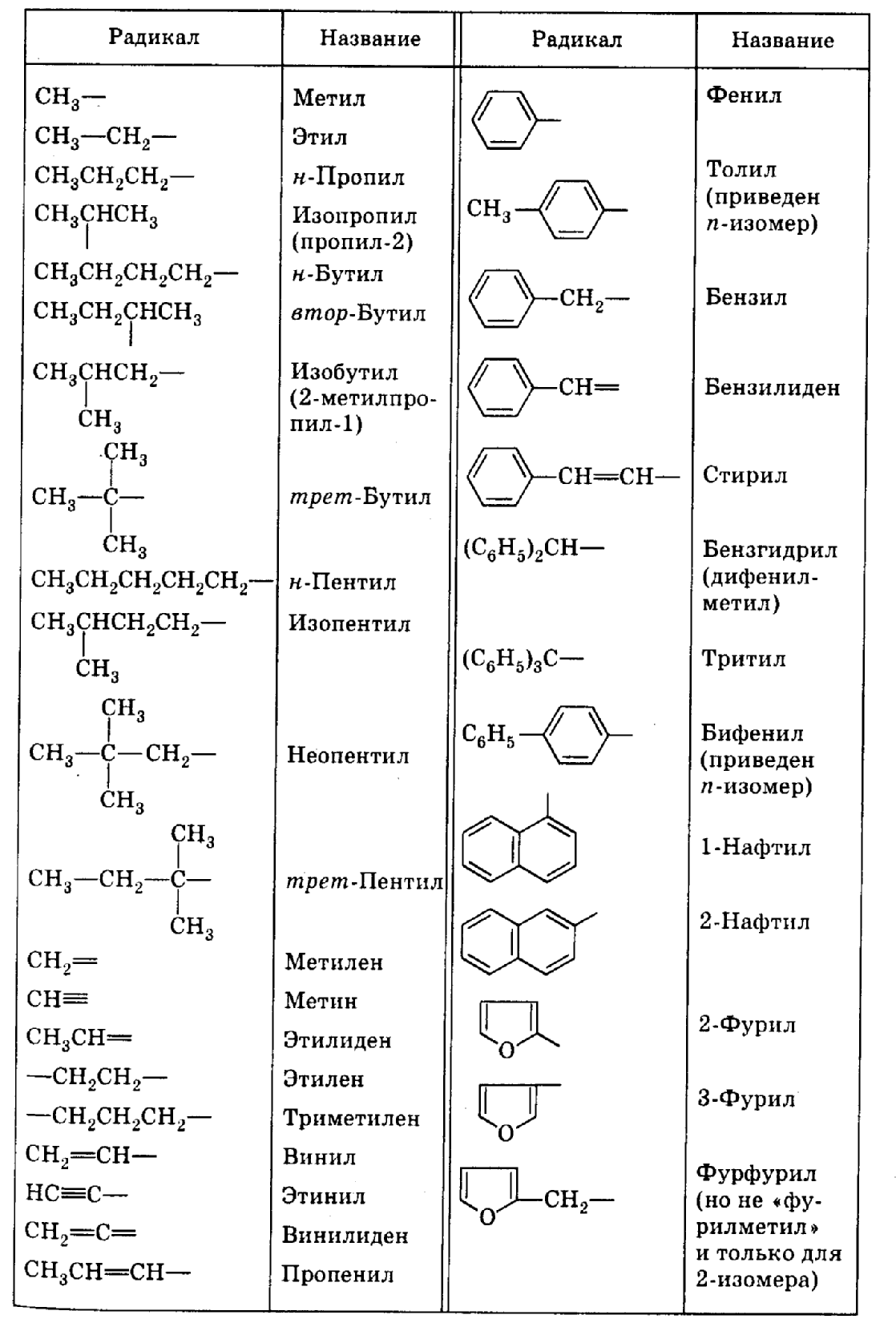
Таблица 2
Названия важнейших радикалов