Тематический план лабораторно-практических занятий по курсу «Биоорганическая химия» для студентов Iкурса специальности «Стоматология» медицинского факультета на 1 семестр 2011-2012 уч года №
| Вид материала | Тематический план |
СодержаниеУчебник, с. 431-456 |
- Тематический план лабораторно-практических занятий по курсу «Механизмы биоорганических, 111.47kb.
- Календарно-тематический план лекций и лабораторно-практических занятий по биоорганической, 134.42kb.
- Календарно-тематический план самостоятельной работы для студентов Iкурса фармацевтического, 133.88kb.
- План лекций и практических занятий по дисциплине «Химия» на 1 семестр 2011-2012, 46.33kb.
- План занятий по курсу «общая химия» для студентов 1 курса до физического факультета, 34.83kb.
- Календарно-тематический план лабораторно-практических занятий по ботанике для студентов, 57.62kb.
- План практических занятий по патофизиологии на 5 семестр 2011-2012 учебного года для, 346.6kb.
- Темы практических занятий по неврологии и нейрохирургии для студентов 4 курса стоматологического, 15.63kb.
- Учебной работе Профессор С. Н. Цыбусов 06. 02 четная неделя Расписание Практических, 17.43kb.
- Тематический план на 2 семестр 2011/2012 уч год по курсу «история медицины», 154.62kb.
ТЕМАТИЧЕСКИЙ ПЛАН
лабораторно-практических занятий по курсу « Биоорганическая химия»
для студентов I курса специальности «Стоматология» медицинского факультета на 1 семестр 2011-2012 уч. года
| № п\п | Тема занятия | Литература | |
| 1. | Введение в лабораторный практикум. Строение, классификация и номенклатура органических соединений. |
| Н.А.Тюкавкина, Ю.И. Бауков, «Биоорганическая химия». М., Мед. 1991 (в дальнейшем – учебник), с. 16-28, 52-54. Н.А. Тюкавкина. «Руководство к лабораторным занятиям по биоорганической химии. М. Мед. 1985г (в дальней-шем – практикум) с. 7-9, 24-26 Беканов М.Х. и др. «Методические указания по изучению номенклатуры биоорганических соединений с контролирующе- обучающей программой на ЭВМ., Нальчик, 1987 |
| 2. | Методы очистки и исследования органических соединений. Конформация ациклических и циклических соединений. |
8. Конформация ациклических соединений. Проекционные формулы Ньюмена. Энергетическая характеристика конформационных состояний. 9. Конформация циклических соединений. Аксиальные и экваториальные связи. | Практикум, с. 10-23. Опыт 2 с. 12. Учебник, с. 54-71, с. 495-512. |
| 3. | Сопряжение. Электронные эффекты. |
| Учебник, с. 29-50 Практикум, с. 34-41 Методические разработки к лекционному курсу «Биоорганическая химия» часть 1. |
| 4. | Кислотные и основные свойства органических соединений. |
| Учебник, с. 100-115 Практикум, с. 42-52, 89-90. Опыты: 10,11,12, с. 52-53 Методические разработки к лекционному курсу «Биоорганическая химия» часть 1. |
| 5. | Реакции электрофильного при- соединения и замещения | 1.Понятие о механизме реакций. Классификация органических реакций.
Правило ориентации в ароматическом кольце. Орентанты 1-го и 2-го рода | Учебник, с. 124-148 Практикум, с 61-80, опыты:17,18, с. 79-80 Методические разработки к лекционному курсу «Биоорганическая химия» часть 1. Методические указания «Реакционная способность органических соединений и факторы, влияющие на реакционную способность ароматических углеводородов», Нальчик 1999. |
| 6. | Реакции нуклеофильного замещения и элиминирования у Sp3-гибридизованного атома углерода. Рейтинг |
| Учебник, с. 149-180 Практикум, с. 81-88 опыты: 19,21. Методические разработки к лекционному курсу «Биоорганическая химия» часть 1. |
| 7. | Реакции нуклеофильного присоединения с участием карбонильной группы. |
Окисление и восстановление альдегидов и кетонов. | Учебник, с. 181-193 Практикум, с. 92-106 опыты: 22,23,26 стр. 106-108. Методические разработки к лекционному курсу «Биоорганическая химия» часть 1. |
| 8. | Реакции нуклеофильного замещения в карбоновых кислотах. |
| Учебник, с. 162, 194-213, 247, 460 Практикум, с. 108-117 опыты: 27,28,29,30. Методические разработки к лекционному курсу «Биоорганическая химия» часть 1. |
| 9. | Реакции окисления и восстановления органических веществ. |
| Учебник, с. 213-230 Практикум, с. 128-134 опыты: 31,32. |
| 10. | Гетерофункциональные соединения, метаболиты и биорегуляторы. Стереоизомерия. |
| Учебник, с. 68-87, 230-274 Практикум, с. 157-158, 138-156 опыты: 36,37,38. |
| 11. | Биологически активные гетероциклические соединения. |
5.Азолы (пиразол, имидазол, тиазол) и их производные. Производные пиразалона-5 6.Диазины (пиридазин, пиримидин) и их производные. 7.Барбитуровая кислота, пурин, ксантин, гипоксантин, мочевая кислота, аденин, гуанин, птиридин. 8.Алкалоиды. 9.Гетероциклические антибиотики. | Учебник, с. 275-304 Практикум, с. 76, 163-179 опыты: 40,41,42, 43,44. |
| 12. | α-аминокислоты Рейтинг |
| Учебник, с. 312-343 Практикум, с. 180-184. опыты: 45,46,47,48,49(1),50,51 с. 198-200. |
| 13. | Пептиды. |
| Учебник, с. 344-377 Практикум, с. 184-198. опыты: 52,53,54. |
| 14. | Моносахариды |
| Учебник, с. 377-407 Практикум, с.201-213 опыты: 55,56,57,58. |
| 15. | Дисахариды |
| Учебник, с. 407-429 Практикум, с. 215-222 опыты: 59,60. |
| 16. | Полисахариды | 1.Гомополисахариды: крахмал (амилоза и целлюлоза), гликоген, декстраны, целлюлоза. 2.Пектины (полигалактуроновая кислота) 3.Первичная структура полисахаридов и их гидролиз. 4.Понятие о вторичной структуре, строение амилозы и целлюлозы. 5.Гетерополисахариды: гиалуроновая кислота, хондроитинсульфаты. 6.Первичная структура. Представление о строении гепарина. 7.Понятие о смешанных биополимерах(пептидогликаны,протеогликаны,гликопротеины, гликолипиды). | |
| 17. | Нуклеозиды и нуклеотиды. Коферменты окисления и восстановления. |
| Учебник, с. 431-456Практикум, с. 222-234 |
| 18. | Липиды. Рейтинг |
| Учебник, с. 413-492 Практикум, с. 118-127 ,235-247.,Опыты 63-64 |
| 19. | Не омыляемые липиды | 1..Неомыляемые липиды. Терпены и терпеноиды: изопреноиды (мирцен, сквален, 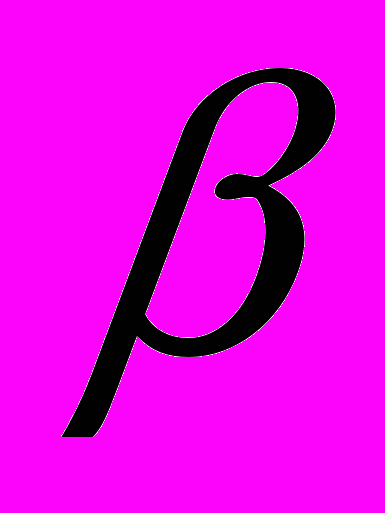 -каротины) -каротины) 2... Моно- и бициклические терпены (лимонен, ментол, камфора, бромкамфора). 3..Стероиды. Конформация 5α и 5β – стероидного скелета. Эстран, андростан, прегнан, холан, холестан и их производные. | Учебник, с. 413-492 Практикум, с. 118-127,235-247.,Опыты 63-64 |
