Нестационарные процессы деградации в щелочных аккумуляторах, закономерности и технологические рекомендации 05. 17. 03 «Технология электрохимических процессов и защита от коррозии»
| Вид материала | Закон |
СодержаниеСодержание диссертационной работы Вторая глава Состав газовой смеси, выделившейся в результате теплового разгона Третья глава Четвертая глава Пятая глава |
- Галушкина Наталья Николаевна тепловой разгон в щелочных аккумуляторах: закон, 314.51kb.
- Катодные процессы на силицидах металлов триады железа в кислых электролитах 05. 17., 237.17kb.
- Локальная коррозия оборудования из нержавеющих сталей при эксплуатации установок переработки, 371.28kb.
- Высокопроизводительные процессы электроосаждения никеля и сплава никель-фосфор из электролитов,, 468.58kb.
- Состояние структуры, электрохимическое поведение и магнитные свойства наноструктурируемых, 327.79kb.
- Выделение серебра из концентрированных хлоридных растворов 05. 17. 03 Технология электрохимических, 229.4kb.
- Электрохимическое получение наноразмерных pt/c катализаторов для твердополимерных топливных, 944.18kb.
- Получение оптически селективных и чёрных оксидных плёнок на алюминии и его сплавах, 222.41kb.
- Реферат по дисциплине " Технологические процессы микроэлектроники " на тему: Технологические, 1398.5kb.
- Учебно-методический комплекс дисциплины «Технологические процессы в сервисе» 2008, 1343.12kb.
СОДЕРЖАНИЕ ДИССЕРТАЦИОННОЙ РАБОТЫ
Литературный обзор состоит из четырех разделов, в которых рассматривается современное состояние вопроса по исследованию и моделированию нестационарных процессов деградации в щелочных аккумуляторах. Это, прежде всего: тепловой разгон; необратимые процессы накопления, приводящие к старению аккумуляторов в процессе их эксплуатации, такие как, накопление водорода в электродах аккумуляторов и накопление дендритов в сепараторе.
Наиболее малоизученным нестационарным процессом в щелочных аккумуляторах является тепловой разгон. Аналитический обзор литературы за последние 20 лет показывает, что работ по исследованию этого явления в аккумуляторах крайне мало. В зарубежной литературе значительно больше работ по изучению теплового разгона. Однако и там основная масса работ выполнена менеджерами по продажам аккумуляторов и имеет статистический или описательный характер, а не научно-исследовательский.
Такое незначительное внимание к явлению теплового разгона малооправданно, так как данный процесс является причиной более половины аварийных ситуаций, связанных с эксплуатацией аккумуляторов.
Подобное невнимание к этому негативному явлению, как нам кажется, можно объяснить двумя причинами. Во-первых, данное явление редкое не представляет ежедневную угрозу для работы приборов и систем, поэтому производители аккумуляторов не вкладывают значительных средств на изучение этой проблемы. Во-вторых, многим кажется очевидным механизм теплового разгона, в то время как до сих пор нет прямых экспериментальных подтверждений данного механизма и его искусственного воспроизведения. Так же нет детального анализа, как в отечественных, так и в зарубежных публикациях, продуктов, получаемых в результате теплового разгона (кроме литиевых аккумуляторов).
Практически все, что указывается о ТР можно свести к следующим утверждениям:
-тепловой разгон, встречается в НК, никель-металлогидридных, никель-водородных, свинцово-кислотных, литиевых, литий-ионных и литий-полимерных аккумуляторах;
-это явление наблюдается в аккумуляторах с длительным сроком эксплуатации;
-тепловой разгон − редкое явление в аккумуляторах;
-сложно создать условия, при которых процесс теплового разгона наступит однозначно, т.е. это спонтанное многофакторное явление.
Содержание обзора распределено по разделам следующим образом.
В первом разделе дана общая характеристика теплового разгона в аккумуляторах разных типов. Однако из анализа работ, не ясно является ли механизм теплового разгона одним и тем же в аккумуляторах различных систем. Из обзора, по крайней мере, очевидно, что в литий-ионных аккумуляторах механизм теплового разгона во многом отличается.
Тем не менее, по современным представлениям механизм теплового разгона в аккумуляторах любых электрохимических систем, в общем, подобен. Даже в случае различия механизмов теплового разгона в различных аккумуляторах между ними бесспорно много общего, это видно хотя бы по внешним признакам. Поэтому в работе дан обзор всех исследований по тепловому разгону, независимо от типа аккумуляторов, тем более их не так много.
В подразделах один – четыре первого раздела дан обзор работ по исследованию теплового разгона в НК, никель-металлогидридных, никель-водородных, свинцово-кислотных, литиевых, литий-ионных и литий-полимерных аккумуляторах. Отмечено, что в целом тепловой разгон является малоизученным процессом, хотя это явление в литиевых аккумуляторах изучено значительно лучше, чем в аккумуляторах других систем.
В данной работе показано, что в процессе эксплуатации НК аккумуляторов в их электродах накапливается очень большое количество водорода, что ведет к деградации электродов. Накопление водорода в электродах приводит к тепловому разгону, а также в целом ухудшает эксплуатационные характеристики аккумуляторов. Поэтому во втором разделе сделан обзор веществ, способных поглощать водород. В подразделах один – два второго раздела дан обзор работ по исследованию таких веществ. В частности дана классификация и общая характеристика накопителей водорода. Рассмотрены исследования процесса накопления водорода в металлогидридах, в углеродных материалах (графит, сажа), которые являются наполнителями в ламельных, намазных и прессованных электродах щелочных аккумуляторов.
В третьем разделе дан обзор работ по исследованию возникновения и роста дендритов через сепараторы и влиянию их на основные параметры аккумуляторов, а также методов борьбы с образованием дендритов в аккумуляторах. Процесс накопления дендритов в сепараторах является одним из исследуемых в данной работе процессов деградации аккумуляторов. Накопление дендритов в сепараторах приводит к тепловому разгону аккумуляторов, а также в целом ухудшает их эксплуатационные характеристики. Так как накопление дендритов в щелочных аккумуляторах является одной из причин ТР, то методы борьбы с образованием дендритов будут одновременно и методами борьбы с ТР. Обычно для борьбы с образованием дендритов используют методы:
-модификация состава или конструкции электродов;
-покрытие электродов пленкой;
-введение, в электролит различных добавок, включая поверхностно активные;
-создание новых сепараторов, включая комбинированные;
-использование новых переменноточных режимов заряда.
В четвертом разделе дан обзор работ по моделированию различных процессов в аккумуляторах и приведена классификация используемых моделей.
При описании процессов в аккумуляторах обычно используют следующие модели: статистические, динамические, конструктивные, структурные.
При статистическом моделировании, на основании экспериментальных данных строится функция регрессии. Такое моделирование используется на начальных этапах исследования какого-либо объекта, когда о нем ничего не известно. При конструктивном моделировании, модель явления или процесса, конструируется на основании разумных предположений, экспериментальных фактов, а также с применением тех или иных физических или химических законов, т.е. данные модели с самого начала строго не опираются на фундаментальные динамические законы природы. При динамическом моделировании, модель строится с самого начала, опираясь на фундаментальные законы природы. Как правило, моделирование выполняется или в рамках макрооднородной модели пористого электрода, или в рамках модели отдельной поры.
Особую группу моделей составляют структурные модели электрохимических явлений. Структурный подход впервые был применен при моделировании процессов в теории импеданса. В настоящее время он с успехом применяется при моделировании явлений в аккумуляторах, причем в сугубо нелинейных областях в отличие от теории импеданса.
Вторая глава состоит из десяти разделов и посвящена исследованию процесса теплового разгона в щелочных аккумуляторах.
В первом разделе на основании анализа литературных источников намечен план экспериментальных исследований. Во втором разделе описана методика циклирования щелочных аккумуляторов с целью обнаружения теплового разгона. Все аккумуляторы заряжались последовательно при постоянных напряжениях: 1,45; 1,67; 1,87; 2,2 В. Нижнее значение исследуемого диапазона зарядных напряжений соответствует буферному напряжению работы аккумуляторов. В третьем разделе описана установка для циклирования аккумуляторов и сбора выделяющегося в результате теплового разгона газа и пара.
В четвертом разделе дана классификация всех существующих аккумуляторов по типу электродов, плотности их упаковки, герметичности и т.д. В результате все аккумуляторы для дальнейших исследований были разбиты на четыре группы: не герметичные аккумуляторы с металлокерамическими оксидно-никелевыми электродами, в этой же группе рассматривались и аккумуляторы с прессованными и намазными оксидно-никелевыми электродами; не герметичные аккумуляторы с ламельными электродами; герметичные призматические аккумуляторы; герметичные цилиндрические и дисковые аккумуляторы.
В пятом разделе описаны результаты циклирования аккумуляторов с металлокерамическими, прессованными и намазными оксидно-никелевыми электродами (с металлокерамическими электродами (НКБН-25-У3, НКБН-40-У3, 2НКБ-32, 2НКБ-15, НКБН-6, НКБН-3.5), с намазными электродами (НКБН-3,5), с прессованными электродами (2КНП-24, 2КНП-20, 3ШНКП-10М-0,5, 2КНБ-2) (по 10 штук каждого типа). Заряд производился при постоянных напряжениях, отмеченных выше, а разряд и контрольно-тренировочные циклы (для исключения эффектов памяти при смене режимов заряда) − в соответствии с инструкцией по эксплуатации конкретных батарей.
На основании проведенных экспериментальных исследований установлено, что ТР довольно редкое явление. Из 640 выполненных зарядно-разрядных циклов для каждого типа аккумуляторов, ТР наблюдался только в двух случаях для аккумуляторов НКБН-25-У3, в двух случаях для НКБН-40-У3 и по одному случаю для аккумуляторов 2НКБ-32 и 2НКБ-15.
Вероятность появления ТР увеличивается с ростом срока эксплуатации аккумуляторов, так как во всех случаях, когда наблюдался ТР, аккумуляторы имели сроки эксплуатации, как правило, больше пяти лет при гарантийном сроке службы в три года. При малых сроках эксплуатации аккумуляторов, ТР никогда не наблюдался.
Вероятность возникновения ТР повышается с ростом напряжения заряда аккумуляторов, так как во всех случаях когда наблюдался ТР, заряд аккумуляторов выполнялся при напряжениях 1,87 В и 2,2 В, что значительно превышает среднее напряжение эксплуатации данных аккумуляторов на объекте в буферном режиме (1,35-1,5 В).
В аккумуляторах с намазными (НКБН-3.5), и прессованными электродами (2КНП-24, 2КНП-20, 3ШНКП-10М-0,5, 2КНБ-2) тепловой разгон не наблюдался. Это может быть связано как с типом электродов, так и с типом используемых сепараторов. В данных аккумуляторах используются сепараторы из толстых тканей. Так как процесс прорастания дендритов кадмия сильно зависит от толщины сепаратора, структуры и диаметра пор, то с увеличением толщины сепаратора и уменьшением диаметра пор процесс существенно замедляется, а дендриты получаются не достаточно надежными для разогрева электродов и запуска теплового разгона.
В экспериментах не пошли на ТР аккумуляторы малой емкости с металлокерамическими электродами (НКБН-6, НКБН-3,5 (керамика)), намазными (НКБН-3,5) и прессованными (2КНБ-2). По всей вероятности для начала ТР важна общая масса аккумуляторов и общий ток заряда.
В подразделах один – пять, пятого раздела выполнены также экспериментальные исследования по измерению параметров аккумуляторов НКБН-25-У3, НКБН-40-У3, 2НКБ-32 и 2НКБ-15 в процессе ТР. Определялись изменение следующих параметров: зарядного тока, напряжения на клеммах аккумуляторов, температуры электродов аккумуляторов, динамики газовыделения.
Исследования показали, что в процессе теплового разгона ток заряда резко возрастает до очень больших значений 6-14Q (Q – номинальная емкость аккумулятора), а затем, резко падает, вследствие выкипания электролита и резкого соответствующего возрастания внутреннего сопротивления аккумуляторов.
Процесс ТР может возникать неоднократно и спонтанно в течение одного заряда (рис. 1), при этом ток заряда то возрастает, то убывает. Возникновение и затухание процесса ТР в каком-либо месте электрода приведет сначала к резкому росту тока заряда, а затем к такому же резкому падению тока вследствие испарения электролита и образования газовой пробки в прогоревшем участке сепаратора. Это, в свою очередь, приведет к увеличению плотности тока в других местах электродов, что является причиной запуска ТР в другом месте, возможно, между другой парой электродов и т.д.
После ТР ток в аккумуляторе может стать или очень маленьким, это можно объяснить резким возрастанием внутреннего сопротивления аккумулятора вследствие выкипания электролита и образования газовых пробок между электродами, или очень большим, вследствие закорачивания электродов в местах сильного прогорания сепараторов рис.1.
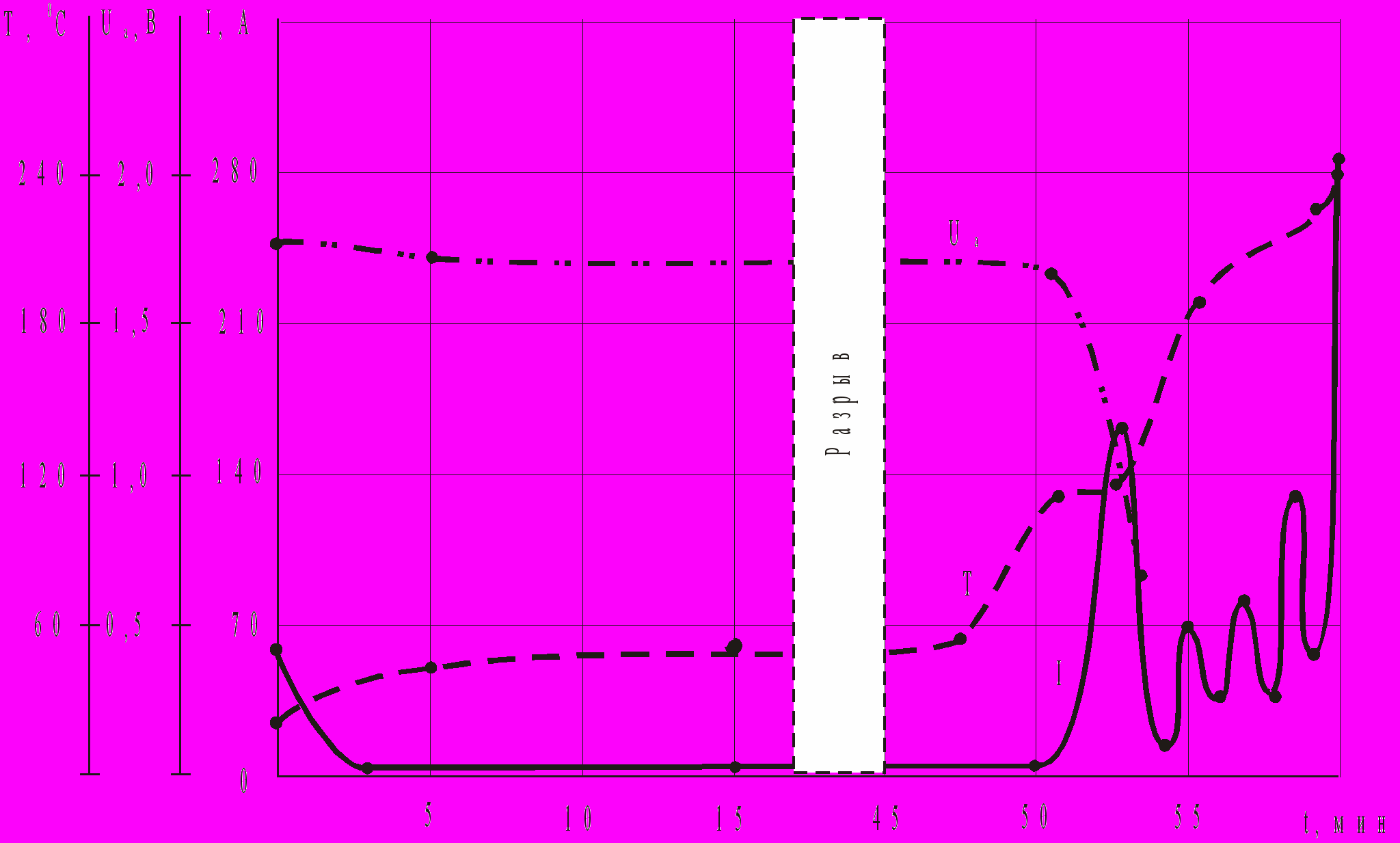
Рис. 1. Изменения параметров аккумулятора НКБН-25-У3 во время теплового разгона: I − ток заряда аккумулятора; Ua − напряжение на клеммах аккумулятора; Т − температура положительной клеммы аккумулятора
В процессе ТР напряжение на клеммах аккумулятора резко падает примерно до 0,5 В. Данное падение напряжения нельзя объяснить только уменьшением внутреннего сопротивления аккумулятора. Единственным объяснением может быть, только предположение, что тепловой разгон связан с протеканием мощной электрохимической реакции, идущей при более низкой разности потенциалов электродов, чем реакция заряда аккумуляторов.
Температура электродов в процессе ТР резко возрастает до очень больших значений (больше 250 0С). При этом однажды полиамидный корпуса аккумулятора НКБН-25-У3 полностью расплавился и загорелся, в других случаях корпус только оплавлялся.
В результате ТР из аккумулятора в течении 2-4 минут выделяется большое количество парогазовой смеси состоявшей на 70-77 % из газа, на 23-30 % из водяного пара. Состав, парогазовой смеси представлен в табл. 1.
Выделившийся в результате теплового разгона газ имел состав: водорода 85-95 %, кислорода 4-14 %, прочих газов менее 1 %. Если предположить, что в результате теплового разгона происходит разложение воды, то в газовой смеси должно быть 33,3 % кислорода и 66,7 % водорода. Экспериментальные результаты показали, что водорода намного больше. Это можно объяснить, только предположив, что водород уже присутствовал в электродах в какой-то форме еще до теплового разгона, а в результате теплового разгона, возможно из-за высокой температуры, он выделился в больших количествах.
Таблица 1
Состав газовой смеси, выделившейся в результате теплового разгона
| Тип аккумулятора | Номер аккумулятора | Общее количество газовой смеси, выделившейся в результате ТР, л | Количество выделившегося пара, л | Оставшийся газ, л |
| НКБН-25-У3 | 1 | 351 | 63 | 288 |
| 2 | 342 | 60 | 282 | |
| НКБН-40-У3 | 1 | 490 | 107 | 383 |
| 2 | 506 | 112 | 394 | |
| НКБ-32 | 1 | 410 | 70 | 340 |
| НКБ-15 | 1 | 205 | 31 | 174 |
В шестом разделе описаны результаты циклирования аккумуляторов с ламельными электродами (3ШНК-10-0,5, КН-10, НК-13, НК-28, НК-55, НК-80, НК-125, КН-150Р, НКЛБ-70, ТНК-350-Т5) (по 10 штук каждого типа). Заряд производился при постоянных напряжениях, отмеченных выше, а разряд и контрольно-тренировочные циклы в соответствии с инструкцией по эксплуатации конкретных батарей. У всех аккумуляторов срок службы превышал гарантийный в полтора-два раза. Несмотря на это, из 320 зарядно-разрядных циклов, выполненных для каждого типа аккумуляторов, тепловой разгон не наблюдался ни в одном случае. Результаты проведенных экспериментальных исследований свидетельствуют о маловероятности или невозможности теплового разгона в НК аккумуляторах данной конструкции.
В седьмом разделе описаны результаты циклирования герметичных призматических НК аккумуляторов (НКГК-3С, НКГК-4СК, НКГ-8К, KCSL 11, KCSL 13, НКГ-10Д, НКГ-30СА, НКГК-33СА, НКГ-50СА, НКГ-100СА) (по 5-10 штук каждого типа). Заряд производился при постоянных напряжениях, отмеченных выше, а разряд и контрольно-тренировочные циклы − в соответствии с инструкцией по эксплуатации конкретных батарей.
На основании проведенных экспериментальных исследований установлено, что тепловой разгон довольно редкое явление в герметичных НК аккумуляторах, так как из 320 выполненных зарядно-разрядных циклов для каждого типа аккумуляторов при больших напряжениях заряда, тепловой разгон наблюдался только в двух случаях для аккумуляторов НКГ-50СА, и по одному случаю для аккумуляторов НКГ-100СА, НКГК-33СА, НКГ-8К.
В экспериментах не пошли на тепловой разгон аккумуляторы малой емкости НКГК-4СК, НКГК-3С. По всей вероятности это общее явление для всех НК аккумуляторов малой емкости.
Вероятность появления теплового разгона увеличивается с ростом срока эксплуатации аккумуляторов и напряжения заряда, та как во всех случаях теплового разгона аккумуляторы имели сроки эксплуатации, примерно в два раза, больше чем их гарантийный срок.
Качественно графики для изменения: тока, напряжения на клеммах аккумуляторов, температуры положительной клеммы аккумулятора и выделившегося газа при тепловом разгоне в герметичных НК аккумуляторах такое же, как и в не герметичных.
Процесс теплового разгона в герметичных аккумуляторах проходит менее интенсивно и с меньшим выделением тепла, чем в не герметичных аккумуляторах той же емкости. Объем выделившейся парогазовой смеси примерно в 8 раз меньше чем из не герметичных аккумуляторов той же емкости. Процентный состав выделившейся парогазовой смеси примерно такой же, как и в не герметичных аккумуляторах.
В восьмом разделе описаны результаты циклирования герметичных цилиндрических и дисковых НК аккумуляторов (Д-0,02С, Д-0,06Д, Д-0,09С, Д-0,26С, Д-0,26Д, Д-0,4С, НКГЦ-0,9, НКГЦ-1,3-2, НКГЦ-1,8-2, НКГЦ-3,5-2) (по 10 штук каждого типа). Заряд производился при постоянных напряжениях, отмеченных выше, а разряд и контрольно-тренировочные циклы − в соответствии с инструкцией по эксплуатации конкретных батарей. Несмотря на длительный срок эксплуатации данных аккумуляторов и выполненные 320 зарядно-разрядных циклов для каждого типа, ни один из исследуемых аккумуляторов не пошел на тепловой разгон. По всей вероятности отсутствие теплового разгона в аккумуляторах малой емкости это общее явления для всех НК аккумуляторов малой емкости.
В девятом разделе описаны результаты никель-железных (НЖ) аккумуляторов (ТЖН-250-У2, ВНЖ-250П-У2, ТНЖ-350-У5, ТНЖШ-400-У5, ТНЖШ-500-У5) (по 5 штук каждого типа). Заряд производился при постоянных напряжениях, отмеченных выше, а разряд и контрольно-тренировочные циклы − в соответствии с инструкцией по эксплуатации конкретных батарей. Несмотря на длительный срок эксплуатации данных аккумуляторов и выполненные 160 зарядно-разрядных циклов для каждого типа, ни один из исследуемых аккумуляторов не пошел на тепловой разгон. Следовательно, в НЖ аккумуляторах с ламельными электродами тепловой разгон или вообще невозможен или крайне вероятен.
В десятом разделе выполнен визуальный анализ последствий теплового разгона и было установлено, что тепловой разгон является локальным явлением, поскольку в результате этого процесса сепаратор прогорает только в определенных местах, а не на всей поверхности электрода.
Круги прогорания сепаратора расположены на различных электродах в совершенно различных местах. Следовательно, можно сделать вывод, что тепловой разгон имеет случайный характер и возникает в случайных местах.
Места прогорания сепаратора имеют форму правильных кругов, причем совершенно различного радиуса. Следовательно, можно предположить, что тепловой разгон начинается из точки и, подобно процессу горения, равномерно распространяется по радиусу от данной точки.
Третья глава состоит из восьми разделов и посвящена исследованию накопления газов в электродах щелочных аккумуляторов, как одного из процессов деградации аккумуляторов.
В первом разделе описана методика эксперимента и экспериментальная установка для исследования процесса выделения газов из электродов аккумуляторов путем их термического разложения. Во втором разделе описана методика анализа состава газовой смеси (водород, кислород) взрывным методом.
В третьем разделе, в предварительных опытах, были найдены параметры для ведения процесса термического разложения электродов. Разложение каждого электрода производилось при температуре 800 0С. Данная температура была выбрана на основании следующих соображений. В предварительных опытах было установлено, что начало заметного выделения газа начинается: для кадмиевого электрода с 340 0С, а для оксидно-никелевого с 660 0С. Существенное выделение газа начинается для оксидно-никелевого и кадмиевого электродов при температурах более 740 0С. Скорость выделения газа увеличивается с ростом температуры, однако, после 800 0С этот рост уже замедляется. Таким образом, температура 800 0С была выбрана как оптимальная для термического разложения как кадмиевого, так оксидно-никелевого электродов.
Разложение каждого электрода происходило в среднем: для кадмиевого электрода за 7 дней, а для оксидно-никелевого за 13 дней, по 11 часов в сутки (для аккумуляторов с металлокерамическими оксидно-никелевыми электродами) и за 7 дней для обоих электродов для аккумуляторов с прессованными, намазными и ламельными электродами. В день из электрода выделялось газа: для кадмиевого электрода от 175 мл/г (миллилитров газа на один грамм веса электрода) в первые дни, до 4 мл/г − в последние; для оксидно-никелевого − от 250 мл/г, до 4 мл/г. Процесс термического разложения прекращался, когда суточное выделение газа оставалось менее 4 мл/г.
В четвертом разделе описаны результаты определения количества газа, выделившегося при термическом разложении оксидно-никелевых и кадмиевых электродов, взятых по три электрода из аккумуляторов следующих типов НКБН-25-У3, НКБН-40-У3, НКБН-6, НКБН-3.5(с металлокерамическими электродами), НКБН-3.5 (с намазными электродами), 2НКБ-32, 2НКБ-15, 2КНП-24, 2КНП-20, 3ШНКП-10М-0,5, 2КНБ-2. На основании результатов экспериментов сделаны обобщения:
-Действительно в электродах НК аккумуляторов с длительным сроком эксплуатации, еще до теплового разгона присутствует очень большое количество водорода. Например, в целом, в авиационной батарее 20НКБН-25-У3 содержится около 805*20=16100 л водорода. Это очень большой объем. Выход такого объема водорода во время теплового разгона из аккумуляторов в салон самолета может привести к взрыву очень большой мощности. Последствия такого взрыва могут быть самыми катастрофическими. Таким образом, аккумулятор НКБН-25-У3 представляет собой источник повышенной опасности.
-В целом в аккумуляторах с прессованными электродами содержится меньше водорода, чем в аккумуляторах с металлокерамическими электродами, при той же емкости аккумулятора. Это может быть связано как с меньшим сроком эксплуатации исследованных аккумуляторов по сравнению с аккумуляторами с металлокерамическими электродами, так и с особенностями эксплуатации данных аккумуляторов.
-В газовой смеси, выделяющейся в результате термического разложения как кадмиевого, так и оксидно-никелевого электродов находится, в среднем, 99 % водорода, 0,7 % кислорода и 0,3 % прочих газов. Подробный состав прочих газов нами не анализировался, так как они не могут оказать какого-либо влияния на процесс ТР, хотя бы из-за их малого количества. К тому же, их количество находится в пределах абсолютной ошибки измерения 0,5 %.
Во втором и третьем подразделах четвертого раздела исследуется зависимость скорости газовыделения из электродов данных аккумуляторов в зависимости от температуры разложения. Оксидно-никелевые электроды разлагались при температурах: 700; 900; 1000; 1100 0С, а кадмиевые − при температурах: 500; 700; 900; 1100 0С. Скорость газовыделения определялась по объему выделившегося газа в течение пяти минут.
Установлено, что скорость газовыделения уменьшается экспоненциально во времени. С ростом температуры разложения, скорость газовыделения и количество выделившегося газа возрастают. То есть чем выше температура, тем больше можно извлечь водорода из электродов. Это можно объяснить, предположив, что водород в электродах находится за некоторым потенциальным барьером (в связанном состоянии). Тогда, чем выше температура, тем большее число молекул водорода, согласно распределению Больцмана, способно преодолеть этот барьер. Данный факт очень важен для понимания формы, в которой водород находится в электродах НК аккумуляторов.
В целом зависимость газовыделения от температуры сильней у металлокерамических оксидно-никелевых электродов, чем у прессованных.
Процесс термического разложения электродов проходил по 9-13 часов в день. На ночь процесс прерывался на 11-15 часов и на следующий день возобновлялся снова. При этом в момент запуска установки на следующий день в первые полчаса, скорость газовыделения всегда была значительно выше скорости газовыделения в момент отключения установки, то есть наблюдался процесс релаксации газовыделения. Данный характер газовыделения свидетельствует о том, что водород находится внутри самого электрода, причем в связанном состоянии. Тогда при термическом разложении, во внешних слоях электрода концентрация водорода постепенно уменьшается и скорость газовыделения падает. Во время отдыха, из-за неравномерности распределения концентрации водорода по глубине электрода, с помощью диффузионных процессов происходит выравнивание концентрации. Тогда на следующий день, в момент включения установки, концентрация в поверхностных слоях электрода будет выше, чем в момент отключения установки. Этим как раз и можно объяснить значительное возрастание скорости газовыделения в момент включения установки. Хочется подчеркнуть, что для наблюдения релаксации газовыделения, водород должен находиться в связанном состоянии. Только этим можно объяснить низкую скорость диффузии водорода к поверхности электрода и, следовательно, обеднение поверхностных слоев в процессе газовыделения. Следствием этих эффектов будут полученные релаксационные кривые. В общем релаксационные процессы в металлокерамических электродах более сильные, чем в прессованных. Это свидетельствует о том, что водород крепче связан в металлокерамических электродах и, следовательно, скорость диффузии его меньше, чем в прессованных электродах.
В четвертом подразделе четвертого раздела описаны результаты термического разложения электродов аккумуляторов с различным сроком эксплуатации. Показано, что чем больше срок эксплуатации аккумуляторов, тем больше водорода содержится в его электродах. Причем в электродах новых аккумуляторов водород полностью отсутствует. Однако, как правило, после трех лет эксплуатации количество водорода в электродах уже не увеличивается, то есть существует предел насыщения электродов водородом. Полученные результаты свидетельствуют о том, что водород накапливается в электродах щелочных аккумуляторов по мере их эксплуатации. Рассмотрим подробно ситуацию с зарядом аккумулятора КНП-20. При его заряде происходит перезаряд на 11-14 А*ч, так как все аккумуляторы перезаряжаются в 1,5-2 раза по сравнению с их номинальной емкостью. Такой перезаряд необходим, так как ток заряда распределяется экспоненциально по глубине пористого электрода поэтому, когда поверхностные слои электрода будут уже заряжены, и на них будет разлагаться электролит, внутренние слои будут продолжать еще заряжаться. Таким образом, данный перезаряд необходим, чтобы полностью зарядить электроды по всей их глубине. Однако при таком перезаряде из аккумулятора выделяется около 5 литров водорода и 2,5 литров кислорода. При длительной эксплуатации, аккумулятор КНП-20 накапливает около 380 литров водорода. Следовательно, теоретически такое количество водорода он мог бы накопить за 380/5=76 зарядно-разрядных циклов. Так как эти аккумуляторы выдерживают до 1000 зарядно-разрядных циклов, то данное количество водорода он вполне мог накопить в процессе эксплуатации.
В пятом разделе описаны результаты определения количества газа, выделившегося при термическом разложении оксидно-никелевых и кадмиевых ламельных электродов, взятых по три электрода из аккумуляторов следующих типов ТНК-350-Т5, НКЛБ-70, КН-150Р, НК-125, НК-80, НК-55, НК-28, НК-13, КН-10, 3ШНК-10-05.
Проведенные исследования показали, что в ламельных электродах НК аккумуляторов, еще до теплового разгона присутствует очень большое количество водорода, как и в аккумуляторах с металлокерамическими и прессованными электродами. Состав газовой смеси такой же, как и в предыдущих аккумуляторах.
В целом графики зависимости скорости газовыделения от температуры для ламельных электродов более близки к аналогичным графикам для прессованных электродов.
Релаксационные процессы газовыделения в прессованных и ламельных электродах подобны. Это свидетельствует о том, что химическая связь водорода в этих электродах подобна.
В шестом разделе описаны результаты определения количества газа, выделившегося при термическом разложении оксидно-никелевых и кадмиевых электродов, взятых по три электрода из герметичных призматических НК аккумуляторов следующих типов НКГК-3С, НКГК-4СК, НКГ-8К, KCSL 11, KCSL 13, НКГ-10Д, НКГ-30СА, НКГК-33СА, НКГ-50СА, НКГ-100СА.
На основании проведенных экспериментальных исследований установлено, что объем водорода в электродах герметичных аккумуляторов примерно в восемь раз меньше, чем в электродах не герметичных аккумуляторов той же емкости и с тем же типом электродов. Данный экспериментальный факт логически следует из герметичности рассматриваемых аккумуляторов. Водород накапливается в электродах НК аккумуляторов в процессе их эксплуатации, за счет разложения электролита на водород и кислород. Однако в герметичных аккумуляторах количество электролита ограничено, так как он не доливается при технологической профилактике аккумуляторов, как это делается в случае не герметичных аккумуляторов. Поэтому водорода в электродах герметичных аккумуляторов может быть накоплено не больше, чем его содержится во всем электролите аккумулятора. Рассмотрим для примера аккумулятор НКГ-50СА. В герметичных аккумуляторах содержится от 2 до 4 см3/(А*ч) электролита, то есть для данного аккумулятора от 100 до 200 мл. По нашим данным в этом аккумуляторе 150-160 мл электролита. Следовательно, при разложении всего электролита можно получить не более 200 литров водорода. Так как в исследованных нами аккумуляторах электролит был, и они работали, следовательно, не весь электролит разложился на водород и кислород. Поэтому в электродах аккумулятора НКГ-50СА могло накопиться водорода только значительно меньше, чем 200 литров, в экспериментах обнаружено примерно 130 л.
В остальном герметичные аккумуляторы подобны не герметичным с тем же типом электродов.
В седьмом разделе исследовалось газовыделение при термическом разложении электродов дисковых и цилиндрических аккумуляторов следующих типов Д-0,02С, Д-0,06Д, Д-0,09С, Д-0,26С, Д-0,26Д, Д-0,4С, НКГЦ-0,9, НКГЦ-1,3-2, НКГЦ-1,8-2, НКГЦ-3,5-2. Полученные результаты подобны результатам для герметичных аккумуляторов с учетом емкости данных аккумуляторов.
В восьмом разделе исследовалось газовыделение при термическом разложении электродов НЖ аккумуляторов следующих типов ТЖН-250-У2, ВНЖ-250П-У2, ТНЖ-350-У5, ТНЖШ-400-У5, ТНЖШ-500-У5. Полученные результаты подобны результатам для НК аккумуляторов с ламельными электродами.
Четвертая глава состоит из тринадцати разделов и посвящена исследованию процесса дендритообразования, как одного из процессов деградации щелочных аккумуляторов.
В первом разделе на основании анализа литературных источников и экспериментальных данных, полученных в предыдущих разделах, намечен план экспериментальных исследований.
Во втором разделе разработан метод искусственного запуска теплового разгона в щелочных аккумуляторах. На основании проведенных исследований, можно утверждать, что точкой запуска теплового разгона является проросший через сепаратор дендрит. В предложенной установке роль дендрита выполняла стальная игла, которая с помощью микровинта максимально близко приближалась к оксидно-никелевому электроду через отверстие сбоку в корпусе аккумулятора и в кадмиевом электроде. Аккумулятор заряжался при постоянном напряжении 1,87 В в течении 8 часов. Когда ток заряда падал до предельно малого значения (примерно 100-150 мА) и не изменялся в течение получаса, включался ключ и подавалось напряжение 2,2; 2,4; 2,8 В между оксидно-никелевыми электродами и стальной иглой. При этом в месте расположения иглы создавалась значительно большая плотность тока, чем в среднем по электроду. Это достигалось как за счет более близкого расположения иглы, так и за счет более высокого напряжения, что способствовало началу теплового разгона. На основании данных экспериментальных исследований можно сделать следующие заключения:
-Тепловой разгон можно вызывать искусственно, что создает большие возможности для изучения этого опасного явления. С помощью предложенной установки с вероятностью около 80 % удавалось запустить аккумулятор на искусственный тепловой разгон.
-Эксперименты на физической модели дендрита однозначно показывают, что причиной начала возникновения теплового разгона является дендрит, проросший от кадмиевого электрода к оксидно-никелевому в процессе эксплуатации аккумуляторов. Проросший дендрит локально разогревает оксидно-никелевый и кадмиевый электроды, что способствует возникновению мощной экзотермической реакции, которая как будет показано в главе 5 и является причиной процесса теплового разгона.
Так как физическая модель дендрита находилась ровно в центре кругов прогорания сепаратора, то можно утверждать, что экзотермическая реакция начинается в месте расположения дендрита, а потом подобно процессу горения распространяется по радиусу от центра.
В третьем разделе анализируются методы борьбы с дендритообразованием в аккумуляторах, а именно: модификация состава или конструкции электродов; покрытие электродов проводящей пленкой; создание новых сепараторов, включая комбинированные; введение в электролит различных добавок включаю поверхностноактивные; использование новых переменноточных режимов заряда. Как мне кажется, наиболее перспективным является пятый метод. Он применим к серийно выпускаемым аккумуляторам, без каких либо их изменений.
В четвертом разделе на основании макрооднородной модели пористого электрода формулируется система уравнений для теоретического анализа распределения тока по глубине пористого электрода при поляризации электрода переменным асимметричным током.
В пятом разделе предлагаются методы для экспериментального нахождения поляризационной функции исследуемого электрода с целью дальнейшего их использования в сформулированной ранее макрооднородной модели пористого электрода.
В шестом разделе решается сформулированная модель пористого электрода в активационно-омическом режиме, при поляризации электрода постоянным током для линейной и квадратичной поляризационных функций. Из решения следует, что при увеличении внешнего поляризующего тока глубина проникновения электрохимического процесса в глубь пористого электрода уменьшается. Таким образом, в случае заряда аккумуляторов при постоянном токе единственным способом улучшения распределение тока по глубине пористого электрода является уменьшение самого поляризующего тока. Это действительно приводит к улучшению распределения тока по глубине пористого электрода и к уменьшению необходимого перезаряда, а, следовательно, и к уменьшению газовыделения при заряде. Однако, это приводит также и к значительному увеличению времени заряда, что не всегда приемлемо на практике.
В седьмом разделе анализируются наиболее перспективные формы тока для заряда аккумуляторов переменным асимметричным током.
В восьмом разделе решается сформулированная модель пористого электрода в активационно-омическом режиме, при поляризации электрода переменным асимметричным током для линейной, но не симметричной поляризационной функции. В девятом разделе решается та же модель, но с учетом процессов миграции и диффузии, т.е. система уравнений вида:
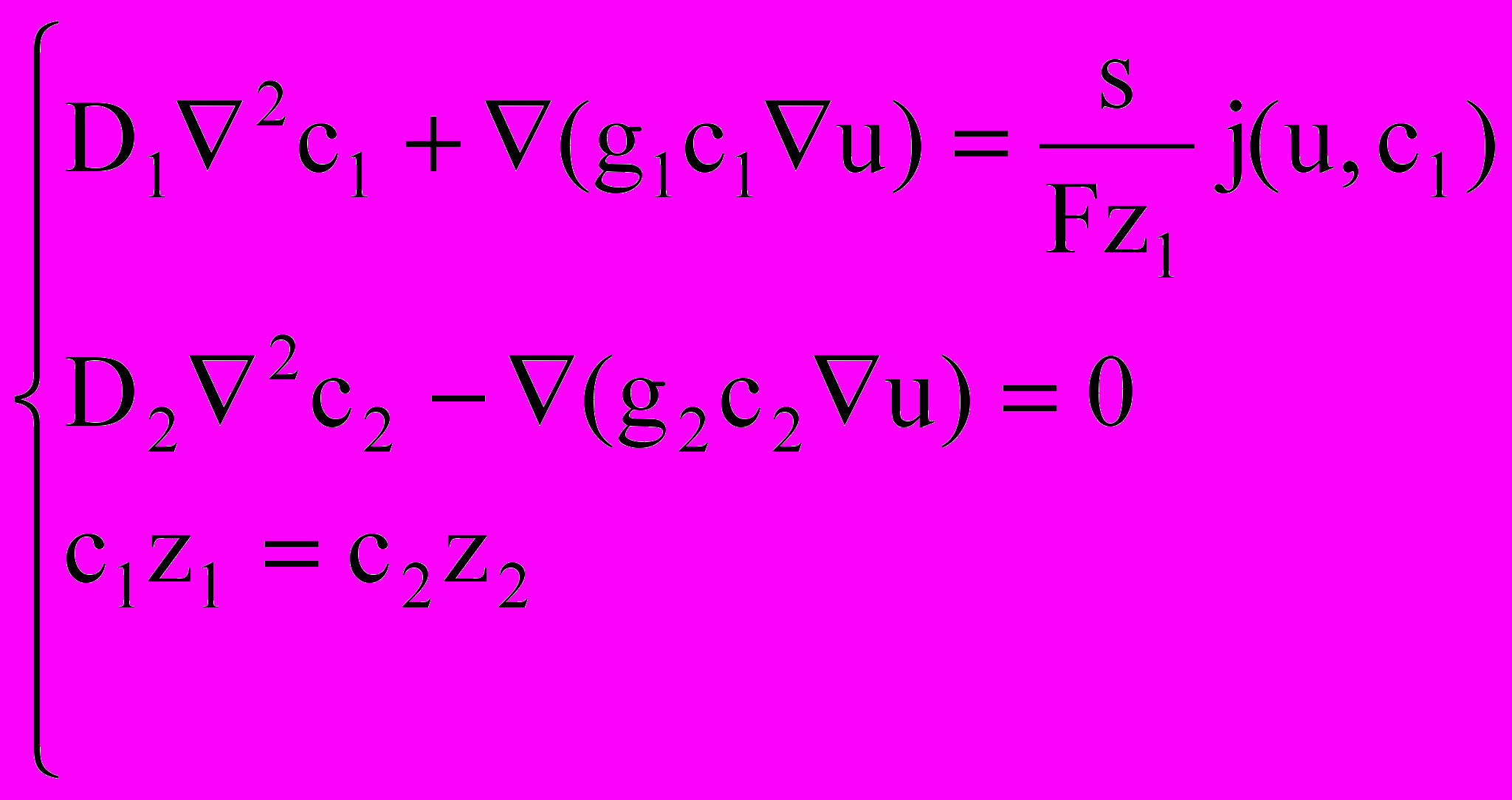
при граничных условиях
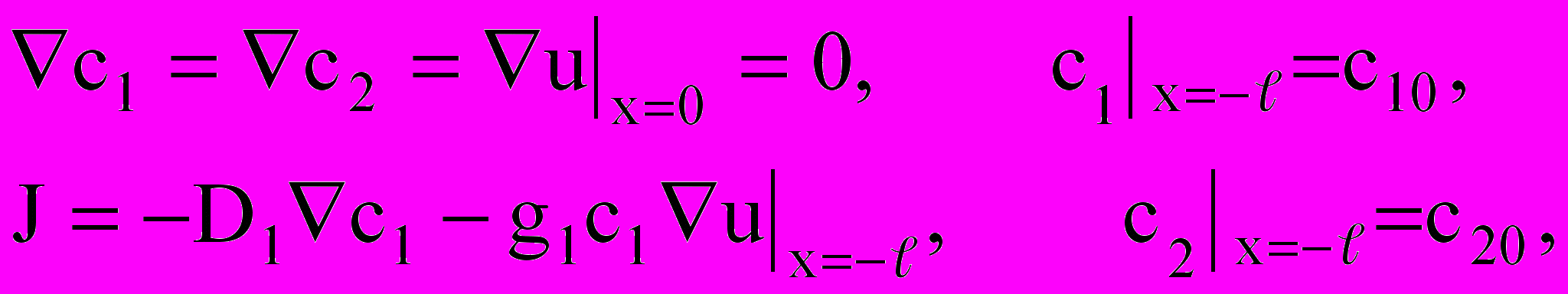
j(u,c1) – поляризационная функция исследуемого электрода, c1, c2 – концентрации ионов участвующих и не участвующих в электрохимической реакции заряда аккумулятора, J – внешний поляризующий ток, u – поляризация по глубине пористого электрода,
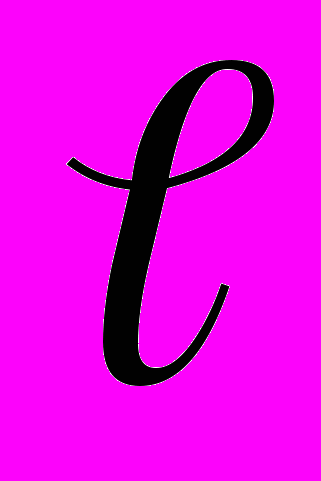 − половина толщины пористого электрода.
− половина толщины пористого электрода. Анализ обоих решений позволяет утверждать, что применение переменного асимметричного тока при заряде аккумуляторов позволяет добиваться любого распределения количества прошедшего электричества по глубине пористого электрода, в том числе и равномерного распределения или распределения с максимумом в центре электрода. В случае равномерного распределения количества прошедшего электричества по глубине пористого электрода, весь электрод будет заряжаться равномерно. При таком режиме заряда отпадает необходимость в перезаряде аккумуляторов. Таким образом, теоретически можно полностью исключить газовыделение при заряде аккумуляторов. Это позволит устранить одну из причин возникновения теплового разгона, а именно накопление водорода в электродах в процессе эксплуатации аккумуляторов. В случае распределения количества прошедшего электричества по глубине пористого электрода с максимумом в центре электрода, кадмий, образующий дендриты, также будет в основном осаждаться в центре пористого электрода. Это позволит исключить рост дендритов на поверхности электродов, и тем самым исключить вторую причину возникновения теплового разгона.
В десятом и одиннадцатом разделах выполнено сравнение полученных теоретических выводов с экспериментальными данными, полученными для физической модели дендрита. В качестве физической модели дендрита была взята тонкая стеклянная трубка с платиновой проволокой, заполненная раствором и поляризуемая с торца. Платиновая проволока моделирует растущий к противоэлектроду дендрит, а стеклянная трубка − ячейку сепаратора через которую растет дендрит. Так как кадмий плохо растворяется в щелочном электролите, то для эксперимента был выбран близкий по свойствам цинкатный электролит. КОН плотности 1,20 г см-3 с добавлением моногидрата лития 20 г·л-1 и Na2SnO3 *H2O 0,2 г·л-1, с концентрацией цинка в нем 25 г·л-1. Это стандартный электролит цинкования, который дает плотный осадок до плотностей тока 20 мА·см-2. Для количественной оценки распределения среднего тока (количества прошедшего электричества) платиновую проволоку с осажденным на неё цинком медленно и равномерно погружали в раствор того же состава, что и раствор физической модели поры. С помощью потенциостата поддерживали постоянный положительный потенциал на платиновой проволоке (рабочем электроде), относительно цинкового электрода сравнения в том же растворе, в точке входа платиновой проволоки в раствор. При этом в ячейке протекает ток, пропорциональный линейной массе осадка в точке входа проволоки в раствор и самописец, подключенный к потенциостату, рисует распределения количества осевшего цинка по длине платиновой проволоки. Данный метод чрезвычайно чувствительный он позволяет уверенно фиксировать неоднородности осадка до 0,01 мм.
На основании сравнения теоретических расчетов и экспериментальных данных можно сделать следующие обобщения:
-Макрооднородная модель пористого электрода позволяет рассчитывать распределение с точностью до 80-90 %.
-Изменяя режимы заряда на переменном асимметричном токе, можно регулировать распределение количества прошедшего электричества по длине дендрита или глубине пористого электрода, достигая нужные оптимальные распределения.
-Полученные теоретические критерии для оценки распределения позволяют заранее устанавливать нужный режим распределения.
-Используя переменный асимметричный ток можно исключить рост дендритов и даже растворять уже образовавшиеся дендриты, перемещая растворенный метал, в глубь пористого электрода.
В двенадцатом разделе проверялась возможность использования переменного асимметричного тока для борьбы с образованием дендритов на реальном оксидно-цинковом электроде. Получены следующие результаты.
При малых плотностях тока заряда оксидно-цинкового электрода (менее 10 мА.см-2), дендриты на нем не образуются. Это соответствует теоретическим исследованиям, так как в этом случае ток более-менее равномерно распределяется по глубине пористого электрода. С возрастанием поляризующего тока глубина его проникновения уменьшается и, следовательно, большая часть поляризующего тока сосредотачивается на поверхности. Это и приводит к росту дендритов.
При средних плотностях тока заряда оксидно-цинкового электрода (10 мА.см-2
Чтобы дендриты не образовывались как при средних плотностях тока заряда, так и при высоких необходимо соблюдать полученные ранее теоретические критерии оптимального распределения среднего тока по глубине пористого электрода.
Используя переменный асимметричный ток всегда можно растворить уже образовавшиеся дендриты.
В тринадцатом разделе проверялась возможность использования переменного асимметричного тока для борьбы с дендритами в реальном НК аккумуляторе. Получены следующие результаты.
Если заряжать НК аккумуляторы переменным асимметричным током, дающим максимум распределения количества прошедшего электричества в центре пористого электрода, то данный режим действительно приводит к растворению дендритов и устранению коротких замыканий вследствие их прорастания через сепаратор.
Заряд переменным асимметричным током НК аккумуляторов, приводит к частичному увеличению их емкости, как правило, на 10-20%.
Пятая глава состоит из двенадцати разделов и посвящена исследованию механизма теплового разгона, как одной из форм деградации аккумуляторов.
В первом разделе на основании экспериментальных данных установлен источник появления водорода в электродах аккумуляторов − это разложение электролита на кислород и водород во время буферного режима работы аккумуляторов или во время их заряда. Кислород уходит из аккумулятора, а водород частично накапливается в электродах, так как при температуре 20 0С коэффициент диффузии водорода в никеле примерно 1010 раз больше, чем коэффициент диффузии кислорода.
Во втором разделе рассмотрены наиболее вероятные формы существования водорода в электродах. Чисто теоретически можно предположить, что водород накапливается или в активном веществе электродов, или в металлокерамической матрице, или в наполнителе (графит, сажа) для ламельных, намазных и прессованных электродов. Если водород накапливается в металлокерамической матрице, то здесь также возможны различные формы накопления. Во-первых, водород, возможно, просто интеркалирован в металл (-фаза металлогидрида). Во-вторых, он, возможно, образует связанное соединение (-фаза металлогидрида). В-третьих, водород, возможно, накапливается в мельчайших микродефектах кристаллической решетки (различных дислокациях и другие дефектах структуры металла) под действием очень большого капиллярного давления.
В третьем разделе выполнена серия экспериментов с целью проверки гипотезы о возможном накоплении водорода в гидроксидах никеля. Если водород просто интеркалирован в гидроксиды никеля, то при взаимодействии гидроксидов с кислотами с образованием растворимых солей внедренный водород должен будет выйти, так как гидроксиды никеля преобразуются в соль, которая переходит в раствор. Для этого можно использовать любую кислоту, которая образовывала бы с гидроксидами никеля растворимые соли, но не взаимодействовала или плохо взаимодействовала с металлической матрицей. В эксперименте использовался 22,6 % раствор серной кислоты, так как данная кислота удовлетворяет отмеченным выше требованиям. Травление оксидно-никелевых электродов выполнялось в течение 30 минут, за это время никаких изменений в никелевой матрице не происходило.
Установлено, что при травлении оксидно-никелевого электрода в серной кислоте водород вообще не выделяется. Из этого следует, что интеркалированного в гидроксид никеля водорода нет.
Потеря веса оксидно-никелевыми электродами в результате их травления в серной кислоте составила 32-36 %. Данные электроды были изготовлены на Уральском электрохимическом комбинате (УЭХК, г. Екатеринбург). По нашему запросу с завода было сообщено, что положительный электрод содержит 30-36 % гидроксидов никеля и 1-2 % гидроксидов кобальта. Полученные в опытах значения потери веса электродами, находятся в данном диапазоне. Поэтому можно утверждать, что в активном веществе оксидно-никелевого электрода нет нерастворимых в серной кислоте соединений водорода.
Таким образом, в активном веществе оксидно-никелевого электрода аккумулятора НКБН-25-У3 водород не содержится ни в виде интеркаляции, ни в виде каких-либо других соединений.
В четвертом разделе выполнена серия экспериментов с целью проверки гипотезы о накоплении водорода в металлокерамической никелевой матрице. С этой целью из оксидно-никелевого электрода предварительно был удален гидроксид никеля растворением в серной кислоте. Затем никелевую матрицу электрохимически растворяли в стандартном сульфатном растворе никелирования (рафинирования). Если водород интеркалирован в никелевую матрицу или находится в микродефектах кристаллической решетки, то он должен был бы выйти при электрохимическом растворении матрицы.
Экспериментально установлено, что при электрохимическом растворении никелевой металлокерамической матрицы оксидно-никелевого электрода водород не выделяется. При любом способе накопления водорода в металле первой стадией должна быть стадия интеркаляции водорода в металл. Однако эксперимент показал, что внедренного в кристаллическую решетку водорода нет. Это можно объяснить дегазацией оксидно-никелевого электрода в процессе хранения аккумулятора после снятия его с эксплуатации. Все исследованные в данном эксперименте аккумуляторы хранились на складе после снятия с эксплуатации не менее года.
В результате растворения металлокерамической никелевой матрицы часть электрода, погруженного в раствор, отделилась и упала на дно колбы. При этом упавшая часть имела вид исходного электрода без каких-либо изменений. Однако при извлечении из раствора и прикосновении к упавшей части, она рассыпалась на порошок в виде мелких кристаллов серого цвета с металлическим блеском. Как известно, все металлогидриды переходных элементов имеют вид светлых и темных кристаллов с металлическим блеском. Таким образом, можно предположить, что упавшая часть исследуемого электрода представляла собой агломераты кристаллов металлогидрида никеля.
Результат взвешивания порошка металлогидрида никеля показал, что он составляет, примерно, половину веса металлокерамической матрицы.
Таким образом, результаты исследований позволяют заключить, что оксидно-никелевый электрод НК аккумулятора, с длительным сроком эксплуатации состоит из трех фаз: активного вещества (гидроксида никеля), возможно металлогидрида никеля и чистого никеля, причем примерно, в равных весовых долях.
В пятом разделе выполнена серия экспериментов с целью проверки выше описанных результатов. С этой целью никелевую матрицу химически растворяли в концентрированной соляной кислоте. В результате растворения выделилось не 6 литров водорода, как этого надо было бы ожидать в случае полного растворения никеля весом около 16 грамм, а, примерно, в два раза меньше. То есть растворилось, в среднем, около восьми грамм никеля. Остальная часть матрицы представляла не чистый никель, а его соединения, нерастворимые в соляной кислоте и выпавшие в виде осадка (предположительно металлогидрид никеля). Таким образом, данные эксперименты подтверждают предыдущие результаты.
В шестом разделе выполнен эксперимент подтверждающий, что образовавшийся в результате растворения никелевой матрицы серый порошок является металлогидридом никеля. Для этого 2 г порошка поместили в керамический тигель, который затем вставили герметичную термокамеру. Затем термокамеру нагревали до температуры 1500-1600 0С. Данная температура была выбрана, для того чтобы никель, находящийся в тигле смог расплавиться. Выделяющийся при нагревании газ собирался в эластичную емкость. Анализ выделившегося газа, выполненный с помощью газоанализатора VOGA-2М, показал, что он полностью состоит из водорода. В тигле после извлечения его из термокамеры находился кусочек металлического никеля. Таким образом, порошок получившийся в результате электрохимического растворения металлокерамической никелевой матрицы состоит из двух элементов - водорода и металлического никеля, то есть он является гидридом никеля.
В седьмом разделе был выполнен расчет энергетического баланса теплового разгона. Расчет показал, что за время теплового разгона исследуемый аккумулятор получил от зарядного устройства 33,7 кДж, накопленная им электрическая энергия составляла 30 кДж, а выделилось более 218 кДж. Таким образом, ни энергия, затраченная зарядным устройством, ни накопленная в аккумуляторе электрическая энергия не являются основными источниками энергии, выделяемой в результате теплового разгона, хотя они, бесспорно, способствуют тепловому разгону, особенно на начальном этапе. Полученные результаты свидетельствуют о том, что тепловой разгон сопровождается мощной экзотермической реакцией с большим выделением тепла.
В восьмом разделе показано, что скорость выделения водорода из электродов во время теплового разгона во много раз больше скорости выделения водорода из электродов при их термическом разложении при 800 0С. Следовательно, выходу водорода из электродов во время теплового разгона способствует некоторая электрохимическая реакция сопровождающая тепловой разгон.
В девятом разделе исследуются электрохимические реакции идущие на гидриде никеля (-фаза) в щелочном аккумуляторном электролите при его катодной и анодной поляризации. Поляризационная кривая ненаводороженного никеля при катодной поляризации представляет собой стандартную кривую разложения электролита с выделением водорода на металлах. Поляризационная кривая при анодной поляризации представляет собой стандартную кривую разложения электролита с выделением кислорода на металлах. Катодные и анодные поляризационные кривые на гидриде никеля (-фаза) существенно отличаются. Они содержат участки предельного тока, как при катодной, так и при анодной поляризациях. Эти участки обусловлены лимитирующей стадией при катодном и анодном процессах. В дальнейшем отдельно исследовался катодный процесс на гидриде никеля (-фаза) (определялась электрохимическая реакция и лимитирующая стадия) и анодный процесс. Сначала была снята зависимость бестокового потенциала гидрида никеля (потенциал коррозии) от времени в щелочном аккумуляторном электролите. Затем теоретически и экспериментально было показано, что потенциал коррозии гидрида никеля (-фаза) эквивалентен потенциалу водородного электрода, а его изменение на хронопотенциограмме коррозии связано с разложением гидрида никеля внутри электрода и диффузией водорода к поверхности электрода. Для нахождения лимитирующей стадии при катодном процессе была снята циклическая вольтамперограмма (ЦВА) в интервале потенциалов от -1 В до -0,5 В, который как раз охватывает область предельного катодного тока. Скорость развертки v=0,001 В*с-1. На циклической вольтамперограмме предельный катодный ток уменьшается с увеличением номера цикла. Такое изменение ЦВА характерно, когда замедлена предшествующая химическая реакция по отношению к основной электрохимической реакции, идущей на электроде. В рассматриваемом катодном процессе предшествующей химической реакцией может быть только реакция распада гидрида никеля. Для выявления кинетики предшествующей лимитирующей стадии была снята катодная хронокулонограмма гидрида никеля, то есть зависимость переносимого катодного заряда q− от времени. Зависимость q−(t) оказалась линейной по времени. Из двух предшествующих стадий (к электрохимической реакции) на гидриде никеля (а именно, распад гидрида никеля и диффузия водорода к поверхности электрода) линейную зависимость от времени имеет только стадия распада гидрида никеля. Следовательно, данные эксперименты однозначно доказывают, что при катодной поляризации на гидриде никеля лимитирующей стадией является стадия распада гидрида никеля (-фазы). Атомарный водород, образовавшийся в результате распада гидрида никеля, диффундирует к поверхности электрода и адсорбируется. Последующей является стадия электрохимической десорбции водорода адсорбированного на поверхности электрода, т.е.
 (1)
(1) Для выяснения характера протекающей электрохимической реакции при анодной поляризации была снята зависимость потенциала электрода от времени при плотности анодного тока ia=0,5 А/м2. При потенциале около -0,58 В (с.в.э) хронопотенциограмма гидрида никеля очень слабо изменялась во времени, что свидетельствует, что около этого потенциала происходит некоторая электрохимическая реакция. Экспериментальная поляризационная зависимость для анодного процесса на гидриде никеля имеет вид уравнения Тафеля, с классическим углом наклона 0,12В и коэффициентом переноса
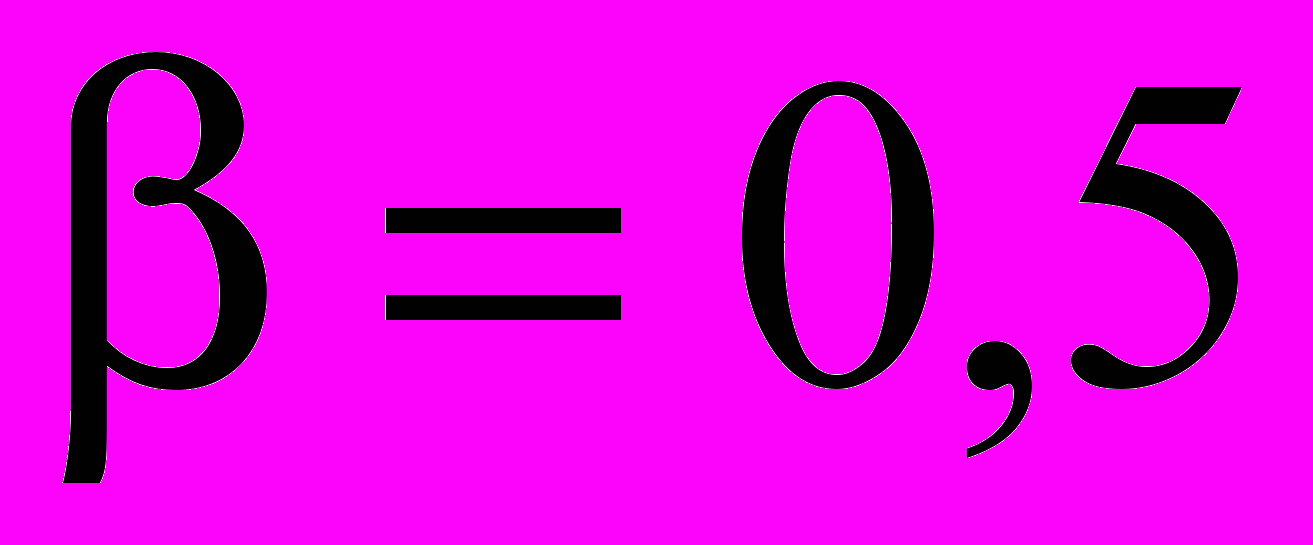 . Оба полученные значения соответствуют электрохимической стадии ионизации водорода.
. Оба полученные значения соответствуют электрохимической стадии ионизации водорода.
Так как в щелочной среде протоны сразу взаимодействуют с ионами OH–, то предыдущую реакцию в конечном итоге необходимо записать в виде:
 , (2)
, (2)что не меняет смысла протекающей электрохимической реакции. Для выявления лимитирующей стадии при анодном процессе была снята циклическая вольтамперограмма в интервале потенциалов от -0,88 В до 0,02 В, который как раз охватывает область предельного анодного тока (скорость развертки 0,05В*с-1), и анодная хронокулонограмма. Такой же анализ, как и для катодного процесса, показал, что и в случае анодного процесса на гидриде никеля (-фаза) лимитирующей стадией является стадия распада гидрида никеля. По экспериментальным данным найдена скорость распада гидрида никеля 8*10-5 A/см2 и константу равновесия распада гидрида никеля К=10.
В десятом разделе на основании всех полученных экспериментальных данных предложен механизм теплового разгона в щелочных аккумуляторах.
Электроды НК аккумуляторов с длительным сроком эксплуатации содержат большое количество водорода, то есть они являются гидридами металлов. Реакции (1, 2) протекают на любых гидридах металлов. Следовательно, при заряде НК аккумуляторов параллельно будут протекать три электрохимические реакции, а именно: основная электрохимическая реакция, связанная с зарядом электродов, электрохимическая реакция разложения электролита в случае перезаряда электродов и электрохимическая реакция на гидридах металлов (1, 2). Суммарной для реакций (1, 2) будет реакция
 . (3)
. (3)т.е. реакция рекомбинации атомарного водорода. Реакция (3) является мощной экзотермической реакцией с тепловыделением 436 кДж/моль(водорода). Данное тепловыделение больше чем при реакции горения водорода в кислороде 285,8 кДж/моль(водорода). На базе реакции рекомбинации атомарного водорода (3) основана водородная сварка, способная создавать пламя до 3700 0С, в то время как кислородно-водородная сварка способна создавать пламя с температурой около 2500 0С. Электрохимическая реакция (3) и есть реакция теплового разгона. При обычных температурах скорость электрохимической реакции (3) небольшая 8*10-5 A/см2. Поэтому она не может оказывать какого-либо заметного влияние на ход процесса заряда НК аккумуляторов. Однако, как было показано в главе 3, при повышении температуры электродов скорость распада металлогидридов резко возрастает (а именно эта стадия является лимитирующей для реакции (3)) и данная реакция может стать определяющей. Это и есть тепловой разгон. На базе электрохимической реакции (3) можно объяснить и другие ранее мало понятные результаты, связанные с тепловым разгоном.
Электрохимическая реакция (1) является одной из составных частей реакции теплового разгона (3). Она фактически является реакцией электрохимической десорбции водорода. Поэтому данная электрохимическая реакция должна сильно ускорять процесс выхода водорода из электродов в процессе теплового разгона, что и наблюдается в экспериментах.
Так как при протекании теплового разгона электрохимическая реакция (3) становится определяющей, а вклад других реакций будет крайне незначительным, то на клеммах аккумулятора должна установиться разность потенциалов соответствующая протеканию именно этих реакций. Согласно исследованиям в предыдущем разделе при протекании электрохимической реакции (2) потенциал положительного электрода будет -0,58 В (СВЭ), а при протекании реакции (1) потенциал отрицательного электрода будет примерно -1,08 В (СВЭ). Следовательно, при возникновении теплового разгона, т.е. реакции (3), разность потенциалов на клеммах аккумулятора должна снизится примерно до 0,5 В, что и наблюдается в экспериментах рис.1. Окончательно можно предложить следующий механизм теплового разгона.
В случае локального разогрева кадмиевого электрода, до 340 0С за счет прорастания в этом месте дендрита начнется массовое разложение гидридов. В этом случае скорость реакций на гидридах (1, 2) возрастет пропорционально возрастанию скорости распада гидридов (так как эта стадия является лимитирующей для реакций (1, 2)), т.е. возрастет в сотни и тысячи раз. Запуск мощной экзотермической реакции (3) приведет к еще более сильному разогреву электродов в месте расположения дендрита и еще к более сильному распаду гидридов т.е процесс будет нарастать лавинообразно. В этом случае электрохимические реакции (1, 2) станут определяющими при заряде аккумуляторов. Поэтому ток заряда аккумуляторов возрастет пропорционально возрастанию скорости этих реакций, т.е. в сотни и тысячи раз, а напряжение на клеммах аккумулятора станет равным разности потенциалов определяющих протекание этих реакций, т.е. приблизительно 0,5 В, что и наблюдается в экспериментах рис.1.
В одиннадцатом разделе на базе метода структурного моделирования процессов в щелочных аккумуляторах предложена модель теплового разгона. Основу модели составляет уравнение кинетики реакции распада гидридов металлов как лимитирующей стадии процесса теплового разгона. В модели учтена возможность прерывания теплового разгона, за счет образования газовой пробки в месте прогорания сепаратора и тем самым физического прерывания реакции (3) в этом месте. Решение, полученное на базе предложенной модели, хорошо согласуются с экспериментальными данными рис.1.
В двенадцатом разделе на базе полученных теоретических и экспериментальных результатов даются рекомендации по предотвращению или блокированию процесса теплового разгона в НК аккумуляторах. Рекомендации относятся как к возможным конструктивным изменениям в аккумуляторах, так и к режимам их эксплуатации. Основными из них являются:
1. Конструктивные изменения, связанные с имитацией ламельных электродов, которые неподвержены тепловому разгону, используя для этого дополнительную перфорированную металлическую фольгу на электродах или их металлизацию, как предлагал Теньковцев В.В.
2. Заряд аккумуляторов переменным асимметричным током, что позволяет уменьшить или полностью исключить процесс дендритообразования на кадмиевом электроде и выделение водорода при заряде, то есть устраняются причины теплового разгона.
3. При работе в буферном режиме или в случае заряда при постоянном напряжении необходимо контролировать температуру аккумулятора (не выше 45 0С), ток заряда, не допуская его увеличения и т.д.
