Резервные возможности кардиореспираторной системы и физическая работоспособность у больных аортальными пороками до и после хирургического лечения 14. 00. 16 патологическая физиология
| Вид материала | Автореферат |
- Комплексная медицинская реабилитация больных ишемической болезнью сердца после кардиохирургических, 31.85kb.
- Консервативного и хирургического лечения, 693.1kb.
- Лобанков владимир Михайлович медико-социальные аспекты хирургического лечения больных, 571.64kb.
- Пояснительная записка Учебно-методический комплекс по курсу «Патологическая физиология», 140.7kb.
- Лекционный курс и вопросы для самостоятельного изучения предмета «Физическая культура», 85.4kb.
- Загрудинный зоб хирургическое лечение, 55.58kb.
- «Московский государственный медико-стома-тологический университет Минздравсоцразвития, 965.91kb.
- Ов курса «Патологическая физиология» для самостоятельного изучения, 13.37kb.
- Список использованных сокращений, 505.52kb.
- Патогенетическое обоснование восстановительного лечения нефропатий, сочетанных с нарушениями, 773.4kb.
Апробация работы и публикации по теме диссертации. Основные положения диссертации были представлены и обсуждены на десятой ежегодной сессии научного центра сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН, Москва (2006), всероссийской научно-практической конференции «Стандартизация медицинских технологий, реабилитация в ангиологии и сосудистой хирургии», Новокузнецк (2006), тринадцатом всероссийском съезде сердечно-сосудистых хирургов научного центра сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН, Москва (2007).
Внедрение результатов исследования. Результаты проведенных исследований по определению резервных возможностей кардиореспираторной системы и физической работоспособности у больных аортальными пороками до и после хирургического лечения внедрены в практическую деятельность Центра хирургии приобретенных пороков сердца и биотехнологий ФГУ «ННИИПК им. акад. Е.Н. Мешалкина Росмедтехнологий».
Публикации. По материалам исследования имеется 10 печатных работ, в том числе 3 статьи в журналах, рекомендованных ВАК.
Структура и объем диссертации. Работа изложена на 144 страницах машинописного текста, иллюстрирована 26 таблицами, 21 рисунком, 2 схемами, состоит из введения, трех глав, обсуждения полученных результатов, выводов и списка литературы. Библиографический указатель включает 189 научных публикаций, в том числе 101 отечественных и 88 иностранных авторов.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Обследовано 299 пациентов мужского пола с приобретенными АоП. Среди них 100 пациентов с аортальным стенозом (средний возраст 43±1,9 года) и 94 пациента с аортальной недостаточностью (средний возраст 39±1,9 года). Диагноз верифицирован специалистами ФГУ «ННИИПК Росмедтехнологий» (г.Новосибирск) на основании клинико-инструментальных методов исследования. После операции протезирования аортального клапана механическим двустворчатым протезом обследовано 105 человек: 35 пациента (средний возраст 43±1,7 года) – в ранние послеоперационные сроки (10–18 суток), 70 человек (средний возраст 45±2,7 года) – в отдаленные сроки от 0,5 до 9 лет. Обследование больных с приобретенными аортальными пороками проводили по назначению лечащего врача (специалиста ФГУ «ННИИПК Росмедтехнологий») и в его присутствии.
В качестве группы контроля обследовано 50 практически здоровых лиц мужского пола без специальной спортивной подготовки, у которых получено добровольное информированное согласие. Данные, полученные при исследовании группы контроля, были приняты за норму. Достоверных различий по возрасту, индексу массы тела между диагностическими группами и группой контроля не отмечено (p>0,05).
Всех больных с аортальными пороками сердца до и после хирургического лечения и группа контроля обследовали по 9 методикам: 1) исследование функции внешнего дыхания; 2) исследование легочного газообмена; 3) велоэргометрия; 4) ЭКГ-контроль; 5) контроль АД; 6) ушная оксиметрия; 7) церебральная оксиметрия, 8) эхокардиография, 9) анкетирование по качеству жизни. Количество показателей, полученных и рассчитанных на основе проведенных методик – 682993.
Толерантность к физической нагрузке оценивали с помощью велоэргометрического тестирования в условиях дозированной непрерывной ступенчато-возрастающей нагрузки различной мощности из расчета 0.5, 1.0, 1.5 Вт/кг массы тела и т.д. (длительность ступеньки составляла 3 мин при постоянной частоте педалирования 60 оборотов в минуту). Параллельно проводили регистрацию электрокардиограммы с определением частоты сердечных сокращений, измерение артериального давления по методу Короткова, легочного газообмена, насыщения артериальной крови кислородом, церебральной оксигенации. На основании измеренных величин рассчитывали:
- показатели центральной гемодинамики (минутный объем кровообращения, ударный объем, общее периферическое сопротивление сосудов);
- показатели энергетической эффективности обеспечения нагрузки (коэффициент полезного действия, кислородный долг);
- показатели, характеризующие миокардиальный резерв (мощность ЛЖ, коэффициент расхода резерва миокарда, индекс энергетических затрат сердца);
- показатели церебральной оксиметрии (церебральная оксигенация, индекс доставки кислорода к тканям, индекс потребления кислорода, коэффициент экстракции кислорода).
Определение резервных возможностей и механических свойств легочной ткани проводили методом спирографии.
Субъективная оценка качества жизни проводили с помощью опросника «Ноттингемский профиль здоровья».
Статистическая обработка полученных результатов проводили с использованием программного пакета Statistica 6.0 (США). Для определения статистической значимости различий для множественных сравнений после проведения дисперсионного анализа использовали t-критерий Стьюдента с поправкой Бонферрони. Для определения статистической значимости различий параметров до и после хирургического лечения использовали парный t-критерий Стьюдента. Для всех проведенных анализов различия считали достоверными при уровне значимости p<0,05. Данные в таблицах и на рисунках представлены как среднее значение ± ошибка среднего (M±m).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Кардиореспираторные резервы и физическая работоспособность у больных приобретенными аортальным стенозом и аортальной недостаточностью до хирургического лечения
По мере прогрессирования аортального порока формируются механизмы, компенсирующие или минимизирующие вызванные пороком нарушения внутрисердечной гемодинамики и кислородного обеспечения организма в целом. Формирование механизмов компенсации зависит от анатомического типа аортального порока (стеноза или недостаточности).
Для аортального стеноза характерна нагрузка на ЛЖ давлением, а для аортальной недостаточности – объемом, что приводит к различным нарушениям внутрисердечной гемодинамики и находит отражение в структурно-функциональных особенностях ЛЖ больных АоП (табл. 1).
В обеих диагностических группах отмечено достоверное увеличение массы миокарда (ММ) ЛЖ, конечного диастолического объема (КДО) и конечного систолического объема (КСО) ЛЖ. При этом АоС характеризуется достоверным увеличением относительной толщины стенки (ОТС) ЛЖ, что свидетельствует о развитии концентрической гипертрофии миокарда ЛЖ, а при АоН развивается эксцентрическая гипертрофия миокарда ЛЖ, при которой увеличение ММ ЛЖ происходит на фоне нормальной ОТС ЛЖ.
Таблица 1.
Эхокардиографические параметры левого желудочка больных аортальными пороками сердца
| показатель группа | ФВ ЛЖ, % | КДР ЛЖ, см | КСР ЛЖ, см | КДО ЛЖ, мл | КСО ЛЖ, мл | ОТС ЛЖ, см | ММ ЛЖ, г |
контроль(n=50) | 67±1,2 | 5,0±0,10 | 3,0±0,10 | 117±4,6 | 38±2,4 | 0,41±0,01 | 219±8,6 |
| АоС (n=100) | 70±5,7 | 5,5±0,11 | 3,7±0,14 | 158±7,6 # | 70±0,7 # | 0,63±0,02 # | 546±21,4 # |
| АоН (n=94) | 64±1,7 | 6,4±0,15 # * | 4,1±0,15 # | 220±12,0 # * | 80±7,7 # | 0,42±0,01 * | 517±31,5 # |
Примечание: # – достоверность различий с группой контроля (p<0,05),
* – достоверность различий с больными аортальным стенозом (p<0,05).
Исследование гемодинамики малого круга кровообращения показало, что максимальное давление в легочной артерии, вычисленное при эхокардиографии как сумма систолического транстрикуспидального градиента давления и давления в правом предсердии, у пациентов с АоС и АоН умеренно повышено (41±1,9 мм рт.ст.) без достоверных отличий между диагностическими группами. Следствием является нарушение легочной вентиляции у больных АоП, что приводит к снижению эффективности легочного газообмена (рис. 1).
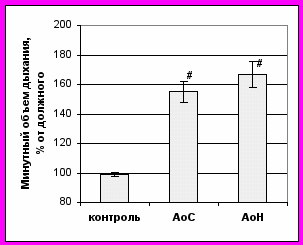
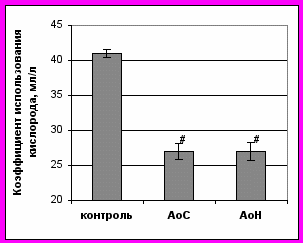
Рис. 1. Легочная вентиляция у пациентов с аортальным стенозом и с аортальной недостаточностью.
Примечание: # – достоверность различий с группой контроля (p<0,05).
Параметры гемодинамики по большому кругу кровообращения у больных АоП имеют свои особенности в зависимости от наличия стеноза или недостаточности аортального клапана (табл. 2).
У больных с АоС по сравнению с АоН гиперфункция ЛЖ обеспечивает достоверное увеличение частоты сердечных сокращений в состоянии покоя. У больных АоН в результате гемодинамических особенностей порока снижен уровень среднего АД, что приводит к компенсаторному снижению периферического сосудистого сопротивления.
Таблица 2.
Гемодинамическое обеспечение организма больных с аортальным стенозом и с аортальной недостаточностью в состоянии покоя
| показатель группа | ЧСС, цикл/мин | АДср , мм рт.ст. | УО, мл | МОК, л/мин | ОПСС, дин*с/см5 | Мощность ЛЖ, Вт |
| контроль (n=50) | 75±1,5 | 90±1,2 | 100±2,7 | 7,3±0,13 | 998±20,4 | 1,4±0,04 |
| АоС (n=100) | 81±2,2 # | 90±1,5 | 96±3,5 | 7,5±0,2 | 994±35,2 | 1,5±0,05 |
| АоН (n=94) | 78±1,9 | 75±2,3 # * | 103±3,9 | 7,9±0,3 | 796±39,9 # * | 1,3±0,07 * |
Примечание: # – достоверность различий с группой контроля (p<0,05),
* – достоверность различий с аортальным стенозом (p<0,05).
При выполнении физической нагрузки показатели системной гемодинамики у больных АоП значительно отличаются от нормальной физиологической реакции без достоверных различий между АоС и АоН (табл. 3).
Таблица 3.
Гемодинамическое обеспечение большого круга кровообращения больных с аортальным стенозом и с аортальной недостаточностью при выполнении физической нагрузки
| показатель группа | Прирост ЧСС на 1 кГм, уд/мин/кГм | Прирост УО на 1 кГм, % | Прирост ОПСС на 1 кГм, % | Прирост МОК на 1 кГм, % | Прирост мощности ЛЖ на 1кГм, у.е. |
контроль(n=50) | 10±0,4 | 1±0,05 | -27±2,3 | 28±3,8 | 3,2±0,17 |
| АоС (n=100) | 20±2,6# | -24±2,5# | 25±5,4# | 6±4,9# | -2,1±1,6# |
| АоН (n=94) | 14±1,1# | -21±3,6# | 18±8,4# | 11±6,5# | -0,1±1,2# |
Примечание: # – достоверность различий с группой контроля (p<0,05).
У больных обеих диагностических групп при нагрузке происходит снижение УО до 20–25% и повышение ОПСС на 45–50% по сравнению с нормой. Как при АоС, так и при АоН отмечено повышение показателей КРРМ и ИЭЗС в 2–4 раза по сравнению с нормой. Однако неадекватно высокие энерготраты сердечной мышцы не в состоянии обеспечить должного прироста мощности ЛЖ, что свидетельствует об ограничении миокардиального резерва у больных АоП. Происходит значительное снижение энергетической эффективности работы: КПД организма при АоС и АоН составляет всего 46% и 36% от нормы соответственно. В результате удельная выполненная работа у больных АоС и АоН составляет 29±3,0 кГм/кг и 38±3,8 кГм/кг соответственно, что в 2,5–3 раза ниже нормы.
Стадии компенсации нарушений кровообращения и легочного газообмена при приобретенных аортальных пороках
В зависимости от степени снижения энергетического обеспечения нагрузки при АоП были выделены 4 стадии развития механизмов компенсации нарушения кровообращения и легочного газообмена. Для 1 стадии характерно адекватное энергетическое обеспечение нагрузки (КПД более 15%), что практически соответствует данным группы контроля. Во 2 стадии энергетическая эффективность умеренно снижено (КПД 10–15%), в 3 стадии КПД снижено до 5–10%, и в 4 стадии снижение КПД характеризовалось критически низкими значениями (менее 5%).
Гемодинамическое обеспечение нагрузки в зависимости от стадий компенсации нарушений кровообращения и легочного газообмена имеет одинаковый характер при АоС и АоН (табл. 4).
Таблица 4.
Показатели центральной гемодинамики, миокардиального резерва и толерантности к физической нагрузке у больных аортальными пороками в зависимости от стадии компенсации
| Тип порока | Стадия компенсации | Прирост УО на 1кГм, % | Прирост ОПСС на 1кГм, % | Прирост мощности ЛЖ на 1кГм, у.е. | КРРМ, у.е. | Ауд., кГм/кг |
| АоС | 1 стадия (n=50) | 0,9±0,05 | -27±2,3 | 3,2±0,17 | 2,6±0,11 | 85±2,2 |
| 2 стадия (n=17) | -17,2±3,26 # | 2±4,8 # | 2,6±0,33 | 3,6±0,34 # | 46±3,1 # | |
| 3 стадия (n=48) | -37,6±4,57 # 1 | 52±9,9 # 1 | -3,1±0,82 # 1 | 4,6±0,92 # | 12±1,1 # 1 | |
| 4 стадия (n=35) | -43,1±2,03 # 1 | 72±7,9 # 1 | -11,5±8,54 # 1 | 16,5±8,49 # 1 | 7±1,6 # 1 2 | |
| АоН | 1 стадия (n=50) | 0,9±0,05 | -27±2,3 | 3,2±0,17 | 2,6±0,11 | 85±2,2 |
| 2 стадия (n=29) | -12,4±3,83 # | -3±6,8 # | 2,9±0,22 | 3,6±0,28 # | 53±3,3 # | |
| 3 стадия (n=51) | -34,1±5,03 # 1 | 48±16,4 # 1 | -3,1±1,67 # 1 | 4,7±1,09 # | 15±2,2 # 1 | |
| 4 стадия (n=14) | -45,5±6,25 # 1 | 98±26,5 # 1 | -15,3±4,93 # 1 2 | 6,1±1,94 # 1 | 7±1,7 # 1 2 |
Примечание: # – достоверность различий с 1 стадией (p<0,05), 1– достоверность различий со 2 стадией (p<0,05), 2– достоверность различий с 3 стадией (p<0,05).
Как видно из таблицы, у больных АоП отмечается стадийное снижение УО и увеличение ОПСС при нагрузке. Снижение мощности ЛЖ при нагрузке на фоне неадекватно высоких энерготрат миокарда приводит к снижению толерантности к физической нагрузке больных.
Показатели легочного газообмена при АоС по сравнению с больными с АоН имеют практически одинаковую динамику в зависимости от стадии компенсации. При АоП наблюдается стадийное увеличение уровня гипервентиляции (увеличение МОД от 140% до 200–250% от должного) за счет увеличения дыхательного объема. При 4 стадии высокий уровень гипервентиляции поддерживается не только высоким дыхательным объемом, но и достоверным увеличением ЧД – в 1,4 раза по сравнению с третьей стадией. Представленные нарушения легочного газообмена приводят к снижению его эффективности, что подтверждается динамикой коэффициента использования кислорода от 2 к 4 стадии (рис. 2). Таким образом, у больных АоП происходит снижение эффективности легочного газообмена за счет прогрессирования нарушений вентиляции.
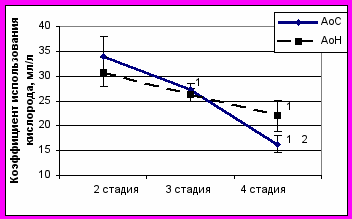
Рис. 2. Эффективность легочного газообмена в зависимости от стадии компенсации у больных приобретенными аортальными пороками.
Примечание: 1– достоверность различий со 2 стадией (p<0,05), 2– достоверность различий с 3 стадией (p<0,05).
В результате снижения эффективности кислородного обеспечения организма от 1 к 4 стадии страдает перфузия головного мозга больных, что проявляется в ухудшении показателей церебральной оксигенации (табл. 5).
Таблица 5.
Кислородное обеспечение головного мозга при нагрузке в зависимости от стадии компенсации у больных приобретенными аортальными пороками
| Тип порока | Стадия компенсации | Церебральная оксигенация, % | Индекс доставки кислорода, у.е. | Индекс потребления кислорода, у.е. | Коэффициент экстракции кислорода, % |
| АоС | 1 стадия (n=50) | 740,7 | 970±20,2 | 190±11,8 | 30±5,6 |
| 2 стадия (n=17) | 59±8,4 # | 1000±98,3 | 327±79,4 # | 86±22,5 | |
| 3 стадия (n=48) | 53±5,2 # | 666±55,6 # | 287±37,6 # | 96±19,1 # | |
| 4 стадия (n=35) | 44±6,4 # | 569±91,4 # 1 | 298±39,7 # | 177±77,7 # 1 | |
| АоН | 1 стадия (n=50) | 740,7 | 970±20,2 | 190±11,8 | 30±5,6 |
| 2 стадия (n=29) | 72±2,5 | 794±108,0 | 239±50,6 # | 41±4,9 | |
| 3 стадия (n=51) | 67±1,7 # | 747±90,1 # | 205±28,5 # | 49±4,2 | |
| 4 стадия (n=14) | 46±1,4 # | 505±90,0 # 1 | 271±35,2 # | 123±30,4 # 1 |
Примечание: # – достоверность различий с 1 стадией (p<0,05), 1– достоверность различий со 2 стадией (p<0,05).
Как видно из таблицы, при 2 стадии адекватное кислородное обеспечения головного мозга поддерживается за счет повышения потребления кислорода. На 3-4 стадиях за счет прогрессирования нарушений системной гемодинамики в 1,5-2 раза снижается индекс доставки кислорода. В результате этого снижение потребления кислорода мозгом на 20-30% по сравнению со 2 стадией сопровождается значительным увеличением коэффициента экстракции кислорода.
Механизмы восстановления резервных возможностей кардиореспираторной системы и физической работоспособности у больных аортальными пороками после клапанного протезирования
Операция имплантации механического протеза в аортальную позицию приводит к снятию патологической нагрузки с ЛЖ, в результате чего в ранние сроки после операции (15±2,7 суток) отмечается тенденция к улучшению структурно-функциональных показателей ЛЖ (табл. 6).
Таблица 6.
Динамика структурно-функциональных показателей ЛЖ больных АоП в ранние сроки после хирургического лечения
| Тип порока | Группа | КДР ЛЖ, см | КСР ЛЖ, см | КДО ЛЖ, мл | КСО ЛЖ, мл | ОТС ЛЖ, см | ММ ЛЖ, г |
| АоС | До операции | 5,5 ±0,11 | 3,7 ±0,14 | 158 ±7,6 | 70 ±0,7 | 0,63 ±0,02 | 546 ±21,4 |
| Ранние сроки после операции | 5,2 ±0,16 | 3,5 ±0,18 | 133 ±10,1 | 55 ±6,8 | 0,63 ±0,04 | 519 ±42,9 | |
| АоН | До операции | 6,4 ±0,15 * | 4,1 ±0,15 | 220 ±12,0 * | 80 ±7,7 | 0,42 ±0,01 * | 517 ±31,5 |
| Ранние сроки после операции | 6,2 ±0.22 * | 4,4 0,28 | 207 ±18,7 * # | 101 ±14,7 * | 0,42 ±0,03 * | 437 ±40,2 |
Примечание: * – достоверность различий с аортальным стенозом (p<0,05), # – достоверность различий с данными до операции (p<0,05).
В ранние послеоперационные сроки отмечается тенденция к нормализации показателей КДР и КДО ЛЖ у больных обеих диагностических групп и КСР и КСО ЛЖ у больных с исходным АоС.
В ранние сроки после аортального протезирования происходит повышение эффективности работы миокарда за счет повышения мощности ЛЖ и снижения расхода резервов миокарда (табл. 7).
У пациентов с исходной АоН повышаются хронотропный и инотропный резервы, для пациентов с исходным АоС характерно повышение только инотропного компонента. Расход резервов миокарда снижается у пациентов с АоС незначительно (до 10%), а у пациентов с АоН в среднем на 23%, что на фоне увеличения прироста мощности ЛЖ свидетельствует о более эффективном энергетическом обеспечении организма больных.
Таблица 7.
Миокардиальный резерв больных аортальными пороками в ранние сроки после хирургического лечения
| Тип порока | Группа | Прирост ЧСС на 1кГм, % | Прирост АДср. на 1кГм, % | Прирост мощности ЛЖ на 1кГм, у.е. | КРРМ, у.е. | ИЭЗС, у.е. |
| АоС | До операции | 11±2,1 | 15±2,7 | -0,8±0,22 | 6±0,7 | 21±4,1 |
| Ранние сроки после операции | 12±2,9 | 19±3,2 | -0,2±0,12 # | 6±0,9 | 19±4,1 | |
| АоН | До операции | 12±2,1 | 8±1,8 | -1,4±0,05 | 11±1,1 | 22±5,0 |
| Ранние сроки после операции | 17±4,1 | 15±3,7 | -1,1±0,10 # | 7±2,4 | 16±3,6 |
Примечание: # – достоверные различия с данными до операции (p<0,05).
Если состояние кардиореспираторной системы больных АоП в ранние сроки после аортального протезирования можно считать ранней адаптацией организма к новым условиям гемодинамики, когда коррекция порока является положительным фактором, а морфологические изменения, сформировавшиеся за время существования порока, а также тяжесть перенесенного хирургического вмешательства – отрицательными, то в отдаленные сроки после хирургического лечения происходит более полная адаптация функционального состояния кардиореспираторной системы. Поэтому в отдаленные сроки после аортального протезирования можно проследить этапы и механизмы восстановления гемодинамики и газообмена после операции.
По данным физической работоспособности и резервным возможностям кардиореспираторной системы в отдаленные сроки после протезирования аортального клапана механическим двустворчатым протезом были выделены 3 периода восстановления функционального состояния организма больных (табл. 8).
Таблица 8.
Показатели центральной гемодинамики и миокардиальный резерв в зависимости от срока после аортального протезирования
| Группы | Прирост ОПСС на 1кГм, %. | Прирост УО на 1кГм, % | Прирост мощности ЛЖ на 1кГм, у.е. | ИЭЗС, у.е. | КРРМ, у.е. | |
| Общая группа до операции | 21±6,7 | -22±2,6 | -1,1±0,7 | 14±2,1 | 4,6±0,52 | |
| После операции | от 0,5 до 2 лет | -7±2,2 # | -6,4±3,38 # | 3,1±0,47 # | 7,9±1,39 # | 3,9±0,67 |
| от 2 до 5 лет | -13±1,5 # | -7,5±3,18 # | 3,1±0,28 # | 6,9±0,57 # | 3,4±0,30 # | |
| от 5 до 9 лет | -5±1,9 # | -8,4±6,87 | 1,9±0,81 # | 9,8±2,71 # | 3,5±0,67 # | |
