На правах рукописи габрусенко сергей Анатольевич
| Вид материала | Автореферат |
- На правах рукописи Ануфриев Сергей Анатольевич организационные основы системы семейной, 365.52kb.
- На правах рукописи енгай Вадим Анатольевич ретроспективный анализ эффективности адьювантной, 278.8kb.
- На правах рукописи санников сергей Викторович произведение иордана, 364.22kb.
- Музыкально-исполнительское творчество, 214.16kb.
- Н. Н. Блохина на правах рукописи пирогов сергей Сергеевич эндоскопические методики, 462.84kb.
- Сергей Анатольевич Батчиков Сергей Георгиевич Кара-Мурза Неолиберальная реформа в России, 1016.62kb.
- М. И. Глинки на правах рукописи чайкин сергей Германович Специфика выразительных средств, 315.44kb.
- Печатная или на правах рукописи, 21.09kb.
- Удк 796/799: 378 , 770.24kb.
- На правах рукописи, 726.26kb.
на правах рукописи
ГАБРУСЕНКО
Сергей Анатольевич
“Гипертрофическая кардиомиопатия :
клинико-инструментальная характеристика, варианты клинического течения, прогноз и особенности медикаментозного лечения”.
14.01.05 - кардиология
Автореферат
диссертация на соискание ученой степени
доктора медицинских наук
МОСКВА - 2009
Работа выполнена в НИИ Кардиологии имени А.Л. Мясникова ФГУ «Российский кардиологический научно-производственный комплекс» МЗ и СР РФ.
Научный консультант:
доктор медицинских наук, профессор, академик РАМН
Беленков Юрий Никитич.
Официальные оппоненты:
доктор медицинских наук, профессор, член-корреспондент РАМН
Кухарчук Валерий Владимирович;
доктор медицинских наук, профессор
Арутюнов Григорий Павлович;
доктор медицинских наук, профессор
Привалова Елена Витальевна.
Ведущая организация: ГОУ ВПО Московский государственный медико-стоматологический университет МЗ и СР РФ.
Защита состоится 27 января 2010 года в 13.30 на заседании диссертационного совета Д 208.073.01 в ФГУ «Российский кардиологический научно-производственный комплекс» МЗ и СР РФ (121552, город Москва, 3-я Черепковская улица, дом 15А).
С диссертацией можно ознакомиться в научной библиотеке РКНПК МЗ и СР.
Автореферат разослан « » ноября 2009 года.
Учёный секретарь
диссертационного совета
доктор медицинских наук, профессор Синицын В.Е.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Кардиомиопатии, по-прежнему, остаются в числе наименее изученных заболеваний и являются объектом активно развивающейся области современной кардиологии [Н.М. Мухарлямов, 1990; E. Braunwald, 2008]. Повышенный интерес к проблеме изучения заболеваний миокарда объясняется необходимостью дальнейшего изучения этиологии и патогенеза, диагностическими и терапевтическими трудностями, многообразием и неспецифичностью клинических проявлений, неоднозначностью прогноза.
Гипертрофическая кардиомиопатия (ГКМП) – одна из основных и наиболее распространенных форм первичных кардиомиопатий. Полувековая история изучения проблемы ГКМП отражает значительную эволюцию знаний в вопросах этиологии, патогенеза, диагностики, клинического течения и прогноза, вариантов лечения заболевания.
В 2003 году создан Международный Комитет по ГКМП и опубликовано сообщение, суммировавшее основные положения, включая стратегию лечебных мероприятий [A Report of the American Collage of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. Eur. Heart J., 2003]. Документ по принципиальным позициям соответствует заявленной в 2006 году новой классификации кардиомиопатий [Contemporary Definitions and Classification of the Cardiomyopathies. Circulation, 2006].
По современным представлениям ГКМП является преимущественно генетически обусловленным заболеванием мышцы сердца, характеризующимся комплексом специфических морфо-функциональных изменений и неуклонно прогрессирующим течением с высокой угрозой развития тяжелых, жизнеугрожающих аритмий и внезапной смерти (ВС). ГКМП характеризуется массивной (более 1,5 см) гипертрофией миокарда левого и/или в редких случаях правого желудочка, чаще асимметрического характера за счет утолщения межжелудочковой перегородки (МЖП) с частым развитием обструкции выходного тракта ЛЖ при отсутствии известных причин (артериальная гипертония, пороки и специфические заболевания сердца). Основным методом диагностики остаётся эхокардиографическое исследование (ЭхоКГ). В зависимости от наличия или отсутствия градиента систолического давления в полости ЛЖ, ГКМП разделяют на обструктивную и необструктивную, что имеет важное практическое значение при выборе тактики лечения.
Типичными являются морфологические изменения: аномалия архитек-тоники сократительных элементов миокарда (гипертрофия и дизориентация мышечных волокон), развитие фибротических изменений, патология мелких интрамиокардиальных сосудов [Cardiomyopathies. Realisations and Expectations. Goodwin J., Olsen E. (Eds.), 1993; E.D. Wigle et al., 1995].
Диапазон клинических проявлений крайне велик: от бессимптомных до неуклонно прогрессирующих и трудно поддающихся лечению форм, сопровождающихся тяжёлой симптоматикой. Cимптомы болезни разно-образны и малоспецифичны, связаны с гемодинамическими нарушениями: диастолическая дисфункция (ДД), динамическая обструкция путей оттока, митральная регургитация (МР), ишемией миокарда, патологией вегетативной регуляции кровообращения и нарушением электрофизиологических процессов в сердце [B.J. Maron, 1997; F. Cecchi et al., 2003].
В настоящее время наблюдается повсеместный рост числа зарегистрированных случаев ГКМП как за счёт внедрения в практику современных методов диагностики, так и, вероятно, в связи с истинным увеличением числа больных [B.J. Maron, 1997; E.D. Wigle et al., 1995]. Согласно имеющимся данным распространённость заболевания в общей популяции является более высокой, чем считалось ранее, и составляет от 0,2% до 0,5 % [B.J. Maron еt al., 1994, 1995]. ГКМП может диагностироваться в любом возрасте от первых дней до последней декады жизни независимо от пола и расовой принадлежности, однако заболевание выявляется преимущественно у лиц молодого трудоспособного возраста [W.P. Fay et al., 1990; B.J. Maron еt al., 1999], что определяет особую социальную важность этой проблемы. Ежегодная смертность больных ГКМП колеблется в пределах от 1 до 6%: у взрослых составляет 1 - 3 % [L. Monserrat et al., 2003; B.J. Maron еt al., 2003], а в детском и подростковом возрасте, у лиц с высоким риском ВС - 4 - 6 % [W.J. McKenna et al., 1981; B.J. Maron еt al., 1982]. Как правило, смерть у больных ГКМП носит внезапный, аритмический характер и может быть первым и единственным проявлением заболевания.
Общепризнанной является концепция о преимущественно наследственной природе ГКМП [L. Fananapazir, 1999; A.J. Marian et al., 1995], при этом основным типом наследования является аутосомно-доминантный. ГКМП является генетически гетерогенным заболеванием, причиной которого являются более 450 описанных мутации нескольких генов, кодирующих белки сердечного саркомера и некоторые несаркомерные белки, а также в митохондриальной ДНК [P. Richard et al., 2003; Hypertrophic cardiomyopathy mutation database. On-line. 2009]. Описанные при ГКМП генетические дефекты характеризуются высокой популяционной специфичностью, разной степенью пенетрантности, выраженности морфологических и клинических проявлений. К наиболее частым причинам ГКМП в странах Западной Европы и США относятся мутации в генах тяжелой цепи сердечного бета-миозина (-МНС) и миозин-связывающего белка-С (MYBPC), при этом в каждой популяции вклад различных генов неодинаков. До настоящего исследования данных о характере и распространенности генетических нарушений в российской популяции больных ГКМП не было.
Основу медикаментозной терапии ГКМП составляют бета-адрено-блокаторы и антагонисты кальция [M.V. Sherrid et al., 2000; E.D. Wigle et al., 1995], оказывающих благоприятное влияние как на диастолическую, так и систолическую функцию сердечной мышцы. При этом эффективность, в частности ретардных форм препаратов, при длительном применении до настоящего времени не выяснена. Также остаётся открытым вопрос о возможности использования этих групп препаратов для улучшения “качества” и прогноза жизни и предотвращения ВС больных ГКМП.
Прогноз заболевания, в целом благоприятный, вариабелен для разных категорий больных ГКМП. Актуальность настоящей работы определяется немногочисленностью и неоднозначностью результатов исследований, посвященных изучению этиологии и патогенезу, длительному наблюдению, уточнению принципов и особенностей лечения больных ГКМП, анализу факторов, влияющих на клиническое течение и прогноз заболевания.
Цель исследования - изучение клинических и гемодинамических проявлений, вариантов течения, “качества” и прогноза жизни, определение оптимальной тактики медикаментозной терапии больных ГКМП на основании результатов комплексного клинико-инструментального обследования в условиях длительного проспективного наблюдения и ретроспективного анализа.
Задачи исследования:
1. Изучить особенности клинической картины, варианты течения ГКМП с учётом возможных этиологических (генетических) факторов, патогенетических механизмов и гемодинамических особенностей.
2. Провести поиск мутаций в гене тяжёлой цепи сердечного -миозина в российской популяции пациентов с ГКМП и изучить их фенотипические проявления.
3. Определить диагностическую ценность клинических проявлений и информативность инструментальных методов исследования (Эхо-КГ, СМЭКГ, ОЭКТ) при различных формах ГКМП.
4. Изучить клиническую значимость динамического определения уровней натрийуретических пептидов в плазме крови у больных ГКМП при проспективном наблюдении.
5. Оценить особенности естественного течения при проведении ретроспективного анализа данных обследования больных ГКМП.
6. Определить факторы, влияющие на клиническое состояние, “качество” жизни, вероятность внезапной смерти и прогноз больных ГКМП.
7. Оценить влияние длительного применения бета-адреноблокаторов, антагонистов кальция, антиаритмических средств (соталол) на клинический, функциональный, гемодинамический статус больных ГКМП и провести сравнительную оценку эффективности различных видов терапии в условиях длительного проспективного наблюдения.
Научная новизна. Впервые на основании обследования российской популяции больных ГКМП в условиях длительного проспективного наблюдения в течение 10 лет и результатов ретроспективного анализа данных за 20-летний период проведено комплексное изучение клинико-гемодинамических, электрокардиографических, некоторых биохимических показателей, параметров кровоснабжения миокарда, а также факторов, определяющих особенности клинического течения и прогноз заболевания.
Впервые в большой выборке российских пациентов с ГКМП был изучен спектр мутаций в гене -МНС и определена их роль в возникновении заболевания, что является важной популяционной характеристикой и имеет большое значение для применения молекулярной диагностики ГКМП в клинической практике. При этом выявлены 6 ранее не описанных в мировой литературе мутаций в гене -МНС, которые могут быть специфичными для российской популяции, и изучены их фенотипические проявления. В случае семи ранее описанных в литературе мутаций установлено, что их фенотипические проявления совпадают с мировыми данными. Среди пациентов с ранее не описанными мутациями выявлены пациенты с тяжёлым течением заболевания и неблагоприятным прогнозом. Описаны основные цели, области применения и стратегия генодиагностики ГКМП.
У больных ГКМП уставлена достоверная связь между преходящими нарушениями перфузии миокарда, выраженностью гипертрофии, гемо-динамических расстройств, наличием синдрома стенокардии и тяжестью СН.
Впервые с использованием метода суточного мониторирования ЭКГ (СМЭКГ) у больных ГКМП проведено детальное изучение особенностей нарушений и вариабельности ритма сердца (ВРС). При анализе ВРС использованы показатели, преобразованные с учётом устранения частотных влияний и возраста обследуемых, что позволило установить не зависящие от ЧСС и возраста границы нормальных значений показателей ВРС. Патологические значения, прежде всего, ультранизкочастотных показателей ВРС, указывают на наличие или предрасположенность больных ГКМП к обморочным состояниям.
Впервые у больных ГКМП изучено содержание натрийуретических пептидов (НУП) в плазме крови в зависимости от клинико-гемодинамических показателей, функционального статуса, характера и тяжести нарушений ритма сердца в исходном состоянии и на фоне длительной терапии бета-адреноблокаторами и антагонистами кальция. Показано, что у больных ГКМП повышенное содержание НУП пептидов в крови ассоциируется с наличием обструкции ВТ ЛЖ, выраженностью ДД и гипертрофии миокарда ЛЖ, тяжестью гемодинамических и функциональных нарушений.
В условиях проспективного наблюдения проведена сравнительная оценка клинической эффективности длительного применения бета-адреноблокаторов (атенолол, бисопролол), антагонистов кальция (верапамил), соталола в лечении больных ГКМП. Показано положительное влияние различных вариантов длительной медикаментозной терапии на клинические проявления, «качество жизни», толерантность к физическим нагрузкам и перфузию миокарда у большинства больных ГКМП.
На большом фактическом материале проведён анализ 5 и 10-летней выживаемости больных ГКМП и определены основные факторы, неблагоприятно влияющие на клиническое течение и прогноз заболевания: мерцательная аритмия (МА), эпизоды неустойчивой желудочковой тахикардии (ЖТ), тяжесть нарушений диастолической функции (ДФ), наличие синкопальных состояний, отсутствие адекватного прироста АД при проведении ВЭМ-теста, СН III ФК (NYHA), обструкция ВТ ЛЖ. В качестве предиктора ВС максимальное значение имеет наличие у больных ГКМП эпизодов неустойчивой ЖТ, пароксизмов фибрилляции предсердий, обмороков и неадекватной реакции при выполнении нагрузочного теста.
Практическая значимость. Определена клиническая ценность и информативность комплекса современных инструментальных и лабораторных методов исследования в диагностике ГКМП. Результаты исследования позволяют разработать рекомендации по диагностике и принципам терапии и тем самым повысить эффективность лечения больных ГКМП в зависимости от вариантов клинического течения и с учётом факторов, определяющих вероятность ВС, “качество” и прогноз заболевания.
Анализ факторов, неблагоприятно влияющих на прогноз заболевания и стратификация риска ВС в практическом плане имеет важное значение для выделения группы больных ГКМП, требующей особого внимания в процессе наблюдения с целью выбора наиболее адекватной тактики лечения.
С учётом роли МА как важнейшего неблагоприятного фактора прогноза и высокой вероятности ВС больных ГКМП разработан методический подход к прогнозированию фибрилляции предсердий по результатам анализа длительности сигнал-усредненной Р-волны при СМЭКГ.
Данная работа является одним из первых исследований генетических аспектов ГКМП в России. Показано, что мутации в гене -МНС имеют большое значение в возникновении ГКМП в российской популяции. Знание спектра мутаций позволяет разработать рутинные методы ДНК-диагностики ГКМП при меньшей стоимости анализа.
Апробация результатов работы.
Основные материалы доложены и обсуждены на 23 съездах, конгрессах и конференциях:
- Российских национальных конгрессах кардиологов: Москва (2000, 2001, 2003 г.г.), Санкт-Петербург (2002 г.), Томск (2004 г.);
- Конгрессах ассоциации кардиологов стран СНГ: Санкт-Петербург (2003 г.), Ташкент (2005 г.);
- I Общероссийском съезде, V Ежегодной конференции Общества специалистов по сердечной недостаточности: Москва (2004 г.); VI ежегодная конференция ОССН, Москва (2005 г.); II Конгрессе (VIII конференции) ОССН «Сердечная недостаточность`2007» (2007 г.);
- I, II и III Международной научной конференции «Лечение гипертрофической кардиомиопатии», Москва (2000, 2001, 2003 г.г.);
- IV Международной научной конференции «Лечение кардиомиопатий и заболеваний миокарда», Москва (2005 г.);
- Первом Российском научном форуме с международным участием «Радиология 2000», Обнинск (2000 г.);
- Международном симпозиуме по кардиомиопатиям, Киото (2000 г.);
- Конгрессах Европейской Ассоциации Ядерной Медицины: Париж (2000 г.), Вена (2002 г.);
- Региональной научно-практической конференции «Современные методы лучевой и радиоизотопной диагностики сердечно-сосудистых заболеваний», Томск (2002 г.);
- Конференции межрегионального общества ядерной медицины «Проблемы ядерной медицины», Дубна (2002 г.);
- Всероссийском конгрессе «Неинвазивная электрокардиология в клинической медицине», Москва (2007 г.);
- V Международный симпозиум Nt-proBNP (ProCardio Symposium), Севилья, Испания (2007 г.);
- 35-ом Международном конгрессе по электрокардиологии, Санкт-Петербург (2008 г.).
Апробация работы проходила на заседании Учёного совета НИИ Кардиологии имени А.Л. Мясникова РКНПК МЗ и СР РФ 23 июня 2009 года. Диссертация рекомендована к защите.
Публикации. По материалам диссертации опубликованы 65 печатных работ, среди которых 11 статей в центральных журналах.
Объём и структура диссертации. Диссертационная работа, согласно основным требованиям, оформлена в печатном варианте на 320 страницах, иллюстрирована 52 таблицами, 48 рисунками и состоит из следующих разделов: введение, клиническая характеристика обследованных больных, 7 глав результатов исследования, заключение, выводы, практические рекомендации, список литературы (428 источников) и приложения. Каждая глава результатов содержит литературный обзор, подглаву «Материалы и методы» и обсуждение.
Настоящая работа была проведена на базе Отделов заболеваний миокарда и сердечной недостаточности и проблем атеросклероза, а также целого ряда лабораторий НИИ Кардиологии имени А.Л. Мясникова РКНПК МЗ и СР РФ. Генетический блок исследований выполнен в условиях лаборатории молекулярной эндокринологии НИИ экспериментальной кардиологии РКНПК и на базе факультета фундаментальной медицины МГУ имени М.В. Ломоносова (кафедра медицинской и биологической химии).
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Настоящее исследование основано на результатах комплексного обследования 174 пациентов ГКМП (59 женщин и 115 мужчин) в условиях длительного (до 10 лет) проспективного наблюдения. Кроме того, проведён ретроспективный анализ данных обследования 302 больных ГКМП (105 женщин и 197 мужчин), находившихся на обследовании и лечении в НИИ Кардиологии имени А.Л. Мясникова с 1989 по 2008 год. Клинический диагноз ГКМП ставился в соответствии с рекомендациями группы экспертов ВОЗ (1995) и Международного комитета АСС/ESC по ГКМП (2003).
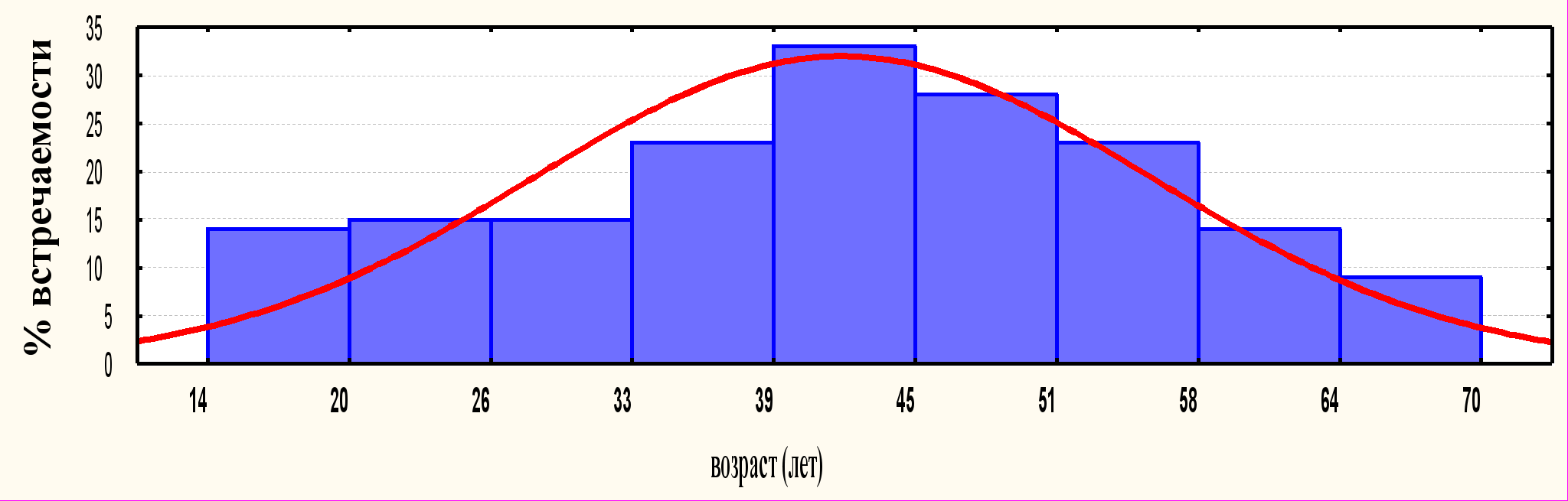
Рисунок 1. Распределение больных ГКМП по возрастным группам
Большинство обследованных больных ГКМП на момент первичного обследования принадлежали к возрастной группе от 33 до 51 года (наиболее активный в творческом и физическом плане период жизни). Средний возраст составил 41,3 13,5 года.
Временной диапазон появления первых симптомов заболевания оказался крайне широк: от первого года жизни до преклонного возраста. При этом средний возраст при установлении диагноза ГКМП (35-36 лет) соответствовал появлению первых признаков СН (табл. 1).
Таблица 1
Возраст и продолжительность заболевания больных Г К М П (М SD)
| | Проспективное наблюдение | Ретроспективный анализ |
| ВОЗРАСТ при появлении первых симптомов заболевания | ( 1 – 70 ) 29.6 14.4 | ( 1 – 70 ) 28.5 13.7 |
| ВОЗРАСТ при установлении диагноза | (4 – 66 ) 36.1 14.6 | ( 4 – 66 ) 35.3 13.9 |
| ВОЗРАСТ при появлении первых признаков СН | ( 8 – 66 ) 36.9 13.6 | ( 7 – 67 ) 35.1 13.5 |
| ВОЗРАСТ при первичной госпитализации | ( 14 – 70 ) 41.3 13.5 | ( 13 – 70 ) 40.5 12.9 |
| Продолжительность заболевания от появления первых симптомов | ( 1 – 32 ) 12.4 11.1 | ( 1 – 50 ) 12.3 10.1 |
Анализ структуры диагностических концепций на этапе, предшествующем поступлению в НИИ Кардиологии имени А.Л. Мясникова, свидетельствует о существенных трудностях первичной диагностики ГКМП. Так по данным, основанным на ретроспективном анализе материалов историй болезни 302 больных ГКМП за 20-летний период, ошибочность первичной диагностики составила более 50%, предположительными и часто направительными диагнозами являлись: ИБС, инфаркт миокарда, порок сердца, миокардит, артериальная гипертония. Некоторое улучшение этой ситуации в последнее десятилетие, прежде всего, связано с большей доступностью инструментальных диагностических методик (ЭхоКГ), и большей осведомленностью врачей в отношении данной патологии.
Первые субъективные проявления заболевания не имели специфических черт: наиболее частыми жалобами являлись одышка при физической нагрузке и болевой синдром в грудной клетке, ощущение сердцебиения и перебоев в работе сердца. При этом у каждого пятого течение болезни долгое время носило бессимптомный характер. Наряду с этим недоступность и/или невостребованность рутинных инструментальных методов обследования, а также игнорирование результатов объективного обследования (в частности наличие систолического шума при аускультации сердца) определили ошибочность первичной диагностики. Следует заметить, что у 9,3% больных ГКМП манифестировалась пароксизмальной или постоянной формой МА.
Субъективная клиническая симптоматика при первичной госпитализации в НИИ Кардиологии, оставаясь по своему характеру неспецифической, оказалась более выраженной. По-прежнему наиболее частыми жалобами были: одышка (81%), боли различного характера в грудной клетке (79,5%), ощущения сердцебиения (57,6%) и перебоев в работе сердца (49,3%), пре- и синкопальные состояния (17,6%), при этом 40% больных имели более 4 симптомов. Обязательное использование инструментальных методик и, прежде всего ЭХОКГ, позволило обосновать диагностическую концепцию ГКМП.
Результаты ЭхоКГ во всех случаях позволили документировать наличие разной степени (от 1,5 до 4,5 см) гипертрофии различных отделов ЛЖ, преимущественно МЖП, с развитием почти у 40% больных обструкции ВТ ЛЖ (Гр. Д > 30 мм рт.ст.). Частое выявление различного характера и локализации систолического шума при аускультации сердца больных ГКМП связано не только с наличием обструкции ВТ ЛЖ, но и наличием МР.
Несколько реже (88,1%) признаки гипертрофии миокарда определялись на стандартной ЭКГ, при этом обращает на себя внимание высокая встречаемость нарушений проводимости (41,7%) и формальных признаков рубцовых изменений миокарда (23,2%). У 17,7% больных в возрасте более 40 лет с жалобами на типичный стенокардитический синдром диагноз ГКМП был подтверждён по результатам коронаровентрикулографии (КВГ).
Таким образом, данные анамнеза, субъективной клинической симптоматики и объективного обследования, как в начальный период заболевания, так и при первичной госпитализации не выявили высокоспецифичных патологических проявлений. Применение, прежде всего Эхо-КГ, позволило преодолеть существенные диагностические трудности.
В проспективное наблюдение были включены 174 больных ГКМП, которым диагноз был выставлен при первичной госпитализации. Начальной точкой исследования считался декабрь 1997 года. Конечной точкой наблюдения был декабрь 2008 года для выживших больных, дата смерти - для умерших и дата последней госпитализации или амбулаторного осмотра, если судьба больных в дальнейшем не могла быть прослежена.
Обследование больных в стационарных условиях или амбулаторно проводилось в плановом порядке не реже одного раза в 1 – 1,5 года или в любые сроки после последней госпитализации при ухудшении состояния. На каждого больного заполнялась регистрационная карта, состоящая из набора унифицированных протоколов по конкретным методам исследования, предназначенная для последующего компьютерного анализа информации.
В рамках проспективного наблюдения проводилось исследование сравнительной эффективности различных вариантов длительного (не менее 1 года) медикаментозного лечения больных ГКМП (табл. 2).
Таблица 2
Характеристика сравниваемых групп больных ГКМП (оценка эффективности различных вариантов медикаментозного лечения)
| АТЕНОЛОЛ n=40 м/ж – 24/16 | ВЕРАПАМИЛ n=43 м/ж – 29/14 | БИСОПРОЛОЛ n=42 м/ж – 28/14 | СОТАЛОЛ n=26 м/ж – 14/12 |
| Ср. возраст (лет) 44.1 11.9 | ср. возраст 42.5 13.3 | ср. возраст 39.7 14.9 | ср. возраст 42.6 13.2 |
| Ср. доза (мг/cутки) 77.3 36.5 | ср. доза 262.2 68.9 | ср. доза 6.4 1.8 | ср. доза 190.8 51.0 |
Первичное обследование проводилось через 7-10 дней после отмены ренее проводимого лечения («безмедикаментозный фон»). Атенолол, верапамил (изоптин-ретард) и бисопролол (конкор) назначался случайным образом, при назначении соталола предпочтение отдавалось больным с тяжёлыми желудочковыми НРС и пароксизмальной МА. Дозы препаратов, назначаемых в виде монотерапии, подбирали индивидуально под контролем ЧСС и уровня АД, результатов СМЭКГ. Критериями увеличения доз были отсутствие снижения средней ЧСС ниже 55 уд/мин и систолического АД < 90 мм рт. ст. при условии хорошей переносимости и отсутствия побочных эффектов.
Методы исследования:
1. Общеклиническое обследование с тщательным сбором анамнеза.
2. Инструментальные методы: ЭКГ в 12 и 35 отведениях; суточное Holter мониторирование ЭКГ; комплексное ультразвуковое исследование сердца, включая допплер-ЭхоКГ, анализ параметров ТМДП и ЛВП, ТМД-ЭхоКГ; велоэргометрическая проба; однофотонная эмиссионная компьютерная томография миокарда с Тс99m МИБИ в покое и при проведении нагрузочного теста; при необходимости ЯМР-томография сердца и КВГ.
3. Методы генодиагностического поиска мутаций в гене -МНС (выделение геномной ДНК, ПЦР-амплификация с праймерами, постановка DHPLC, DHPLC-секвенирование с определением типа мутации).
4. Иммуноферментный метод определения концентраций N-концевого фрагмента предшественника мозгового (Nt-proBNP) и N-концевого фрагмента предшественника предсердного (Nt-proANP) натрийуретических пептидов в плазме крови.
В настоящей работе были проанализированы более 100 количественных и 90 качественных показателей.
Для оценки «качества жизни» больных ГКМП использовался адаптированный “Миннесотский опросник качества жизни больных с сердечной недостаточностью” (MLHFQ).
Статистическая обработка результатов проводилась с использованием статистического пакета программ «STATISTICA 7.0». Применялись непараметрические методы анализа. Межгрупповое сравнение показателей проводили с помощью теста Манн-Уитни; внутригрупповое сравнение переменных – с помощью парного теста Вилкоксона. Данные в тексте и таблицах приведены как M SD для признаков, имеющих нормальное распределение, и медиана и интерквартильный размах для признаков, не имеющих нормального распределения. Достоверность различий в частоте выявления признаков определяли по тесту Фишера. С целью выявления взаимосвязи количественных переменных рассчитывали коэффициент корреляции r по Спирмену. Оценка взаимосвязи между качественными переменными проводилась с использованием таблиц сопряжённости и критерия согласия χ2. При изучении прогноза проводилось построение кривых дожития по методу Каплан-Мейера с анализом различия по группам согласно критерию Мантель-Кокса и регрессионный анализ, основанный на модели пропорциональных рисков Кокса для отбора независимых переменных. Различия считали достоверными при p<0,05. Для построения графических моделей значимости клинических проявлений, оценки оптимального уровня отсечения (точности положительного и отрицательного предсказаний, чувствительности и специфичности признака), и сравнения предсказательной эффективности признаков использовали ROC-анализ.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Роль мутаций в гене тяжёлой цепи сердечного b - миозина
в российской популяции больных гипертрофической кардиомиопатией
В исследование было включено 100 больных ГКМП. У 57 пациентов (53,8%) установлена семейная форма ГКМП. Критерием семейной формы заболевания являлось наличие документированного случая у родственника или случаи ВС у родственников первой степени родства.
Суммарно 129 человек были проанализированы по 20 экзонам гена -МНС. В результате генодиагностического поиска выявлено 13 вариантов аберрантных хроматограмм у 14 неродственных пробандов - больных ГКМП, соответствовавших миссенс-мутациям, которые вызывали замену одной аминокислоты в белке. У двух неродственных больных была одна и та же мутация Ala729Pro.
Мутации в гене -МНС явились причиной заболевания в 17% всех случаев (17 из 100 пробандов) и в 25% семейных случаев (14 из 57 пробандов с семейной формой ГКМП). По данному показателю обследованная российская популяция занимает промежуточное положение между немецкой, датской (13%) [J. Erdmann et al., 2003; S.L. Van Driest et al., 2003] и североаме-риканской (США - 19%-48%) когортами больных ГКМП [H. Watkins et al., 1992; S.A. Mohiddin et al., 2003].
Семь из 13 выявленных миссенс-мутаций были описаны ранее в других популяциях. 6 мутаций выявлены впервые (табл. 3).
Таблица 3
Результаты генодиагностического поиска мутаций в гене -МНС
| Ранее описанные мутации | Arg453Cys, Val606Met, Glu846Lys, Arg870Cys, Gly741Arg, Arg723Cys, Ala797Thr |
| Впервые выявленные мутации | Ala13Thr, Ala729Pro, Trp827Cys, Lys835Thr, Gly584Ser, Ala850Thr |
Для определения характерных особенностей клинико-гемодинами-ческих проявлений ГКМП, обусловленной мутациями в гене -МНС (n=17, из них 14 пробандов и 3 родственника с ГКМП), было проведено их сравнение с группой больных ГКМП без мутаций в данном гене (n=83).
Группа больных с мутациями в гене -МНС характеризовалась более ранним началом заболевания и более молодым возрастом на момент постановки диагноза и включения в исследование (p<0,01), большей тяжестью клинических проявлений, большей выраженностью СН и более низким уровнем КЖ (p<0,03), большим количеством проведённых операции миоэктомии, достоверно большей долей больных с обмороками (p<0,05).
У больных ГКМП - носителей мутаций в гене -МНС достоверно чаще (р<0,02) была установлена семейная форма заболевания. По сравнению с больными без мутации в гене -МНС, в данной группе отмечен достоверно больший ИММЛЖ (p<0,04) за счёт гипертрофии МЖП. Значения КДР и КДО были достоверно меньше (p<0,03), а соотношение ЛП/КДР достоверно выше (p<0,02) в группе больных с мутациями в гене -МНС. Достоверно более высокой (p<0,05) оказалась выраженность ДД и степень МР. Не было отмечено различий в размерах ЛП, ТЗСЛЖ, КСР, частоте обструктивной формы ГКМП, размере аорты и ФВ ЛЖ.
Фенотипические и клинические проявления известных мутаций существенно не отличались от их фенотипа в других популяциях. Как и в случае с ранее не описанными мутациями, клиническая картина заболевания у пациентов с ГКМП – носителей уже известных мутаций, характеризовалась выраженным клиническим полиморфизмом. Мутации Arg453Cys, Val606Met, Glu846Lys и Arg870Cys фенотипически проявились в виде более тяжелой клинической картины заболевания (раннее появление симптомов, наличие выраженной гипертрофии и обструкции ВТ ЛЖ). У пациентов с мутациями Arg723Cys и Glu846Lys заболевание имело более доброкачественное течение.
Четыре из шести ранее не описанных мутаций (Ala13Thr, Ala729Pro, Trp827Cys, Lys835Thr) фенотипически проявились относительно большей тяжестью клинических проявлений, а в трёх случаях (Ala13Thr, Ala729Pro, Lys835Thr) были сопряжены с неблагоприятным прогнозом - летальный исход (ВС) в молодом возрасте.
Российская популяция характеризуется значительной национальной и генетической гетерогенностью. На её формирование оказали влияние различные этногенетические процессы, происходившие на обширном географическом пространстве в течение ряда веков, включавшие многочисленные миграции, смешивание и интеграцию [Г.Т. Тавадов, 2002]. Поэтому неизбежно и разнообразие мутаций, обнаруженных в данной работе.
Характерные для ГКМП генетические дефекты характеризуются высокой популяционной специфичностью, разной степенью пенетрантности, выраженностью морфологических и клинических проявлений.
Дизайн настоящего исследования, основанного на анализе большой когорты пациентов без акцента на каждой семье, важен для внедрения генодиагностических методов в широкую клиническую практику. Мутации в гене -МНС играют важную роль в этиологии ГКМП у российских пациентов, однако, вероятно, это не единственный ген, ответственный за развитие заболевания. Для определения стратегии ДНК-диагностики ГКМП в России необходимо определить роль других кандидатных генов и идентифицировать ещё неизвестные локусы, этиологически связанные с развитием заболевания.
Особенности гемодинамики, структурных нарушений сердца
и роль нарушений диастолической функции при ГКМП
Комплексное ЭхоКГ-исследование, включающее оценку ДФ ЛЖ с помощью импульсного доплеровского исследования трансмитрального кровотока (ТМДП) и кровотока в лёгочных венах (ЛВП), а также импульсного доплеровского тканевого исследования (ТМД-ЭхоКГ) было выполнено на ультразвуковых аппаратах Vivid 3 Expert фирмы «GE», Sonos 7500 фирмы «Hewlett Packard» и HDI-5000 фирмы «Philips» двумя независимыми опытными специалистами.
У всех обследованных больных ГКМП при первичном ЭхоКГ-исследовании определялся основной признак заболевания – различной выраженности и локализации гипертрофия миокарда ЛЖ. Размеры ЛП, ТМЖП, ТЗСЛЖ, ИММ ЛЖ значительно превышали норму. При этом ТМЖП – от 15 до 42 мм, ТЗСЛЖ – от 9 до 26 мм, ИММ ЛЖ – от 77 до 347 г/м2, размер ЛП составил от 29 до 65 мм. Средние показатели размеров полости ЛЖ и его сократительной функции не отличались от нормальных значений.
Асимметрическая гипертрофия ЛЖ наблюдалась у подавляющего числа (92,5%) больных, в том числе гипертрофия базального отдела МЖП - у 30,5% пациентов, гипертрофия среднего отдела МЖП - 9,2%, гипертрофия МЖП на всем ее протяжении ― 51 (29,3%), апикальная гипертрофия - 5,2%, гипертрофия задней стенки ЛЖ - 2%. Симметрическая (концентрическая) гипертрофия ЛЖ встречалась лишь у 7,5% больных ГКМП.
У 42% пациентов была выявлена обструктивная форма заболевания (ОГКМП), диагностированная на основании повышения градиента давления
в ВТ ЛЖ до уровня от 30 до 132 мм рт. ст. При этом в 28,2% случаев регистрировалась выраженная обструкция ВТ ЛЖ в покое (Гр. Д > 50 мм рт.ст.). Переднее систолическое движение створок митрального клапана, являющееся одним из основных механизмов обструкции ВТ ЛЖ, отмечено у 44% обследованных больных. МР разной степени выявлена у 93% пациентов.
Больные с ОГКМП и НОГКМП не отличались по возрасту, продолжительности заболевания, гендерной принадлежности и частоте встречаемости семейной формы болезни. При этом отмечена большая частота и выраженность клинических проявлений заболевания, тяжесть функциональных нарушений, более низкие значения «качества жизни» и толерантности к физическим нагрузкам (p<0,001) у больных с обструктивной ГКМП. По данным ЭхоКГ определяется достоверно большая выраженность гипертрофии миокарда ЛЖ, больший размер ЛП (p<0,001), большая частота выявления выраженной ДД (псевдонормальный и рестриктивный тип) и значимой степени МР (p<0,001) у больных ОГКМП, достоверно чаще (р<0,01) регистрировалась пароксизмальная форма МА. По данным корреляционного анализа обнаружена тесная взаимосвязь между уровнем обструкции ВТ ЛЖ и ФК СН, ИММ ЛЖ, размером ЛП и ЛП/КДР, показателями ВЭМ-теста и некоторыми показателями ТМДП.
Большинство обследованных больных ГКМП (85%) имели выраженную гипертрофию преимущественно МЖП, при этом ИММ ЛЖ у них превысил 100 г/м2 и у 60% пациентов толщина МЖП – 20 мм. При разделении больных ГКМП по выраженности гипертрофии миокарда ЛЖ (по медиане ИММЛЖ) достоверные различия были обнаружены в отношении ФК СН и показателя КЖ, уровня обструкции ВТ ЛЖ, размера ЛП и соотношения ЛП/КДР (p<0,001), результатов нагрузочного ВЭМ-теста, выраженности ДД и МР (p<0,01). При этом в группе больных ГКМП с ИММЛЖ > 125 г/м2 отмечено достоверное преобладание обструктивной формы заболевания (52,3% против 31,8%, р<0,005). Обнаружена тесная корреляционная зависимость между ИММЛЖ и ФК СН, уровнем обструкции ВТ ЛЖ, размером ЛП, тяжестью ДД и степенью МР, показателями КЖ и нагрузочного теста, а также некоторыми показателями ТМДП, спектра ЛВП и ТМД-ЭхоКГ
При ранжировании по степени тяжести ДД ЛЖ у подавляющего большинства обследованных больных ГКМП (87,6%) были выявлены те или иные диастолические расстройства (рис. 2). У 56,2% больных регистри-ровалась выраженная ДД (псевдонормальный или рестриктивный тип наполнения ЛЖ). Нормальный тип наполнения был выявлен лишь у 12,4% от всех обследованных.
 Рисунок 2. Распределение больных ГКМП по выраженности
Рисунок 2. Распределение больных ГКМП по выраженности диастолической дисфункции ЛЖ
Больные ГКМП с выраженными и умеренными нарушениями ДФ ЛЖ не различались по возрасту, полу, продолжительности заболевания и принадлежности к семейной форме. При этом возраст и длительность заболевания пациентов с нормальным типом наполнения ЛЖ оказались достоверно (p<0,05) меньшими, чем у больных с ДД ЛЖ.
Больные ГКМП с выраженными нарушениями ДФ характеризовались большей тяжестью клинической симптоматики. При этом в группе с выраженными диастолическими нарушениями достоверно (p<0,05) чаще встречались больные с обструктивной формой ГКМП, оказалась более выраженной гипертрофия миокарда за счет большей (p<0,04) толщины МЖП и чаще (p<0,02) регистрировалась митральная недостаточность 2-3 степени. Обнаружена тесная зависимость между выраженностью ДД ЛЖ и ФК СН (p<0,001), ИММЛЖ, уровнем обструкции ВТЛЖ, размером ЛП и степенью МР (p<0,01), показателями нагрузочного ВЭМ-теста (p<0,001)
В целом полученные результаты свидетельствуют о наличии тесной зависимости между тяжестью функциональных нарушений (ФК СН) и выраженностью гипертрофии, обструкции, ДД ЛЖ, степенью МР, показателями «качества жизни» (табл. 3).
Таблица 3
Результаты корреляционного анализа
(функциональный класс сердечной недостаточности)
| | ФК СН (NYHA) r p | |
| ИММ ЛЖ | 0.49 | 0.00001 |
| ТМЖП | 0.44 | 0.00001 |
| ТЗСЛЖ | 0.29 | 0.001 |
| Градиент давления ВТ ЛЖ | 0.42 | 0.00001 |
| Размер ЛП | 0.44 | 0.00001 |
| Соотношение ЛП/КДР | 0.41 | 0.00001 |
| Тип ДД ЛЖ | 0.32 | 0.0001 |
| Степень МР | 0.40 | 0.00001 |
| «Качество жизни» | 0.55 | 0.00001 |
| Em/ Em sept | 0.43 | 0.0023 |
| Em lat | - 0.28 | 0.049 |
Определенные в настоящей работе основные морфометрические характеристики больных ГКМП в полной мере соответствуют результатам большинства крупных исследований. При этом все исследователи отмечают существенное преобладание (70 - 95% случаев) асимметричной гипертрофии ЛЖ за счет преимущественного вовлечения в процесс МЖП [E. Wigle, 2001; H.G. Klues et al., 1995; P. Spirito et al., 1997].
Умеренное преобладание среди обследованных больных НОГКМП (58%) связано с выбором принятого в соответствие с существующими рекомендациями жёсткого критерия – градиент давления ВТ ЛЖ в покое более 30 мм рт. ст. При этом у значительного числа (28,2%) обследованных больных ОГКМП регистрировалась выраженная обструкция ВТ ЛЖ в покое (Гр. Д > 50 мм рт. ст.), что имеет важное значение не только с точки зрения общей клинико-гемодинамической характеристики, но и для выбора адекватной лечебной тактики в отношении этой категории больных. Именно разделение больных на ОГКМП и НОГКМП позволило выявить достоверные различия в тяжести клинических проявлений и функциональном состоянии пациентов, выраженности гипертрофии, ДД ЛЖ и МР, частоте развития МА. На наличие этих ассоциаций указывают многие исследователи [Ю.Н. Беленков и соавт., 2008; I. Olivotto et al., 2001]. Однако по мнению некоторых авторов для ГКМП характерно несоответствие между степенью гипертрофии миокарда ЛЖ, выраженностью диастолических нарушений и тяжестью клинических проявлений [E. Wigle, et al., 1995; P. Spirito et al., 1997].
Богатый опыт B.J. Maron и соавт. (1995, 2002, 2003) свидетельствует о том, что ДД регистрируется не менее чем у 80% больных ГКМП, достигая наибольшей выраженности именно при этом заболевании.
Важным обстоятельством, отмеченным в данной работе, является выявленное наличие тесной взаимосвязи между выраженностью обструкции ВТ ЛЖ, гипертрофии и ДД ЛЖ, что подтверждается результатами корреляционного анализа. Этот результат может быть связан с выбранным подходом качественного разделения больных по выраженности ДД ЛЖ в условиях комплексного анализа показателей не только ТМДП, но ЛВП и ТМД-ЭхоКГ – наиболее информативного метода оценки ДФ. С практической точки зрения такой подход представляется наиболее оправданным в связи с известными трудностями в интерпретации результатов обычного ДЭхоКГ-исследования.
Таким образом, полученные результаты свидетельствуют о том, что при ГКМП наличие существенной обструкции ВТ ЛЖ, выраженность гипертрофии миокарда и ДД ЛЖ являются важнейшими и тесно связанными между собой детерминантами тяжести клинических проявлений, функциональных нарушений и «качества жизни» больных.
Особенности перфузии миокарда больных ГКМП
О
 днофотонная эмиссионная компьютерная томография (ОЭКТ) с Тс99m –МИБИ в покое и после нагрузочного ВЭМ-теста выполнена по стандартному протоколу 86 больным ГКМП (м/ж – 57/29, ср. возраст 44,7 12,0 лет). Использовали цифровую ротационную гамма-камеру «Sophy camera DSX» («Sopha Medical», Франция).
днофотонная эмиссионная компьютерная томография (ОЭКТ) с Тс99m –МИБИ в покое и после нагрузочного ВЭМ-теста выполнена по стандартному протоколу 86 больным ГКМП (м/ж – 57/29, ср. возраст 44,7 12,0 лет). Использовали цифровую ротационную гамма-камеру «Sophy camera DSX» («Sopha Medical», Франция).Рисунок 3. Нарушения перфузии миокарда ЛЖ у больных ГКМП
У 83,9% обследованных больных ГКМП выявлены нарушения перфузии миокарда ЛЖ, при этом у 33,9% - стабильные ДП, у 12,9% - преходящие ДП, у 21% больных – стабильные и преходящие ДП. Таким образом, преходящие ДП выявлены у 33,9% больных, стабильные ДП – у 54,8%, у 16,1% больных обнаружены ДП только в покое (рис. 3). Лишь 16,1% больных не обнаружили каких-либо нарушений перфузии. Аналогичные результаты были получены другими исследователями [S. T. Li et al., 2000; S. Morishita et al., 2001].
При сопоставлении отмеченных нарушений перфузии с клиническими проявлениями оказалось, что частота выявления синдрома стенокардии среди пациентов с ГКМП, имеющих преходящие ДП, достоверно выше (75% против 24%, p<0,01), чем у больных, не имеющих преходящих ДП.
При проведении корреляционного анализа была у больных ГКМП установлена положительная достоверная связь между ФК стенокардии и глубиной (r=0,72, p=0,0002), а также площадью (r=0,47, p=0,041) преходящих нарушений перфузии миокарда ЛЖ. Подобные данные были получены и другими исследователями [Y. Kagaya et al., 1992]. Однако в некоторых работах указывалось на отсутствие связи между преходящими ДП и наличием в клинической картине больных ГКМП синдрома стенокардии [S. Hirasaki et al., 1999], поэтому данный вопрос остаётся до сих пор спорным и требует дальнейшего изучения.
Полученные результаты, согласующиеся с данными других исследо-вателей [M. Yamada et al., 1998], свидетельствуют о том, что степень обструкции ВТ ЛЖ не оказывает определяющего влияния на перфузию миокарда.
Больные с выраженной гипертрофией ЛЖ характеризуются большей частотой выявления (96,3%, р<0,01), площадью и глубиной нарушений перфузии миокарда ЛЖ в покое и/или при нагрузке (р<0,05). Обнаруженная зависимость между степенью гипертрофии и частотой встречаемости преходящих ДП, отражающих ишемию миокарда, вероятно, объясняется прогрессированием относительной коронарной недостаточности.
Таким образом, томосцинтиграммы большинства больных ГКМП демонстрируют неравномерность перфузии миокарда, которая находится в зависимости от выраженности гипертрофии и наличия дефектов перфузии миокарда ЛЖ и не связана с наличием или отсутствием обструкции его выносящего тракта. Преходящие и стабильные дефекты перфузии миокарда ЛЖ чаще встречаются у больных с выраженной гипертрофией. При этом у больных с выраженной гипертрофией миокарда выявляются преимущественно крупноочаговые изменения, в то время как у пациентов с умеренной гипертрофией чаще обнаруживаются поверхностные стабильные дефекты перфузии. Участки максимального включения радиофармпрепарата и преходящих дефектов перфузии наиболее часто локализуются в зонах максимальной гипертрофии, стабильные дефекты перфузии – в областях, расположенных вне максимального утолщения миокарда ЛЖ.
Нарушения и вариабельность сердечного ритма у больных ГКМП
СМЭКГ для изучения характера и нарушений сердечного ритма (НРС) и проводимости было проведено всем 174 больным ГКМП, включенным в проспективное наблюдение. С целью детального изучения особенностей ВРС и влияния медикаментозной терапии проведено отдельное исследование с включением 82 пациентов (м/ж – 50/32, ср. возраст 43,513,0 лет). Методы исследования помимо СМЭКГ включали ЭхоКГ и пробу с физической нагрузкой на велоэргометре. СМЭКГ проводили с использованием аппаратуры Astrocard® Holtersystem Elite, «ЗАО Медитек» (Россия). ЭКГ регистрировали на магнитный носитель в двух и трёх отведениях при помощи регистраторов с диапазоном пропускания частот от 0,05 до 100 Гц.
В связи с существующим представлением о прогрессирующем характере течения ГКМП через нарастание ДД, обструкции ВТ ЛЖ, дилатации и дисфункции ЛП, развитие в результате фибрилляции предсердий [K. Robinson et al., 1990; А.S. Abadag et al., 2005] в процессе проспективного наблюдения у обследованных больных был проанализирован характер сердечного ритма с учётом наличия, в том числе по данным анамнеза и информации из медицинских документов, пароксизмальной МА (рис. 4).
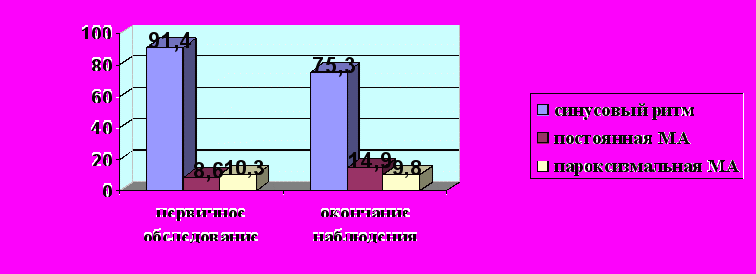 Рисунок 4. Характер сердечного ритма больных ГКМП
Рисунок 4. Характер сердечного ритма больных ГКМПв ходе проспективного наблюдения
На момент первичного обследования пароксизмальная форма МА регистрировалась у 10,3%, постоянная МА - у 8,6% больных ГКМП. Следует отметить, что пароксизмы фибрилляции предсердий были зарегистрированы только у 3% обследованных больных ГКМП и только анализ анамнести-ческих данных и имевшейся в наличие медицинской документации позволил установить фактическую картину.
По данным СМЭКГ те или иные НРС были выявлены у 167 (96,5%) больных ГКМП, что соответствует литературным данным. Атриовентрику-лярная блокада I-II cтепени зарегистрирована у 5 (3%), синдром WPW – 4 (2,5%), миграция водителя ритма – у 1 (0,6%) пациентов.
Результаты изучения характера и частоты встречаемости различных НРС у обследованных больных ГКМП представлены на рисунке 5.
%
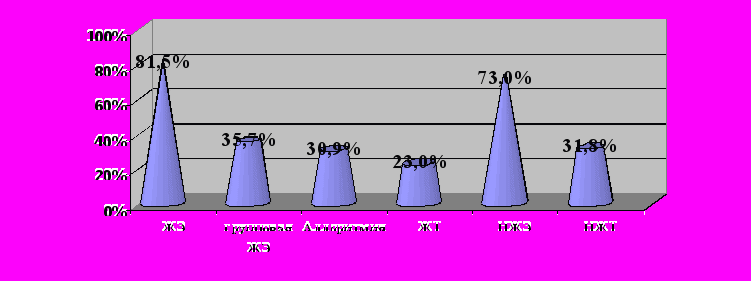 Рисунок 5. Характер и частота встречаемости НРС у больных ГКМП
Рисунок 5. Характер и частота встречаемости НРС у больных ГКМППодгрупповой анализ выявил достоверное (p<0,01) преобладание числа больных с пароксизмальной МА и НЖЭ среди пациентов с обструктивной формой ГКМП по сравнению с НОГКМП как при первичном обследовании, так и в ходе проспективного динамического наблюдения. При этом в обеих группах отмечается увеличение доли больных с пароксизмальной МА и переходом в целом ряде случаев в её постоянную форму. По частоте выявления при СМЭКГ ЖЭ, эпизодов над-, и желудочковой тахикардии сравниваемые группы больных с ОГКМП и НОГКМП достоверно не различались.
Разделение больных ГКМП в зависимости от степени нарушения ДФ ЛЖ обнаружило достоверную (p<0,01) динамику в появлении в ходе наблюдения новых случаев заболевания, сопровождающихся МА, среди больных с выраженной ДД ЛЖ. В этой группе достоверно (p<0,001) чаще регистрировалась НЖЭ; в отношении ЖЭ, пароксизмов ЖТ и НЖТ тенденция не достигала уровня достоверности.
В рамках исследования изучались суточные характеристики частоты синусового ритма и ВРС у больных ГКМП на безмедикаментозном фоне. Максимальная и средняя частоты у больных ГКМП достоверно ниже, чем в группе здоровых лиц (табл. 4). Причем данная особенность ЧСС у больных ГКМП не обусловлена влиянием предшествующей медикаментозной терапии (в первую очередь, β-адреноблокаторов) на эти показатели.
