Синтез, свойства и биологическая активность енаминоамидов ацилпировиноградных кислот 14. 04. 02-фармацевтическая химия, фармакогнозия
| Вид материала | Автореферат диссертации |
- Синтез соединений на основе химических превращений производных α- оксокарбоновых кислот, 643.93kb.
- Синтез, свойства, биологическая активность n-гетериламидов α-оксокислот и продуктов, 367.21kb.
- Синтез, химические свойства и биологическая активность 1,4-дизамещенных 5-арил-3-гидрокси-3-пирролин-2-онов, 667.95kb.
- Синтез, свойства и биологическая активность продуктов взаимодействия 1,2,4-триазолов, 669.98kb.
- Синтез и свойства новых производных 2 (1,2,4 триазолил 5 тио)уксусных кислот 15. 00., 240.9kb.
- Синтез и биологическая активность карбо- и гетероциклов на основе тетрацианоэтилена, 673.64kb.
- Синтез, свойства и биологическая активность производных 2-хлорникотинонитрилов, 264.36kb.
- Примерная программа рекомендуется для направления подготовки (специальности) 111801, 717.4kb.
- Программа курса «Аналитическая химия» специальность «Фармация», 92.69kb.
- Тематический план лекций по дисциплине «Фармацевтическая химия», 32.57kb.
На правах рукописи
Бородин Антон Юрьевич
СИНТЕЗ, СВОЙСТВА И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ ЕНАМИНОАМИДОВ АЦИЛПИРОВИНОГРАДНЫХ КИСЛОТ
14.04.02-фармацевтическая химия, фармакогнозия
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Пермь -2011
Диссертационная работа в ГОУ ВПО «Пермская государственная фармацевтическая академия Росздрава»
Научный руководитель: доктор фармацевтических наук,
доцент Игидов Назим Мусабекович,
ГОУ ВПО «Пермская государственная фармацевтическая академия Росздрава»
Научный консультант: кандидат биологический наук,
доцент Чащина Светлана Викторовна,
ГОУ ВПО «Пермская государственная фармацевтическая академия Росздрава»
Официальные оппоненты:
доктор фармацевтических наук,
профессор Михалёв Александр Иванович,
ГОУ ВПО «Пермская государственная фармацевтическая академия Росздрава»
доктор химических наук,
профессор Масливец Андрей Николаевич,
ГОУ ВПО «Пермский государственный университет»
Ведущая организация: Институт технической химии УРО РАН, г. Пермь
Защита диссертации состоится «20» сентября 2011 г. в 13 часов
на заседании Диссертационного совета Д 208.068.01 при ГОУ ВПО
«Пермская государственная фармацевтическая академия Росздрава» по
адресу: 614990, г. Пермь, ул. Полевая, 2.
С диссертацией можно ознакомиться в библиотеке Пермской государственной фармацевтической академии по адресу: г. Пермь, ул. Крупской, 46.
Дата размещения объявления о защите диссертации на сайте ПГФА
http: // www.pfa.ru « » ______________ 2011 г.
Автореферат разослан « 05 » июля 2011 г.
Ученый секретарь
диссертационного совета Д 208.068.01,
кандидат фармацевтических наук, доцент Липатникова И.А.
Актуальность темы. Поиск перспективных и малотоксичных соединений, обладающих выраженными фармакологическими свойствами, составляет одну из важнейших задач фармацевтической науки.
Химическая модификация структуры ацилпировиноградных кислот (АПК) путем введения различных фармакофорных групп дает неисчерпаемые возможности для получения новых высокоэффективных соединений, обладающих направленным специфическим действием.
Среди ациклических производных АПК более подробно исследованы эфиры, а также продукты дециклизации 5-арил-2,3-фурандионов - амиды, гидразиды, которые обладают противомикробной, противовоспалительной, анальгетической, противовирусной и другими видами активности при низкой токсичности.
Наименее изученными производными АПК являются енаминоамиды ацилпировиноградных кислот. В связи с этим весьма актуальным представляется дальнейшее исследование их свойств и возможностей применения в органическом синтезе и фармации.
Цель работы. Целью настоящей работы является разработка и усовершенствование известных методов синтеза новых биологически активных енаминоамидов ацилпировиноградных кислот.
Задачи исследования. Для достижения поставленной цели необходимо решить следующие задачи:
- Осуществить синтез новых енаминопроизводных на основе взаимодействия ацилпировиноградных кислот с первичными аминами.
- Циклодегидратацией енаминокислот получить 3-замещенные 2-фураноны.
- Дециклизацией 3-замещенных 2-фуранонов под действием первичных аминов получить енаминоамиды АПК.
- Осуществить синтез N-замещенных амидов 4-арил-2-(β,β-диэтиламиноэтиламино)-4-оксо-2-бутеновых кислот реакцией амидов АПК с N,N-диэтиламиноэтиламином и перевести их в водорастворимые соли.
- Изучить биологическую активность синтезированных соединений и выявить взаимосвязь структуры с действием
Научная новизна
Установлено, что при взаимодействии ароилпировиноградных кислот с азотсодержащими гетериламинами образуются 4-арил-2-гидрокси-4-оксо-2-бутеноаты оксадиазолия и пиридиния.
Впервые отмечено, что 2-ариламино-5,5-диметил-4-оксогекс-2-еновые кислоты вступают в реакцию с уксусным ангидридом в циклической форме с образованием продуктов ацилирования гидроксильной группы 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетатов.
Выявлено, что дециклизация 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетатов под действием первичных аминов приводит к образованию енаминоамидов пивалоилпировиноградной кислоты.
Предложен синтез ранее не известных N-замещенных амидов 4-арил-2-(β,β -диэтиламиноэтиламино) -4-оксо-2-бутеновых кислот.
Впервые обнаружена местноанестезирующая активность в ряду
N-замещенных амидов 4-арил-2-(β,β-диэтиламиноэтиламино)-4-оксо-2-бутеновых кислот и 4-арил-2-гидрокси-4-оксо-2-бутеноатов 3-метил-пиридиния.
На основании данных ИК,- ПМР спектроскопии и масс-спектрометрии выявлены особенности строения полученных соединений.
Среди синтезированных соединений обнаружены вещества, обладающие противомикробной, местноанестезирующей, противовоспалительной и анальгетической активностью. Выявлены некоторые закономерности между строением и биологической активностью полученных соединений. Новизна исследования подтверждена патентом РФ на изобретение и решением о выдаче патента на изобретение.
Практическая значимость. Усовершенствованы или предложены новые методы синтеза 2-ариламино-5,5-диметил-4-оксо-2-гексеновых кислот, 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетатов, N-замещенных амидов 2-ариламино-5,5-диметил-4-оксо-2-гексеновых кислот, N-замещенных амидов 4-арил-2-(β,β-диэтиламиноэтиламино)-4-оксо-2-бутеновых кислот. Синтезировано 141 новое соединение, из них 21 соль. Полученные результаты используются на кафедрах органической химии, физиологии и патологии, микробиологии Пермской государственной фармацевтической академии в научно-исследовательской работе, а также при выполнении дипломных работ.
Публикации. По материалам диссертации опубликованы 2 статьи в журналах, рекомендованных ВАК, 9 статей и 13 тезисов докладов в сборниках и материалах научных конференций различного уровня, получены 1 патент РФ на изобретение и решение о выдаче патента на изобретение.
Апробация работы. Материалы диссертационной работы обсуждались на итоговых научных конференциях профессорско-преподавательского состава Пермской государственной фармацевтической академии 2006-2010 гг.; на международной научной конференции «Инновационный потенциал естественных наук», Российской научно-практической конференции, посвященной 70-летию ПГФА Пермь 2007 г., Международной конференции «Техническая химия. От теории к практике» Пермь. 2008 г.; Российской научно-практической конференции ПГФА, «Медицина и здоровье» Пермь. 2008 г.; Ежегодной областной конференции «Фармация и общественное здоровье» Екатеринбург. 2009-2010 гг.; Научно-практической школе - конференции, посвященной 75-летию со дня рождения Ю.С. Андрейчикова «Химия поликарбонильных соединений» Пермь. 2009 г.; Конференции посвященной 175-летию со дня рождения отечественного Д.И. Менделеева и 140-летию открытия им Периодического закона «Разработка, исследование и маркетинг новой фармацевтической продукции» Пятигорск. 2009 г. А также на украинской научно-практической конференции, посвященной памяти профессора П.А. Петюнина – Харьков, 2009 г.
Связь задач исследования с проблемным планом фармацевтических наук. Диссертационная работа выполнена в соответствии с планом научно-исследовательских работ ГОУ ВПО «Пермская государственная фармацевтическая академия Росдрава» (№ государственной регистрации 01.9.50 007418).
Конкретное участие автора в получении научных результатов. Изучены и обобщены данные отечественной и зарубежной литературы по методам получения и биологической активности производных АПК. Разработаны или усовершенствованы методы синтеза 2-ариламино-5,5-диметил-4-оксо-2-гексеновых кислот, 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетатов, N-заме-щенных амидов 2-ариламино-5,5-диметил-4-оксо-2-гексеновых кислот, N-заме-щенных амидов 4-арил-2-(β,β-диэтиламиноэтиламино)-4-оксо-2-бутеновых кислот. Структура полученных соединений подтверждена данными ИК,- ПМР спектроскопии и масс-спектрометрии. На основании данных фармакологического скрининга синтезированных соединений выявлены некоторые закономерности качественной зависимости структура-активность. Осуществлен целенаправленный синтез соединений, обладающих местноанестезирующей активностью в ряду производных АПК. Изучено влияние анионной части молекулы на показатель глубины при поверхностной анестезии и продолжительность действия.
Объём и структура диссертации. Содержание работы изложено на 179 страницах машинописного текста и состоит из введения, 4 глав, выводов и списка литературы. Список литературы включает 152 работы отечественных и зарубежных авторов. Диссертация содержит 35 таблиц и 16 схем.
Основное содержание работы
Взаимодействие АПК с первичными аминами
С целью дальнейшего изучения химических свойств, особенностей строения, а также для поиска новых биологически активных веществ нами синтезирован ряд не описанных в литературе N-замещенных 2-амино-4-арил-4-оксобут-2-еновых кислот (2а-м) и N-замещенных 2-амино-5,5-диметил-4-оксогекс-2-еновых кислот (3а-н) взаимодействием АПК (1) с ароматическими первичными аминами в среде этанола или толуола.
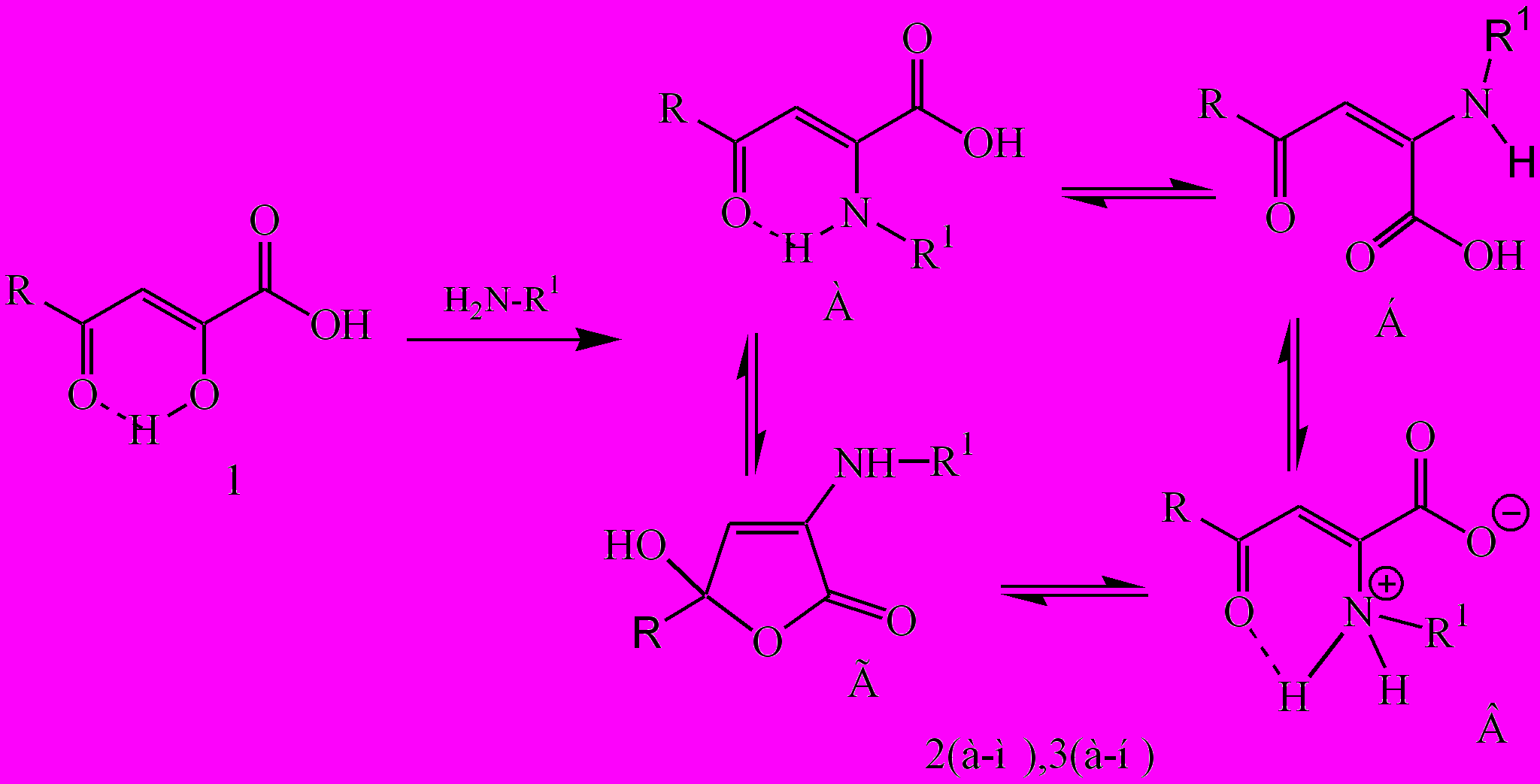
R=C6H5 (1а, 2а-е), 4-СН3C6H4 (1б, 2ж, 2з), 2,4-(СН3)2C6H3 (1в, 2и), 4-FC6H4 (1г, 2к, 2л), 4-СlC6H4 (1д, 2м), (СН3)3(3а-н);
R1=2,4-(СН3)2C6H3 (2а, 3б), 2,6-(СН3)2C6H3 (2б, 3в), 2,4,6-(СН3)3C6H2 (2в, 3г), 3-СF3C6H4 (2г), 2-СН3-5-NO2C6H3 (2д, 2ж, 3к), 4-C2H5OOCC6H4 (2к, 3л), 2-НО-3-i-Pr-6-СН3C6H2 (2е, 2з, 2и, 2л, 2м, 3н), 4-СН3ОС6Н4 (3а), 2-BrC6H4 (3д), 2-JC6H4 (3е), 4-BrC6H4 (3ж), 2,4-(Br)2C6H3 (3з), 2,4-(Cl)2C6H3 (3и), (C2H5)2N(CH2)2OOCC6H4 (3м),
Полученные соединения представляют собой бесцветные или окрашенные в желтый цвет кристаллические вещества, растворимые в бензоле, эфире, ацетоне, диметилсульфоксиде, диметилформамиде, малорастворимые в ацетонитриле, пропаноле-2, не растворимые в гексане и воде.
Ранее в литературе строение продуктов взаимодействия ароилпировиноградных кислот с азотсодержащими в цикле гетериламинами было интерпретировано по-разному. В продолжение исследований химического поведения АПК с гетериламинами, нами изучено их взаимодействие с 2-амино-3-метилпиридином и 2-амино-5-фенил-1,3,4-оксадиазолом. Установлено, что кратковременное нагревание эквимолярных количеств реагентов в спирте или уксусной кислоте приводит к образованию 4-арил-2-гидрокси-4-оксо-2-бутеноатов 3-метил-2-пиридиламмония (4а-д) и 4-арил-2-гидрокси-4-оксо-2-бутеноатов 5-фенилоксадиазолиламмония (4е-и) соответственно.
 R=C6H5 (4а, 4е), 4-СН3C6H4 (4б, 4ж), 4-С2Н5OC6H4 (4в), 4-FC6H4 (4г, 4з), 4-СlC6H4 (4д, 4и); R1=3-CH3-2-пиридил (4а-д), оксадиазолил (4е-и)
R=C6H5 (4а, 4е), 4-СН3C6H4 (4б, 4ж), 4-С2Н5OC6H4 (4в), 4-FC6H4 (4г, 4з), 4-СlC6H4 (4д, 4и); R1=3-CH3-2-пиридил (4а-д), оксадиазолил (4е-и)Синтезированные вещества представляют собой бесцветные или слегка желтоватые вещества, растворимые в ацетоне, диметилсульфоксиде, диметилформамиде, малорастворимые в этаноле, воде (4а-д), ацетонитриле, и нерастворимые в эфире, гексане.
Химические свойства енаминокислот
Имеющиеся в литературе сведения о строении продуктов взаимодействия пивалоилпирувамидов с первичными аминами ошибочны. В связи с необходимостью пересмотра ранних структурных решений и устранения неоднозначных выводов нами изучено поведение некоторых енаминокислот (3а, 3е, 3и) с 2-пиридиламинами. Было установлено, что при кратковременном нагревании эквимолярных количеств реагентов в спирте образуются 2-ариламино-5,5-диметил-4-оксо-2-гексеноаты 2-пиридиламмония (5а, б) и 3-метил-2-пириди-ламмония (5в, г)
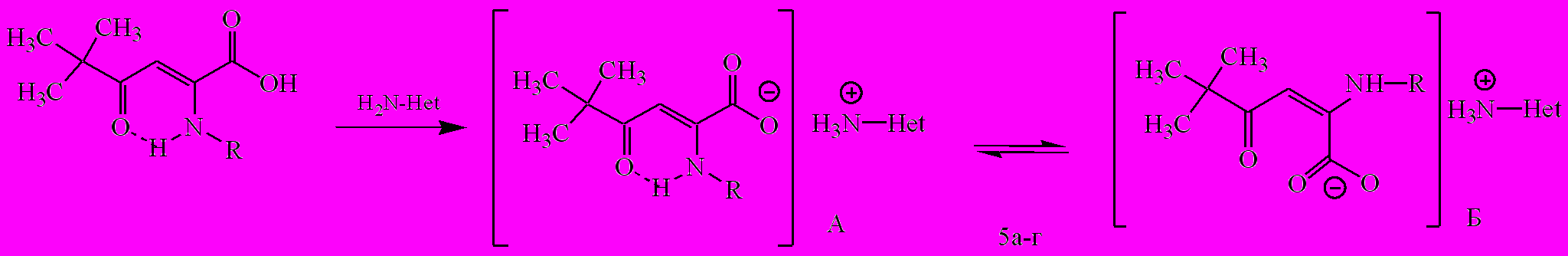
R= 4-СН3ОС6Н4 (3а, 5а), 2-J-C6H4 (3е, 5б, 5в), 2,4-(Cl)2C6H3 (3и, 5г), Het= 2-пиридил (5а, 5б), 3-СН3-2-пиридил (5в, 5г)
Известно, что 2-аминопроизводные ароилпировиноградных кислот подвергаются циклодегидратации в среде уксусного ангидрида с образованием 5-арил-3-имино-2,3-дигидро-2-фуранонов. До наших исследований отсутствовали данные о 5-алкилзамещенных иминофуранонах. Несколько иначе протекает реакция 2-ариламино-5,5-диметил-4-оксогекс-2-еновых кислот (3) в уксусном ангидриде. При взаимодействии енаминокислот (3д-л), находящихся в растворе в трех формах А, Б, Г с уксусным ангидридом, были выделены лишь продукты ацилирования гидроксильной группы формы Г – 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетаты (6а-ж).
Енаминокислоты (3б-г) нам не удалось подвергнуть в таких условиях циклодегидратации, при этом были выделены исходные соединения (3б-г) в енаминокетонной форме Е-конфигурации.
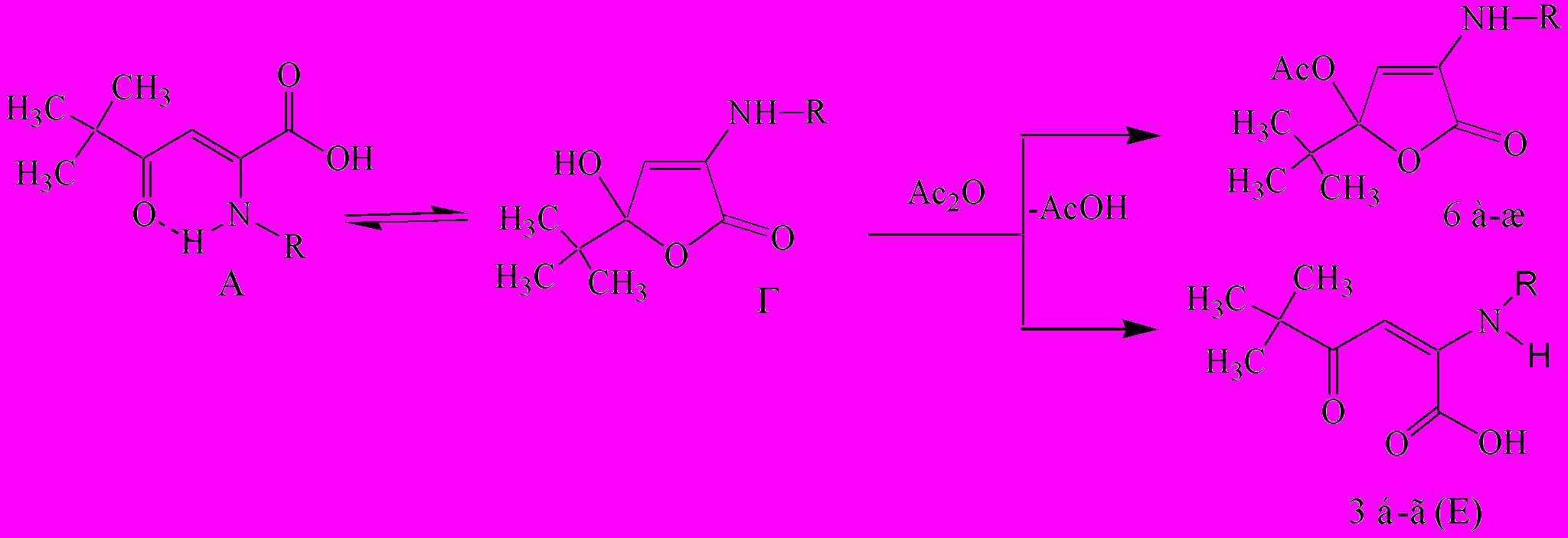

R= 2,4-(СН3)2C6H3 (3б), 2,6-(СН3)2C6H3 (3в), 2-BrC6H4 (6а), 2-JC6H4 (6б), 4-C2H5OOCC6H4 (6в), 4-BrC6H4 (6г), 2,4-(Br)2C6H3 (6д), 2,4-(Cl)2C6H3 (6е), 2-CH3-5-NO2C6H3 (6ж)
Фураноны (6а-ж) – бесцветные или слегка желтоватые кристаллические вещества, устойчивые при хранении без доступа влаги, растворимые в большинстве органических растворителей.
В ИК спектрах соединений (6а-ж) присутствуют полосы поглощения: в области 3350-3368 см-1, характерные для валентных колебаний NH группы, 1770-1782 см-1 валентных колебаний лактонного карбонила фуранового цикла, сложноэфирного карбонила при 1735-1742 см-1.
Нами для сравнительной оценки реакционной способности, а также для дальнейшего поиска потенциальных биологически активных веществ был получен ранее неизвестный 3-(2-метил-5-нитрофенилимино)-5-(4-метилфенил)-2,3-дигидро-2-фуранон (7) по известной методике, циклизацией енаминокислоты 2ж в уксусном ангидриде.
Дециклизация 3-замещенных 2-фуранонов под действием первичных аминов
В литературе отсутствуют сведения о химических превращениях иминофуранонов, имеющих в положении 5 цикла алкильный радикал. Нами при проведении реакции 4-ариламино-2-трет-бутил-2,5-дигидро-5-оксофуран-2-илацетатов (6а, 6г, 6е, 6ж) с первичными аминами в среде абсолютного толуола или бензола были получены продукты дециклизации N-замещенные амиды 2-амино-5,5-диметил-4-оксо-2-гексеновых кислот (8а-я, 9а-ф). С целью биологического тестирования нами был расширен ряд енаминоамидов АПК (9). Для этого был введен в реакцию 3-(2-метил-5-нитрофенил)имино-5-(п-толил)-2,3-дигидро-2-фуранон 7 с первичными аминами в среде абсолютного бензола при нагревании в течение 5-10 минут. В результате были выделены N-замещенные амиды N-2-(2-метил-5-нитрофенил)амино-4-оксо-4-(4-метилфенил)-2-бутеновой кислоты (8аа, 9х, 9ц)
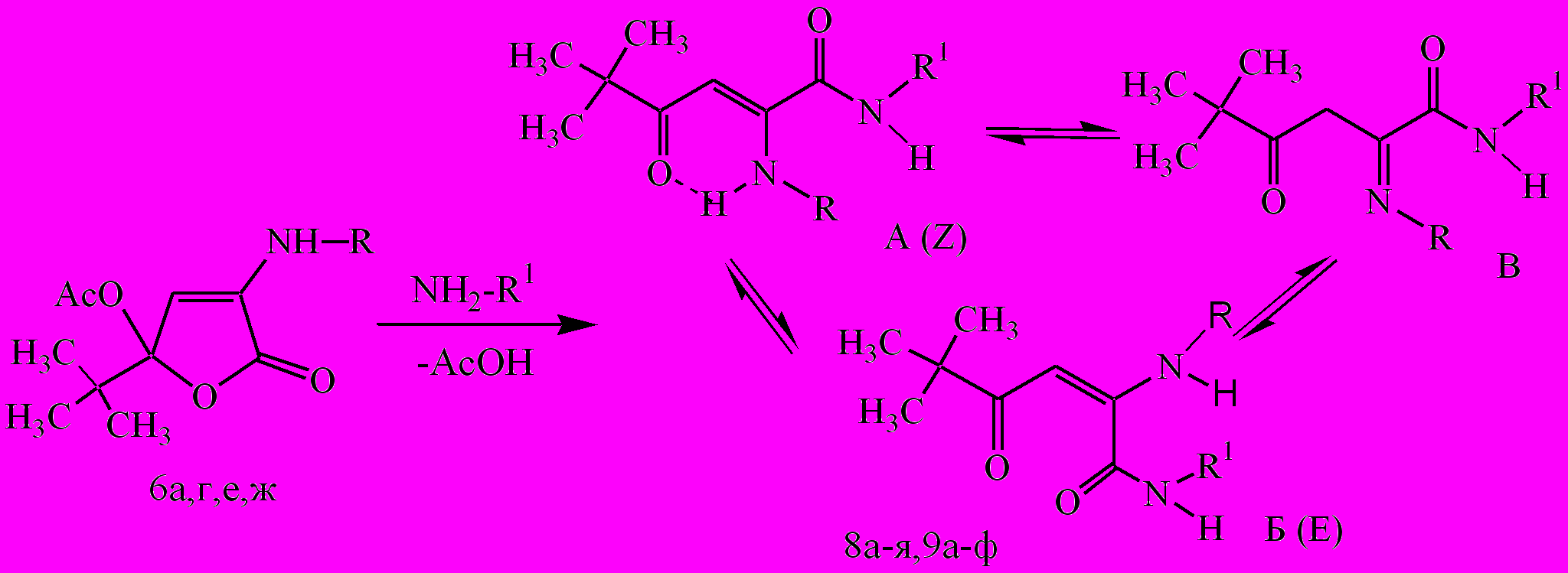
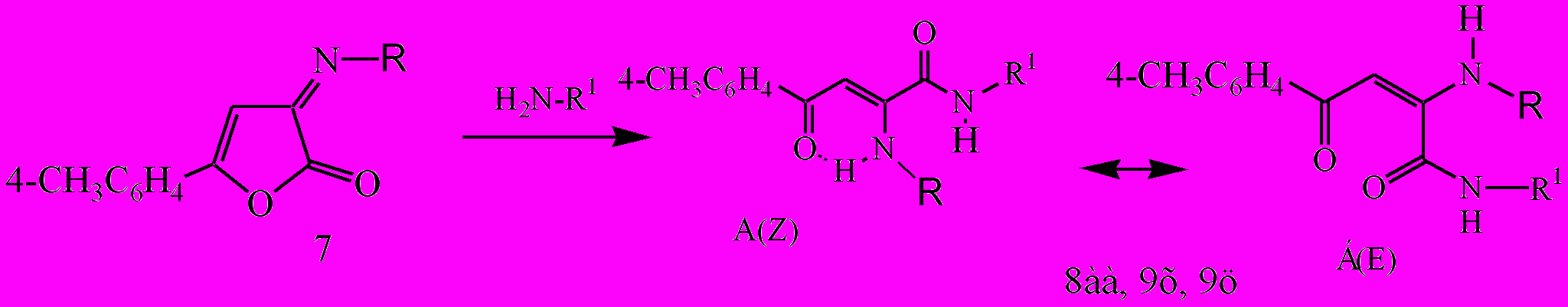
R=2-BrC6H4 (6а, 8а-и, 9а-е), 4-BrC6H4 (6г, 8к-т, 9ж-л), 2-CH3-5-NO2C6H3 (6е, 8у, 8ф, 8аа 9м, 9н, 9х, 9ц), 2,4-(Cl)2-C6H3 (6ж, 8х-я, 9о-ф)
R1=C6H5 (8а, 8к), 4-CH3C6H4 (8б, 8л, 8у,8аа), 4-CH3OC6H4 (8х), 2,6-(CH3)2C6H3 (8в), 4-NO2C6H4 (8г, 8м), 4-C2H5OOCC6H4 (8д, 8н, 8ц), 2-BrC6H4 (8е, 8о, 8ч), 2-JC6H4 (8ж, 8п), 4-BrC6H4 (8з, 8р, 8ш), 4-ClC6H4(8и, 8э), 2-CH3-5-NO2C6H3 (8с, 8ф, 8ю), 2,4-(Cl)2C6H3 (8т, 8я), 2-тиазолил (9а, 9м, 9о,9х), 4-фенил-2-тиазолил (9ж, 9п,9ц), 2-тиадиазолил (9н), оксадиазолил (9б, 9р), 2-пиридил (9в, 9з, 9с), 3-пиридил (9г, 9и), 4-пиридил (9д, 9к, 9т), 3-CH3-2-пиридил (9е, 9л, 9у), 4-CH3-2-пиридил (9ф),
Полученные соединения представляют собой бесцветные или окрашенные в желтый цвет кристаллические вещества, растворимые в диметилсульфоксиде, диметилформамиде, бензоле, трудно растворимые в этаноле, пропаноле-2, ацетонитриле, этилацетате, не растворимые в воде и гексане.
Взаимодействие амидов АПК с N,N-диэтилэтилендиамином
Известно, что местноанестезирующая активность современных препаратов обусловлена наличием в молекуле липофильной группы (часто в виде ароматического кольца), соединенной через промежуточную цепь (обычно включающую эфирную или амидную группу) с ионизируемой группой (как правило, третичным амином). Для оптимальной активности требуется баланс между гидрофильными и липофильными группами. В качестве матрицы для целенаправленного синтеза соединений с местноанестезирующей активностью были использованы амиды АПК (11а-н), полученные дециклизацией 5-арил-2,3-дигидрофуран-2,3-дионов (10) под действием 2,6-диметил-, 2,4,6-триметилани-линов и 4-амино-3-изопропил-5-метилфенола.
Полученные амиды АПК это желтоватые кристаллические вещества, не растворимые в воде и гексане. растворимые в большинстве органических растворителей.
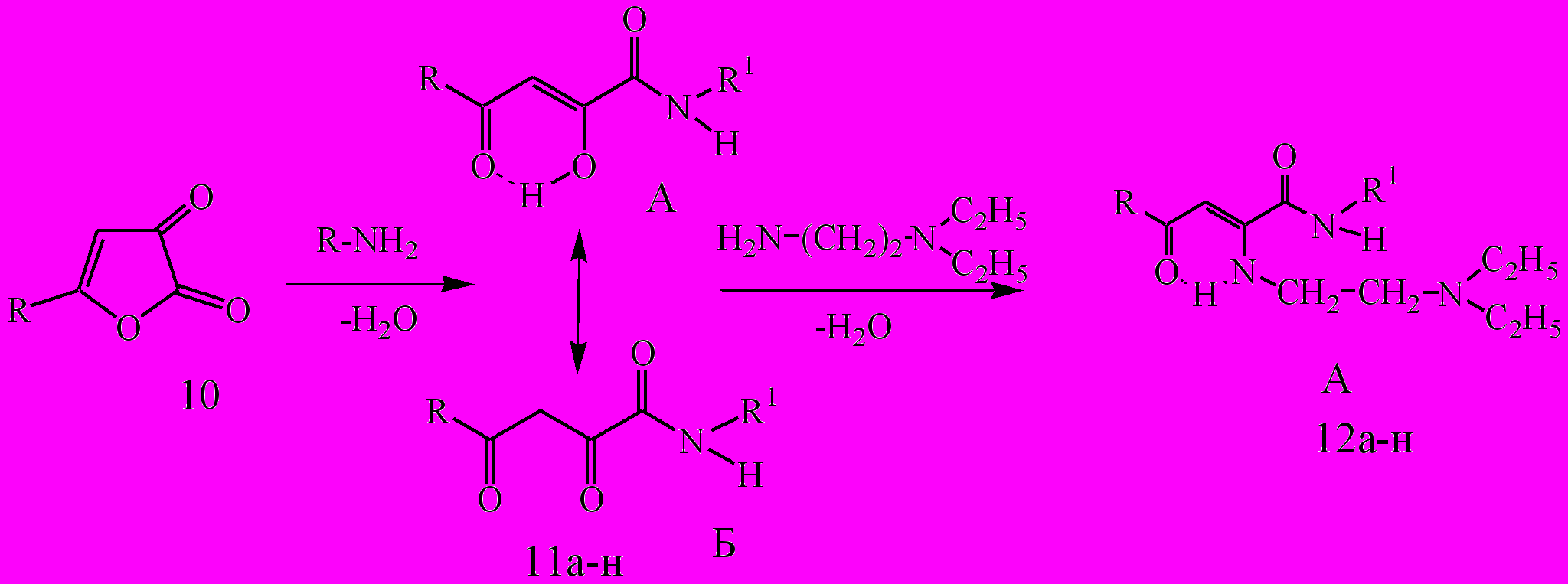
R=C6H5 (10а, 11а, 11б, 12а, 12б), 4-СН3C6H4 (10б, 11в-д, 12в-д), 4-СН3OC6H4 (10в, 11е, 11ж,12е, 12ж), 4-С2Н5OC6H4 (10г, 11з, 11и,12з, 12и), 4-FC6H4 (10д, 11к, 12к), 4-СlC6H4 (10е, 11л-н, 12л-н);
R1=2,6-(СН3)2C6H3 (11а, 11в, 11е, 11з, 11к, 11л,12а, 12в, 12е, 12з, 12к, 12л), 2,4,6-(СН3)3C6H2 (11б, 11г, 11ж, 11и, 11м, 12б, 12г, 12ж, 12и, 12м), 2-НО-3-i-Pr-6-Me-C6H2 (11д, 11н, 12д, 12н)
При кипячении эквимолярных количеств амидов АПК (11а-н) с N,N-диэтиламиноэтиламином в среде толуола в течение 15-30 минут были получены N-замещенные амиды 4-арил-2-(β,β-диэтиламиноэтиламино)-4-оксо-2-бутеновых кислот (12а-н).
Синтезированные соединения (12а-н) представляют собой бесцветные (12в, г, з, и, к, л, м) или окрашенные в розоватый (12а, б, д, е, ж, н) цвет кристаллические вещества, растворимые в этаноле, толуоле, диметилсульфоксиде, диметил-формамиде, хлороформе, ацетоне, эфире, труднорастворимые в циклогексане, не растворимые в воде и гексане.
С целью проведения биологических испытаний соединения (12а-г, е-м) были переведены в водорастворимую форму – гидрохлоридов (13а-ж), сукцинатов (14а-л) и гидротартратов (15а, 15б).

R=C6H5 (13а, 13б,14а, 14б,15а, б), 4-СН3C6H4 (13в, 13г,14в, 14г), 4-СН3OC6H4 (14д, 14е), 4-С2Н5OC6H4 (13д, 14ж, 14з), 4-FC6H4 (14и), 4-СlC6H4 (13е, 13ж, 14к, 14л); R1=2,6-(СН3)2C6H3 (13а, 13в, 13д, 13е, 14а, 14в, 14д, 14ж, 14и, 14к, 15а), 2,4,6-(СН3)3C6H2 (13б, 13г, 13ж, 14б, 14г, 14е, 14з, 14л, 15б); Х= Cl- (13а-ж), HOOC-CH2-CH2-COO- (14а-л), HOOC-CH(OH)-CH(OH)-COO-(15а, б)
