Работа выполнена в фгу «нцаг и п им. В. И. Кулакова Росмедтехнологий» директор академик рамн, профессор Сухих Г. Т
| Вид материала | Автореферат |
- На правах рукописи, 569.42kb.
- Влагалища и шейки матки у детей, 313.83kb.
- Протекторная и регенерационная терапия при остром и хроническом повреждении почки 14., 558.09kb.
- Проект «Мать и Дитя Федеральное государственное учреждение «Научный центр акушерства,, 1694.96kb.
- Передняя резекция прямой кишки у пациентов пожилого и старческого возраста 14. 00., 442.25kb.
- На правах рукописи, 1315.73kb.
- Клинические и экспериментальные аспекты изучения молекулярно-биологических маркеров, 476.4kb.
- Лотоков артур мустафович современные аспекты неотложной хирургии в абдоминальной онкологии, 638.51kb.
- Автореферат на соискание ученой степени, 643.39kb.
- Феохромоцитома/параганглиома: клинико-генетические аспекты диагностики и лечения. 14., 338.24kb.
На правах рукописи
ШМАКОВ РОМАН ГЕОРГИЕВИЧ
РЕПРОДУКТИВНОЕ ЗДОРОВЬЕ ЖЕНЩИН С ОНКОГЕМАТОЛОГИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ
14.00.01- акушерство и гинекология
А в т о р е ф е р а т
диссертации на соискание ученой степени
доктора медицинских наук
Москва - 2008
Работа выполнена в ФГУ «НЦАГ и П им. В.И. Кулакова Росмедтехнологий» (директор – академик РАМН, профессор Сухих Г.Т.)
Научные консультанты:
| К  улаков Владимир Иванович улаков Владимир Иванович | доктор медицинских наук, профессор, академик РАМН |
| Демина Елена Андреевна | доктор медицинских наук |
Официальные оппоненты:
| Мурашко Людмила Евгеньевна | доктор медицинских наук, профессор |
| Кирющенков Александр Прокофьевич | доктор медицинских наук, профессор |
| Поддубная Ирина Владимировна | доктор медицинских наук, профессор, член корреспондент РАМН |
Ведущая организация:
Российский Университет Дружбы народов
Защита состоится ____________ в _______ часов на заседании диссертационного совета Д. 208.125.01 при ФГУ «НЦАГ и П им. В.И. Кулакова Росмедтехнологий» (Москва, улица академика Опарина, 4)
Автореферат разослан «___» ________ 2008г.
Ученый секретарь диссертационного совета,
Доктор медицинских наук Калинина Е.А.
Список сокращений
| АФС | Антифосфолипидный синдром |
| БГМ | Болезнь гиалиновых мембран |
| ВА | Волчаночный антикоагулянт |
| ВЗРП | Внутриутробная задержка развития плода |
| ИРЛ | Интерфероновая реакция лейкоцитов |
| ИФН- | Интерферон-альфа |
| КОК | Комбинированные оральные контрацептивы |
| ЛПЗ | Лимфопролиферативные заболевания |
| ЛТ | Лучевая терапия |
| ЛХ | Лимфома Ходжкина |
| ОРВИ | Острые респираторно-вирусные заболевания |
| МПКТ | Минеральная плотность костной ткани |
| МТГФР | Метилентетрогидрофолатредуктаза |
| НХЛ | Неходжкинская лимфома |
| ПХТ | Полихимиотерапия |
| РДС | Респираторный дистресс-синдром |
| ХМПЗ | Хронические миелопролиферативные заболевания |
| ЭКО и ПЭ | Экстракорпоральное оплодотворение и перенос эмбриона |
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Гемобластозы являются довольно распространенными онкологическими заболеваниями среди женщин репродуктивного возраста, из них лимфома Ходжкина – самое часто встречающееся онкологическое заболевание среди женщин в возрасте от 15 до 24 лет [Glaser S.L., 1994]. В последние годы появились эпидемиологические данные, свидетельствующие как об истинном увеличении распространенности гемобластозов, так и увеличении когорты молодых женщин, у которых современная специфическая терапия приводит к излечению от заболевания. Увеличение числа молодых женщин, излечившихся от гемобластоза, делает актуальной проблему реализации у них репродуктивной функции и повышения качества их жизни.
Проблема сохранения беременности у онкологических больных до сих пор остается дискуссионной. В отечественной литературе существует догма, что если во время беременности диагностируется онкогематологическое заболевание (лимфома Ходжкина, неходжкинские лимфомы, лейкоз и др.), то необходимо экстренное прерывание беременности [Неупокоева И.А., 1995; Шехтман М.М. 1999]. Появление же в последние годы новых программ лечения, включающих препараты, не проникающие через плаценту, потребовали пересмотра этого мнения. Как показал опыт зарубежных клиник, использование противоопухолевого лечения возможно во II и III триместрах, когда уже произошла закладка всех органов плода.
Одним из побудительных мотивов для начала данной научной работы явилось изучение функциональных систем у беременных при гемобластозах с различной активностью и агрессивностью, а также длительностью ремиссии заболевания. Было проведено сопоставление состояния иммунитета, интерферонового статуса с частотой вирусных и бактериальных заболеваний во время беременности при лимфопролиферативных заболеваниях (лимфома Ходжкина, неходжкинская лимфома).
Для другой группы гемобластозов - хронических миелопролиферативных заболеваний характерным является склонность к тромбогеморрагическим осложнениям и нарушениям микроциркуляции, что существенно снижает выживаемость и качество жизни этих больных. До появления новых препаратов и разработки современных подходов к лечению этих заболеваний неблагоприятные исходы беременности наблюдались в 50-60% случаев. Поэтому, в основном, в данной группе изучались особенности нарушения гемостаза, наличие дополнительных факторов тромбофилии и методы их коррекции.
Высокая токсичность цитостатических препаратов и лучевой терапии приводит не только к излечению, но и к повреждению здоровых органов и тканей. Наиболее чувствительны и подвержены цитотоксическому действию делящиеся клетки, находящиеся в митотическом цикле [Ганцев Ш.Х., 2003], и необратимо в яичниках, где число ооцитов ограничено и определено еще внутриутробно, к тому же эти клетки не могут регенерировать, и таким образом химио- и лучевая терапия может индуцировать овариальную атрофию и аменорею [Apperly JF, et al., 1995; Blumenfeld Z, et al, 1999; Oktay K, et al., 2000]. В связи с этим, в течение многих лет вопрос о способах возможной защиты функции яичников во время проведения противоопухолевого лечения привлекает внимание исследователей. Предварительные результаты применения комбинированных оральных контрацептивов, а также агонистов ГнРГ во время противоопухолевого лечения показали хороший эффект по защите яичников [Blumenfeld Z, et al., 2002]. Однако до сих пор нет исследований, сравнивающих эффективность этих двух методов, не разработаны показания для необходимости криоконсервации ткани яичника и эмбрионов, поэтому актуальным является разработка комплекса реабилитационных мероприятий, предполагающих в перспективе восстановление и реализацию репродуктивной функции.
Цель исследования
Клинико-патогенетическое обоснование тактики ведения беременности и родов, оценка состояния новорожденных, а также оптимизация методов сохранения и восстановления репродуктивной функции у женщин с онкогематологическими заболеваниями.
Задачи исследования
- Проанализировать особенности течения беременности, родов и послеродового периода у женщин с гемобластозами в зависимости от их вида, стадии заболевания, длительности ремиссии. Определить оптимальные сроки наступления беременности после лечения, возможные показания к прерыванию беременности, а также медикаментозную терапию гемобластоза во время беременности.
- Изучить особенности функционирования иммунной и интерфероновой систем у беременных с лимфопролиферативными заболеваниями, частоту вирусных и бактериальных инфекций и оптимизировать методы профилактики и лечения.
- Определить особенности функционирования системы гемостаза, частоту тромбогеморрагических осложнений у беременных с миелопролиферативными заболеваниями и разработать методы их коррекции.
- Изучить влияние полихимиотерапии на минеральную плотность кости у женщин с гемобластозами и определить основные факторы, влияющие на нее.
- Оценить состояние здоровья новорожденных и детей, рожденных матерями с гемобластозами в НЦ АГиП за период 1986-2007гг.
- Определить влияние беременности и родов на течение гемобластоза.
- Сравнить эффективность различных методов защиты яичников (а-ГнРГ или КОК) от повреждающего воздействия химиопрепаратов во время лечения лимфомы Ходжкина.
- Разработать показания для криоконсервации ткани яичника или эмбрионов у женщин с гемобластозами перед лучевой и химиотерапией.
- На основании полученных данных разработать систему по ведению беременности, родов и послеродового периода, а также сохранению и восстановлению репродуктивной функции у женщин с онкогематологическими заболеваниями.
Новизна исследования
Новизна исследования состоит в том, что на большом материале рассмотрены:
- особенности течения беременности, родов и послеродового периода в зависимости от вида гемобластоза, стадии и активности заболевания, а также применение различных схем противоопухолевого лечения во время беременности;
- вопросы влияния самого заболевания и проводимого противоопухолевого лечения на функционирование свертывающей, иммунной, эндокринной и костной систем;
- вопросы влияния как самого заболевания на течение беременности, так и беременности на течение онкологического заболевания, общую выживаемость и частоту рецидивов.
Впервые установлено, что выраженность иммунодефицита у женщин с лимфопролиферативными заболеваниями после противоопухолевого лечения зависит от активности процесса и длительности ремиссии заболевания. При короткой ремиссии заболевания во время беременности наблюдается снижение показателей иммунитета и нарушение интерферонообразования, что приводит к активации вирусных заболеваний у беременных. Изучены механизмы функционирования системы гемостаза во время беременности при миелопролиферативных заболеваниях, проанализирована частота встречаемости дополнительных факторов тромбофилии и на основании этих данных составлен алгоритм лечения и ведения беременности.
Рассмотрены основные аспекты защиты яичников от повреждающего воздействия цитотоксических препаратов и последующего восстановления репродуктивной функции. Изучено защитное действия агонистов ГнРГ и КОК в сохранении функции яичников при воздействии различных схем полихимиотерапии.
Практическая значимость
Разработаны акушерская тактика ведения беременности, родов и послеродового периода и показания к прерыванию беременности при различных видах гемобластозов. В связи с сохраняющимся иммунодефицитом в течение 3-5 лет в зависимости от схем полихимиотерапии, наиболее частой реактивацией вирусной инфекции и ее рецидивированием, а также, учитывая то, что две трети рецидивов лимфом возникают именно в первые 3 года после окончания лечения, оптимальным сроком наступления беременности у женщин с лимфомой Ходжкина и неходжкинскими лимфомами при ремиссии заболевания является период в 3-5 лет после окончания противоопухолевого лечения.
Разработанные алгоритм ведения беременности при миелопролиферативных заболеваниях, схемы лечения (циторедуктивная, антиагрегантная и антикоагулянтная терапия) позволили снизить частоту тромбогеморрагических осложнений и репродуктивных потерь.
Проведена оценка состояния новорожденного с учетом отягощающих факторов: стадия и форма гемобластоза, характер химиотерапии, длительность ремиссии, применение противоопухолевого лечения во время беременнности, состояние функциональных систем во время беременности.
Показано, что в качестве выбора препарата для защиты яичников у женщин с лимфомой Ходжкина в возрасте старше 25 лет при проведении интенсивной полихимиотерапии (по схеме ВЕАСОРР) предпочтение необходимо отдавать агонистам ГнРГ. Дополнительные методы репродуктивных технологий (криоконсервация ткани яичника, эмбриона и т.д.) возможно, а иногда необходимо использовать у женщин с лимфомой Ходжкина старше 30 лет и желающим иметь ребенка.
Положения, выносимые на защиту:
- Во время беременности при лимфопролиферативных заболеваниях (лимфома Ходжкина, неходжкинские лимфомы) в активной фазе болезни или с короткой длительностью ремиссии снижена антивирусная и иммуномодулирующая активность систем иммунитета и интерфернонообразования, что проявляется высокой частотой развития вирусных инфекций.
- Хронические миелопролиферативные заболевания являются причиной специфических изменений гемостаза: гипертромбоцитоза, высокой частоты дополнительных факторов тромбофилии (АФС, гипергомоцистеинемии, наличие мутаций МТГФР, аномалии Лейдена V фактора и протромбина), снижения агрегационной функции тромбоцитов, что вызывает различные осложнения (от кровотечения до тромбозов) и обуславливает репродуктивные потери. Адекватная коррекция данных изменений во время беременности (циторедуктивная, антиагрегантная и антикоагулянтная терапия) позволяет избежать данных осложнений.
- Беременность не влияет на общую выживаемость больных и частоту рецидивов у женщин с лимфомой Ходжкина. Состояние детей у матерей с гемобластозами не отличается от здоровья детей в общей популяции.
- В качестве выбора препарата защиты яичников у женщин с лимфомой Ходжкина в возрасте старше 25 лет при проведении полихимиотерапии по схеме ВЕАСОРР предпочтительнее агонисты ГнРГ. Женщинам старше 30 лет, желающим иметь ребенка, возможно использование дополнительных методов репродуктивных технологий (криоконсервация ткани яичника, эмбриона и т.д.).
Апробация работы
Материалы и основные положения диссертации доложены и обсуждены на XII Российском национальном конгрессе «Человек и лекарство» (Москва, 2005); семинаре «Актуальные вопросы экстрагенитальной патологии в акушерстве и гинекологии» (Москва, 2005); семинаре «Современные технологии родоразрешения» (Москва, 2005); XVI Международной конференции РАРЧ «Вспомогательные репродуктивные технологии сегодня и завтра» (Ростов-на-Дону, 2006); XIV Российском национальном конгрессе «Человек и лекарство» (Москва, 2007); I Международном семинаре «Инфекция в акушерстве и перинатологии» (Москва, 2007), IX Всероссийском научном форуме «Мать и дитя» (Москва, 2007).
Внедрение результатов работы в практику
Практические рекомендации, основанные на результатах исследования, используются в работе акушерских отделений ФГУ «НЦ АГиП им. В.И. Кулакова Росмедтехнологий». По результатам исследования опубликовано 34 научных печатных работы.
Структура и объем диссертации.
Диссертация изложена на 273 страницах машинописного теста и состоит из введения, 7 глав, выводов, практических рекомендаций, списка литературы. Библиография включает в себя 362 источников литературы, в том числе 70 отечественных и 292 зарубежных. Работа иллюстрирована 59 таблицами и 16 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования
С учетом задач исследования проведена оценка влияния специфического лечения гемобластозов на репродуктивную функцию, особенности течения беременности, родов и послеродового периода у 207 женщин с гемобластозами (лимфома Ходжкина, хронические лейкозы, неходжкинские лимфомы) и проанализировано состояние здоровья их новорожденных. Дизайн исследования состоял из двух направлений, которые определили выделение двух основных групп женщин. В 1 группу вошла 131 женщина, перенесшая разные формы гемобластоза. Течение беременности и ее исходы проанализированы у 71 беременной проспективно с 2002 по 2008 годы (1а подгруппа), у 60 – ретроспективно (1б подгруппа) за период 1986-2001 годы. Вторую группу (2 группа) составили 76 пациенток, которым проводилось лечение по программе ВЕАСОРР-стандартный от 4 до 8 циклов. В этой программе суммарная курсовая доза циклофосфана равна или превышает 8гр, и является наиболее токсичной схемой для функции яичников. Из 76 женщин 52 больных (2а подгруппа) с целью защиты яичников получали комбинированные оральные контрацептивы (марвелон непрерывно или циклично, регулон непрерывно на протяжении всего лечения) и 24 пациенток (2б подгруппа) – а-ГнРГ - золадекс (6-8 подкожных введений 1 раз в 28 дней). Период наблюдения за женщинами 2а подгруппы составил с 2000 по 2007 годы, а 2б – с 2004 по 2007 годы. Все пациентки получали противоопухолевое лечение в ГУ РОНЦ им Н.Н. Блохина РАМН.
Специфика онкогематологических заболеваний позволила разделить про- и ретроспективную группы две подгруппы: лимфопролиферативные и миелопролиферативные заболевания. При лимфопролиферативных заболеваниях опухолевой трансформации подвергаются лимфоциты, в функцию которых в норме входит формирование иммунного ответа на внедрившиеся в организм бактерии и вирусы. В связи с этим особое внимание при исследовании уделялось изучению именно функционированию иммунной системы у этих женщин во время беременности. При миелопролиферативных заболеваниях нарушения возникают в миелоидном звене кроветворения, в том числе в тромбоцитарном, поэтому как вне, так и во время беременности наблюдаются именно тромбогеморрагические осложнения. В связи с этим при исследовании пациенток данной группы особое внимание уделялось исследованию сосудисто-тромбоцитарного и плазменного звена гемостаза, а также дополнительных факторов тромбофилии (АФС, гипергомоцистеинемии, наличие мутаций МТГФР, аномалии Лейдена V фактора и протромбина).
1а (проспективную) подгруппу составили 59 (83,1%) беременных с лимфопролиферативными заболеваниями (рис. 1). Из них 50 (84,7%) женщин перенесли лимфому Ходжкина и 9 (15,3%) – неходжкинскую лимфому. В проспективную группу вошли 12 (16,9%) женщин с хроническими миелопролиферативными заболеваниями. В 1б подгруппе распределение по нозологическим формам было идентичным (рис. 1). Преобладание беременных с лимфомой Ходжкина связано с частотой ее встречаемости в репродуктивном возрасте, меньшей агрессивностью заболевания и большей выживаемостью больных.
.
207 женщин с гемобластозами

1 группа - 131 женщина с гемобластозами (беременность)
2 группа - 76 женщин с Лимфомой Ходжкина (репродуктивная функция)


1а проспективная подгруппа (n=71)
1б ретроспективная подгруппа (n=60)
2а защита яичников КОК (n=52)
2б защита яичников аГнРГ (n=24)



МПЗ (n=12)
ЛПЗ (n=53)
МПЗ (n=7)
ЛПЗ (n=59)




Эссенциальная тромбоцитемия – 4;
Сублейкемический миелоз – 2;
Эритремия – 2;
Хронический миелолейкоз - 4
Лимфома Ходжкина – 46;
Неходжкинская лимфома – 7.
Эссенциальная тромбоцитемия – 3;
Сублейкемический миелоз – 1;
Эритремия – 1;
Хронический миелолейкоз - 2
Лимфома Ходжкина – 50;
Неходжкинская лимфома – 9.

Рис. 1. Распределение по группам женщин, вошедших в исследование.
До наступления настоящей беременности лимфому Ходжкина перенесли 42 (84%) и 39 (84,8%) женщин 1а и 1б подгрупп, и у них диагностировалась полная ремиссия заболевания. В про- так и ретроспективном исследовании рецидивы отмечены у 4 и 3 женщин в 1а и 1б подгруппах. В 1а подгруппе у 3-х женщин были поздние рецидивы, причем у двух женщин рецидив наблюдался во время данной беременности, и у одной женщины был один ранний рецидив заболевания. Общая частота рецидивов лимфомы Ходжкина в 1 группе составила 9%, а во время беременности – 3,8%. У 8 (16%) и 7 (15,2%) женщин в 1а и 1б подгруппах лимфома Ходжкина диагностирована во время данной беременности. То есть, всего у 18 (18,7%) беременных (10 и 8 женщин 1а и 1б подгрупп) лимфома Ходжкина была в активной фазе.
У всех больных диагноз лимфомы Ходжкина верифицирован гистологически по биоптату лимфоузла в паталогоанатомическом отделении РОНЦ. Распределение по стадиям и гистологическому варианту лимфомы Ходжкина не отличалось в 1а и 1б подгруппах (рис. 2).
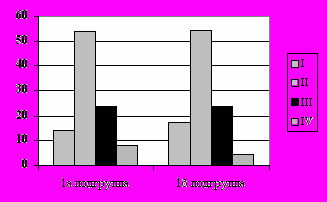
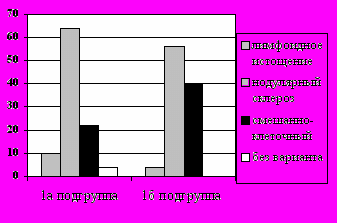
Рис. 2. Распределение больных лимфомой Ходжкина по стадиям и гистологическому варианту.
Противоопухолевое лечение больным с лимфомой Ходжкина проводилось у 42 и 39 женщин в 1а и 1б подгруппах. В основном проводилось комбинированное химио-лучевое лечение у 85,7% и 76,9% женщин 1а и 1б подгрупп, остальным проводилась полихимиотерапия или лучевая терапия. У 8 и 7 беременных женщин в 1а и 1б подгрупп лимфома Ходжкина диагностирована впервые во время данной беременности, и лечение проводилось или во время беременности или после родоразрешения, как и у 3-х женщин с рецидивом заболевания.
До диагностики онкологического заболевания из всей 1-й группы только у 15 (11,5%) женщин были дети, поэтому сохранение беременности было очень необходимо для большинства женщин. Отметим, что у 9 женщин 1 группы было выполнено прерывание беременности в связи с перенесенной лимфомой Ходжкина. У 7 (16,6%) и 5 (12,8%) женщины с лимфомой Ходжкина ретро- и проспективной групп после лечения основного заболевания наблюдалось бесплодие длительностью от 4 до 8 лет.
Встречаемость неходжкинских лимфом в популяции более низкая, чем лимфомы Ходжкина. Вследствие агрессивности течения, а также низкой частоты встречаемости в репродуктивном возрасте, гораздо реже отмечены сочетания различных форм неходжкинской лимфомы с беременностью. Возраст женщин при данном заболевании как в про- так и ретроспективной группе колебался в основном от 23 до 35 лет и в среднем составил 27,6±2,7 года. До заболевания неходжкинской лимфомой в 1 группе первобеременных было 7 женщин, повторнобеременных – 9 женщин, из них 6 – повторнородящие, у 5 женщин были аборты в анамнезе и у одной самопроизвольный выкидыш во время проведения противоопухолевого лечения. После проведенного противоопухолевого лечения неходжкинских лимфом частота абортов внутри 1 группы была одинаковой, производились они только по медицинским показаниям, роды были у 2-х и одной женщины в 1а и 1б подгруппах.
До данной беременности неходжкинскую лимфому перенесли 12 женщин, а о время данной беременности у 4-х женщин 1 группы была диагностирована неходжкинская лимфома. Длительность ремиссии у женщин, перенесших неходжкинскую лимфому, составила от 1 до 15 лет и в среднем равнялась 4,2±2,1 года.
Специфическое противоопухолевое лечение получали все женщины, перенесшие неходжкинскую лимфому до беременности, включающую полихимиотерапию от 4 до 10 курсов, а также 7 женщинам – лучевая терапия, а трем женщинам - оперативное удаление опухоли. Рецидивов опухоли до настоящей беременности не отмечено ни у одной женщины.
Полихимиотерапия и лучевая терапия, как известно, могут вызывать повреждение яичников и с последующим нарушением менструальной функции. Состояние менструальной и репродуктивной функции у женщин 1-й и 2-й групп до заболевания гемобластозом не отличалось от популяционных значений, что позволило оценить влияние противоопухолевого лечения на их функциональное состояние.
О нарушениях менструальной функции после химиотерапии можно говорить только у женщин после менархе, т.к. при проведении ПХТ до менархе ни у одной женщины не отмечено нарушений менструальной функции (рис. 3.).

Рис. 3. Зависимость нарушения функции яичников после ПХТ от возраста
При анализе менструальной функции в исследуемой группе женщин выявлено, что чем старше возраст женщины при проведении ПХТ, тем выше частота нарушений менструального цикла. Нарушения менструального цикла у женщин с лимфомой Ходжкина после ПХТ в нашем исследовании составили 31,2% и 33,3% случаев в возрастной категории 18-25 лет, и значительно выше у 54,5% и 71,4% женщин старше 25 лет соответственно в 1а и 1б подгруппах. Частота и тяжесть нарушения менструального цикла зависели от следующих факторов: возраста женщин, стадии заболевания и, соответственно, применяемых схем ПХТ. Высокая частота этих нарушений делает актуальной проблему защиты яичников у женщин, получавших ПХТ в возрасте старше 18 лет. В 1а подгруппе противоопухолевое лечение получали до беременности 42 женщин с лимфомой Ходжкина и 6 - с неходжкинской лимфомой, в 1б подгруппе - 39 и 6 пациентов соответственно.
Второй подгруппой анализируемых заболеваний были хронические миелопролиферативные заболевания. Следует отметить наибольшую частоту встречаемости хронического миелолейкоза и эссенциальной тромбоцитемии при проспективном исследовании (рис.1.). Возраст женщин при диагностике ХМПЗ как в про- так и ретроспективной подгруппе колебался в широком диапазоне от 18 до 43 лет и в среднем составил 24,4±4,9 и 27,4±5,9 года в 1а и 1б подгруппах соответственно.
При установлении диагноза ХМПЗ у 4 из 8 женщин проспективной подгруппы пальпировалась селезенка на 1-2 см ниже реберной дуги; по данным УЗИ ее размеры превышали норму (50см2) в 1,2-1,5 раза у 6 пациенток. Выраженная спленомегалия (+15 см ниже реберной дуги, по данным УЗИ – 160 см2) и увеличение печени (+4см) были только у одной больной с сублейкимическим миелозом в период развития тромбоза печеночных вен (синдром Бадда-Киари).
В основном миелопролиферативные заболевания диагностировались до беременности. Во время беременности диагностирована эссенциальная тромбоцитемия у двух женщин 1а подгруппы, по одной женщине в 1а и 1б подгруппах - хронический миелолейкоз. Продолжительность от момента диагностики до наступления беременности в 9 из 12 случаев составила 24-72 месяца в 1а подгруппе, в 1б подгруппе 24-48 месяцев. Соответственно лечение женщин с ХМПЗ до беременности проводилось 9 и 6 женщинам проспективной и ретроспективной подгрупп. Всем женщинам проспективной подгруппы с хроническим миелолейкозом до беременности назначался иматиниб (гливек) – ингибитор протеинтирозинкиназы, который отменялся при наступлении беременности, так как имеются данные о возможном его тератогенном воздействии. Одна женщина с хроническим миелолейкозом ретроспективной подгруппы получала гидреа. При диагностике ХМПЗ до беременности 3 женщинам проспективной подгруппы назначались современные препараты рекомбинантного ИФН-a (роферон, интрон А, реаферон) по 9-21млн МЕ в неделю подкожно в течение 14-30 мес, ацетилсалициловую кислоту (тромбоАСС) по 100 мг, а также тиклопидин (тиклид) или клопидогрель (плавикс), или дипиридамол (курантил). Двум больным 1а подгруппы проводили лечение гидроксимочевиной (гидреа) более чем за год до беременности. В ретроспективной подгруппе при диагностике ХМПЗ назначались препараты гидроксимочевины и антиагреганты по показаниям.
В связи с тем, что ХМПЗ характеризуются миелопролиферацией, проявляющейся гипертромбоцитозом, течение беременности очень часто осложняется в связи с тромбозами сосудов плаценты. Это проявилось частым прерыванием предыдущих беременностей у 5(55,6%) и 3 (50%) женщин в 1а и 1б подгруппах соответственно, что связано с отсутствием адекватной циторедуктивной и антиагрегантной терапии. Так, у одной женщины 1б подгруппы наблюдалось 7 самопроизвольных выкидышей. У одной пациентки 1а подгруппы первая беременность была прервана искусственным абортом, завершившимся профузным маточным кровотечением, что послужило причиной гематологического обследования и установления диагноза эссенциальной тромбоцитемии.
Вторым этапом данной работы явилось изучение возможности защиты функции яичников от повреждающего воздействия полихимиотерапии у женщин с лимфомой Ходжкина (рис.1). Средний возраст женщин во 2а и 2б подгруппах составил 24,4±5,6 и 24,7±5,7 лет соответственно. При анализе особенностей менструальной функции у женщин 2 группы с лимфомой Ходжкина до противоопухолевого лечения выявлено, что средней возраст менархе в группе женщин, получавших КОК или аГнРГ, не отличался и составлял 12,7±0,5 и 13,1±0,6 лет соответственно. Анализ не позволил выделить каких-либо других особенностей менструальной функции у женщин исследуемых групп. Так, регулярный менструальный цикл от 27 до 37 дней (в среднем 26,9±1,3 дня) был у 45 (86,5%) и 17(85%) женщин соответственно, получавших КОК и аГнРГ. Меноррагия до лечения наблюдалась у 3-х женщины, получавших КОК и у 1- аГнРГ. Нарушения менструальной функции до противоопухолевого лечения были у 4 и 1 женщин соответственно, получавших КОК и аГнРГ.
Во 2 группе у 58(76,3%) женщин до заболевания лимфомой Ходжкина беременностей не было. У 2-х женщин заболевание возникло во время беременности, которая закончилась преждевременным родоразрешением на 34 неделе в одном случае, и прерыванием беременности по медицинским показаниям во втором случае. У одной женщин после противоопухолевого лечения были одни своевременные роды. Небольшое количество родов после лечения обусловлено малыми сроками наблюдения: максимум 7 лет во 2а и 4 года – во 2б подгруппах. Распределение по стадиям и гистологическому варианту лимфомы Ходжкина не отличалось во 2а и 2б подгруппах (рис.4).
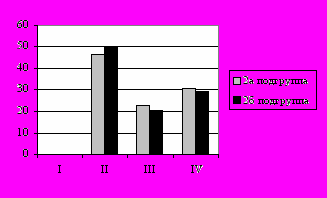
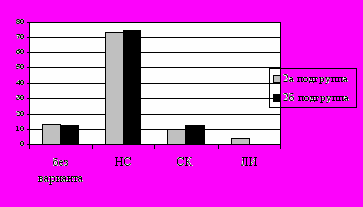
Рис. 4. Распределение больных лимфомой Ходжкина (2 группа) по стадиям и гистологическому варианту
Таким образом, в данной группе были в основном молодые женщины репродуктивного возраста, у 76,3% из них не было детей и был высокий риск повреждения яичников высокими дозами алкилирующих препаратов при лечении лимфомы Ходжкина, что определяло необходимость защиты яичников. Различий в возрасте, стадии заболевания, гистологическом варианте опухоли и программе лечения у женщин, получавших КОК или аГнРГ с целью защиты яичников, не было.
Для изучения особенностей течения беременности в 1а (проспективной) подгруппе использовались следующие методы:
- Исследование состояния иммунной системы, которое включало оценку ее клеточного звена с помощью фенотипического изучения мононуклеарных клеток крови и гуморального звена с помощью определения концентрации основных классов иммуноглобулинов в сыворотке крови. Фенотипический анализ клеточных популяций лейкоцитов периферической крови проводили методом проточной цитометрии на цитофлуориметре “FACScan” фирмы “Becton Dickinson”.Концентрацию иммуноглобулинов трех основных классов (A, M, G) определяли с помощью метода радиальной иммунодиффузии по Манчини с использованием диагностических наборов и аппарата TDx фирмы «Abbott» (США) (лаборатория клинической иммунологии ФГУ НЦ АГиП, руководитель - академик РАМН, профессор Г.Т.Сухих).
- Исследование параметров гемостаза. На автоматическом анализаторе Behring coagulation timer определялись следующие параметры системы гемостаза: концентрация фибриногена, активированное время рекальцификации, активированное частичное тромбопластиновое время, протромбиновый индекс. (лаборатория клинической иммунологии ФГУ НЦ АГиП (руководитель - академик РАМН, профессор Г.Т.Сухих).
- Определение мутаций генов метилентетрогидрофолатредуктазы, аномалии Лейдена V фактора и протромбина, сопряженных с тромбофилией, проводили в лаборатории молекулярной гематологии ГНЦ РАМН (зав.- проф. Судариков А.Б.) методом аллель-специфической полимеразной цепной реакции в оригинальной модификации.
- Ультразвуковое, допплерометрическое исследование во время беременности проводилось на аппарате « B&K 3535» (Дания). Мониторное наблюдение за состоянием плода осуществлялось с использованием антенатальной кардиотокографии, начиная с 34 недель беременности с интервалом в 1-2 недели (по показаниям), при помощи кардиотокографа 8030А фирмы Hewlett Packard и МТ-801 фирмы Toitu (Япония) (лаборатория функциональной диагностики ФГУ НЦ АГиП, руководитель – профессор В.Н.Демидов).
- Микроскопия вагинальных мазков, бактериологические методы, выявление вирусных инфекций методом ПЦР (лаборатория микробиологии ФГУ НЦ АГиП, руководитель – профессор Анкирская А.С.).
- Сразу после рождения оценивалось состояние детей по шкале Апгар, определялись массо-ростовые показатели. В раннем неонатальном периоде изучалось течение адаптационного периода, частота заболеваемости. При оценке показателей физического развития новорожденных пользовались популяционными нормативами, разработанными Г.М.Дементьевой, Е.В.Короткой, 1981; К.М.Сотниковой и соавт., 1985. Критериями задержки развития плода являлось снижение массо-ростовых показателей ниже 10 перцентили для соответствующего гестационного возраста.
- Для оценки состояния костной ткани измеряли ее минеральную плотность методом двухэнергетической рентгеновской абсорбциометрии (ДЭРА) в области поясничного отдела позвоночника (L1-L4) и проксимального отдела левого бедра на рентгеновском костном денситометре «Lunar» (США).
- Диагностика онкологического заболевания во время беременности осуществлялась с помощью следующих методов: трепанобиоптат костного мозга, спонтанное колониеобразования эритроидных клеток – предшественников при культивировании клеток крови и/или костного мозга в метилцеллюлозе (ГУ Гематологический научный центр РАМН, лаб культивирования костного мозга, зав. – проф. Н.И.Дризе); пункция и последующая биопсия лимфатического узла, в сложных случаях с иммунофенотипированием; рентгенография легких – обязательно в прямой и боковой проекциях (во время беременности использовался специальный свинцовый фартук для защиты плода); ультразвуковое исследование всех групп периферических, внутрибрюшных и забрюшинных лимфатических узлов, печени и селезенки, щитовидной железы при больших лимфатических узлах шеи (ГУ РОНЦ им. Н.Н. Блохина РАМН).
Для сравнительной оценки различных методов защиты яичников у пациентов 2 группы применялись следующие методы:
- Определялся уровень ФСГ, ЛГ, Е2, прогестерона, на 5-6 день менструального цикла до и через 6 месяцев после проведения противоопухолевого лечения (ПХТ и ЛТ). Концентрацию гормонов определяли методом иммуноферментного или радиоиммунного анализа с помощью соответствующих тест-систем.
- Ультразвуковое исследование выполнялось до проведения противоопухолевого лечения и через 6 – 12 месяцев после окончания лечения.
- Статистические методы. Полученные числовые результаты обрабатывали методом вариационной статистики. Определяли среднюю величину М, среднеквадратичное отклонение G, ошибку средней m. Определение достоверности различий проводилось с использованием критерия Стьюдента для несвязанных совокупностей. Различие между сравниваемыми величинами считали достоверными при уровне значимости р<0,05. Статистическую обработку полученных данных проводили на компьютере с использованием стандартных программ Windows2000: Microsoft Excel в разделе программы «Анализ данных», подразделение «Описательная статистика» и программы МАТLAB 6,0.
