Клинико-функциональные и метаболические характеристики ишемической болезни сердца у женщин и дифференцированная терапия 14. 00. 06-кардиология
| Вид материала | Автореферат |
- Задачи : Формирование 2-х клинических групп обоего пола: 30 пожилого возраста (65-86, 127.2kb.
- Задачи : Формирование 2-х клинических групп обоего пола: 30 пожилого возраста (65-86, 118.29kb.
- Клинико-генетическое прогнозирование риска развития ишемической болезни сердца 14., 572.45kb.
- Антибактериальная терапия инфекций нижних дыхательных путей в амбулаторных условиях, 123.18kb.
- Клинико-неврологические и нейропсихологические особенности ишемической болезни мозга, 367.52kb.
- Лечение и профилактика наиболее распространенных заболеваний кровообращения: гипертонической, 5.54kb.
- Многоэлементный состав крови у мужчин без и с ишемической болезнью сердца 14. 00., 479.06kb.
- Диагностическое и прогностическое значение уровней рарр-а и маркеров воспаления у больных, 308.52kb.
- «Факторы коронарного ангиогенеза и влияние на них различных методов лечения у больных, 366.72kb.
- Керимович хроническая сердечная недостаточность у больных ишемической болезнью сердца:, 509.58kb.
Таблица 3.
Сывороточные концентрации циклических нуклеотидов, активность ренина и ПНУП
| Симптомы | Контроль-ная группа | Больные ИБС | |||
| Всего | Возрастные группы | ||||
| <45 лет | 45-59 лет | 60 лет и > | |||
| Ренин, нг/мл·час | 1,84±0,12 | 2,61±0,13 *** | 2,37±0,32 | 2,61±0,27 ** | 2,82±0,35 ** |
| ПНУП, пг/мл | 83,2±7,9 | 114,7±4,6 *** | 95,2±11,8 | 113,2±8,0 ** | 132,7±13,6 *** ∆ |
| цАМФ/цГМФ | 2,44±0,14 | 3,04±0,14 ** | 3,45±0,43 * | 3,09±0,31 | 2,66±0,27 |
Примечание: ПНУП – предсердный натрийуретический пептид, цАМФ - 3´-,5´-циклический аденозин-монофосфат, цГМФ - 3´-,5´-циклический гуанозин-монофосфат.
Нами подтверждены описанные ранее (В.П.Сметник, 2006) данные о том, что гормональный профиль у женщин с ИБС характеризуется гипоэстрогенией, гиперпролактинемией, гиперкортизолемией, дисбалансом между ФСГ и ЛГ в сторону преобладания последнего. Наряду с этим обнаружена коморбидная тиреоидная дисфункция: субклинический тиреотоксикоз у больных молодого и среднего возраста, трансформирующийся в субклинический гипотиреоз у пожилых, синдром низкого Т3 у больных преимущественно пожилого возраста с рефрактерной к терапии СК, что, по-видимому, может рассматриваться как компенсаторная реакция, гипоэргоз, приводящий к уменьшению потребности миокарда в кислороде. Установлено, что на фоне прогрессирующей с возрастом распространенности и выраженности гипоэстрогении развивается относительная гиперандрогения. Степень гипоэстрогении у больных ИБС коррелировала с частотой приступов СК ( ), выраженностью эндотелиальной дисфункции ( ), ригидным ритмом сердца ( ), продолжительностью ББИМ по данным СМ-ЭКГ ( ), ФВ (r=0,39, р=0,003) и ОПСС (r=-0,44, р<0,001). Наличие гипоэстрогении у женщин с ИБС сочеталось с более высокой базальной симпатикотонией и с большей степенью нарастания гемодинамического ответа и симпатических влияний на ритм сердца во время выполнения теста с 6-минутной ходьбой. Отношение цАМФ/цГМФ у больных ИБС было достоверно выше, в среднем, на 24,6%, по отношению к аналогичному показателю в контрольной группе, также отражая дисбаланс ВНС в сторону симпатикотонии.
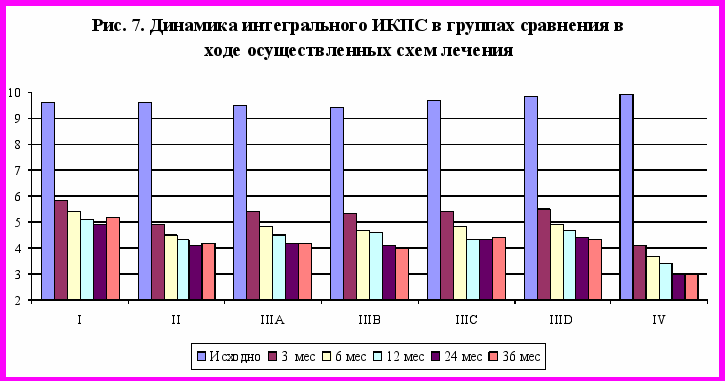
При сравнительной оценке эффективности у больных ИБС женщин длительного применения антагониста кальция ВП, миокардиального цитопротектора ТМЗ-МВ, индивидуализированной ЗГТ - как изолированно в качестве монотерапии, так и в различных комбинациях, во всех группах сравнения зарегистрировано положительное влияние осуществленного лечения на частоту СК, потребность в дополнительном приеме короткодействующих НТ, толерантность к физической нагрузке, выраженность ишемического и сопутствующего аритмического синдромов, по данным СМ-ЭКГ, в результате чего регистрировалось улучшение показателя КЖ по данным SAQ. Параллельно зафиксировано увеличение субъективной толерантности к повседневной физической нагрузке, уменьшение случаев возникновения «стартовой» СК и СК покоя, в результате чего интегральный индекс клинических проявлений стенокардии (ИИКПС) достоверно снизился во всех группах сравнения уже через 3 мес. терапии, сохраняясь в течение всего периода наблюдения на более низких уровнях. Вместе с тем степень снижения (градиент) ИИКПС была различной. В течение первых 3 мес. он снизился в I группе – на 30,2%, II группе – на 33,3%, IIIA группе – на 33,7%, IIIB группе – на 31,9%, IIIC группе – на 37,1%, IIID группе – на 36,6%, IV группе – на 53,5%. При последующем наблюдении максимальная степень снижения ИИКПС в группах сравнения на фоне лечения составила в I - 46,9%, II – 55,2%, IIIA – 52,5%, IIIB – 51,1%, IIIC – 55,7%, IIID – 53,1%, IV – 65,7%. При применении комбинации ВП и ТМЗ-МВ градиент ИИКПС был достоверно более высоким у больных с постинфарктным кардиосклерозом и ожирением (в 1,21 раза у больных с ИМТ≥30 кг/м2 по сравнению с пациентками, имеющими ИМТ≤25 кг/м2, р<0,05). В IIIA и IIIB группах на фоне применения комбинации ВП с препаратами «фемостон 1/5» и «фемостон 2/10» градиент ИИКПС был выше у больных более молодого возраста (в 1,95 раза у больных в возрасте до 50 лет по сравнению с пациентками в возрасте 60 лет и старше, р<0,05), в перименопаузе, с большей выраженностью КС (в 2,04 раза у больных при ММИ более 40 баллов по сравнению с больными, имеющими ММИ менее 20 баллов, р<0,01), с малоизмененными КА по данным КАГ (в 1,73 раза при стенозе ≤50% по сравнению со стенозами ≥75%, р<0,05). В IIIC группе, у перенесших гистерэктомию, на фоне комбинации ВП с 17-эстрадиолом в дозе 2 мг/сут градиент ИИКПС был более высоким при меньшем сроке, прошедшем после операции (в 2,09 раза у больных со сроком после операции до 1 года по сравнению с больными, у которых после операции прошло более 3 лет, р<0,02). В IIID группе, на фоне использования комбинации ВП с трансдермальным 17-эстрадиолом, более высокий градиент ИИКПС отмечен у больных со II ФК СК (в 1,38 раз по сравнению с больными, имеющими III ФК СК, р<0,05). В IV группе на фоне комбинации ВП, ТМЗ и препарата «фемостон 1/5» большие значения градиента ИИКПС регистрировались у больных молодого и среднего возраста (в 1,42 раза по сравнению с пожилыми, р<0,01) с меньшим «стажем» ИБС (в 1,38 раза при стаже до 24 мес, по сравнению со стажем более 48 мес, р<0,05), малоизмененными КА (в 1,58 раза при стенозе ≤50% по сравнению со стенозами ≥75%, р<0,05)
Полный антиангинальный эффект монотерапии ВП через 3 мес. лечения регистрировался лишь у 12,9% больных и оставался неизменным в течение всего периода наблюдения, составляя через 12 мес. 14,4%. Частичный эффект отмечен в указанные сроки у 67,1% и 65,7% больных. Отсутствие эффекта и учащение СК на фоне монотерапии ВП в аналогичные сроки регистрировалось у 20,0% и 18,7% соответственно.














































































П







 римечание: здесь и далее - достоверность различий между показателями внутри групп по сравнению с исходными значениями при р<0,001; - достоверность различий между группами по сравнению с контрольной ( - р<0,05, - p<0,01, - p<0,001).
римечание: здесь и далее - достоверность различий между показателями внутри групп по сравнению с исходными значениями при р<0,001; - достоверность различий между группами по сравнению с контрольной ( - р<0,05, - p<0,01, - p<0,001).Включение ТМЗ-МВ в схему комбинированной терапии позволяло повысить антиангинальную и антиишемическую эффективность ВП до 26,7%. Выявлен синергический характер взаимодействия ВП и ТМЗ-МВ у больных стабильной ИБС, у которых отсутствовал клинически явный антиишемический эффект ВП. При наличии антишемического эффекта ВП его комбинированное назначение с ТМЗ-МВ не оказывало значимого аддитивного антиишемического воздействия. Позитивные эффекты ТМЗ-МВ сохранялись во всех возрастных группах, не зависели от длительности и тяжести течения ИБС, а также наличия сопутствующих заболеваний, в то время как ЗГТ была наиболее эффективна у больных более молодого возраста в период менопаузального перехода, ранней постменопаузе, с выраженными климактерическими расстройствами, с малоизмененными КА и относительно сохранной функцией эндотелия. Наиболее высокая степень прироста показателей КЖ определялась у больных, получавших комбинированную терапию, включавшую в качестве одного из компонентов ТМЗ-МВ. В отличие от результатов, полученных в ходе монотерапии ВП и сочетания ВП с ТМЗ-МВ, комбинированная терапия с включением средних доз эстрогенных и эстроген-гестагенных препаратов, либо комбинации низкодозированной эстроген-гестагенной ЗГТ с миокардиальной цитопротекцией способствовала формированию позитивной динамики эмоционального статуса больных. Максимально выраженные положительные сдвиги произошли у больных с субклинически выраженной тревогой, что обеспечило нормализацию состояния части больных. ЗГТ и её сочетание с ТМЗ-МВ способствовали уменьшению депрессивной симптоматики у больных ИБС, ассоциирующейся с КС, особенно в период менопаузального перехода.
Включение у женщин в состав антиангинальной терапии ЗГТ, независимо от изученных нами режимов, вызывало высокодоствоверную редукцию КС с более ранним исчезновением нейровегетативных его проявлений. Антиклимактерическая эффективность ЗГТ зависела от режима ЗГТ, тяжести исходных проявлений КС, сопутствующей АГ, МС, функционального состояния печени и фоновой гинекологической патологией, уменьшаясь при трансдермальном пути введения гормонов, избыточной массе тела, АГ, большей длительности постменопаузального периода.
На фоне приема ВП в сроки через 6 мес. отмечена тенденция к уменьшению величин DQTc, сохраняющаяся в течение всего последующего периода наблюдения, что обеспечило редукцию доли больных с DQTc выше пороговых значений. Во II группе на фоне комбинации с ТМЗ-МВ указанный эффект регистрировался в более ранние сроки (через 3 мес.). При добавлении к ВП ЗГТ в IIIA, IIIB, IIIC, IIID и IV группах уменьшения DQTc не регистрировалось. Более того, через 3 мес. терапии в IIIA, IIIB, IIIC и IV группах на фоне пероральной ЗГТ, независимо от её состава и дозировки, отмечались достоверно более высокие (р<0,05), по отношению к I группе, значения DQTc, сохраняющиеся в течение всего периода наблюдения. Аналогичные изменения DQTc в IIID группе на фоне трансдермальной ЗГТ регистрировались через 6 мес. Таким образом, курсовая терапия ВП, независимо от его















































































































лекарственной формы, у больных ИБС женщин обеспечила определенное уменьшение DQTc с редукцией доли больных, имеющих DQTc выше пороговых значений. Добавление ЗГТ, независимо от её состава, дозировки и пути введения, нивелировало вызываемые ВП изменения DQTc и через 3-6 мес. приводило к более высоким значениям указанного показателя, что, с учетом известных данных о том, что увеличение DQTc отражает функциональную негомогенность миокарда и является предиктором фатальных нарушений сердечного ритма и внезапной сердечной смерти, свидетельствует о возможном проаритмогенном эффекте ЗГТ, обусловливая необходимость динамического контроля за DQTc в ходе её применения.
При динамической оценке показателей вариабельности ритма сердца в процессе терапии во всех группах, получавших ВП, отмечено достоверное увеличение квадратного корня дисперсии (SDNN). В случае монотерапии ВП и при комбинации ВП с ТМЗ-МВ этот эффект проявлялся через 6 мес. Прирост SDNN составил 36,4% и 38,7% в I и II группах соответственно (р<0,05). Добавление к ВП ЗГТ ускоряло процесс увеличения SDNN, который регистрировался во всех группах ЗГТ через 3 мес., колеблясь от 35,3% (р<0,05) до 49,5% (р<0,01). Максимальная выраженность увеличения SDNN отмечалась через 12 мес. в IIIB и IV группах, когда значения показателя возрастали соответственно на 71,5% (р<0,001) и 70,1% (р<0,001) по отношению к исходным уровням и появлялись достоверные различия величин по сравнению с контрольной группой. В результате через 12 мес. во всех группах достоверно уменьшились доля женщин, имеющих значения SDNN<50 мс (р<0,05), и доля женщин, имеющих SDNN<100 мс (р<0,01), что может свидетельствовать об улучшении клинического прогноза у женщин, получающих в качестве базисной терапию ВП.
По данным ТШХ, во всех группах сравнения, получавших в составе терапии ВП, в сроки до 3 мес. произошло достоверное возрастание ТФН, степень увеличения которой была более ранней и выраженной при применении комбинации ВП, ТМЗ-МВ и ЗГТ, а также достоверно большее увеличение доли больных с положительным эффектом терапии. Антиишемическое действие ВП у больных с исходно нарушенной толерантностью к глюкозе и повышением базального уровня HbAlc выше 6,5% было достоверно меньше, по сравнению с больными, имеющими нормальную толерантность к глюкозе и соответствующие нормогликемии уровни HbAlc (менее 5,5%). Комбинированная терапия с добавлением к ВП ТМЗ-МВ в дозе 70 мг/сут, либо ЗГТ в виде перорально и трансдермально назначаемого 17-эстрадиола в дозе 1-2 мг/сут, или его комбинации с дидрогестерона в дозе 5-10 мг/сут повышала, по данным ВЭП, толерантность к физической нагрузке, что проявлялось ростом пороговой мощности физической нагрузки (при использовании трансдермальной ЗГТ), или пороговой мощности физической нагрузки и объема выполненной работы – для остальных изучаемых нами комбинаций. Антиишемическая эффективность ТМЗ-МВ была выше у больных с исходной систолической дисфункцией миокарда ЛЖ. Антиишемическое действие ЗГТ отмечалось преимущественно у больных в возрасте до 50 лет со значениями ММИ более 40 баллов, практически отсутствовало у женщин старше 55 лет при значениях указанного показателя менее 25 баллов.
Наиболее высокая антиаритмическая эффективность базисной терапии ВП отмечалась при тахизависимых желудочковых ЭС: параллельно с уменьшением ЧСС отмечалось более значительное уменьшение выраженности ЖЭС, чем у больных с исходной нормокардией. Добавление ТМЗ-МВ усиливало антиаритмическое действие ВП в равной степени как по отношению к НЖЭ, так и по отношению к ЖЭ. Добавление ЗГТ к ВП не изменяло его антиаритмической эффективности.
Монотерапия ВП вызывала снижение сократительной способности миокарда левого желудочка, нивелируемое при добавлении к терапии ТМЗ-МВ или ЗГТ. При учете исходной величины ФВ ЛЖ установлено, что ВП снижал указанный показатель при исходно повышенных значениях, не влиял достоверно при его нормальных значениях и умеренно повышал, либо не изменял, сократимость при исходно сниженной величине ФВ. Положительный инотропный эффект ЗГТ реализовывался с большей скоростью при пероральном применении эстроген-гестагенных препаратов в средних терапевтических дозах, либо при комбинации низкодозированных эстроген-гестагенных лекарственных средств с ТМЗ-МВ. На фоне базисной терапии ВП во всех группах начиная с 3 мес. и до завершения наблюдения регистрировалось высокодостоверное увеличение показателя VЕ/VА, свидетельствуя об улучшении диастолической функции миокарда ЛЖ, которое наблюдалось преимущественно у больных с диастолической дисфункцией ЛЖ нерестриктивного типа. В процессе терапии ВП отмечалась тенденция к уменьшению ИММЛЖ. Пероральная ЗГТ усиливала выраженность указанного эффекта, в результате чего уменьшение ИММЛЖ у принимавших комбинацию ВП с пероральной ЗГТ становилось через 12 мес. достоверным. Трансдермальная ЗГТ не влияла на ИММЛЖ. Во всех группах в контрольные сроки регистрировалось достоверное увеличение прироста диаметра плечевой артерии (∆dПА) при проведении пробы с эндотелийзависимой вазодилатацией (ЭЗВД). Добавление к терапии ТМЗ-МВ не изменяло степень ∆dПА. Добавление к ВП ЗГТ увеличивало ∆dПА в большей степени, чем монотерапия ВП, однако достоверные различия отмечались только в IIIB и IV группах на фоне пероральной ЗГТ. Выраженность положительной динамики ∆dПА на фоне всех использованных режимов ЗГТ имела прямую корреляцию средней силы с исходным состоянием эндотелия – достоверно более высокие показатели достигались у больных с исходно более низкими значениями ЭЗВД. Эффективность ВП от функционального состояния эндотелия не зависела. Терапия ВП и комбинацией ВП с ТМЗ-МВ не вызывала изменений липидного спектра крови и гликемического контроля. Добавление к указанной терапии пероральной ЗГТ, наряду со снижением ХС ЛПНП, ИА и значений HbAlc, повышало ХС ЛПВП и ТГ. Трансдермальная ЗГТ, наряду с позитивным влиянием на уровни ХС ЛПНП, ХС ЛПВП и ИА, не вызывала гипертриглицеридемию.
На фоне терапии ВП в I группе отмечалось недостоверное увеличение значений ПНУП с максимумом к 6 мес., когда его величина возрастала на 8,6% с последующей стабилизацией. Напротив, в IIIB группе на фоне сочетания ВП с пероральной эстроген-гестагенной комбинацией (эстрадиол в дозе 2 мг/сут и дидрогестерон 10 мг/сут) регистрировалось постепенное уменьшение значений ПНУП, достигающее к 12 мес. достоверных различий (-12,5%) по сравнению с исходными показателями. При этом начиная с 3 мес. в течение всего периода наблюдения определялись достоверные различия значений ПНУП по сравнению с контрольной группой на 17,1-21,4%. Во II и IV группах, где в составе комбинированной терапии использовался ТМЗ-МВ, начиная с 3 мес. регистрировалось достоверное снижение ПНУП в каждой группе по отношению к исходным значениям – к 12 мес. на 18,1% (р<0,05) и 19,5% (р<0,01) соответственно, так и по отношению к контрольной группе – на 25,3% (р<0,01) и 28,9% (р<0,001) соответственно. Выявление концентраций ПНУП более 120 пг/мл позволяло идентифицировать больных с бессимптомной левожелудочковой дисфункцией, которым относительно противопоказано применение ВП и отмечается его меньшая антиангинальная активность, но указанное ограничение, по нашим данным, может быть снято при сочетании ВП с ТМЗ-МВ.
При оценке влияния различных схем лечения ИБС у женщин на первичные конечные точки (ИМ и смерть от ИБС) достоверные различия между группами в течение 36 мес. отсутствовали. В IV группе, получавшей комбинированную антиангинальную терапию с добавлением ЗГТ и миокардиальных цитопротекторов, установлено достоверное уменьшение частоты нестабильной СК за 3-летний период, что сопровождалось достоверным снижением количества вызовов специализированных кардиологических бригад скорой медицинской помощи и госпитализаций в связи с обострением ИБС в целом за 3 года, а также проведенных в стационаре койко-дней. Уменьшение количества койко-дней в стационаре отмечалось и в группе, получавшей комбинацию ВП с ТМЗ-МВ.
ВЫВОДЫ
1. ИБС (стабильная СК) у женщин характеризуется выраженной вариабельностью клинических проявлений: высокой распространенностью, особенно у больных молодого и среднего возраста, атипичного ангинозного синдрома, сочетанием СК с кардиалгиями, спонтанными колебаниями толерантности к физической нагрузке, «отсроченной» депрессией сегмента ST при нагрузочных тестах, зависимостью частоты СК от фазы менструального цикла. С увеличением возраста женщины нарастает «метеозависимость» СК, увеличиваются зоны иррадиации боли, частота астматического эквивалента СК, её сочетание с манифестированной общей слабостью, снижается эффективность НТ. Атипичная СК ассоциируется с наличием эпизодов ББИМ, типичная СК в большей мере свидетельствует о наличии изолированной БИМ или её сочетания с ББИМ. В структуре ишемического синдрома эпизоды БИМ составляют 37,7%, ББИМ – 15,0%, их сочетание – 47,3%. Тяжелая форма КС в перименопаузе ассоциируется с более тяжелыми клинико-функциональными проявлениями ИБС. Тяжесть коронарной и хронической сердечной недостаточности у больных стабильной ИБС женщин коррелирует с содержанием в крови предсердного натрийуретического пептида.
2. У женщин, больных стабильной ИБС, выявлена умеренная распространенность (у 50,5% больных) локального гемодинамически значимого стеноза с преимущественной локализацией (у 37,4% больных) в передней межжелудочковой ветви левой КА. Установлены достоверная возрастная прогрессия распространенности и степени стенозирующего коронаросклероза, высокая распространенность диффузного коронаросклероза и феномена замедления коронарного кровотока с медленным заполнением КА контрастом. Определена относительно высокая частота ангиоспазма у больных молодого (14,3%) и среднего (9,5%) возраста и развитие у 11,0% женщин из старшей возрастной группы коллатерального коронарного кровотока по интракоронарным анастомозам.
3. Для больных стабильной ИБС женщин характерны коморбидность коронарной недостаточности и тревожно-депрессивных расстройств, прямая корреляция психоэмоциональных факторов с возрастом, клинико-функциональной тяжестью коронарной недостаточности, частотой ФР и уровнем эстрогенной недостаточности, низкой приверженностью к лечению и КЖ.
4. С возрастом среди причин прекращения физической нагрузки нарастает частота снижения САД и аритмического синдрома, хронотропной и инотропной несостоятельности миокарда, его электрической гетерогенности, случаев неэффективности гемодинамического обеспечения нагрузки, регистрируется «затяжная» относительная гипогликемия. В постнагрузочном периоде у молодых женщин определяется запаздывающая нормализация сегмента ST, в то время как у пожилых зарегистрирована опережающая, по отношению к купированию СК, нормализация сегмента ST.
5. Увеличение временных параметров интервала QT сопровождается нарастанием гетеротопного желудочкового автоматизма. Распространенность и выраженность аритмического синдрома нарастает с увеличением возраста больных, продолжительности и тяжести эстрогенного дефицита, степени стенозирующего поражения КА, систолической и диастолической дисфункции ЛЖ.
6. Клинические характеристики ишемического синдрома коррелируют с увеличением среднесуточных, среднедневных и средненочных значений САД, ДАД и ПАД, среднесуточных и средненочных значений ЧСС и ДП, высокой вариабельностью САД как днем, так и ночью, увеличенной вариабельностью ДАД в ночные часы. В старших возрастных группах достоверно уменьшается число больных с нормальным суточным профилем АД (дипперов). Одновременно увеличиваются (преимущественно в ночные часы) значения ДП, индексы времени и площади как повышенного, так и пониженного САД и ДАД с уменьшением индексов времени нормального САД и более высокие значения величины и скорости утреннего повышения САД. Последнее коррелирует с высокой частотой утренней спазмофилии и стартовой СК. Выявленное увеличение индекса площади гипотонии как для САД (днем), так и ДАД (ночью) у больных среднего и пожилого возраста имеет самостоятельное значение в провокации и усугублении эпизодов ББИМ. У пожилых установлено увеличение продолжительности и выраженности чрезмерного снижения САД (в дневные часы) и ДАД (в ночные часы) с уменьшением среднесуточного нормотензивного периода для САД.
7. У больных стабильной ИБС женщин диастолическая дисфункция ЛЖ встречается в 3,1 раза чаще, чем систолическая. С увеличением возраста, продолжительности и тяжести коронарной недостаточности формируется структурно-геометрическое и функциональное ремоделирование ЛЖ с параллельно протекающими равнозначными процессами дилатации полости ЛЖ и гипертрофии его стенки. Стресс-эхокардиография выявляет прогрессирующее с возрастом снижение толерантности к фармакологической нагрузке в сочетании с уменьшением числа больных, имеющих двухфазную реакцию сократимости миокарда в зонах диссинергии или стойкое повышение локальной сократимости в той же зоне на протяжении всей пробы. У 89,4% больных на фоне сосудистого ремоделирования выявлены признаки ЭД, прямо коррелирующей с овариальной недостаточностью.
8. Атерогенные сдвиги липидного спектра характерны для молодых больных, выраженность последних уменьшается в пожилом возрасте. У больных ИБС регистрируется более высокая скорость нарастания ТГ и более поздняя их элиминация на фоне пролонгированной гиперинсулинемии в ответ на жировую нагрузку, характерны базальная и затяжная глюкозоиндуцированная гиперинсулинемия в сочетании с гипергликемией. Установлено повышение транспортного и запасного фондов железа, железа эритрона, что рассматривается как один из механизмов формирования коронарной ишемии.
9. Для больных ИБС женщин характерными являются гипоэстрогения, гиперпролактинемия, гиперкортизолемия, дисбаланс между ФСГ и ЛГ, тиреоидная дисфункция. На фоне прогрессирующей с возрастом гипоэстрогении определяется относительная гиперандрогения, гипергонадотропный гипогонадизм и синдром субклинического гипотиреоза.
10. Полный антиангинальный и антиишемический эффект монотерапии верапамилом через 12 недель лечения регистрируется у 12,9% больных ИБС, продолжаясь в течение всего 36-месячного периода наблюдения. Частичный эффект зарегистрирован у 67,1% больных. Включение в схему терапии триметазидина-МВ потенцирует антиангинальный эффект верапамила: полное купирование установлено в 26,7% случаев. ЗГТ у женщин с сопутствующим КС усиливает частоту полного антиангинального эффекта до 22,0% случаев. Комбинация верапамила с триметазидином-МВ и ЗГТ демонстрирует более высокую антиангинальную эффективность (38,6%). Наилучший клинический эффект установлен при назначении комбинированной терапии в перименопаузе у больных в возрасте до 50 лет со II ФК СК и ИМТ менее 27 кг/м2, при исходном положительном остром лекарственном тесте с оценкой поток-зависимой дилатации плечевой артерии. У 16,7% женщин аддитивное антиангинальное действие ЗГТ отсутствовало. Наличие в составе комбинированного гормонального препарата прогестагена дидрогестерона не «блокирует» антиангинальный (антиишемический), антиаритмический, антигипертензивный и гиполипидемический эффекты 17β-эстрадиола. Низкодозовая ЗГТ сопоставима по антиангинальной эффективности с применением среднетерапевтических доз овариальных гормонов.
