Молекулярно-генетическая диагностика и дифференцированная терапия гистиоцитарных пролиферативных заболеваний у детей 14. 01. 08 педиатрия 14. 01. 21 гематология и переливание крови
| Вид материала | Автореферат |
СодержаниеДТ-responder, n=12 Трансплантация гемопоэтических стволовых клеток. Острая РТПХ. Хроническая РТПХ. Вторая трансплантация. Выживаемость и анализ летальности. Общий анализ результатов терапии |
- Молекулярно-генетическая природа первичных гемофагоцитарных лимфогистиоцитозов в россии, 381.26kb.
- Аллогенная трансплантация гемопоэтических стволовых клеток в лечении врожденных и приобретенных, 1375.99kb.
- Факторы риска и контроль вирусных инфекций после трансплантации гемопоэтических стволовых, 767.07kb.
- Красняков Владимир Кириллович Совершенствование донорства крови и ее компонентов, 921.41kb.
- Прямое переливание крови (методические рекомендации), 154.15kb.
- Оптимизация инновационных технологий трансфузионного пособия пациентам регионального, 1245.79kb.
- Неопухолевые лимфаденопатии. 14. 00. 29 гематология и переливание крови, 1061.02kb.
- Обеспечение качества получения и клинического применения компонентов крови в субъекте, 404.49kb.
- кальцинированный аортальный стеноз-состояние системного гемостаза и реологических, 538.36kb.
- Иммуногематологическая оценка методов гемокомпонентной терапии у онкологических больных, 340.82kb.
| Таблица 12 ЮММЛ: клинико-генетическое сопоставление | |||||||||||
| | PTPN11, n=13 | CBL, n=5 | RAS, n=9 | PTPN11 vs CBL | PTPN11 vs RAS | CBL vs RAS | |||||
| медиана | разброс | медиана | разброс | медиана | разброс | Mann-Whitney, p = | |||||
| Возраст манифестации, мес | 24 | 1-97 | 8,5 | 5,4-50 | 6,7 | 0,4-13 | 0.6331 | 0.0252 | 0.3856 | ||
| Возраст диагноза, мес | 35 | 2-102 | 13,4 | 11-57 | 10,7 | 1-19 | 0.5028 | 0.0033 | 0.1898 | ||
| Гепатомегалия, см | 5 | 4-8 | 4 | 3-12 | 6 | 3-9 | 0.2067 | 0.9999 | 0.5418 | ||
| Спленомегалия, см | 7,5 | 3-17 | 6 | 4-13 | 5 | 4-12 | 0.4249 | 0.4098 | 0.9999 | ||
| Лейкоциты, х109/л | 42 | 11-107 | 25 | 6,9-41 | 29 | 4-100 | 0.0460 | 0.6164 | 0.6064 | ||
| Моноциты, % | 14 | 1-33 | 19 | 9-29 | 20 | 12-39 | 0.3486 | 0.0325 | 0.5045 | ||
| Моноциты, х109/л | 4,9 | 1-14 | 3,5 | 1,3-12 | 5,9 | 1.6-25 | 0.6218 | 0.5041 | 0.2398 | ||
| Тромбоциты, х109/л | 32 | 4-116 | 37 | 22-150 | 39 | 22-197 | 0.3486 | 0.3850 | 0.9467 | ||
| Бласты, кровь, % | 3 | 0-8 | 1 | 0-18 | 0,5 | 0-2 | 0.3703 | 0.0146 | 0.5752 | ||
| Незрелые гранулоциты, кровь, % | 13 | 2-33 | 9 | 1-27 | 7,5 | 1-33 | 0.2355 | 0.3460 | 0.9414 | ||
| HbF, % | 21 | 3-77 | 5,5 | 2-9 | 4,6 | 1,7-11 | 0.0059 | 0.0008 | 0.7337 | ||
| Бласты, к/м, % | 5,6 | 1-10 | 9,2 | 2,8-18 | 7 | 1-10 | 0.2175 | 0.9201 | 0.3163 | ||
| Моноциты, к/м, % | | | | | | | | | | ||
| ЛДГ, МЕ/л | 811 | 230-1970 | 271 | 234-755 | 383 | 196-644 | 0.1377 | 0.1259 | 0.5273 | ||
| Продолжительность жизни, месяцев | 23 | 3-84 | 17 | 10-39 | 27 | 0,3-75 | 0.8490 | 0.1687 | 0.2222 | ||
| | |||||||||||
| | n | % | n | % | n | % | | | | ||
| Пол, м:ж | 10:3 | 77:23 | 2:3 | 40:60 | 5:4 | 56:44 | 0.2682 | 0.3762 | 1.00 | ||
| Лимфаденопатия | 12 | 92 | 4 | 80 | 9 | 100 | 0,4902 | 1,0 | 0,3571 | ||
| Сыпь | 9 | 69 | 2 | 40 | 3 | 33 | 0,3260 | 0,1920 | 1,0 | ||
| Цитогенетика | 0(6) | 0 | 1(4) | 25 | 1(3) | 33 | 0,4000 | 0,3333 | 1,0 | ||
| Нормобласты, кровь | 10 | 77 | 2 | 40 | 6 | 66 | 0,2682 | 0,6550 | 0,5804 | ||
| ГМ-колонии | 8 | 73 | 1(3) | 33 | 7(8) | 87,5 | 0,5500 | 0,3359 | 0,1515 | ||
| Бласты, кровь | 11 | 85 | 3 | 60 | 5 | 55 | 0,5327 | 0,1778 | 1,0 | ||
| Бласты, км, > 5% | 8 | 62 | 4 | 80 | 4 | 44 | 0,6148 | 0,6656 | 0,3007 | ||
| | |||||||||||
| ДТ | 8 | 62 | 4 | 80 | 6 | 66 | 0,6148 | 1,0 | 1,0 | ||
| ВХТ | 2 | 15 | 1 | 20 | 2 | 22 | 1,0 | 1,0 | 1,0 | ||
| ТГСК | 8 | 62 | 2 | 40 | 3 | 33 | 0,6078 | 0,3870 | 1,0 | ||
| | |||||||||||
– 6, ПО - 3), 8 (47%) пациентов не ответили на терапию. Среди 9 пациентов, ответивших на ВХТ, 3 пациента живы в ППР после ТГСК, 4 умерли, 2 потеряны из- под наблюдения. Среди 8 пациентов, не ответивших на ВХТ, 1 жив после ТГСК, 7 умерли (2 после ТГСК). Десять пациентов получили ВХТ после неудачи ДТ, у 4 (40%) был достигнут ЧО, у 6 (60%) – ПЗ. Среди пациентов с ЧО всем выполнена ТГСК, 2 живы в ППР. Среди пациентов с ПЗ, 2 выполнена ТГСК, оба пациента умерли от прогрессии ЮММЛ. 5-летняя рОВ в группе ВХТ составила 28±11%. Рис. 15
| Таблица 14.ЮММЛ: анализ ответа на дифференцировочную терапию 13-RA и AraC | |||||
| | ДТ-responder, n=12 | ДТ-non-responder, n=15 | Mann-Whitney, p | ||
| Медиана | разброс | медиана | разброс | | |
| Возраст манифестации, месяцев | 6,5 | 1-34 | 11,3 | 4,8-97 | 0,0299 |
| Возраст диагноза, месяцев | 12,8 | 2,9-34 | 19,6 | 7-102 | 0,0318 |
| Интервал манифестация-диагноз, мес | 3,9 | 0-9,7 | 3,5 | 0-48 | 0,9610 |
| Моноциты, % | 16,5 | 5-28 | 19 | 10-49 | 0,0632 |
| Бласты, кровь, % | 0,25 | 0-3,5 | 1 | 0-8 | 0,0474 |
| HbF, % | 6,8 | 1,7-15,3 | 15 | 2,0-48 | 0,0166 |
| Бласты, к/м, % | 7 | 3,5-18 | 3,2 | 0,8-11,4 | 0,0256 |
| рОВ, % ± SE | 75±15 | 9±8 | 0,0005 | ||
| | n | % | n | % | |
| PTPN11 | 1 | 8 | 6 | 40 | 0,0914 |
| RAS | 4 | 33 | 1 | 6,6 | 0,139 |
| CBL | 3 | 25 | 1 | 6 | 0,2940 |
| NF1 | 2 | 8 | 3 | 20 | 1,0 |
| CBL+RAS | 7 | 58 | 2 | 13 | 0,0369 |
| ТГСК | 2 | 16 | 8 | 53 | 0,1071 |
Трансплантация гемопоэтических стволовых клеток. Первичное приживление достигнуто у 13 пациентов. Медиана восстановления нейтрофилов составила 16 (8-32) дней. Четырем пациентам с первичной недостаточностью трансплантата была выполнена вторая трансплантация. Медиана выполнения второй трансплантации составила 128 (54-292) дней. Приживление после второй ТГСК достигнуто у всех пациентов с медианой восстановления гемопоэза 13(12-16) дней. Кумулятивная вероятность первичного приживления составила 76,510%, финального приживления – 100% .
Острая РТПХ. Острая РТПХ II-IV степени развилась после первой трансплантации у 10 (58%) пациентов, III-IV степени – у 3-х (23%) пациентов. У двух пациентов оРТПХ стала основной причиной смерти. Химеризм. Систематический мониторинг гемопоэтического химеризма проводился 13-и пациентам. У 4-х пациентов зарегистрирован смешанный химеризм на сроках 38 (16-116) дней. Во всех случаях была отменена профилактическая ИСТ и выполнена инфузия нативных донорских лимфоцитов (DLI). В результате иммунологического вмешательства у 2-х пациентов зарегистрировано развитие клиники оРПТХ. У одного пациента произошло восстановление полного донорского химеризма, сохранение гематологической ремиссии и формирование экстенсивной хРТПХ. В одном случае достигнуто временное восстановление донорского химеризма и развитие развернутого рецидива через 180 дней от детекции смешанного химеризма. В двух случаях, несмотря на DLI, развился гематологический рецидив.
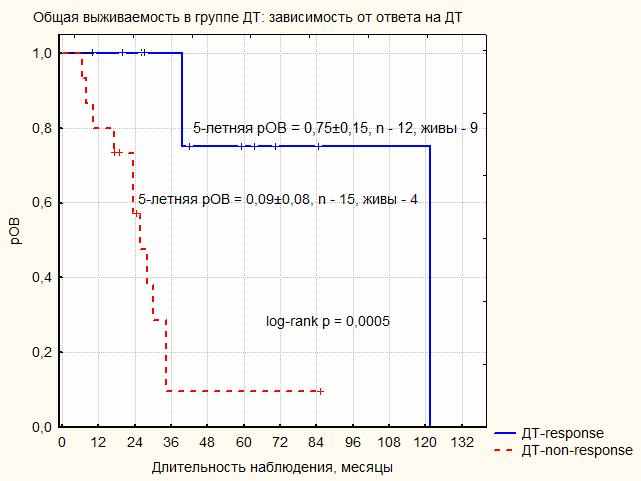 |
| Рисунок 13. Общая выживаемость пациентов с ЮММЛ в зависимости от ответа на дифференцировочную терапию |
Хроническая РТПХ. Диагноз хРТПХ установлен у 4 из 12 пациентов (33%). Экстенсивная форма хРТПХ у 3-х пациентов. У 1 пациента развитие хРТПХ сопровождало DLI. Среди пациентов в продолжающейся ремиссии доля пациентов с хРТПХ составила 57% (4 из 7), среди пациентов с рецидивом – 0% (0 из 5), p = 0,08.
Рецидивы. Гематологический рецидив развился у 5 пациентов. Медиана развития рецидива ЮММЛ составила 49 (46-116) дней от даты первой трансплантации. Безрецидивная выживаемость (рБРВ) составила 66±12%. Три пациента в качестве терапии рецидива получили ТГСК от исходного (n=1) или альтернативного (n=2) донора. Два пациента получали химиотерапию и иммунотерапию (DLI и интерлейкин-2). Все рецидивировавшие пациенты умерли от прогрессии заболевания.
Вторая трансплантация. Шести пациентам была выполнена вторая трансплантация. Четырем пациентам в связи с первичным неприживлением, двум пациентам в связи с рецидивом лейкоза. В 2 случаях трансплантация выполнена от исходного донора. В 4 случаях от альтернативного донора (2 – MUD, 2 - MMRD). В 5 случаях проведено миелоаблативное кондиционирование. Приживление достигнуто у 4 пациентов. Четыре из 6 пациентов умерли от прогрессии заболевания, один от поздней (14 месяцев) ЦМВ-инфекции. Один пациент жив на сроке наблюдения 35 месяцев с экстенсивной хронической РТПХ.
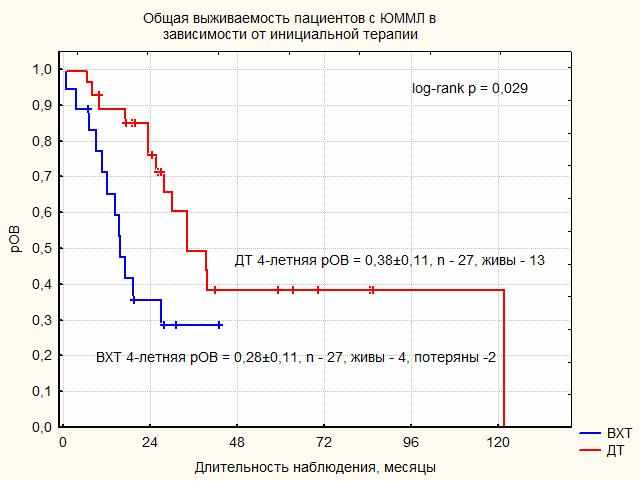 |
| Рисунок 15 Общая выживаемость пациентов с ЮММЛ в зависимости от инициальной терапии |
Выживаемость и анализ летальности. На момент анализа данных живы и находятся в полной клинико-гематологической ремиссии 8 пациентов с медианой наблюдения 31 (3-82) месяц. Четыре пациента умерли от причин, связанных с трансплантацией (1-оРТПХ (день +32), 1-ЦМВ-инфекция/оРТПХ (день+118), 1-ЦМВ-инфекция (день+429), 1-сепсис/полиорганная недостаточность (день+16)). Трансплантационная смертность составила 2812%. Пять пациентов умерли от прогрессии основного заболевания. рОВ составила 3813%, рБСВ составила 4012%.
Общий анализ результатов терапии
Медиана наблюдения 61 пациента с ЮММЛ составила 19,4 месяцев. На момент анализа результатов терапии были живы 20 пациентов, потеряны из под наблюдения 5 пациентов. 5-летняя рОВ составила 28 ± 7%. Рис.16. Анализ выживаемости показал, что, парадоксальным образом, рОВ в группе пациентов, получивших ТГСК, не отличается от рОВ в группе пациентов, которым ТГСК не была выполнена. Рис. 17. Детальный анализ группы пациентов, живущих в статусе ПО или ЧО без ТГСК, показал, что эти пациенты относятся к группе ДТ-R. При исключении этих пациентов из анализа выживаемости очевидным становится преимущество ТГСК в обеспечении длительной выживаемости пациентов с ЮММЛ. Рис. 18
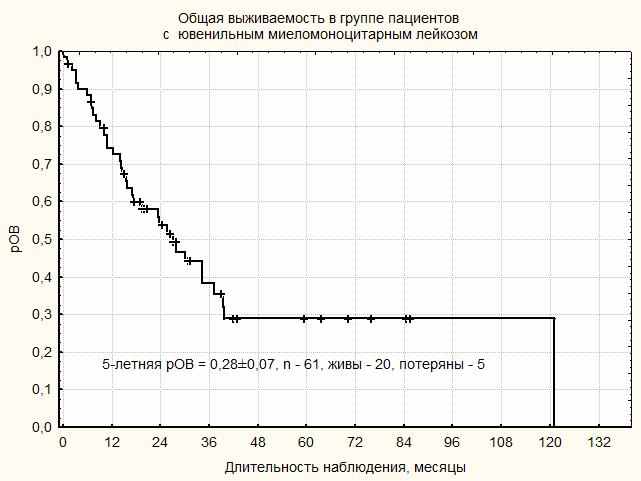 |
| Рисунок 16. Общая выживаемость пациентов с ЮММЛ |
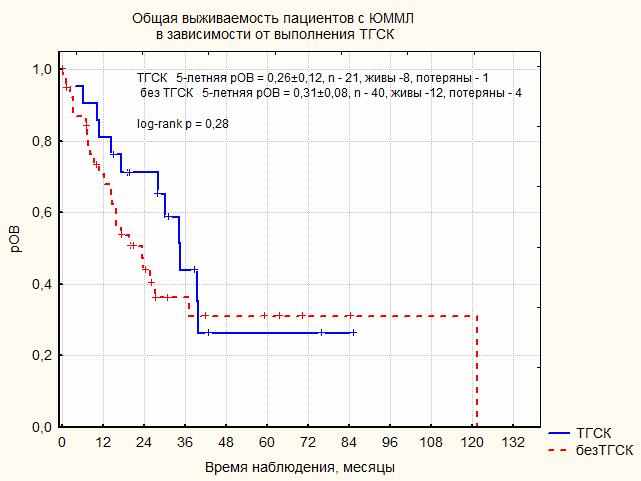 |
| Рисунок 17. Общая выживаемость пациентов с ЮММЛ в зависимости от выполнения ТГСК |
 |
| Рисунок 18. Общая выживаемость пациентов с ЮММЛ в зависимости от выполнения ТГСК (исключая пациентов, ответивших на ДТ) |
