Директор Инженерной Академии Док вет наук, проф. Е. Б. Никитин 2009 г. Автор: преподаватель И. В. Тимофеева Кафедра «Прикладная биотехнология» методические указания
| Вид материала | Методические указания |
- Директор Инженерной Академии Док вет наук, проф. Е. Б. Никитин 2009 г. Автор: преподаватель, 952.2kb.
- Директор Инженерной Академии Док вет наук, проф. Е. Б. Никитин 2009 г. Автор: ст преподаватель, 451.34kb.
- Директор Инженерной Академии Док вет наук, проф. Е. Б. Никитин 200 г. Автор: канд техн, 983.06kb.
- Директор Инженерной Академии д вет н., профессор Е. Б. Никитин " " 2009г. Автор:, 433.94kb.
- Директор Инженерной Академии Докт вет наук, профессор Е. Б. Никитин " " 2009г. Автор:, 1007.64kb.
- Директор Инженерной Академии Никитин Е. Б. " " 2009 г. Автор: ст преподаватель Чернетченко, 370.81kb.
- Директор Инженерной Академии Никитин Е. Б. " " 2009 г. Автор: д т. н.,профессор Никифоров, 453.83kb.
- Директор Инженерной Академии Никитин Е. Б. " " 2009 г. Автор: ст преп., магистр Плевако, 410.07kb.
- Директор Инженерной Академии Никитин Е. Б. " " 2009 г. Автор: ст преп. Харченко, 566.59kb.
- Директор Инженерной Академии Никитин Е. Б. " " 2009 г. Автор: преп. Жумагулов, 428.14kb.
Практическая работа №5
Получение моноклональных антител
Высокая специфичность антител в отношении антигена превращает их в мощный инструмент для идентификации различных веществ, будь то макромолекулы, клеточные фрагменты или целые клетки.
Начало широкому использованию антител в диагностических целях положил в 1955 году американский иммунолог А. Кунс. Он присоединил к антителам светящийся краситель. Флюоресцирующие антитела сделали видимыми места расположения интересующих его молекул в клетке. Этот метод получил название иммунофлюоресцентного. Чувствительность метода можно повысить несколькими путями.
В первом случае иммунный ответ усиливается за счет применения антител нескольких порядков:
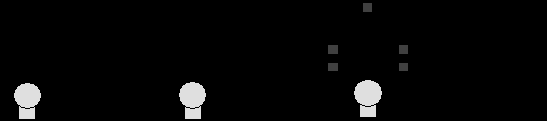
Антиген иммобилизуется на подложке, к нему добавляются антитела 1-го порядка, связывающиеся непосредственно с антигеном. В исследуемый образец добавляются антитела 2-го порядка, связывающиеся с антигенными детерминантами антител 1-го порядка. Антитела 2-го порядка имеют флюоресцирующую (или другую) метку. Поскольку участков связывания может быть несколько, то реакция проявляется более отчетливо.
Другая система усиления сигнала основана на высоком сродстве биотина (низкомолекулярного растворимого витамина) к стрептавидину (бактериальному белку). Здесь возможны два варианта:
А. Если возможно ковалентно связать биотин непосредственно с антителами, то стрептавидин метят маркером и используют аналогично антителам второго порядка:

Б. Система “биотин-антитело + стрептавидин + меченый биотин”:

В этом случае образуется целая сеть из молекул стрептавидина, связанного с меченым биотином. Следовательно, происходит многократное усиление сигнала.
Применение антител второго и третьего порядков позволяет также упрощать процедуру определения микроорганизмов в мазке. При этом не обязательно иметь меченые антитела против всех бактерий. Достаточно иметь обычные антитела кролика или мыши против интересующего микроорганизма и меченые МКА против этих иммуноглобулинов. Если микроорганизм в мазке присутствует, то к нему “приклеятся” специфические антитела, а к ним уже - меченые. В результате мазок будет светится при люминесцентной микроскопии. Фотометрические или флуоресцентные методы могут быть использованы не во всех случаях, например, если измерение про¬водят очень мутной среде.
Кроме красителя в качестве метки можно использовать фермент (иммуноферментный анализ) или радиоактивный изотоп (иммунорадиологический). От чувствительности детекции маркера зависит чувствительность метода анализа.
Радиоактивные метки.
Выбор маркера и способа его «привязки» к антигену является одним из важных этапов в проведении анализа. Первоначально широко применялись радиоизо тонные метки (радиоиммунный анализ - РИА), предложенные амери¬канскими исследователями (С. А. Берсон, Р. С. Ялоу, 1959). Однако в последние годы все более широкое использование в Качестве маркеров находят ферменты. Это обусловлено рядом принципиальных трудностей, связанных с применением изотопныx маркеров. Так, изотоп 125I имеет время полураспада 60 суток, чем ограничивается срок его использования. Изотоп 3Н имеет длительное время жизни (12.5 лет), однако под действием бэта-излучения происходит распад молекул антигена, в результате чего время жизни меченых 3Н-соединений тоже ограничено. Кроме того, эффективность счета трития существенно ниже, чем 125I. Ограничивающими факторами РИА являются сложность и высо¬кая стоимость оборудования, необходимость централизованной системы распределения иммунохимических наборов, меченных радиоактивными изотопами, определенная опасность изотопов для окружающей среды. Учитывая трудности использования ра¬диоизотопных меток, были предложены в качестве маркеров ферменты.
При иммуноферментном анализе антиген связывается с поверхностью лунки полистирольного планшета. В лунку добавляют антитела, несущие фермент в качестве метки, инкубируют и отмывают. Далее приливают субстрат, который меняет окраску при взаимодействии с этим ферментом. Изменение окраски можно измерить с помощью спектрофотометрии. Таким способом проводится индикация и количественная оценка биоорганических соединений с чувствительностью до 10-12 г/литр.
В настоящее время известно более 2000 разных ферментов, однако только некоторые находят применение в иммуноферментном анализе. Это объясняется высокими требованиями, предъявляемыми к свойствам ферментов. Фермент должен быть высоко активен, а продукты его реакции детектироваться с высокой чувствительностью, он должен быть стабилен, так чтобы его активность сохранялась не менее одного года. Содержание фермента-маркера в определяемом образце должно быть минимальным. Именно из-за этого для разных объектов используют разные ферменты. Во многих случаях, когда необходим качественный ре¬зультат, оценка иммунохимической реакции может быть проведена визуально.
Для введения ферментативной метки разработано много разных химических, биохимических и иммунологических способов.
Первым реагентом, использованным для синтеза иммуноферментных конъюгатов, был глутаровый альдегид, реагирующий с аминогруппами лизина белковых молекул. С помощью глутарового альдегида получены конъюгаты антител и антигенов с пероксидазой, щелочной фосфатазой, глюкоамилазой. В настоящее время широко используются иммунопероксидазные конъюгаты и конъюгаты с бэта-галактозидазой.
Ковалентные методы получения иммуноферментных конъюгатов нашли весьма широкое распространение, однако к некоторых случаях действие сшивающего реагента отрицательно сказывается на ферментативной и иммунологической активности компонентов гибридной макромолекулы. В связи с этим определенный интерес представляют иммунологические методы введения ферментной метки.
Один из подходов получил название метода «гибридных антител». Ферментативным гидролизом получают Fab-фрагменты молекул антител против определяемого антигена и используемого фермента. Затем смесь продуктов гидролиза подвергают восстановлению меркаптоэтанодом; при этом Fab-фрагменты обратимо диссоциируют на симметричные части. После удаления восстанавливающего агента молекулы снова ассоциируют, образуя гибридные молекулы антител, специфичные к определяемому антигену и ферменту. При добавлении фермента образуется комплекс антитело—фермент (рис. 19, а). Гибридомная технология открывает принципиально новый путь получения гибридных антител, который заключается в том, что сливаются моноклональные клетки, специфичные против данного антигена и фермента-маркера, в результате чего образуются гибридомы второго поколе¬ния, синтезирующие антитела, с двумя специфичностями.
Другой путь заключается в том, что получают антитела одного и того же вида животного (например, кролика) против определяемого антигена и фермента, которые соединяют между собой через антитела другого вида животных (антитела барана против кролика). Добавление фермента к такой тройной молекуле также приводит к образованию комплекса антитело—фермент. В настоящее время разрабатываются подходы получения гибридных антител методами клеточной и генной инженерии, что позволит существенно упростить способ их получения.
Стабильность иммуноферментных конъюгатов при хранении — важнейший параметр, обусловливающий возможность их практического использования. Методы направленной стабилизации конъюгатов пока еще не разработаны. Не существует также корреляции между стабильностью конъюгатов и методом их получения. Однако высокая стабильность гибридных молекул обеспечивает их применение на практике и значительно превосходит стабильность антител и антигенов, меченных радиоактивными изотопами. В лиофилизованном состоянии ферментные конъюгаты сохраняют свои свойства до двух лет.
Кроме ферментов в качестве маркеров могут быть использованы субстраты. В частности, в иммунокофакторном анализе применяются в качестве меток АТФ и НАД, которые могут быть «пришиты» к молекуле антигена через адениновый остаток таким образом, что сохраняется их способность взаимодействовать с ферментом. Аналогично были использованы субстраты пероксидазы (люминол, изолюминол), которые могут быть окислены пероксидом водорода в реакции хемилюминесценции, катализируемой пероксидазой.
Контрольные вопросы:
- Что такое моноклональные антитела?
- Что представляет собой иммунофлюоресцентный метод получения моноклональных антител.?
- Каким образом можно вызвать усиление сигнала?
- Как действует система «биотин-антитело + стрептавидин + меченый биотин»?
- Какие вещества используют в качестве маркеров при получении моноклональных антител?
Задание для СРСП:
1. Система «антиген-антитело»
2. Получение моноклональных антител.
Задание для СРС:
Оформить результаты практической работы № 5. Ответить на вопросы для самопроверки. Подготовиться к опросу по темам лекции и СРСП. Составить 20 тестовых заданий по темам лекции и практической работы № 5.
Практическая работа № 6
Выделение чистых культур.
Физиологию, биохимические свойства, циклы развития микроорганизмов исследуют, как правило, при работе с чистыми культурами. Чистой, или аксенической, культурой называют такую культуру, которая содержит микроорганизмы одного вида. Умение выделить микроорганизмы одного вида из смешанной популяции, существующей в природе, и поддерживать чистоту культуры — необходимое условие работы с микроорганизмами. Выделение чистой культуры обычно включает три этапа: получение накопительной культуры; выделение чистой культуры; определение чистоты выделенной культуры.
ПОЛУЧЕНИЕ НАКОПИТЕЛЬНОЙ КУЛЬТУРЫ
Накопительной называют такую культуру, в которой преобладают представители одной физиологической группы или даже одного вида микроорганизмов. Метод накопительных культур был введен в практику микробиологических исследований С. Н. Вино-градским и М. Бейеринком. Сущность его заключается в создании элективных, т. е. избирательных условий, которые обеспечивают преимущественное развитие желаемых микроорганизмов или группы микроорганизмов из смешанной популяции.
При создании элективных условий необходимо знать физиологию или четко представлять те особенности, которыми должны обладать выделяемые микроорганизмы. Элективные условия создают чаще всего, подбирая соответствующие среды, поскольку различные микроорганизмы для своего развития предъявляют неодинаковые требования к источникам питания. Например, микроорганизмы, способные фиксировать молекулярный азот, могут расти в среде, из состава которой исключены связанные формы азота. Если внести в такую среду почву, то из громадного разнообразия имеющихся в ней микроорганизмов в первую очередь будут развиваться азотфиксаторы. Накопительные культуры ав-тотрофных микроорганизмов получают на средах, где единственным источником углерода служит углекислота. Отсутствие в среде других соединений углерода задерживает развитие гетеротрофов. Такие специфические питательные среды, удовлетворяющие потребности преимущественно одной группы микроорганизмов, носят название элективных. В зарубежной литературе большее распространение получили термины «накопительные» или «селективные» среды.
Накопительные культуры микроорганизмов, обладающих высокой требовательностью к составу питательных сред, получают иначе. При их выделении используется неодинаковая чувствительность клеток смешанной популяции к продуктам обмена веществ, накапливающимся в среде. Примером могут служить молочнокислые бактерии, для накопления которых используют солодовое сусло без мела, т. е. среду, первоначально не обладающую элективностью. После внесения природного материала, содержащего молочнокислые бактерии, в среде вначале наряду с молочнокислыми бактериями хорошо развиваются представители родов Enterobacter и Escherichia. Однако по мере накопления в среде молочной кислоты и этилового спирта, образуемого гетерофер-ментативными видами, условия для развития энтеробактерий и эшерихий постепенно ухудшаются, тогда как молочнокислые бактерии, которым свойственна высокая кислото- и спиртоустойчи-вость, продолжают расти. Таким образом, в результате развития молочнокислых бактерий среда приобретает необходимую степень элективности, что и обеспечивает получение накопительной культуры этих бактерий. Другим примером могут служить уксуснокислые бактерии, которые характеризуются высокой устойчивостью к этиловому спирту. Накопление этих бактерий осуществляют на сусле, к которому добавляют 4—5% этанола.
Иногда при выделении микроорганизмов из природных популяций в среду включают антибиотики, которые отличаются специфичностью действия и позволяют избирательно подавить рост определенной группы микроорганизмов. Так, элективные условия для развития грамотрицательных бактерий можно создавать внесением в среду пенициллина в концентрации от 0,2 да 100 мг/л, поскольку многие виды грамположительных бактерий при этом или совсем не развиваются, или развиваются медленно. Чтобы создать благоприятные условия для развития бактерий и, напротив, подавить рост мицелиальных грибов, к средам рекомендуют добавлять нистатин в концентрации от 0,1 до 20 мг/л или гризео-фульвин в концентрации от 1 до 20 мг/л.
При создании элективных условий следует учитывать неодинаковое отношение различных микроорганизмов к аэрации, температуре, кислотности среды и т. д. Поэтому при получении накопительной культуры аэробных микроорганизмов обеспечивают большую поверхность контакта среды с воздухом, а для обогащения среды анаэробными микроорганизмами тем или иным способом создают анаэробные условия. Культивирование при высокой температуре (50° и выше) исключает развитие мезофильных микроорганизмов и обеспечивает рост термофилов. Селективным фактором может служить также неодинаковая скорость роста различных микроорганизмов при данной температуре. Например, на минеральной среде при освещении и температуре 35° удается почги полностью подавить рост зеленых водорослей и получить культуру, обогащенную цианобактериями.
При получении накопительных культур следует учитывать и такие особенности микроорганизмов, как способность к образованию эндоспор. Для накопления спорообразующих бактерий среды ино-кулируют, как правило, субстратом, который предварительно пастеризуют, т. е. кратковременно прогревают при высокой температуре (10 мин при 75° или 2—5 мин при 80°). Таким образом можно полностью или почти полностью исключить развитие бактерий, не образующих опоры.
Следует иметь в виду, что элективные условия далеко не всегда оптимальны для роста выделяемых микроорганизмов, однако они лучше переносятся ими, чем сопутствующими формами.
О получении накопительной культуры судят по появлению характерных признаков развития выделяемых микроорганизмов — помутнение среды, иногда сопровождаемое пигментацией, появление пленки, осадка, выделение газов. Помимо визуального наблюдения накопительную культуру микроскодируют и выявляют присутствие желаемых форм. Иногда необходимо определить продукты метаболизма, образование которых свойственно выделяемым микроорганизмам. Например, о развитии нитрифицирующих бактерий свидетельствует появление в среде нитрит- и нитрат-ионов и уменьшение или даже полное исчезновение иона аммония.
Основные условия элективности, позволяющие получить накопительные культуры микроорганизмов с разным типом обмена веществ, суммированы в табл. 9.
ВЫДЕЛЕНИЕ ЧИСТОЙ КУЛЬТУРЫ
После того как получена накопительная, приступают к выделению чистой культуры. Чистая культура может быть получена из отдельной колонии или одной клетки.
Выделение чистой культуры из отдельной колонии
Основным методом выделения чистых культур микроорганизмов является метод, предложенный Р. Кохом. Принцип его заключается в получении чистой культуры из отдельной колонии. Однако этот метод неприменим для выделения микроорганизмов, которые не растут или плохо растут на плотных средах. К числу таких микроорганизмов относятся некоторые бактерии, многие водоросли и простейшие.
При выделении чистой культуры аэробных микроорганизмов накопительную культуру высевают на поверхность плотной среды. Порядок работы следующий. Расплавленную на кипящей водяной бане стерильную питательную среду, содержащую агар или желатину, разливают в стерильные чашки Петри. После того как среда застынет, на ее поверхность из пипетки наносят каплю накопительной культуры или ее разведения в стерильной воде и стерильным стеклянным шпателем Дригальского распределяют каплю сначала по одной половине поверхности среды в чашке Петри,

Рис 1. Рассев культуры микроорганизмов на поверхность плотной среды шпателем:
А — шпатель Дригальского; Б — рассев; В — рост микроорганизмов после рассева
затем по второй половине, после чего этим же шпателем протирают поверхность плотной среды последовательно во 2-й, 3-й и 4-й чашках. Обычно в первых двух чашках после инкубации наблюдают сплошной рост микроорганизмов, тогда как в последующих — изолированные колонии (рис. 1). Рассевать накопительную культуру можно петлей методом истощающего штриха. В этом случае накопительную культуру или ее разведение отбирают петлей и на поверхности .плотной среды проводят штрихи в таком порядке, как указано на рис. 2. Перед каждым новым штрихом петлю стерилизуют в пламени горелки.
После посева чашки помещают в термостат крышками вниз» чтобы конденсационная вода, образовавшаяся на крышке чашки-Петри при застывании агара, не помешала получить изолированные колонии. Чашки выдерживают в термостате в течение 1—7 суток в зависимости от скорости роста микроорганизмов. Выросшие изолированные колонии отсевают петлей на поверхность скошенной плотной среды в пробирки или в жидкую среду.
Рис. 2. Схема рассева культуры микроорганизмов на поверхность-плотной ореды петлей
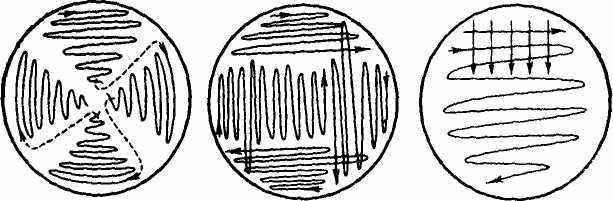
Изолированные колонии аэротолерантных микроорганизмов и факультативных анаэробов чаще получают методом глубинного досева. Для этого плотную питательную среду предварительно разливают в пробирки по 15—20 мл и стерилизуют. Непосредственно перед посевом пробирки помещают в кипящую водяную баню, чтобы среда расплавилась. Высев проводят из разведений накопительной культуры в стерильной водопроводной воде. Разведения готовят с таким расчетом, чтобы при высеве 0,5—1,0 мл разведения получить изолированные колонии. Степень разведения определяется плотностью накопительной культуры. Высевы делают, как правило, из трех-четырех последних разведений. Для этого в пробирку с расплавленной и остуженной до 48—50°агаризованной средой вносят 0,5—1,0 мл одного из разведений накопительной культуры. Посевной материал тщательно перемешивают, вращая пробирку между ладонями. Затем около пламени горелки вынимают из пробирки пробку, обжигая края пробирки в пламени горелки, и быстро выливают содержимое пробирки в чашку Петри. После того как агаризованная среда застынет, чашки Петри помещают в термостат. Колонии, выросшие в /толще среды, вырезают стерильным скальпелем или извлекают стерильными капиллярными трубками или просто петлей и переносят в жидкую среду, благоприятную для развития выделяемых микроорганизмов.
Особые трудности возникают при выделении чистых культур облитатных анаэробов. Если контакт с молекулярным кислородом не вызывает сразу же гибели клеток, то посев проводят на поверхность среды в чашки Петри, но после посева чашки тотчас помещают в анаэростат. Однако чаще пользуются методом разведения. Сущность его заключается в том, что разведения накопительной культуры проводят в расплавленной и охлажденной до 45—50° агаризованной питательной среде. Делают 6—10 последовательных разведений. Затем среду в пробирках быстро охлаждают и заливают поверхность слоем стерильной смеси парафина и вазелинового масла (соотношение 3:1), что препятствует проникновению воздуха в толщу агаризованной среды.
Иногда агаризованную питательную среду после посева и тщательного перемешивания переносят в стерильные трубки Бурри. Можно использовать капиллярные пипетки Пастера, в которые набирают соответствующее разведение накопительной культуры в расплавленной агаризованной питательной среде. Конец капилляра запаивают. При удачно выбранном разведении накопительной культуры в одной из пробирок (пипеток Пастера, трубок Бурри) вырастают изолированные колонии. Чтобы извлечь образовавши-
еся колонии, поступают следующим образом. Удаляют стерильной иглой слой парафина и вазелинового масла, а столбик агаризованной среды осторожно выдувают из пробирки в стерильную чашку Петри, пропуская газ, не содержащий кислорода, через капилляр, который помещают между стенкой пробирки и агаризованной средой. Агаризованную среду из трубки Буррл выдувают, пропуская газ через ватную пробку.
Иногда плотную среду из пробирки извлекают иначе. Пробирку слегка нагревают, все время быстро вращая ее над пламенем горелки. При этом агар, непосредственно прилегающий к стенке, плавится и содержимое пробирки в виде агарового столбика легко выскальзывает в стерильную чашку Петри. Столбик агара разрезают стерильным ланцетом и извлекают колонии, захватывая их стерильными капиллярными трубками или петлей. Можно также вырезать их стерильным ланцетом. Извлеченные колонии переносят в жидкую среду, благоприятную для развития выделяемых микроорганизмов. Если изолированные колонии получены в капилляре, то после тщательной дезинфекции поверхности его разламывают стерильным пинцетом и участки капилляра, содержащие изолированные колонии, переносят в стерильную среду.
Для получения изолированных колоний методом глубинного посева и методом разведений рекомендуется использовать осветленные питательные среды.
Когда хотят получить изолированные колонии облигатных анаэробных бактерий, характеризующихся особенно высокой чувствительностью к кислороду (экстремальные анаэробы)-, используют метод вращающихся пробирок Хангейта. Сущность этого метода заключается в следующем. Расплавленную агаризованную среду засевают бактериями при постоянном токе через пробирку инертного газа, освобожденного от примеси кислорода. Затем пробирку закрывают резиновой пробкой и помещают горизонтально в зажим, вращающий пробирку. Агаризованная среда при этом равномерно распределяется по стенкам пробирки и застывает тонким слоем. Применение тонкого слоя агаризованной среды в пробирке, заполненной газовой смесью, позволяет получить изолированные колонии, хорошо видимые невооруженным глазом (рис. 42).
В некоторых случаях бывает достаточно одного посева в плотную среду, чтобы получить чистую культуру. Однако чаще посев в плотную питательную среду повторяют 2—3 раза. В качестве посевного материала при этом используют культуру, полученную из отдельной колонии.
Выделение чистой культуры из одной клетки
Чистую культуру из одной клетки можно выделить капельным методом, с помощью микроманипулятора или микроселектора.
Капельный метод Линднера используют при работе с крупными микроорганизмами: дрожжами, мицелиальными грибами, водорослями. Порядок работы следующий. Накопительную культуру разводят в стерильной среде с таким расчетом, чтобы в небольшой капле были одиночные клетки микроорганизмов. Затем на поверхность стерильного покровного стекла стерильным стальным пером наносят ряд капель приготовленного разведения. Готовят препарат «висячая капля». Нанесенные на покровное стекло капли просматривают под микроскопом и отмечают те, в которых обнаружена только одна клетка. После этого препарат помещают в термостат во влажную камеру, которой обычно служит чашка Петри с увлажненной фильтровальной бумагой на дне. Через. 12—24 ч отмеченные капли вновь микроскопируют. Те капли, в. которых наблюдается образование микроколоний, осторожно снимают с покровного стекла кусочками стерильной фильтровальной бумаги и переносят в пробирки со стерильной средой.
Выделение отдельных клеток с помощью микроманипулятора-Микроманипулятор — прибор, позволяющий с помощью специальной микропипетки или микропетли извлекать одну клетку и» суспензии. Эту операцию контролируют под микроскопом. Микроманипулятор имеет два операционных штатива, между которыми расположен обычный микроскоп. На предметном столике микроскопа установлена влажная камера, в которую помещают препарат «висячая капля». В держателях операционных штативов закреплены микропипетки (микропетли), перемещение которых в поле зрения микроскопа осуществляется с микронной точностью благодаря системе винтов и рычагов. Микропипетки вводят во-влажную камеру таким образом, чтобы их концы оказались в висячей капле. Исследователь, глядя в микроскоп, извлекает отдельные клетки микропипетками и переносит их в пробирки со» стерильной жидкой средой.
Выделение отдельных клеток с помощью микроселектора Перфильева. Наиболее существенной частью микроселектора Перфильева является стеклянный микрокапилляр, имеющий строга прямоугольное сечение. Благодаря этому канал капилляра хорошо просматривается даже с иммерсионным объективом. Стерильный капилляр заполняют исследуемой суспензией клеток в агари-зованной питательной среде и при большом увеличении микроскопа находят участок с одной клеткой. Специальным приспособлением этот участок капилляра стерильно выбивают в приемник, и* которого затем переносят в стерильную среду. Микроселектор Перфильева можно использовать для выделения как крупных, так и мелких микроорганизмов.
ОПРЕДЕЛЕНИЕ ЧИСТОТЫ ВЫДЕЛЕННОЙ КУЛЬТУРЫ
Чистота выделенной культуры микроорганизмов должна быть тщательно проверена. Это осуществляется обычно несколькими способами: визуальным, микроскопическим контролем и высевом на ряд питательных сред. При визуальном контроле просматривается рост микроорганизмов по штриху на поверхности скошенной агаризованной среды. Если рост по штриху неоднороден, культура загрязнена. Такой контроль возможен только для культур, способных расти на поверхности плотных сред.
Чистоту культур микроорганизмов обязательно нужно контролировать под микроскопом. Для этого следует приготовить препарат фиксированных окрашенных клеток и просмотреть его с иммерсионной системой или препарат живых клеток и просмотреть его, используя фазово-контрастное устройство. Чистая культура многих микроорганизмов, как правило, морфологически однородна; допустимо лишь незначительное варьирование размеров клеток. Однако необходимо помнить, что клетки некоторых бактерий, например, микобактерий, нокардий и др., очень полиморфны, поэтому определение чистоты таких культур при микроскопировании вызывает некоторые затруднения. Чистоту культур микроорганизмов обязательно проверяют высевом на питательные среды. Прежде всего выделенную культуру высевают на питательную среду, благоприятную для ее роста. Однородность выросших колоний — свидетельство чистоты культуры. Обязателен посев на мясо-пеп-тонный агар — среду, которая обеспечивает рост многих хемоге-теротрофов. Критерием чистоты культуры является однородность выросших колоний или отсутствие роста, если данные микроорганизмы на мясо-пептонном агаре не развиваются. Следует иметь в виду, что заключение о чистоте некоторых культур микроорганизмов нельзя сделать только по результатам высева на МПА. Особенно это касается автотрофных микроорганизмов, а также представителей гетеротрофов, склонных развиваться с одним или несколькими спутниками. Чистоту таких культур микроорганизмов проверяют высевом еще на ряд сред — сусло, мясо-пептон-ный бульон, картофельный агар и др. Набор сред и их состав определяются особенностями метаболизма выделенных микроорганизмов, а также их возможных спутников.
Контрольные вопросы:
- Какую культуру можно считать чистой?
- Что такое накопительная культура?
- Каковы условия получения накопительной культуры?
- Каковы особенности выделения чистой культуры из отдельной колонии?
- Каковы особенности выделения чистой культуры из отдельной клетки?
Задания для СРСП:
- Выделение чистой культуры.
- Определение чистоты культуры.
Задание для СРС:
Оформить результаты практической работы № 6. Ответить на вопросы для самопроверки. Подготовиться к опросу по темам лекции и СРСП. Составить 30 тестовых заданий по темам лекции и практической работы № 6.
