Рекомендації, Павленко В. В, учитель хімії зош №28, Рибіна С. Ф., учитель хімії Миколаївської гімназії №2
| Вид материала | Урок |
СодержаниеТип уроку |
- Відділ освіти Овруцької райдержадміністрації Овруцька загальноосвітня школа №3 Позакласна, 579.77kb.
- Клас хімії при Розсошенській гімназії, 7.3kb.
- Опис досвіду вчителя хімії зош і–ііі ступенів с. Павлівка Іваничівського району Волинської, 121.4kb.
- Методичні рекомендації щодо вивчення хімії у 2011 2012 навчальному році Олена Бобкова, 178.03kb.
- Горького Кафедра фармацевтичної та токсикологічної хімії методичні вказівки для студентів, 2971.74kb.
- Кафедра фармацевтичної та токсикологічної хімії методичні вказівки для студентів, 2193.23kb.
- Методичні рекомендації до технології розвитку креативного мислення при вивченні хімії, 313.08kb.
- Програма комплексного фахового екзамену з хімії для вступу на навчання для здобуття, 189.84kb.
- V всеукраїнський фестиваль науки Вчені нту «хпі» Міжнародному року хімії, 118.36kb.
- Про організацію навчально-виховного процесу з хімії в загальноосвітніх навчальних закладах, 110.65kb.
Мета уроку: - вивчити фізичні і хімічні властивості сульфатної кислоти;
- навчити розпізнавати за специфічними властивостями розбавлену і концентровану сульфатну кислоту;
- закріпити знання про ряд активності металів;
- розвивати в учнів креативні здібності, логічне мислення, пам’ять, уміння робити узагальнення і висновки;
- виховувати зацікавленість предметом, старанність та наполегливість.
Тип уроку: Урок засвоєння знань
Форми роботи: Індивідуальна, групова, фронтальна
Обладнання: Сульфатна кислота розбавлена і концентрована, індикатор метиловий оранжевий, вапняк, порошок магнію, мідна проволока, сахароза, пробірки, штатив; таблиця «Розчинність кислот, солей, основ у воді», періодична система елементів, мультимедійна система
Хід уроку
І. Організаційний момент
ІІ. Актуалізація опорних знань. Мотивація навчальної діяльності, повідомлення теми й мети уроку.
1 учень (біля дошки виконує завдання)
Установити відповідність:
N
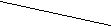
 2O5 H2CO 3 N2O5 H2CO3
2O5 H2CO 3 N2O5 H2CO3 SO2 HNO3 SO2 HNO3
SO2 HNO3 SO2 HNO3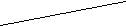 CO2 H2SO4 CO2 H2SO4
CO2 H2SO4 CO2 H2SO4SO3 H2SO3 SO5 H2SO3
2 учень: Дає характеристику Сульфуру за місцем у періодичній системі.
3 учень: біля дошки здійснює хімічні перетворення:
F



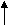 eS2 SO2 SO3 H2 SO4
eS2 SO2 SO3 H2 SO44

 FeS2 + 11O2 2Fe2O3 8SO2
FeS2 + 11O2 2Fe2O3 8SO22
 SO2 + O2 2SO3
SO2 + O2 2SO3S
 O3 + H2O 2H2SO4
O3 + H2O 2H2SO4Декілька учнів працюють за картками (кожна правильна відповідь – 1 бал)
І рівень (слабкі учні) – 6 балів
Закінчити рівняння реакцій, дати назви сполукам, що утворились:
S

 O + H2O SO + H2O H2SO3 – сульфітна кислота
O + H2O SO + H2O H2SO3 – сульфітна кислотаN

 2O5 + H2O N2O5 + H2O 2HNO3 – нітратна кислота
2O5 + H2O N2O5 + H2O 2HNO3 – нітратна кислотаC

 O2 + H2O CO2 + H2O H2CO3 – карбонатна кислота
O2 + H2O CO2 + H2O H2CO3 – карбонатна кислотаІІ рівень (достатній) – 9 балів
З яким із запропонованих речовин реагує сульфур (VІ) оксид:
H2O; Ca(OH)2; Mg; NaCl; Fe(OH)2; HCl AgNO3
- Записати рівняння можливих реакцій:
H
 2O + SO3 H2SO4 m (H2SO4) – 122,5
2O + SO3 H2SO4 m (H2SO4) – 122,5 C
 a(OH)2 + SO3 CaSO4 + H2O m (CaSO4) – 170 m(H2O) – 22,5
a(OH)2 + SO3 CaSO4 + H2O m (CaSO4) – 170 m(H2O) – 22,5F
 e(OH)2 + SO3 FeSO4 + H2O m (FeSO4) – 190 m(H2O) – 22,5
e(OH)2 + SO3 FeSO4 + H2O m (FeSO4) – 190 m(H2O) – 22,5Для будь – якої реакції розрахуйте маси речовин, що утворяться в результаті змішування двох реагентів, якщо маса сульфур (VІ) оксиду 100 г (6 балів)
ІІІ рівень (високий) – 12 балів
Скласти рівняння реакцій за схемою:
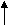 NaSO4
NaSO4


 S SO2 SO3 H2SO4 CuSO4
S SO2 SO3 H2SO4 CuSO4
H2
 S + O2 SO2
S + O2 SO2 2SO2 + O2 2SO3
2SO2 + O2 2SO3 SO3 + H2O H2SO4
SO3 + H2O H2SO4 H2SO4 + 2NaOН Na2SO4 + 2H2O
H2SO4 + 2NaOН Na2SO4 + 2H2O H2SO4 + Mg MgSO4 + H2
H2SO4 + Mg MgSO4 + H2 H2SO4 + CuO CuSO4 + H2O
H2SO4 + CuO CuSO4 + H2OРозрахувати масу сульфур (VІ) оксиду, яку отримали з 50 л сульфур (ІV) оксиду, якщо вихід продукту - 90% (6 - балів)
50 л

 2SO2 + O2 2SO3
2SO2 + O2 2SO3 2 * 22,4 л/моль 2 * 80 г/моль
2 * 22,4 л/моль 2 * 80 г/мольх = 50 л х 160 г/моль = 178,5 г х = 178,5 х 0,9 = 160 г
 44,8 л/моль
44,8 л/моль Відповідь: 160 г SO3
ІІІ. Вивчення нового матеріалу
Учитель: Темою вивчення сьогоднішнього уроку є сульфатна кислота. Вона являється важливим продуктом хімічної промисловості, що виробляє неорганічні кислоти, луги, солі, мінеральні добрива. За різноманітністю застосування сульфатна кислота посідає перше місце серед кислот, вона застосовується майже в усіх галузях виробництва.
Деякі учні на минулих уроках отримали випереджувальне домашнє завдання – створити проекти для мультимедійної установки з теми «Сірчана кислота». Підсумки цієї роботи ми підіб’ємо у вигляді презентації цих проектів за планом:
- Сульфатна кислота. Фізичні властивості.
- Хімічні властивості сульфатної кислоти.
- Одержання сульфатної кислоти.
- Застосування сульфатної кислоти та сульфатів.
Повідомлення 1. Сульфатна кислота. Фізичні властивості.
Повідомлення 2. Хімічні властивості сульфатної кислоти.
І. Розбавлена кислота: а) дисоціація відбувається ступінчасто;
б) взаємодія з оксидами металів;
в) взаємодія з гідроксидами (основами);
г) взаємодія з солями;
д) взаємодія з металами.
Інструктаж з техніки безпеки під час роботи з кислотами.
Демонстрація «Хімічні властивості розведеного розчину сульфатного кислоти»:
- дія на індикатори;
- взаємодія з магнієм, ферумом;
- взаємодія з основами;
- взаємодія з солями.
-
ІІ. Концентрована кислота (специфічні властивості) взаємодіє:
- з малоактивними металами;
- з неметалами;
- з цукром;
- якісна реакція на сульфат-іон.
-
Демонстрація «Взаємодія концентрованої сульфатної кислоти з міддю».
Повідомлення 3. Одержання сульфатної кислоти.
Повідомлення 4. Застосування сульфатної кислоти та сульфатів.
ІV. Закріплення вивченого матеріалу (фронтальне опитування).
- Назвіть природні сполуки, що містять Сульфур (природна сірка, сірчаний колчедан, сірководень).
- Що собою являє олеум? (Розчин сульфур оксиду в концентрованій кислоті)
- Чим концентрована сульфатна кислота відрізняється від розбавленої? (Хімічними специфічними властивостями)
- Які правила техніки безпеки треба дотримуватись, розчиняючи концентровану сульфатну кислоту? (Кислоту доливати у воду).
- У цистернах з яких металів можна транспортувати концентровану сульфатну кислоту? (Сплави заліза (стальні), свинцеві).
- Чому саме ці цистерни не можна використовувати для перевезення розчиненої сульфатної кислоти? (розведена сульфатна кислота взаємодіє з металами, що в ряді напруг стоять до Гідрогену).
V. Підсумки уроку. Релаксація.
Вчитель: Прошу закрити очі, згадати моменти уроку і відповісти на питання:
- Що нового дізнались на уроці?
- Що було незрозумілим?
- Який етап уроку найбільше запам’ятався?
Вчитель оголошує і коментує рівень компетентності учнів. Комплексна оцінка виставляється після перевірки самостійної роботи.
VІ. Домашнє завдання.
Вивчити § 9. Виконати завдання: І рівень – 1, ІІ рівень – 3, ІІІ рівень -4*
Павленко В.В,
учитель хімії
Миколаївської загальноосвітньої
школи І-ІІІ ступенів №50
Рибіна С.Ф.
учитель хімії
Миколаївської гімназії №2
Компетентнісний підхід при викладанні хімії
/особливості практичних питань конкретного змісту/
рекомендації
Згідно з програмою з хімії для загальноосвітніх навчальних закладів Міністерства Освіти і Науки України, метою навчання хімії є формування засобами навчального предмета ключових компетентностей учнів, необхідних для соціалізації, творчої самореалізації особистості, розуміння природничо-наукової картини світу, вироблення екологічного стилю мислення і поведінки та виховання громадянина демократичного суспільства.
Після вивчення пропедевтичного інтегрованого курсу «Природознавство» в якому учні повинні одержати мінімум знань про речовини та хімічні явища, перед вчителем хімії постає завдання знайти такі форми і методи, які б дали змогу на етапі основної школи здобути базові знання з хімії.
Компетентнісний підхід є необхідним в умовах сьогодення для успішного досягнення цілей в реальних життєвих ситуаціях. Виходячи із структури уроку можливе на кожному із етапів формування різних видів компетентностей.
За одним із означень, поняття компетентність визначається, як спроможність кваліфіковано проводити діяльність, виконувати завдання або роботу. Це поняття вміщує певний набір знань, навиків і ставлень, що дають змогу ефективно працювати в певній галузі, як здатність застосовувати знання та вміння. Зміст освіти повинен передбачати досвід здійснення відомих способів діяльності, що втілюється разом із знаннями в уміннях і навиках, досвід творчої, пошукової діяльності з розв'язанням нових проблем, перетворенням раніше засвоєних знань у нові способи діяльності. У структурі освіти чільне місце повинен посідати досвід ціннісного ставлення до природного і соціального довкілля. В цьому плані (охорона довкілля) можна використати уроки хімії, продемонструвавши зворотну (негативну) сторону хімічного виробництва. На заняттях з хімії слід звернути увагу на вираз "кислотні дощі" та пояснити його походження. Тут доцільно назвати ще один, а власне: "лисячі хвости" і розповісти, що так називали викиди в атмосферу N02 (бурого кольору) азотно-тукових заводів. Надати учням можливість самим зробити висновок. Що може цей газ утворити з водяною парою, яка завжди присутня в повітрі (суміш нітратної та нітритної кислот). Подібне явище спостерігається і при виробництві сульфатної та деяких інших кислот. З цього приводу підкреслити важливість проектування не лише досконалих очисних споруд, а створення безвідходного виробництва в хімічній промисловості.
Хімія, як одна з фундаментальних природничих наук, має. всі можливості формувати в учнів спеціально-предметні компетентності.
Предметна компетенція - це сукупність знань, умінь та характерних рис, і на їх основі формуються загально предметні компетентності. До закінчення школи в учня повинні бути сформовані всі основні компетенції. Пізніше вони будуть лише доповнюватися та розвиватися. Ще із шкільної парти учень повинен усвідомлювати, де і як він зможе застосувати набуті знання, уміння та досвід. Адже за визначенням міжнародного департаменту стандартів для навчання «компетентність — це спроможність кваліфіковано проводити діяльність, виконувати завдання або роботу».
Безперечно, для успішного засвоєння такої науки, як хімія, велике. значення мають лабораторні роботи (досліди). Для експериментальної компетенції необхідне виконання експерименту під керівництвом вчителя з описом дослідів. Однак, для вміння аналізувати, порівнювати, встановлювати причинно-наслідкові зв'язки, робити висновки необхідні базові теоретичні знання основних понять, законів і принципів хімії.
Для оцінювання результатів роботи учнів на уроці істотне значення має виконання письмових завдань. Письмова робота дає можливість осмислити відповідь, перевірити її, виправити помилки.
Немаловажне значення мають завдання для порівняння. Вони - передбачають вміння аналізувати та порівнювати істотні ознаки об'єктів, що вивчаються, тобто, уміння встановлювати подібність та відмінність між предметами або їх окремими елементами і ознаками. Завдання краще подавати із зростанням складності, тобто, здійснювати перехід від окремого до загального.
Важливе завдання сучасного викладача хімії - забезпечити засвоєння учнями предмета на рівні функціональної грамотності, а у профільних класах - на рівні освітньої компетентності. Навчання хімії передбачає формування і більш загальних компетентностей: освітньої (вміння вчитися, розкривати суть і значення теоретичних побудов і символіко-графічних форм, давати їм різну інтерпретацію, оперувати мовою науки та ін.); методологічної, комунікативної; експериментально - практичної; задачної тощо.
Зміст предмету «Хімія» бере також участь у формуванні різноманітних надпредметних компетентностей: комп'ютерної; екологічної; валеологічної; соціокультурної тощо.
Виділяємо пріоритетну роль хімії у формуванні екологічної компетентності, оскільки більшість екологічних проблем сучасності мають хімічну природу, а для їх вирішення активно використовуються хімічні засоби та методи. Недостатність хімічної грамотності погрожує загрозою людині та природі, недооцінюванню ролі хімії у розв'язанні екологічних проблем, хемофобією. Екологічна освіта та виховання розглядається нами як складова частина всіх ступенів шкільної хімічної освіти.
Таким чином, компетентнісний підхід у системі сучасної національної освіти практично можливий лише за умови органічного поєднання двох його взаємопов'язаних ланок : компетентнісний педагог і компетентнісний учень.
Компетентнісний учитель, на наше переконання, інтегрує в собі високий рівень професійних, педагогічних, психологічних, соціальних якостей та здійснює системний підхід до визначення цілей, актуальних для розвитку особистості учня;
відбору змісту навчання з предмета, якому він навчає,організації освітнього процесу з врахуванням реалій сьогодення та найближчого майбутнього учня
відбору та впровадження у навчальний процес сучасних освітніх технологій,
діагностики, корекції та контролю результатів навчання кожного учня.
Компетентнісний випускник 11-річної школи - це особистість, яка вміє: гнучко адаптуватися в мінливих життєвих ситуаціях, самостійно здобуваючи необхідні знання, вміло використовуючи їх на практиці для вирішення різноманітних проблем; самостійно критично мислити, бачити в реальній дійсності проблеми та шукати шляхи їх раціонального вирішення, використовуючи сучасні технології, чітко усвідомлювати де та яким чином набуті знання можуть бути застосовані в довкіллі; генерувати нові ідеї, творчо мислити, грамотно працювати з інформацією (вміти збирати необхідні для розв'язання певної проблеми факти, аналізувати їх, пропонувати гіпотези, робити необхідні узагальнення, співставлення з аналогічними чи альтернативними варіантами вирішення, встановлювати статистичні закономірності, робити аргументовані висновки, застосовувати отримані висновки для виявлення і розв'язання нових проблем);
бути комунікабельним, контактним у різних соціальних групах, уміти працювати у групах у різноманітних сферах діяльності у різних ситуаціях запобігаючи і вміло виходячи з конфліктних ситуацій; самостійно працювати над розвитком власної моралі, інтелекту, культурного рівня; аналізувати власну діяльність і діяльність інших; оцінювати соціальні звички, пов'язані із здоров'ям, навколишнім середовищем.
Як відомо, провідною діяльністю учнів 8-11-х класів є міжособистісне спілкування та професійне самовизначення, намагання зайняти своє місце в житті. У результаті спільної діяльності учнів відбувається формування внутрішніх та соціальних мотивів навчання як на уроках, так і в позаурочній роботі. Тому, використовуємо такі педагогічні засоби, які спрямовані на різноманітні способи взаємодії з іншими учнями: встановлення контакту, вибір певної соціальної позиції у відносинах з оточенням, отримання їх схвалення.
Найефективнішим засобом у вирішенні питання формування компетентної особистості, вважаємо групову навчальну діяльність школярів, організація якої забезпечує включення учнів в активне спілкування та співробітництво. Цей вид діяльності заохочує учнів до самостійного дослідження змісту навчального матеріалу, взаємного використання один одного як джерела навчальної інформації. Протягом останніх років ми успішно використовуємо групову навчальну діяльність учнів під час роботи з опорно-логічними схемами, практичних занять, захисті проектів тощо. Учням пропонуються різноманітні види завдань:проблемні запитання; тести; вправи зростаючої складності; комбіновані та творчі завдання; уявний експеримент; експериментальні та розрахункові задачі;моделювання тощо. Заслуговує на увагу групова робота учнів під час підготовки до нестандартних уроків, які займають чільне місце в нашій системі роботи. У даному випадку групи завчасно отримують завдання, готують його .
Одним із способів активізації пізнавальної діяльності учнів є проведення на навчальних заняттях дидактичних ігор, які збуджують думку та стимулюють творчу ініціативу. Ігрова модель навчання сприяє формуванню різних компетентностей, тому що:надає можливості у самовизначенні,розвиває творчу уяву,формує навички співпраці,створює умови для вільного висловлювання учнями власної думки, визначення певної аргументованої позиції. Важливим елементом у процесі формування компетентної особистості вважаємо реалізацію проблемного навчання. Навчити вчитися - це значить навчити вирішувати проблеми, вбудовані у структуру навчально-пізнавальної діяльності школяра.
Проблемно-пошукова діяльність, в яку учні включаються у процесі вирішення проблеми - важливий фактор набуття ключових та предметних компетентностей. Життєвою необхідністю обумовлюється введення у практику активних форм навчання, зокрема проблемних лекцій і семінарів.
Разом із тим компетентнісний підхід вступає у протиріччя з багатьма усталеними в системі освіти стереотипами, існуючими критеріями оцінювання навчальної діяльності учнів, педагогічною діяльністю педагогів, роботою шкільної адміністрації .Одним із найбільш суттєвих протиріч є протиріччя між ускладненими цілями хімічної освіти, новими державними стандартами природничої освіти, скороченим часом на опрацювання навчального матеріалу та вимогами якісного оволодіння цим предметом з одночасним виконанням спільних цілей природничо-наукової освіти.
Зняти це протиріччя частково допомагають, встановлення причинно-наслідкових зв'язків, узагальнення, систематизація і формалізація знань (схематизація, згортання у символіко-графічні форми, моделювання, виділення інваріантів ,найважливіших систем понять, організація на мінімумі знань максимуму різноманітних дій та інше).
Мінімум цілісних знань із хімії, отриманий на основному ступені освіти як найбільш масової, необхідній кожній людині для розумного використання речовин, забезпечення безпеки життєдіяльності в сучасному світі. Саме тому ми розглядаємо хімічну освіту, отриману у школі, не лише як обов'язковий компонент загальної освіти, але й як невід'ємну частину загальної культури людини.
Степанова В.Ф.
учитель хімії Миколаївського муніципального колегіуму
Аналіз завдань ЗНО з хімії та методичні рекомендації до підготовки ЗНО
Зовнішнє незалежне оцінювання є важливим чинником поліпшення якості освіти, забезпечення рівного доступу до вищої освіти.
Досвід упровадження зовнішнього незалежного оцінювання з 2007 р. дозволив зробити певні узагальнення.
По-перше, невміння учнів працювати з тестовими завданнями.
По-друге, тестові завдання найчастіше містять матеріал на закріплення знань, яким недостатньо володіють наші учні.
По-третє, аналіз відповідей учасників тестування засвідчив, що переважна більшість учнів правильно розв’язує лише репродуктивні завдання на відтворення фактичних знань.
Також є завдання, які відсутні в програмі ЗОШ:
1.Аміни. Анілін.
2.Розрахунки молярної маси суміші, якщо відомі об’єми газів, що входять до складу суміші.
Окремо хотілось би зазначити слабку матеріальну базу шкільних кабінетів. Відсутність або недостатність експериментальних робіт не дозволяє учням пам’ятати про ознаки перебігу тих чи інших реакцій. А це також погіршує результати ЗНО учнів.
Враховуючи всі ці недоліки, необхідно звернути увагу вчителів на знання учнями основних питань шкільного курсу хімії, а саме:
- Знання найважливіших законів і теорій хімії;
- Володіння хімічною мовою, вміння користуватись назвами і символами хімічних елементів, назвами простих і складних речовин;
- Вміння складати хімічні формули і рівняння хімічних реакцій, розв’язувати розрахункові і експериментальні задачі;
- Розуміння зв’язку між складом, будовою, фізичними та хімічними властивостями речовин, способами їх добування, галузями застосування;
- Знання про найважливіші природні та штучні речовини: їх будову, способи добування та галузі застосування;
- Розуміння наукових основ певних хімічних виробництв;
- Обізнаність з деякими екологічними проблемами, пов’язаними з хімією: озонові “дірки”, кислотні дощі, забруднення повітря промисловими і транспортними викидами, водойм – промисловими та побутовими стоками;
- Розуміння ролі хімії у розв’язанні глобальних проблем людства: раціональному природокористуванні, забезпеченні продуктами харчування, захисті довкілля від забруднення промисловими і побутовими відходами.
Для належної підготовки учнів до зовнішнього тестування протягом навчального року слід використовувати тестові завдання під час тематичного контролю знань і поточного оцінювання. Окрім цього, тестові завдання використовуються і на етапі актуалізації вивчення тієї чи іншої теми, на етапі закріплення знань тощо. Така форма роботи не лише сприятиме адаптуванню учнів до системи зовнішнього оцінювання, а й стане у нагоді в повсякденній роботі вчителя, адже тести прості у застосуванні, значно економлять час при проведенні опитування, дозволяють використати його на інші форми роботи на уроці.
Окрім того, тестові завдання виконують не лише функцію контролю якості знань, а й навчальні функції. Переваги використання тестових завдань полягають у високій інформативності; чіткій стандартизації, процедури оцінювання, що створює однакові умови для всіх учасників і зменшує вплив на результат сторонніх факторів; простоті і доступності у використанні; однозначності системи обробки та інтерпретації одержаних кількісних показників; репрезентативності завдань. При доборі чи розробленні тестових завдань, які входять до складу тесту, враховуються певні правила.
По-перше, структура тесту залежить від мети тестової перевірки знань.
Правильно розроблені тестові завдання дають можливість перевірити не лише початкові, репродуктивні знання предмету, а й когнітивні уміння на рівнях: знання, застосування та обґрунтування.
По-друге, завдання і відведений час на їх розв’язання відповідають віковим особливостям учнів.
По-третє, вимоги до форми тестових завдань. Усі тестові завдання поділяються на закриті та відкриті. Відкриті завдання - це завдання, які не мають варіантів відповіді. До закритих тестових завдань належать, так звані, альтернативні завдання. У них, крім питання, містяться два взаємовиключаючі варіанти відповіді.
Окрім цього, існують тестові завдання на встановлення відповідності. У таких завданнях у двох частинах пропонуються переліки - з 3-4 тверджень з лівої частини та 4-5 з правової частини, між якими треба встановити зв'язок.
Також існують завдання на відтворення послідовності. Сутність цих завдань полягає в необхідності перекомбінувати наведені дані або елементи.
"Зовнішнє незалежне оцінювання з хімії є письмовим за формою і складається з 60 завдань. На виконання тесту з хімії відводиться 150 хвилин. Щодо форм тестових завдань, то у зошити розміщені:
завдання з вибором однієї правильної відповіді з чотирьох запропонованих;
завдання на встановлення відповідності (логічні пари), які складаються зі спільного вступного запитання та чотирьох завдань ,позначених буквами, до кожної з яких потрібно добрати один варіант відповіді з п'яти запропонованих і позначених цифрою, і записати його в таблицю; завдання на встановлення правильної послідовності, у яких потрібно розташувати певні дії (поняття, формули, характеристики) у правильній послідовності, де перша дія (поняття, формула, характеристика відповідає цифрі 1 - друга - 2 тощо, і записати цю послідовність у таблицю).
Окрім цих трьох типів завдань у тестовому зошиті з хімії включені завдання відкритої форми з короткою відповіддю. Запропоновані завдання передбачають запис певного числа, які і є відповіддю на поставлене запитання . серед завдань такого типу можуть зустрічатися задачі на обчислення, написання реакцій з подальшим підрахунком суми коефіцієнтів, складання електронного балансу рівняння наведеної реакції з вказуванням у відповіді числа прийнятих електронів тощо.
Степанова В.Ф.
учитель хімії Миколаївського муніципального колегіуму
