Исследование пломбирования кровеносных сосудов генератором «ligasure» иего применение в хирургии щитовидной железы 14. 00. 27 хирургия
| Вид материала | Исследование |
- Современные методы лечения узловых образований щитовидной железы, 110.17kb.
- Использование малоинвазивного электрохимического лизиса при доброкачественных узловых, 305.06kb.
- Хирургическая тактика при узловых образованиях щитовидной железы в условиях крупного, 472.21kb.
- Заболевания щитовидном железы, 94.48kb.
- Заболевания щитовидном железы (лекции), 219.78kb.
- Хирургическое лечение щитовидной железы, 32.35kb.
- Комплексный подход к диагностике и хирургическому лечению заболеваний щитовидной железы, 1223.26kb.
- Применение лазерной фотостимуляции в детской хирургии (экспериментально-клиническое, 554.39kb.
- Оценка параметров качества жизни больных, оперированных по поводу доброкачественных, 381.94kb.
- Применение миллиметровой терапии в лечении доброкачественных заболеваний молочной железы, 28.38kb.
На правах рукописи
Катков Андрей Николаевич
ИССЛЕДОВАНИЕ ПЛОМБИРОВАНИЯ КРОВЕНОСНЫХ СОСУДОВ ГЕНЕРАТОРОМ «LIGASURE» И ЕГО ПРИМЕНЕНИЕ В ХИРУРГИИ
ЩИТОВИДНОЙ ЖЕЛЕЗЫ
14.00.27 – хирургия
Автореферат диссертации на соискание ученой степени
кандидата медицинских наук
Нижний Новгород, 2006
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Нижегородская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию» (ректор – член-корреспондент РАМН, доктор медицинских наук, профессор Шкарин В. В.) на кафедре общей хирургии им. А. И. Кожевникова (заведующий – заслуженный врач РФ, доктор медицинских наук, профессор Овчинников В. А.), на базе областной клинической больницы им. Н. А. Семашко (главный врач – заслуженный врач РФ Зайцев Р. М.)
Научный руководитель:
заслуженный врач РФ, доктор медицинских наук, профессор
Овчинников Вадим Александрович
Официальные оппоненты:
доктор медицинских наук, профессор Зубеев Павел Сергеевич
доктор медицинских наук, профессор Романов Михаил Дмитриевич
Ведущая организация: Государственное образовательное учреждение высшего профессионального образования «Башкирский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Защита диссертации состоится «___» __________2006 года в ___ часов
на заседании Диссертационного Совета Д 084.39.02 при Государственном образовательном учреждении высшего профессионального образования «Нижегородская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию» (603005 г. Нижний Новгород пл. Минина 10/1).
С диссертацией можно ознакомиться в библиотеке Государственного образовательного учреждения высшего профессионального образования «Нижегородская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию» (603104 г. Нижний Новгород, ул. Медицинская, 3а)
Автореферат разослан «___»_______________2006 года
Ученый секретарь Диссертационного Совета:
доктор медицинских наук профессор В. В. Паршиков
^ ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
В последние годы наметился рост количества больных с патологией щитовидной железы. По данным ВОЗ, от 4 до 7 % населения Земли страдают данной патологией (Ветшев П. С., 2002; Герасимов Г. А., 1999; Дедов И. И., 1999). WM. Aschcraft и AJ. Van Herle (1981) сообщают, что прирост выявленных узловых образований щитовидной железы в США составляет 0,09 % в год. Л. Ф. Винник (1996) указывает, что частота впервые выявленной тиреоидной патологии по г. Санкт-Петербургу и Ленинградской области за год возросла на 53,7 %. Аналогичные данные по Московскому региону приводит и А. П. Калинин (2004) – прирост за период с 1995 по 1996 годы составил от 19 до 79 %. Возрастает и количество хирургических вмешательств на этом органе, что не может не повышать требования к технике выполнения таких операций.
Имеющиеся на сегодняшний день в арсенале хирургов «классические» методы оперативного лечения тиреоидной патологии не всегда отвечают современным требованиям. При их применении остаются нерешенными вопросы снижения травматичности вмешательства, уменьшения интраоперационной кровопотери, сокращения числа специфических и неспецифических осложнений (Калинин А. П., 2004).
В последнее десятилетие началось активное внедрение в хирургию щитовидной железы мини-доступа и эндоскопических технологий. Пионерами применения подобных методик явились: В. Н. Егиев (2002), А. И. Никитенко (2002 – 2005), Ю. Т. Цуканов (1999 – 2001), R. Bellantone (1999 – 2003), C. G. S. Huscher (1997), Р. Miccoli (1999 – 2005). Резекция щитовидной железы из мини-доступа позволила снизить травматичность операции, значительно улучшить косметический эффект вмешательства, уменьшить послеоперационный койко-день. Однако перед хирургами возникла новая проблема: лигатурный гемостаз при мини-доступе оказался непростой манипуляцией, требовал много времени, в связи с чем продолжительность вмешательства значительно увеличилась по сравнению с «классическими» операциями, на что указывают: Д. Д. Долидзе (2004), В. Н. Егиев (2002), А. И. Никитенко (2002 – 2005), А. С. Юшкин (2003), R. Bellantone (1999 – 2003), Р. Miccoli (1999 – 2005). Эту проблему пытаются решить путем использования новых физических технологий гемостаза (Lombardi CP., 2004 – 2006; Miccoli Р., 1999 – 2005; Sandonato L, 2003). Однако и физические методы гемостаза не лишены недостатков, что в совокупности с их высокой стоимостью делает проблему гемостаза в хирургии щитовидной железы весьма актуальной.
^ Цель исследования: обосновать применение для гемостаза генератора «LigaSure» и изучить его эффективность при оперативном лечении заболеваний щитовидной железы.
^ Задачи исследования:
- Сконструировать прибор для измерения давления, при котором происходит разрыв «коллагеновой пломбы», создаваемой генератором «LigaSure», в различных кровеносных сосудах.
- Определить на трупном материале прочность «коллагеновой пломбы», создаваемой с помощью генератора «LigaSure» в артериях различного диаметра, покрытых и непокрытых паравазальной клетчаткой.
- Определить на трупном материале прочность «коллагеновой пломбы», создаваемой с помощью генератора «LigaSure», в артериях различного диаметра, пораженных и непораженных атеросклерозом.
- Определить на трупном материале прочность «коллагеновой пломбы», создаваемой с помощью генератора «LigaSure», в венах различного диаметра.
- Изучить интраоперационную кровопотерю, количество лигатур, использованных для гемостаза, интра- и послеоперационные осложнения и продолжительность оперативного вмешательства при «классических» вариантах операций на щитовидной железе.
- Изучить интраоперационную кровопотерю интра- и послеоперационные осложнения и продолжительность оперативного вмешательства при операциях на щитовидной железе из мини-доступа с применением для гемостаза и диссекции тканей генератора «LigaSure».
^ Научная новизна исследования:
- Впервые дана объективная оценка прочности «коллагеновой пломбы» на трупном материале в различных кровеносных сосудах с помощью генератора «LigaSure».
- Впервые изучена прочность «коллагеновой пломбы» в щитовидных артериях.
- Впервые доказана более высокая прочность «пломбы», наложенной на сосуды, покрытые паравазальной клетчаткой, по сравнению с непокрытыми паравазальной клетчаткой сосудами.
- Обращено внимание, что прочность «коллагеновой пломбы» обратно пропорциональна диаметру сосуда.
- Доказано, что «коллагеновая пломба», наложенная на артерии с наличием атеросклеротического поражения их стенки, менее прочная, чем в артериях без атеросклеротического поражения.
- Впервые при микроскопическом исследовании «коллагеновой пломбы» в артериях с атеросклеротическими изменениями выявлены разрывы в ее структуре.
- Доказана более высокая эффективность операций на щитовидной железе с использованием генератора «LigaSure» по сравнению с «классическими» операциями на этом органе.
^ Практическая значимость исследования. При выполнении клинической части исследования доказано:
- Применение генератора «LigaSure» для гемостаза и диссекции тканей позволяет выполнять операции на щитовидной железе практически бескровно.
- Применение генератора «LigaSure» для гемостаза дает возможность при операциях на щитовидной железе полностью отказаться от перевязки сосудов лигатурами, которые, являясь инородными телами, приводят к образованию гранулем, а в ряде случаев и к нагноению послеоперационной раны.
- Применение генератора «LigaSure» при операциях на щитовидной железе дает возможность оперировать в «сухом» операционном поле, что облегчает визуализацию возвратного нерва и паращитовидных желез, а, следовательно, уменьшает риск их повреждения во время вмешательства.
^ Внедрение в практику. Основные положения диссертации используются в практической работе хирургической клиники имени А. И. Кожевникова Нижегородской областной больницы имени Н. А. Семашко.
^ Апробация работы. Материалы диссертации докладывались и обсуждались на клинических конференциях хирургов Нижегородской областной больницы, а также на заседаниях научного общества хирургов Нижегородской области. Материалы диссертации представлены в тезисах докладов VII съезда Российского общества эндоскопических хирургов (Москва, 2004 год), Всероссийской конференции хирургов с международным участием (Москва, 2005 год), VIII съезда Российского общества эндоскопических хирургов (Москва, 2005 год), X Нижегородской сессии молодых ученых (Нижний Новгород, 2005 год), Всероссийской научно-практической конференции «Актуальные вопросы тиреодологии» (Нижний Новгород, 2006 год), V научной сессии «Современное решение актуальных научных проблем в медицине» (Нижний Новгород, 2006 год).
Публикации. По материалам диссертации опубликовано семь работ, из них четыре в центральной печати. Получена приоритетная справка на изобретение и один патент на полезную модель.
^ Объем и структура диссертации. Диссертационная работа изложена на 138 страницах машинописного текста и состоит из введения, 5 глав, заключения, выводов, практических рекомендаций и указателя литературы. Последний содержит 192 наименования, включая 89 работ отечественных и 103 иностранных авторов. Работа проиллюстрирована 36 таблицами, 27 фотографиями, 7 диаграммами и 2 рисунками.
^ Положения, выносимые на защиту:
- Наиболее прочно генератором «LigaSure» пломбируются артерии диаметром до 8 мм, покрытые паравазальной клетчаткой и без признаков атеросклеротического поражения.
- Генератор «LigaSure» позволяет в равной мере пломбировать и венозные сосуды.
- Операции на щитовидной железе из мини-доступа с использованием для гемостаза генератора «LigaSure» выполняются бескровно, за более короткое время, в отличие от лигатурного гемостаза, и с отсутствием неспецифических осложнений.
^ СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы
В основу настоящей работы положено исследование результатов оперативного лечения 226 пациентов с патологией щитовидной железы, находившихся в хирургической клинике имени А. И. Кожевникова на базе Нижегородской областной больницы имени Н. А. Семашко за период с 1999 по 2005 годы, и исследование результатов прочности «заваривания» генератором «LigaSure» 160 кровеносных сосудов, извлеченных из трупов.
Из 226 больных женщин было 206 (91 %), а мужчин 20 (9 %). Средний возраст больных составил 48 ± 13 лет (от 16 до 79 лет). Возраст и пол пациентов представлен в таблице 1.
Больные были разделены на две группы.
В первую группу было включено 172 пациента, оперированных с использованием лигатурного гемостаза, из них 89 «классическим» способом и 83 – из мини-доступа.
Среди пациентов первой группы преобладали женщины, их было 157
(91 %), мужчин – 15 (9 %). Средний возраст больных в первой группе составил 49 ± 13 лет (от 16 до 79 лет).
Таблица 1.
Распределение больных по полу и возрасту
| Пол | Возрастные группы | ||||||
| До 20 лет | 21 – 30 | 31 – 40 | 41 – 50 | 51 – 60 | 61 – 70 | 71 и старше | |
| Мужчины | 2 | 2 | 1 | 7 | 6 | 1 | 1 |
| Женщины | 4 | 15 | 26 | 75 | 46 | 31 | 9 |
| Всего | 6 | 17 | 27 | 82 | 52 | 32 | 10 |
Во вторую группу было включено 54 пациента, оперированных из мини-доступа с использованием для гемостаза и диссекции тканей генератора «LigaSure». Соотношение женщин и мужчин во второй группе составило 49 (91 %) и 5 (9 %) соответственно. Средний возраст – 46 ± 12 лет (от 17 до 78 лет).
Больные по видам патологии, по степени увеличения щитовидной железы и по объему оперативных вмешательств были сопоставимы. Клинические диагнозы и объем оперативных вмешательств в исследуемых группах представлены в таблицах 2,3.
Больным перед операцией проводилось обычное обследование, включающее в себя: общий анализ крови, общий анализ мочи, биохимические анализы крови (уровень глюкозы, билирубин, аминотрансферазы, показатели свертывающей системы), ЭКГ, ФВД. Кроме того, в обязательном порядке выполнялись: УЗИ щитовидной железы, ТАБ под контролем УЗС, уровень гормонов (Т3, Т4, ТТГ) и по показаниям сцинтиграфия радиофармпрепаратом 99Тс.
У пациентов исследуемых групп изучались следующие показатели:
- Интраоперационная кровопотеря;
- Продолжительность оперативного вмешательства (от момента разреза кожи до момента ее зашивания);
- Количество лигатур, затраченных для гемостаза;
- Интра- и послеоперационные осложнения.
Таблица 2.
Структура патологии в исследуемых группах
| Вид патологии | Общее количество, n (%) | Первая группа, n (%) | Вторая группа, n (%) |
| Многоузловой эутиреоидный зоб | 99 (43,8 %) | 82 (47,7 %) | 17 (31,5 %) |
| Узловой эутиреоидный зоб | 61 (27,0 %) | 36 (20,9 %) | 25 (46,3 %) |
| Рак щитовидной железы | 21 (9,3 %) | 18 (10,5 %) | 3 (5,6 %) |
| ДТЗ | 19 (8,4 %) | 15 (8,8 %) | 4 (7,4 %) |
| Рецидивный узловой зоб | 9 (4,0 %) | 7 (4,1 %) | 2 (3,7 %) |
| УДФА | 7 (3,1 %) | 5 (2,9 %) | 2 (3,7 %) |
| МДФА | 5 (2,2 %) | 4 (2,3 %) | 1 (1,9 %) |
| АИТ Хашимото | 3 (1,3 %) | 3 (1,7 %) | 0 |
| ДДФА | 2 (0,9 %) | 2 (1,2 %) | 0 |
| Всего: | 226 (100 %) | 172 (100 %) | 54 (100 %) |
Интраоперационная кровопотеря рассчитывалась гравитационным методом. Для этого собирались все шарики и салфетки, использованные во время операции для осушения раны, и взвешивались на рычажных весах с ценой деления 0,1 г и погрешностью 0,1 г. Масса кровопотери определялась путем вычитания из полученного результата взвешенной массы сухого материала. Для расчета объема кровопотери эта величина делилась на среднюю плотность крови (1,05 г/мл), и вычислялся показатель кровопотери в миллилитрах (мл).
Таблица 3.
Объем оперативных вмешательств в исследуемых группах
| Объем операции | Общее количество, n (%) | Первая группа, n (%) | Вторая группа, n (%) |
| Резекция обеих долей щитовидной железы | 106 (46,9 %) | 85 (49,4 %) | 21 (38,9 %) |
| Резекция одной доли щитовидной железы | 57 (25,2 %) | 48 (28,0 %) | 9 (16,7 %) |
| Гемитериоидэктомия | 40 (17,7 %) | 19 (11,1 %) | 21 (38,9 %) |
| Субтотальная резекция щитовидной железы | 11 (4,9 %) | 8 (4,6 %) | 3 (5,6 %) |
| Резекция одной доли с перешейком | 7 (3,1 %) | 7 (4,1 %) | 0 |
| Тиреоидэктомия | 3 (1,3 %) | 3 (1,7 %) | 0 |
| Удаление перешейка | 2 (0,9 %) | 2 (1,2 %) | 0 |
| Всего: | 226 (100 %) | 172 (100 %) | 54 (100 %) |
^ Материалы исследования пломбирования кровеносных сосудов
генератором «LigaSure» на трупном материале
Во время патологоанотомического вскрытия 10 трупов (7 мужчин и 3 женщины) было извлечено и исследовано 119 артерий различного диаметра и 41 вена также различного диаметра. Средний возраст умерших составил 58 ± 12 лет (от 43 до 82 лет). Структура патологии, приведшей к летальному исходу, была следующей: сахарный диабет II типа – 5 случаев, злокачественные заболевания системы крови – 3 случая, рак желудка – 1 случай, цирроз печени – 1 случай.
Производился отбор извлеченных артерий на предмет наличия атеросклеротического поражения. В крупных артериях (от 6 мм в диаметре) наличие поражения определялось пальпаторно и визуально до начала опыта. В более мелких артериях (до 6 мм в диаметре) факт наличия или отсутствия атеросклероза устанавливался при морфологическом исследовании по завершении опыта. Было исследовано 63 артерии различного диаметра без атеросклеротических бляшек и 56 артерий с наличием таковых.
Извлеченные артерии и вены сразу же после забора подвергались воздействию генератором «LigaSure» с использованием насадок: Atlas (15 мм) и Precise (5 мм), в зависимости от диаметра исследуемого сосуда.
Воздействие на сосуды осуществлялось как на препарированном, то есть свободном от паравазальной клетчатки участке, так и на участке, покрытом клетчаткой, сквозь ее толщу. Всего после «заваривания» просвета было исследовано 63 непораженных атеросклерозом препарированных артерий и 53 непораженных непрепарированных; 56 пораженных атеросклерозом препарированных артерий и 47 пораженных непрепарированных.
Все исследованные вены «заваривались» как на свободном от паравазальной клетчатки участке, так и на покрытом ею. Исследуемые вены были разделены на две группы. В первую группу была включена 21 вена диаметром до 6 мм; во вторую группу – 20 вен диаметром более 6 мм в диаметре. Первая группа представлена 11 притоками внутренней яремной вены – 11, 6 непарными и 4 полунепарными венами. Во вторую группу были включены: 10 внутренних яремных вен, 8 почечных вен и 2 подключичные вены.
Для определения давления, при котором наступает разрыв «биологической коллагеновой пломбы», окклюзирующей просвет сосуда после воздействия на него генератором «LigaSure», был сконструирован прибор. Он состоял из насоса для нагнетания воздуха, манометра и ПВХ-трубок, соединяющих насос, манометр и исследуемую структуру. Шкала манометра была градуирована в миллиметрах ртутного столба (мм рт. ст).
Насосом в сосуд, «заваренный» «LigaSure», нагнетался воздух, при этом его давление фиксировалось манометром вплоть до момента разрыва «пломбы», когда давление резко падало. Максимальный показатель давления, при достижении которого наступал разрыв сосуда, и считался давлением разрыва.
Все 119 исследованных артерий были разделены на четыре группы в зависимости от диаметра сосуда и атеросклеротических изменений в них (см. табл. 4).
Таблица 4.
Разделение артерий на группы в зависимости
от диаметра и атеросклеротического поражения
| Исследуемые группы | Диаметр, мм | Без признаков атеросклероза, n | С признаками атеросклероза, n | Всего, n: |
| 1 группа | от 1,5 до 3,9 | 18 | 14 | 32 |
| 2 группа | от 4,0 до 5,9 | 17 | 16 | 33 |
| 3 группа | от 6,0 до 7,9 | 18 | 17 | 35 |
| 4 группа | от 8,0 до 11,5 | 10 | 9 | 19 |
В первой группе исследовались: 22 щитовидных артерии, 5 межреберных артерий и 2 артерии желчного пузыря. Во вторую группу были включены: 8 левых желудочных артерий, 11 селезеночных артерий, 10 нижних брыжеечных и 3 правых печеночных артерии. В третью группу были включены: 10 почечных артерий, 2 общих печеночных артерии, 10 верхних брыжеечных, 5 наружных сонных артерий, 8 внутренних сонных артерий. В четвертой группе «заваривались» на свободном от паравазальной клетчатки участке следующие артерии: общие сонные артерии – 11 и чревные стволы – 6.
Статистическая обработка полученных результатов проводилась с помощью компьютерной программы Statistica 6.0 для MS Windows XP.
^ Результаты исследования прочности «коллагеновых пломб»
и их обсуждение
«Коллагеновая пломба», наложенная на препарированные от клетчатки артерии, непораженные атеросклерозом, оказалась в 1,3 – 2 раза прочнее, чем в пораженных артериях, и это различие достоверно во всех группах.
При сравнении прочности «коллагеновых пломб» сосудов, непораженных атеросклерозом выяснилось, что на препарированных участках прочность «пломбы» обратно пропорциональна диаметру сосуда. Максимальное давление при разрыве «пломбы» зарегистрировано в первой группе: 880 ± 57 мм рт. ст., минимальное – в четвертой группе: 294 ± 59 мм рт. ст. Различие показателей во второй и третьей группах для непораженных артерий (602 ± 39 и 589 ± 44 мм рт. ст.) статистически недостоверно (р > 0,05). При анализе показателей давления, при котором наступал разрыв пломбы, для атеросклеротически измененных препарированных артерий выявлены те же закономерности.
При «заваривании» артерий, покрытых паравазальной клетчаткой, но без признаков атеросклеротического поражения, давление, при котором разрывалась «коллагеновая пломба», достоверно выше, чем в пораженных артериях в 1,6 – 2 раза. Для непораженных атеросклерозом артерий максимальная прочность «коллагеновой пломбы» была у артерий второй группы. Давление в момент разрыва «пломбы» в них достигало 1030 ± 66 мм рт. ст. Этот показатель достоверно выше показателя в первой группы – 887 ± 62 мм рт. ст., но при сравнении с показателем третьей группы – 944 ± 72 мм рт. ст. – достоверных различий не выявлено (р > 0,05). При сравнении прочности «коллагеновых пломб», наложенных на артерии, содержащие атеросклеротические бляшки сквозь паравазальную клетчатку, статистически значимой зависимости прочности пломбы от диаметра сосуда выявить не удалось.
При сравнении показателей давления в момент разрыва «коллагеновой пломбы» в артериях, непораженных атеросклерозом, на препарированных и на непрепарированных участках было выявлено, что в первой группе при показателях давления 880 ± 57 и 887 ± 62 мм рт. ст. различие недостоверно (р > 0,05). Во второй группе – 602 ± 39 и 1030 ± 66 мм рт. ст. различие было достоверно (р < 0,05), то есть «коллагеновая пломба», наложенная на артерии второй группы сквозь паравазальную клетчатку, в 1,6 раза прочнее пломбы, наложенной на препарированный сосуд. В третьей группе показатели 589 ± 44 и 944 ± 72 мм рт. ст. также достоверно различаются (p < 0,05), то есть воздействие сквозь толщу окружающей сосуды клетчатку делает «коллагеновую пломбу» прочнее в 1,5 раза.
При статистической обработке результатов давления при разрыве «коллагеновой пломбы» на свободных и покрытых клетчаткой атеросклеротически измененных артерий участках получены следующие данные. В первой группе – 511 ± 47 и 530 ± 37 мм рт. ст. – различие оказалось недостоверным (р > 0,05), во второй группе – 317 ± 44 и 488 ± 35 мм рт. ст. – различие достоверно (р < 0,05), в третьей группе – 273 ± 52 и 501 ± 44 мм рт. ст. – различие также достоверно (р < 0,05).
Максимальное давление, выдерживаемое «коллагеновой пломбой», зарегистрировано при воздействии генератором на почечную артерию диаметром 5,9 мм сквозь паравазальную клетчатку без признаков атеросклеротического поражения, оно равнялось 1840 мм рт. ст. Это была почечная артерия диаметром 5,9 мм, воздействие осуществлялось сквозь паравазальную клетчатку, сосуд не был поражен атеросклерозом. Минимальное давление – 200,6 мм рт. ст. было зафиксировано в момент разрыва «пломбы» в сонной артерии диаметром 11,5 мм, пораженной атеросклерозом при воздействии на участок сосуда, свободный от клетчатки.
Атеросклеротическое поражение снижает надежность пломбирования в 1,3 – 2 раза в зависимости от диаметра сосуда. По-видимому, для пломбирования артерий четвертой группы диаметром от 8,0 до 11,5 мм генератор «LigaSure» можно применять с обязательным укреплением «коллагеновой пломбы» клипсой или лигатурой.
Воздействие сквозь паравазальную клетчатку повышает резистентность пломбы к разрыву для артерий второй и третьей групп примерно в 1,5 раза, что справедливо как для артерий, содержащих атеросклеротические бляшки, так и для артерий, их не содержащих. На прочность пломбы артерий первой группы, как пораженных, так и не пораженных атеросклерозом, характер воздействия не влияет.
Прочность «коллагеновой пломбы» на препарированных участках артерий обратно пропорциональна их диаметру, в то время как на непрепарированных участках этой обратной линейной зависимости нет. При воздействии на пораженные атеросклерозом артерии сквозь паравазальную клетчатку обратная линейная зависимость прочности «пломбы» от диаметра сохраняется, хотя достоверных различий в этом, в отличие от препарированных артерий, нет.
При микроскопическом исследовании «коллагеновой пломбы», наложенной на непораженные атеросклерозом щитовидные артерии, как на препарированном, так и на непрепарированном участках, отчетливо прослеживается полная окклюзия сосуда гомогенной субстанцией, при этом на участках до и после «пломбы» стенка остается неизмененной.
На участках артерий, покрытых паравазальной клетчаткой, микроскопическая картина «коллагеновой пломбы» не отличалась от картины «пломбы», наложенной на препарированные участки.
При микроскопическом исследовании артерий, пораженных атеросклерозом, было выявлено наличие разрывов в гомогенной структуре «коллагеновой пломбы», наложенной непосредственно на атеросклеротическую бляшку с кальцинозом (Рис. 1).
Р
 ис. 1. Микрофотография участка
ис. 1. Микрофотография участка «коллагеновой пломбы с разрывами
в ее структуре (1), увеличение х12.
Прочность «коллагеновой пломбы» в венозных сосудах также была обратно пропорциональна их диаметру, при этом показатель давления в момент разрыва препарированных вен первой группы был достоверно выше, чем показатель давления при разрыве препарированных вен второй группы, это же выяснилось и для непрепарированных вен первой и второй групп. В случае воздействия генератором сквозь паравазальную клетчатку на вены первой группы прочность «коллагеновой пломбы» достоверно возрастала в 1,5 раза. Для вен второй группы эта закономерность статистически не подтверждена.
^ Техника операций из мини-доступа с использованием
генератора «LigaSure»
В ходе работы была усовершенствована техника видеоассистированных операций на щитовидной железе из мини-доступа путем использования «плавающего разреза» и генератора «LigaSure» для гемостаза и диссекции ткани щитовидной железы (Справка о приоритете на изобретение № 2004.123.057/14 от 27.07.04). Кроме того, было сконструировано устройство, облегчающее выполнение вмешательств на щитовидной железе, предложенным способом (Решение о выдаче патента на полезную модель от 17.03.06 по заявке № 2006101305/22 от 16.01.06).
Операция выполняется следующим образом. Положение больного на операционном столе на спине с валиком под лопатками. Обезболивание – внутривенный наркоз с искусственной вентиляцией легких. На передней поверхности шеи на 2 – 3 см выше яремной вырезки осуществляется поперечный разрез длиной от 2 до 5 см. Длина разреза зависит от размеров большего узла в щитовидной железы. Кожа с подкожной клетчаткой, I фасция шеи, платизма, II фасция шеи тупым и острым путем отслаиваются во все стороны от разреза на протяжении 5 – 6 см («плавающий разрез»), что обеспечивает подвижность кожно-фасциального лоскута на большом протяжении и адекватный доступ ко всем областям щитовидной железы. Поверхностные вены шеи не пересекаются, что предупреждает отек раны в послеоперационном периоде за счет сохраненного венозного кровообращения. Третья фасция рассекается продольно по средней линии, претрахеальные мышцы разводятся в стороны. Тупфером создается полость между III и IV фасциями для адекватного доступа к щитовидной железе. Генератором «LigaSure» прецизионно коагулируются и пересекаются последовательно безымянная щитовидная артерия и вена, перешеек щитовидной железы, верхние щитовидные артерии (при выполнении гемитиреоидэктомии), боковые вены щитовидной железы. Для осуществления тракции отпрепарированных кожно-фасциальных лоскутов, адекватной визуализации зоны операционного действия и установки видеокамеры, дымоуловителя, вакуум-аспиратора используется созданный нами крючок. По мере выполнения этапов операции крючок смещается, делая доступной ту или иную зону операционного действия. Доля щитовидной железы отводится медиально, и прослеживается ход возвратного нерва, расположение паращитовидных желез и коммуникантной ветви между верхней и нижней щитовидной артериями (см. Рис. 2 А, Б). Генератором «LigaSure» коагулируются ветви нижней щитовидной артерии. Резекция ткани щитовидной железы выполняется путем ее поэтапной коагуляции. Операция завершается дренированием и наложением внутрикожного косметического шва рассасывающейся синтетической нитью.
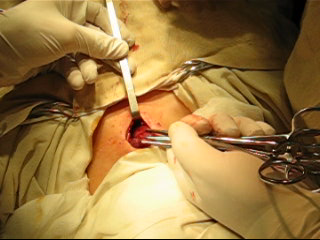
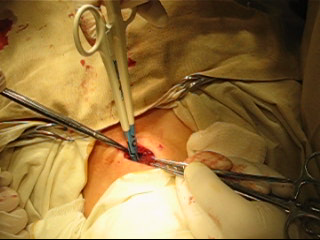 Рисунок 2 А. Рисунок 2 Б.
Рисунок 2 А. Рисунок 2 Б.Рис. 2 А, Б. Этапы мобилизации щитовидной железы генератором «LigSure»
Операция с применением генератора «LigaSure» проводится в «сухом» поле, при этом не образуется дым, не происходит карбонизация тканей. Предлагаемый способ дает возможность полностью отказаться от лигатурного гемостаза, что существенно уменьшает риск травматизации соседних со щитовидной железой образований, которая имеет место при использовании кровеостанавливающих зажимов с последующим лигированием (см. Рис.3,4).
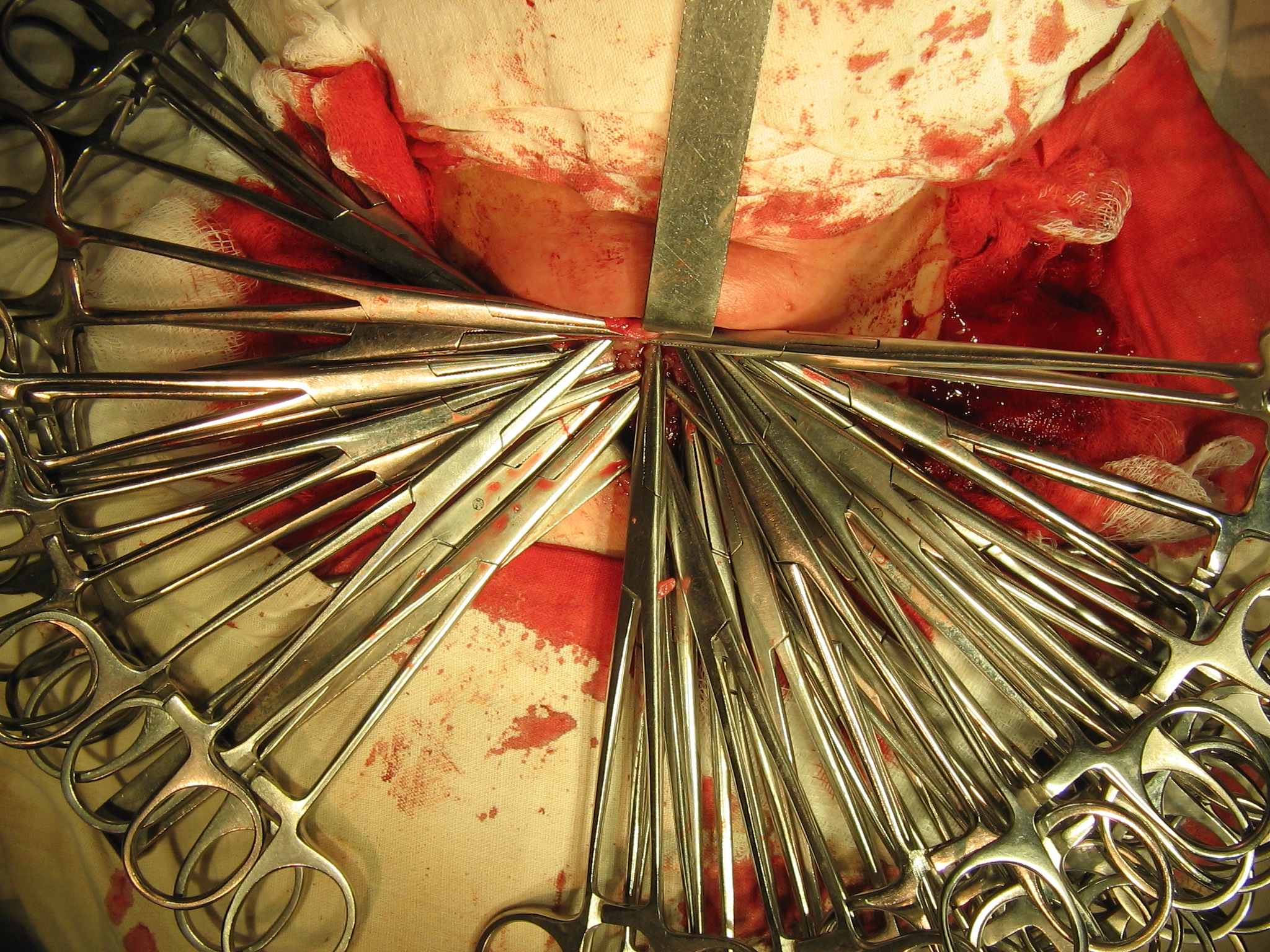
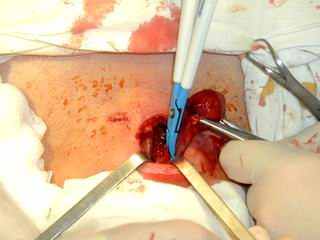
Рис. 3. Операция «классическим» способом
Рис. 4. Операция с применением «LigaSure»
Результаты «классических» операций на щитовидной железе
и операций из мини-доступа с применением генератора «LigaSure»
^ Исследование интраоперационной кровопотери. В первой группе имело место 5 случаев развития интраоперационного кровотечения. Максимальная кровопотеря в случае соскальзывания лигатуры с ветви верхней щитовидной артерии составляла 567,9 мл, из них 375,0 мл больной потерял во время остановки кровотечения. Средний показатель кровопотери в первой группе составил 47,0 ± 11,4 мл и был достоверно выше показателя средней кровопотери во второй группе – 10,1 ± 2,4 мл (р < 0,05). Достоверное различие величины кровопотери в обеих группах выявлено и при многоузловом зобе (в первой – 42,5 ± 8,1 мл, во второй – 10,2 ± 4,1мл), и при узловом зобе (34,3 ± 6,6 мл и 8,5 ± 3,5 соответственно). Показатели кровопотери в обеих группах достоверно различались и при операциях по поводу II и III степени увеличения щитовидной железы. При II степени увеличения железы соотношение составило – 34,9 ± 7,7 мл в первой группе и 7,5 ± 2,5 мл во второй (р < 0,05), III степени увеличения – 44,7 ± 8,9 мл и 10,7 ± 3,1 мл – соответственно (р < 0,05). Та же закономерность выявилась и при сравнительном анализе интраоперационной кровопотери в зависимости от объема вмешательства. При резекции обеих долей соотношение величин кровопотери в первой и второй группах составило 45,4 ± 8,7 мл и 10,2 ± 1,1 мл, при резекции одной доли – 36,0 ± 6,5 мл и 6,8 ± 1,9 мл, при гемитиреоидэктомии 43,5 ± 8,2 мл и 9,8 ± 1,5 мл соответственно.
Использование кровеостанавливающих зажимов влечет риск развития неконтролируемого кровотечения в случае отрыва сосуда вместе с зажимом. Во время остановки такого кровотечения возрастает риск ранения паращитовидных желез или возвратного нерва, так как теряется визуальный контроль над зоной вмешательства. Применение же «LigaSure» позволяет оперировать в «сухом» поле, что снижает риск повреждения соседних структур, и не создает предпосылок к развитию послеоперационных кровотечений.
В первой группе на одну операцию для остановки кровотечения в среднем было затрачено 60 ± 23 лигатуры. Во второй группе для гемостаза во время операции не использовано ни одной лигатуры. Лигатуры, являясь инородным телом, провоцируют развитие воспаления в операционной ране, скопление экссудата, что ведет к риску нагноения.
^ Исследование длительности операции. Для адекватного сравнения продолжительности оперативного вмешательства первая клиническая группа больных, у которой для гемостаза использовались лигатуры, была разделена на две подгруппы: операции из «классического» доступа (89 пациентов) и операции из мини-доступа – 83 пациента, поскольку производство самого мини-доступа значительно увеличивает продолжительность операции на щитовидной железе.
Продолжительность операции в подгруппе с «классическим» доступом составила 58,8 ± 11,8 мин, в подгруппе с мини-доступом – 91,2 ± 7,0 мин, во второй группе – 62,6 ± 10,8 мин. Временные показатели при «классическом» доступе и во второй группе были достоверно (р < 0,05) ниже, чем при мини-доступе с лигатурным гемостазом, а между собой они достоверно не различались (р > 0,05). Эта же закономерность выявлена при сравнении групп в зависимости от патологии, степени увеличения щитовидной железы и объема вмешательства. Продолжительность операции по поводу многоузлового зоба при использовании «классического» способа с лигатурным гемостазом составила 58,1 ± 3,6 мин. При мини-доступе с лигатурным гемостазом время выполнения вмешательства достоверно увеличивалось до 98,7 ± 7,3 мин. При использовании же генератора «LigaSure» увеличения продолжительности достоверно не происходило – 68,3 ± 5,1 мин. Операция из «классического» доступа по поводу узлового эутиреоидного зоба длилась 34,9 ± 8,1 мин, из мини-доступа – 70,8 ± 4,7 мин, а во второй группе – 60,3 ± 2,4 мин. Этот показатель достоверно не отличался от показателя при «классическом» доступе (р > 0,05), однако был достоверно ниже, чем при мини-доступе с лигатурным гемостазом (р < 0,05). При II и III степени увеличения щитовидной железы средняя продолжительность вмешательства в подгруппе с «классическим» доступом (58,3 ± 6,1 мин – II степень и 54,1 ± 8,9 мин – III степень) и с мини-доступом (82,7 ± 6,4 мин – II степень и 86,3 ± 1,5 мин – III степень) различались достоверно (р < 0,05). При сравнении продолжительности операции во второй группе и в подгруппе операций из мини-доступа при тех же степенях увеличения щитовидной железы также выявлено достоверное различие (р < 0,05). При этом различие временных показателей в подгруппе с «классическим» доступом и во второй группе при таких же степенях увеличения щитовидной железы оказалось недостоверным (p > 0,05). Аналогичная закономерность зарегистрирована и при сравнении клинических групп по объему вмешательства. При резекции обеих долей, осуществленной из «классического» доступа, продолжительность операции составила 55,5 ± 9,4 минут, что было достоверно ниже (р < 0,05), чем при мини-доступе – 88,5 ± 4,9 минут, и недостоверно ниже (p > 0,05), чем во второй группе – 77,2 ± 2,5 минуты. Резекция одной доли в первой группе у больных, оперированных из «классического» доступа, длилась 37,0 ± 9,5 минут; у пациентов, оперированных из мини-доступа – 74,9 ± 4,7 минуты; у больных второй группы – 48,4 ± 7,2 минуты. Временные показатели в подгруппе с «классическим» доступом и во второй группе достоверно отличались (р < 0,05) от этого показателя в подгруппе с мини-доступом, между собой они различались недостоверно (р > 0,05). Длительность гемитиреодэктомии в подгруппе «классического доступа составляла – 55,8 ± 16,2 минуты, в подгруппе мини-доступа – 94,4 ± 3,6 минуты, во второй группе – 51,5 ± 8,2 минуты. При других объемах операции показатели ее продолжительности из «классического» доступа и из мини-доступа с использованием «LigaSure» достоверно между собой не различались (р > 0,05), но они были достоверно ниже показателя в подгруппе операций из мини-доступа (р < 0,05) с лигатурным гемостазом.
^ Послеоперационные осложнения. При анализе осложнений в первой и во второй группах мы не получили достоверных различий. В первой группе имели место 5 (2,9 %) случаев развития неконтролируемого интраоперационного кровотечения, 5 (2,9 %) случаев одностороннего преходящего пареза гортани и один случай нагноения послеоперационной раны. Структура осложнений в первой группе соответствует данным, полученным при ретроспективном анализе 3 927 историй болезни пациентов, оперированных в клинике имени А. И. Кожевникова за период с января 1994 года по 2003 год. Все случаи кровотечений – 16 (0,41 %) за десятилетний период – были обусловлены соскальзыванием лигатуры с сосуда, также как и у анализируемых больных первой группы. 11 (0,28 %) нагноений послеоперационной раны, зарегистрированных за это же время, были вызваны присутствием в ней лигатур. Во второй группе был зафиксирован только один случай преходящего пареза гортани.
^ Послеоперационный койко-день. При сравнении среднего послеоперационного койко-дня во второй группе (5,33 ± 1,84 койко-дня) с показателем, полученным путем ретроспективного анализа 3 927 историй болезней пациентов, оперированных с использованием лигатурного гемостаза (7,84 ± 2,28 койко-дня), выявлено их достоверное различие (р < 0,01). Использование генератора «LigaSure» в хирургии щитовидной железы позволяет достоверно снизить продолжительность пребывания больного в стационаре после операции.
Выводы
- Судя по исследованиям, проведенным на трупном материале, генератор «LigaSure» для обеспечения надежного гемостаза допустимо применять при пломбировании артерий диаметром не более 8 мм и вен диаметром не более 6 мм.
- Прочность «коллагеновой пломбы», создаваемой генератором «LigaSure» в артериях и венах, уменьшается по мере увеличения диаметра сосуда.
- «Коллагеновая пломба» в сосудах, освобожденных от паравазальной клетчатки, при испытании ее на разрыв под давлением менее прочная, чем в сосудах, покрытых этой клетчаткой.
- «Коллагеновая пломба» в артериях с атеросклеротическим поражением стенки сосудов разрывается при давлении в 1,5 – 2 раза меньшем, чем в артериях без атеросклеротического поражения.
- При создании «коллагеновой пломбы» в щитовидных артериях, независимо от выделения их из окружающих тканей и наличия атеросклеротических изменений, сосуды в зоне пломбы разрываются при давлении, превышающем в 2,5 – 4,5 раза физиологическое давление крови.
- При микроскопическом исследовании «коллагеновой пломбы» в щитовидных артериях с атеросклеротически измененной стенкой наблюдаются разрывы ее структуры.
- Применение для гемостаза и диссекции тканей генератора «LigaSure» дает возможность выполнять оперативное вмешательство бескровно, без перевязки сосудов лигатурами.
- Продолжительность операций на щитовидной железе из мини-доступа с применением генератора «LigaSure» достоверно ниже, чем операций из мини-доступа, но с лигатурным способом гемостаза.
- При операциях на щитовидной железе с применением генератора «LigaSure» операционное поле остается «сухим» и открытым, что позволяет четко визуализировать возвратные нервы и паращитовидные железы и избежать их повреждения.
- Отсутствие в тканях лигатур после операций с использованием генератора «LigaSure» позволяет прогнозировать более гладкое течение раневого процесса и срастание тканей без грубого рубцевания в последующем.
^ Практические рекомендации
- Разрез кожи и подлежащих тканей при операциях на щитовидной железе из мини-доступа определяется размером узлов и не превышает 5 см.
- При выполнении любого по объему оперативного вмешательства на щитовидной железе и любой степени ее увеличения для достижения надежного гемостаза целесообразно использовать генератор «LigaSure».
- Пломбирование кровеносных сосудов с использованием генератора «LigaSure» рекомендуется осуществлять сквозь толщу окружающей сосуд ткани щитовидной железы.
- При пломбировании генератором «LigaSure» артерий более 8 мм в диаметре и вен более 6 мм в диаметре «биологическую коллагенновую пломбу» необходимо укреплять лигатурой или клипсой.
^ Список научных работ, опубликованных по теме диссертации
- Применение генератора «LigaSure» в хирургии щитовидной железы. //Сборник тезисов Первого конгресса Московских хирургов «неотложная и специализированная хирургическая помощь». Москва, 2005, с. – 348 – 349 (соавторы: А. И. Никитенко, В. А. Овчинников).
- Результат использования генератора «LigaSure» в видеоассистированной хирургии щитовидной железы из мини-доступа. // Журнал «Эндоскопическая хирургия», №1, т. 11, 2005, с. – 92. (соавторы: А. И. Никитенко,А. М. Желаннов, А. А. Пузанков, К. А. Гошадзе).
- Экспериментально-клинический опыт применения генератора «LigaSure» в эндовидеохирургии. // Журнал «Эндоскопическая хирургия», №1, т. 11, 2005, с. 93 – 94. (соавторы: А. И. Никитенко,А. М. Желаннов, А. А. Пузанков, К. А. Гошадзе).
- Применение генератора «LigaSure» и технологии «плавающего разреза» в хирургии щитовидной железы. // «Нижегородский медицинский журнал», № 2, 2005, с.112 – 117. (соавторы: А. И. Никитенко,А. М. Желаннов, А. А. Пузанков, К. А. Гошадзе).
- Достоинства и недостатки хирургии щитовидной железы с применением генератора «LigaSure» и традиционными способами. // Х нижегородская сессия молодых ученых. Естественно научные дисциплины: Тезисы докладов. – Н. Новгород:. Изд. Гладкова О. В. 2005, с. 219 – 221.
- Эндоскопический крючок. // Решение о выдаче патента на полезную модель № 2006101305/22 (001405) от 17.03.06. (соавторы: А. И. Никитенко,А. М. Желаннов, А. А. Пузанков, К. А. Гошадзе).
- Обоснование применения генератора «LigaSure» для заваривания сосудов. // «Нижегородский медицинский журнал», № 4, 2006, с. 11 – 15. (соавторы: А. И. Никитенко, С. И. Никитенко, В. А. Овчинников).
^ Список условных обозначений
АИТ – аутоимммунный тиреоидит,
ДДФА – диссеминированная декомпенсированная функциональная автономия,
ДТЗ – диффузно-токсический зоб,
МДФА – мультифокальная декомпенсированная функциональная автономия,
ПВХ – поливинилхлорид,
ТАБ – тонкоигольная аспирационная биопсия,
ТТГ – тиреотропный гормон,
УДФА – унифокальная декомпенсированная функциональная автономия,
УЗИ – ультразвуковое исследование,
УЗС – ультразвуковое сканирование,
ФВД – функция внешнего дыхания,
ЭКГ – электрокардиография.
