Мисник Андрей Вячеславович Диагностика и лечение нарушений мочеиспускания у больных хроническим простатитом 14. 00. 40 «Урология» автореферат
| Вид материала | Автореферат |
- Оценка показателей водного баланса у больных с хроническим легочным сердцем, 89.38kb.
- Расстройства мочеиспускания у больных первично выявленным раком предстательной железы., 216.22kb.
- Автореферат диссертации на соискание ученой степени, 473.05kb.
- Применение ударно-волновой терапии в комплексном лечении и реабилитации больных хроническим, 390.8kb.
- Автореферат диссертации на соискание ученой степени, 445.33kb.
- Мануальная терапия в лечении больных с простатодинией и тазовыми болями, обусловленными, 40.04kb.
- Нарушение мочеиспускания как мультидисциплинарная проблема, 30.67kb.
- Га различной этиологии: цереброваскулярные болезни нарушение артериального и венозного, 111.36kb.
- Расписание занятий по курсу госпитальной терапии, 138.36kb.
- Диагностика и хирургическое лечение варусной деформации проксимального конца бедренной, 325.02kb.
На правах рукописи
УДК: 616.65-002.2-616.62-008.22-08
Мисник Андрей Вячеславович
Диагностика и лечение нарушений мочеиспускания у больных хроническим простатитом
14.00.40 – «Урология»
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2009
Работа выполнена в ГОУ ВПО «Московский государственный медико-стоматологический университет Росздрава»
Научный руководитель:
Доктор медицинских наук, профессор Яков Дмитриевич Кан
^ Научный консультант:
Доктор медицинских наук, профессор Татьяна Ивановна Гришина
Официальные оппоненты:
Доктор медицинских наук, профессор Авдошин Владимир Павлович
^ ГОУ ВПО «Российский университет дружбы народов» Минобрнауки РФ
Доктор медицинских наук, профессор Кривобородов Григорий Георгиевич
ГОУ ВПО «Российский государственный медицинский университет» Росздрава
Ведущая организация:
ГОУ ВПО «Московская медицинская академия имени И.М. Сеченова» Министерства Здравоохранения и социального развития РФ
Защита состоится __ ________________2009 года в ____ часов на
заседании диссертационного совета Д 208.041.06 при ГОУ ВПО «Московский государственный медико-стоматологический университет Росздрава» по адресу: 127473, г. Москва, ул. Делегатская, 20/1.
С диссертацией можно ознакомиться в библиотеке Московского государственного медико-стоматологического университета (127206, Москва, ул. Вучетича, д. 10 а).
Автореферат разослан __ ________________2008 год.
Ученый секретарь
диссертационного совета
д.м.н., профессор М.М. Умаханова
- ^ ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Хронический простатит является самым распространенным воспалительным заболеванием в современной урологии у мужчин репродуктивного возраста (Степанов В.Н., 2001; Nickel J.C., 1999; Ghobish A.A., 2000). Среди множества проблем, возникающих при данном заболевании, проблема нарушений мочеиспускания остается одной из наиболее актуальных и дискутабельных. Несмотря на большое количество исследований, посвященных данной тематике, до сих пор остаются нерешенными вопросы этиопатогенеза, ранней диагностики, профилактики и лечения нарушений мочеиспускания у больных хроническим простатитом.
В настоящее время предложено множество концепций, объясняющих возникновение нарушений акта мочеиспускания у больных хроническим простатитом (ХП). Одна из наиболее распространенных концепций, рассматривает возникновение нарушений мочеиспускания как осложнение хронического простатита (Гогичаев В.Г., Кораев К.Н., 1984; Лопаткин Н.А., 1998; Сегал А.С., 2002). Другие исследователи, считают, что в большинстве случаев происходит неправильная постановка диагноза (Nickel J.C., 2004; Mayo M.E., Ross S.O., 1998). Так Stiven Kaplan с соавторами (1994) полагают, что у таких больных в первую очередь необходимо подозревать склероз шейки мочевого пузыря (СШМП), а первоначальный диагноз «хронический простатит» в большинстве случаев является ошибочным.
В последние годы изучается роль нарушений иммунного статуса как возможного механизма возникновения хронического простатита и следующего за ним рубцово-склеротического поражения шейки мочевого пузыря и простатического отдела уретры (Голубчиков В.А., Краевой С.А., 1998; Зиганшин О.Р., 2001; Медведев А.А., 2003; Duan Z.G., Yang W.M., 2005; Samy E.T., Setiady Y.Y., 2006).
В ряде работ отмечается, что у больных хроническим простатитом возможны различные нейрогенные нарушения со стороны мочевого пузыря и нейромышечные расстройства тазового дна, которые и вызывают появление симптомов нарушений мочеиспускания (Кузьмин Г.Е., Осипов В.П., 1991; Амидий Р.Э., Кузьмин И.В., 1997; Сегал А.С., 2001; Лоран О.Б., Пушкарь Д.Ю., 2001; Вишневский А.Е., Пушкарь Д.Ю., 2004).
Существующие урологические методики, в том числе и самые современные, позволяют фиксировать лишь результат развившихся осложнений (инфравезикальную обструкцию, гиперактивный мочевой пузырь). В тоже время, используемые методики не позволяют выделить больных, предрасположенных к появлению данного вида осложнений. Это в свою очередь ведет к отсутствию какой-либо профилактики и несвоевременности назначения лечения.
Таким образом, проблема нарушений акта мочеиспускания у больных ХП остается актуальной и требует дальнейшего изучения.
Основной идеей нашего исследования был поиск возможных механизмов развития рубцово - склеротических осложнений у больных ХП и на основании полученных данных, разработка принципов ранней диагностики этих осложнений, их профилактика и лечение. Исходя из этой концепции, были разработаны цель и задачи предстоящего исследования.
^ Цель и задачи исследования
Цель исследования – совершенствование диагностики и результатов лечения больных ХП с нарушением акта мочеиспускания.
Для достижения цели были сформулированы следующие задачи:
- Оптимизировать алгоритм обследования больных ХП с нарушением акта мочеиспускания.
- Определить клинико-диагностические особенности больных ХП с нарушением мочеиспускания на основании новых методов исследования.
- Определить предрасполагающие факторы развития рубцово-склеротических осложнений у больных ХП.
- Провести сравнительный анализ показателей иммунного статуса у больных ХП и склерозом шейки мочевого пузыря.
- Оценить патогистологистологические особенности воспаления предстательной железы в свете возможного возникновения рубцово-склеротических осложнений.
- Уточнить показания для назначения -адреноблокаторов у больных ХП с симптомами нарушений мочеиспускания и оценить их терапевтический эффект.
- Оценить возможности современных иммуномодулирующих препаратов в качестве средства профилактики послеоперационных осложнений у больных ХП, сочетающимся с доброкачественной гиперплазией предстательной железы (ДГПЖ).
^ Научная новизна
Данное исследование позволило впервые выявить факторы, предрасполагающие к развитию рубцово-склеротических осложнений у больных ХП. Выполненный сравнительный анализ показателей иммунного статуса у больных хроническим простатитом и больных склерозом шейки мочевого пузыря позволил выявить общие механизмы формирования склероза шейки мочевого пузыря. На основании результатов данного исследования были определены клинико-иммунологические особенности ХП с симптомами нарушений мочеиспускания, ХП с сопутствующим склерозом шейки мочевого пузыря, а также ХП, сочетающегося с ДГПЖ, что позволило использовать полученные результаты для дифференциальной диагностики этих заболеваний.
Были разработаны методы профилактики и лечения послеоперационных осложнений у больных ХП, сочетающимся с ДГПЖ, и выявлены лабораторные показатели эффективности выполненного лечения.
^ Практическая значимость работы
Результаты проведенного исследования позволили оптимизировать диагностический подход у больных ХП с симптомами нарушений мочеиспускания, внедрить новые методы диагностики, профилактики и лечения рубцово-склеротических осложнений у больных ХП. Кроме того, были внедрены методы послеоперационного контроля эффективности выполненной операции и выявлены клинико-иммунологические показатели формирования послеоперационного склероза у больных ХП, сочетающимся с ДГПЖ. По результатам данного исследования, были определены показания для назначения - адреноблокаторов у больных ХП.
Использование полученных в ходе настоящей работы данных будет способствовать уменьшению количества диагностических ошибок, а также позволит осуществлять профилактику и лечение рубцово-склеротических осложнений у больных ХП.
^ Основные положения, выносимые на защиту
Стандартное обследование больных хроническим простатитом целесообразно дополнить комплексным исследованием иммунного статуса для выявления предрасположенности развития рубцово-склеротических осложнений.
Для больных ХП, имеющих предрасположенность к развитию рубцово-склеротических осложнений, диагностическую значимость имеет повышенный уровень аутоантител к основным компонентам соединительной ткани и снижение концентрации циркулирующих иммунных комплексов.
У больных ХП, сочетающимся с ДГПЖ, и у больных ХП, с сопутствующим склерозом шейки мочевого пузыря (СШМП), выявлены общие механизмы развития склерозирования шейки мочевого пузыря.
Степень вовлечения предстательной железы в воспалительный процесс не влияет на возможность возникновения рубцово-склеротических осложнений у больных ХП.
Для профилактики возникновения послеоперационных осложнений у больных ХП с сопутствующей ДГПЖ целесообразна иммуномодулирующая терапия Галавитом.
Внедрение
Результаты исследования внедрены в практику урологических отделений ГКБ №50, в учебный процесс кафедры урологии и клинической иммунологии лечебного факультета МГМСУ.
Апробация
Результаты диссертационной работы доложены на заседании кафедры урологии лечебного факультета МГМСУ и кафедры клинической иммунологии МГМСУ 21 марта 2008 г.
^ Личный вклад
Автором лично было проведено обследование 99 больных ХП, включенных в исследование. В ходе сбора материала для диссертационной работы соискателем были освоены методики диагностики, профилактики и лечения нарушений мочеиспускания у исследуемых больных, а также новые методы клинико-иммунологического обследования.
Публикации
По материалам диссертации опубликовано 4 работы, из них 3 работы в журналах и изданиях, рекомендованных ВАК России.
^ Объем и структура диссертации
Диссертация изложена на 167 страницах машинописного текста и состоит из введения, 5 глав, заключения, практических рекомендаций и выводов. Работа иллюстрирована 49 таблицами. Библиографический указатель содержит 189 источников.
^ 2. СОДЕРЖАНИЕ РАБОТЫ
Общая характеристика больных
В работе представлен анализ результатов обследования и лечения 99 больных хроническим абактериальным простатитом (категория III A по классификации NIDDK/NIH), имеющих продолжительность заболевания более пяти лет. Из них 76 больных имели подтвержденные нарушения мочеиспускания, 23 пациента не имели нарушений мочеиспускания и составили контрольную группу. После детального обследования и уточнения диагноза у 76 больных ХП с нарушением мочеиспускания, были сформированы 3 исследуемые группы.
^ Первую группу – 14 человек (18,4%) – составили больные ХП с нарушением мочеиспускания.
Вторую группу – 48 человек (63,2%) – больные, у которых ХП сочетался с доброкачественной гиперплазией предстательной железы (ДГПЖ).
^ Третью группу – 14 человек (18,4%) – больные, у которых ХП сочетался со склерозом шейки мочевого пузыря (СШМП).
Критериями исключения из исследования являлись:
- Наличие хронического бактериального простатита.
- Неврологические заболевания, вызывающие нейрогенные расстройства функции мочевого пузыря.
- Сопутствующая аутоиммунная патология, в том числе и в анамнезе.
- Рак предстательной железы.
- Болезнь Мариона.
6.Высокая активность простатита.
Методы исследования
Для решения вопроса о выборе тактики лечения все пациенты проходили комплексное обследование, которое состояло из основных и дополнительных (иммунологических) методов исследования.
^ Основные методы исследования включали: клинические, общелабораторные, ультразвуковые, рентгенологические, уродинамические, эндоскопические и морфологические методы обследования.
Для решения поставленных в работе задач основные методы были дополнены комплексным исследованием иммунного статуса.
^ Дополнительные (иммунологические) методы исследования включали: исследование субпопуляций лимфоцитов, определение фагоцитарной активности нейтрофилов, исследование уровня ЦИК, определение концентрации иммуноглобулинов, определение наличия аутоантител.
Исследование субпопуляций лимфоцитов осуществлялось иммуноферментным методом, при помощи наборов моноклональных антител к различным CD антигенам лимфоцитов человека: CD3+, CD4+, CD8+, CD16+, CD20+, на реактивах фирмы DAKO (Швеция), методом меченного стрептавид – биотина (LSAB). Иммунорегуляторный индекс рассчитывался по формуле: ИРИ = CD4+/CD8+.
Оценка фагоцитарной активности нейтрофилов крови осуществлялась по их поглотительной способности частиц латекса в стандартных наборах фирмы Диа-М. При этом определялись следующие показатели:
а) Фагоцитарная активность – процент «активных» нейтрофилов (нейтрофилы, которые поглотили латекс) из общего числа нейтрофилов (норма-50-90%).
б) Фагоцитарное число – это среднее число фагоцитированных частиц латекса на один активный нейтрофил (норма – 2-9)
в) Резерв фагоцитарной активности, которая определяет резервную возможность фагоцитоза при стимуляции зимазаном по отношению к исходному уровню.
Исследование концентрации иммуноглобулинов трех классов (IgA, IgG, IgM) в сыворотке крови осуществлялось при помощи иммунодиффузионных планшетов фирмы «Реафарм», по методу простой радиальной иммунодиффузии в агаровом геле (по Манчини) с помощью моноспецифических сывороток.
Циркулирующие иммунные комплексы двух классов (ЦИК3%; ЦИК4%) определялись методом преципитации с 3% и 4% раствором полиэтиленгликоля на спектрофотометре при длине волны 25 мм.
При исследовании уровня аутоантител использовалиcь стандартные наборы, изготовленные институтом им. Мечникова.
Иммунологическое обследование всех больных проводилось до начала лечения, а у больных второй группы – трижды: до лечения, через 1,5 месяца после оперативного лечения, выполненного по поводу ДГПЖ, и через 4,5 месяца после оперативного лечения. Увеличение количества исследований у данной группы больных было выполнено в целях ранней диагностики развития рубцово-склеротических осложнений и определения возможности их предотвращения.
^ Методы лечения исследуемых больных
Первая группа больных получала консервативную терапию препаратом Альфузозин производства Syntelabo-sanofi (Франция) в дозе 10 mg в сутки.
У больных второй группы консервативная терапия оказалась неэффективной, что послужило показанием к оперативному лечению – трансуретральной резекции предстательной железы (ТУРП). При этом, наряду с традиционной антибактериальной профилактикой, для уменьшения риска развития ранних и поздних послеоперационных осложнений, части больных проводилась терапия препаратом Галавит производства ЦСМ Медикор (Россия).
Третьей группе больных проводилась только оперативная коррекция шейки мочевого пузыря (трансуретральная резекция – девяти больным и трансуретральная инцизия шейки мочевого пузыря – пяти больным).
Контрольная группа больных в рамках нашей работы специального лечения не требовала.
При статистической обработке полученных результатов были применены методы вариационной статистики и математического моделирования с определением средней величины (М), стандартной ошибки средней величины (m) и стандартного отклонения (δ). Статистический анализ полученных результатов в группах сравнения, проводили параметрическим методом с использованием критерия Стьюдента (t), доверительной вероятности (Р) и уровня значимости (р). Достоверным считалось различие при Р ≥ 95% и р≤ 0,05.
Статистическая обработка полученных данных проводилась с помощью формул для расчета стандартного отклонения и стандартной ошибки. Это позволяло произвести наиболее точное вычисление исследуемых параметров. Обработка полученных данных проводилась на персональном компьютере IBM PC с помощью программ «STATISTIKA 5.5» (StatSoft, США) и Exel 7.0.
Результаты исследования
Данные сравнительного анализа показателей иммунного статуса у обследованных больных
До назначения лечения, проводилось комплексное исследование иммунного статуса у всех больных и выполнялся сравнительный анализ полученных результатов.
Таблица №1 ^ Результаты сравнительного анализа фенотипирования лимфоцитов.
| Показатель | Контрольная группа (М±m) | 1группа (М±m) | 2группа (М±m) | 3группа (М±m) | Норма (М±m) |
| CD3+ (%) (Зрелые Т-лимфоциты) | 52,6 ±2,09** | 51,3±2,54*** | 54,6 ±0,8*** | 49,3±1,56*** ** | 70±1,10 |
| CD4+ (%) (Т- хелперы/ индукторы) | 34,5± 2,04* | 34,4± 1,06** | 32,6±0,77*** | 26,4±1,15*** *** | 44±1,21 |
| CD8+ (%) Т- цитотоксические. | 21,04 ±1,46* | 20,4 ±0,9** | 19,2±0,51*** | 17,0±0,50*** ** | 27,5±1,26 |
| CD16+ (%) NK- клетки. | 17,04 ± 1,5* | 18,4 ± 2,4* | 15,3 ± 1,22* | 15,0 ± 1,97 | 11,5±0,93 |
| CD20+ (%) В- лимфоциты | 23,4 ± 1,15** | 22,3 ± 2,8* | 21,5±0,77*** | 21,1±2,37* | 14,5±0,93 |
| CD4+/CD8+ Иммунорегуляторный индекс. | 1,73 ± 0,11 | 1,69 ± 0,07 | 1,70 ± 0,05 | 1,62 ± 0,05* | 1,75±0,03 |
*-сверху – сравнение с нормой
*- снизу сравнение данных третьей группы с результатами других групп.
*-различие достоверно р≤ 0,05
**- различие достоверно р≤0,01
***- различие достоверно р≤0,001
При исследовании показателей клеточного иммунитета было выявлено достоверное снижение уровня зрелых Т-лимфоцитов (CD3+), а также Т-хелперов (CD4+) и Т- цитотоксических (CD8+) у всех обследованных групп больных. При этом наиболее значимые нарушения данных показателей, достоверно отличающиеся от показателей других групп, определялись у больных третьей группы. По остальным параметрам, полученным при фенотипировании лимфоцитов (СD16+; CD20+; CD4+/CD8+), достоверных отличий между обследованными группами больных выявлено не было.
Таким образом, у больных ХП, с сопутствующим СШМП (3группа), отмечались наиболее выраженные нарушения Т – звена иммунной системы.
При сравнительной оценке показателей фагоцитоза было установлено, что при сравнении с нормой, во всех группах больных отмечалось достоверное снижение фагоцитарной активности и фагоцитарного числа. При этом, наиболее существенное снижение фагоцитарного числа, достоверно отличающееся от значения первой и контрольной групп, определялось у больных второй и третьей групп.
По остальным параметрам фагоцитоза (фагоцитарной активности и резерву фагоцитарной активности) достоверных отличий между группами больных не отмечалось.
Таблица №2. ^ Результаты сравнительного анализа показателей фагоцитоза
| Показатель | контрольная группа (М±m) | 1группа (М±m) | 2группа М±m) | 3 группа (М±m) | Норма (М±m). |
| ФА(%) | 49,8± 2,58** | 49,3± 1,3** | 50,8± 1,15** | 48,4± 3,26*** | 70±2,20 |
| ФЧ | 3,92± 0,27** | 3,74± 0,26** | 3,13± 0,1*** * | 3,10± 0,13*** * | 5,5±0,38 |
| Резерв. (%) | 61,9±1,71 | 60,3±0,90 | 60,3±1,25 | 63,6±2,30 | - |
*-сверху – сравнение с нормой
*- снизу сравнение с результатами контрольной и первой групп.
*-различие достоверно р≤ 0,05
**- различие достоверно р≤0,01
***- различие достоверно р≤0,001
При исследовании показателей гуморального иммунитета было установлено, что наиболее выраженное снижение уровня ЦИК3%, отмечалось у больных третьей группы (28,7 (р≤0,001)). Менее выраженное снижение данного показателя, но также статистически достоверное по отношению к результатам первой и контрольной групп, отмечалось у больных второй группы (35,6 (р≤0,05)). По концентрации ЦИК 4% достоверных отличий между группами больных отмечено не было.
Таблица №3. ^ Результаты сравнительного анализа уровня циркулирующих иммунных комплексов.
| Показатель.(Усл. ед.) | контр. группа (М±m). | 1группа (М±m) | 2группа (М±m) | 3группа (М±m) |
| ЦИК3% | 44,2±2,03 | 41,8±2,05 | 35,6±3,36* | 28,7 ±2,46*** |
| ЦИК4% | 61,04±6,2 | 51,06±2,21 | 49,6±3,6 | 47,7 ±4,18 |
*- сравнение с результатами первой и контрольной групп.
*-различие достоверно р≤ 0,05
***- различие достоверно р≤0,001
Анализ концентрации иммуноглобулинов сыворотки крови не выявил характерных различий между группами больных.
Таблица №4. ^ Результаты сравнительного анализа уровня иммуноглобулинов.
| Показатель | контр. группа (М±m) | 1группа (М±m) | 2группа (М±m) | 3группа (М±m) | Норма (М±m). |
| IgА (мг/мл) | 2,8±0,18 | 2,98±0,3 | 2,22±0,12 | 3,10 ± 0,28 | 2,7±0,20 |
| IgМ (мг/мл) | 1,99±0,15** | 2,12±0,19** | 1,88±0,01** | 1,83 ± 0,11** | 1,3±0,08 |
| IgG (мг/мл) | 15,3±0,61 | 14,5±0,73 | 12,85±0,36 | 14,36 ± 0,54 | 14±0,66 |
**-различие достоверно при сравнении с нормой р≤ 0,01
По результатам сравнительной оценки содержания аутоантител было отмечено достоверное увеличение (до 0,17 (р≤0,001)) уровня аутоантител к эластину в третьей группе больных как по сравнению с нормой, так и по отношению к результатам исследования других групп. Менее высокое значение данного показателя (0,12 (р≤ 0,05)), но также достоверно повышенное по отношению к значению контрольной и первой групп, было зафиксировано у больных второй группы.
Уровень аутоантител к коллагену среди обследованных групп больных достоверно не отличался.
Таблица №5. ^ Результаты сравнительного анализа уровня аутоантител.
| Показатель. (в усл. единицах) | контр. группа (М±m) | 1группа (М±m) | 2группа (М±m) | 3группа (М±m) | Норма (М±m) |
| Уровень антител к коллагену | 0,11±0,01 | 0,12±0,01 | 0,11±0,01 | 0,12±0,01 | 0,1±0,01 |
| Уровень антител к эластину. | 0,11±0,007 | 0,1±0,002 | 0,12±0,006 * | 0,17±0006*** *** | 0,1±0,01 |
*-сверху – сравнение с нормой
*- снизу сравнение с результатами контрольной и первой групп .
*-различие достоверно р≤ 0,05
**- различие достоверно р≤0,01
***- различие достоверно р≤0,001
Результаты комплексного исследования иммунного статуса показали, что у больных третьей группы наблюдается следующая патогенетическая цепочка, приводящая в итоге к рубцовому поражению шейки мочевого пузыря: снижение уровней зрелых Т-лимфоцитов и ЦИК (связанных аутоантител) приводит к повышению уровня цитотоксических аутоантител к эластину и в последующем – к развитию склероза шейки мочевого пузыря (см рис №1) .
Рис.
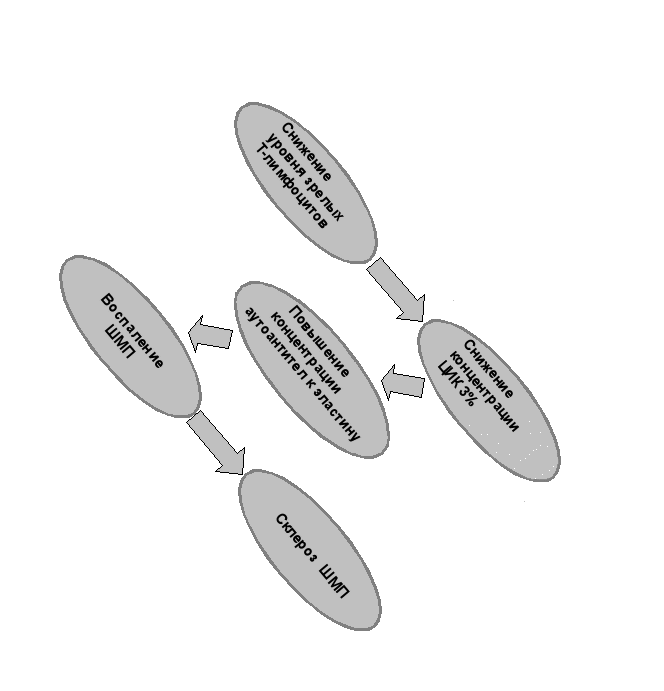 №1 Механизм формирования склероза шейки мочевого пузыря у
№1 Механизм формирования склероза шейки мочевого пузыря убольных хроническим простатитом
^
Результаты лечения исследуемых больных
- Результаты лечения больных первой группы.
При лечении больных первой группы в составе комплексной терапии был использован препарат альфузозин (Дальфаз) в дозе 5 мг 2 раза/сут. В результате, через три месяца после начала терапии, отмечена выраженная положительная динамика по всем исследуемым параметрам. Выявлено повышение максимальной скорости мочеиспускания (в среднем до 20,5 мл/с) и снижение балла IPSS (в среднем до 5,2 баллов), по сравнению с результатами исследования до начала терапии. Несмотря на благоприятные результаты лечения больных данной группы, хотелось бы предостеречь от повсеместного назначения 1-адреноблокаторов у больных ХП, особенно у пациентов с наличием инфравезикальной обструкции и повышенным уровнем аутоантител к эластину, поскольку вышеназванные факторы, в большинстве случаев, указывают на наличие у больного другой патологии, ответственной за возникновение нарушений мочеиспускания, (склероза шейки мочевого пузыря или доброкачественной гиперплазии предстательной железы) и требуют иной лечебной тактики.
Таблица №6. ^ Результаты лечения больных первой группы (n=14).
| | Балл IPSS Ирритат симтомы | QOL | Qmax (мл/сек) | Объем мочеисп. (мл) | Кол-во мочеис.в сутки. |
| До лечения | 7,2±1,44 | 3,4±0,71 | 17,4±1,83 | 182,5±32,3 | 12,5±2,2 |
| Через 3 месяца после терапии | 5,2±1,6 | 2,9±0,54 | 20,5±1,94 | 215±29,4 | 9,2±1,8 |
- ^ Результаты лечения больных второй группы.
В рамках лечения больных данной группы была выполнена апробация современного иммуномодулирующего препарата Галавит, с заявленной противовоспалительной и антифиброзирующей активностью. При этом 25 больным (подгруппа Б) была назначена традиционная антибиотикопрофилактика, а 23 больным (подгруппа Г) наряду с традиционной антибиотикиопрофилактикой, в состав комплексной терапии был добавлен Галавит по схеме: 18 однократных внутримышечных инъекций по 0,1 г с интервалом через два дня. Применение препарата Галавит у больных подгруппы Г отразилось на результатах течения раннего и позднего послеоперационного периода. В этой подгруппе наблюдался достоверно более высокий процент благоприятного течения раннего послеоперационного периода и значительно меньший процент развития послеоперационных осложнений. У больных подгруппы Г было отмечено только 2 случая (4,2%) уретральной лихорадки, в то время как у больных контрольной подгруппы Б было выявлено 7 (18%) случаев уретральной лихорадки и 2 случая острого эпидидимоорхита.
Применение данного препарата отразилось и на отдаленных результатах оперативного лечения. Мы наблюдали стойкое исчезновение признаков инфравезикальной обструкции у 100% больных, получавших терапию Галавитом, а в контрольной подгруппе у 84% больных. У 4 (16%) больных, не получавших лечение Галавитом, в течение 1 года наблюдения развился послеоперационный склероз шейки мочевого пузыря.
Таблица №10 ^ Результаты лечения больных второй группы (n=48).
| Исход | Подгруппа Г (галавит) n=23 Кол-во человек (%) | ПодгруппаБ(контроль) n=25 Кол-во человек (%) |
| ^ Ранний послеоперационный период | ||
| Благоприятное течение | 21 (91,3%) | 16 (64%) |
| Уретральная лихорадка | 2 (8,6%) | 7(28%) |
| Острый эпидидимоорхит | _ | 2(8%) |
| ^ Отдаленные результаты | ||
| Благоприятный исход | 23(100%) | 21(84%) |
| Послеоперационный СШМП | _ | 4 (16%) |
р≤0,05 по сравнению с контрольной подгруппой.
^ Результаты контрольного иммунологического исследования у больных второй группы
Контрольное иммунологическое исследование у больных второй группы проводилось через 1,5 и 4,5 месяца после оперативного вмешательства.
При анализе послеоперационной динамики показателей клеточного иммунитета было установлено, что спустя 1,5 месяца после оперативного вмешательства, в подгруппе больных, получавших Галавит, отмечалось достоверное увеличение содержания зрелых Т-лимфоцитов (CD3+), Т-хелперов (CD4+), а также фагоцитарной активности нейтрофилов. При этом, достоверное повышение зрелых Т-лимфоцитов (CD3+), Т-хелперов (CD4+) и фагоцитарной активности нейтрофилов прослеживалось у больных подгруппы Галавита и спустя 4,5 месяца после оперативного вмешательства, в то время как в контрольной подгруппе указанные параметры достоверно не изменялись на протяжении всего периода наблюдения.
Таблица №10. ^ Послеоперационная динамика показателей клеточного иммунитета у больных подгрупп Б и Г.
| | Контрольная подгруппа Б (М±m) | Исследуемая подгруппа Г(М±m). | ||||
| Показатель | До операции (n=25) | 1,5 месяца после операции (n=20) | 4,5месяца после операции (n=18) | До операции (n=23) | 1,5 месяца после операции (n=21) | 4,5 месяца после операции (n=20). |
| CD3+(%) | 52,6±1,68 | 52,9±1,34 | 54,1±1,28 | 54,1±1,14 | 59,3±1,15** | 64,5±1,01** |
| CD4+ (%) | 31,1±1,01 | 30,6±0,74 | 31,2±1,0 | 31,0±1,08 | 35,3±1,14** | 36,4±0,8** |
| ФА(%) (Фагоц. активность) | 48,7± 2,01 | 49± 2,01 | 51,1± 1,17 | 48,6± 1,2 | 56,1± 1,2** | 58,5±1,34** |
*- сравнение с данными контрольной подгруппы
**-различие достоверно р≤0,01
При исследовании послеоперационной динамики уровня аутоантител у больных второй группы было установлено, что спустя 1,5 месяца после оперативного вмешательства у больных, пролеченных Галавитом, происходит достоверное увеличение уровня аутоантител к эластину, с последующей нормализацией данного показателя к 4,5 месяцам, в то время как в контрольной подгруппе Б уровень аутоантител к эластину достоверно не менялся на протяжении всего периода наблюдения, а уровень аутоантител к коллагену оставался без изменений как в контрольной, так и в исследуемой подгруппах. По нашим данным, противофиброзирующее действие препарата галавит проявляется в быстром выводе цитотоксических аутоантител к эластину из зоны операции с последующей их элиминацией к 4,5 месяцам после проведенного оперативного лечения.
Таблица №11. ^ Послеоперационная динамика уровня аутоантител у больных подгрупп Б и Г.
| | Контрольная подгруппа Б (М±m) | Исследуемая подгруппаГ (М±m) | ||||
| Показатель (усл.единицы) | До операции (n=25) | 1,5 месяца после операции (n=20) | 4,5 месяца после операции (n=18) | До операции (n=23) | 1,5 месяца после операции (n=21) | 4,5 месяца после операции (n=20) |
| Уровень антител к коллагену | 0,1±0,01 | 0,1±0,01 | 0,1±0,01 | 0,13±0,01 | 0,12±0,01 | 0,12±0,01 |
| Уровень антител к эластину. | 0,12±0,01 | 0,13±0,01 | 0,13±0,01 | 0,14±0,01 | 0,16±0,01* | 0,12±0,01 |
*- сравнение с результатами контрольной подгруппы
*-различие достоверно р≤0,01
Р
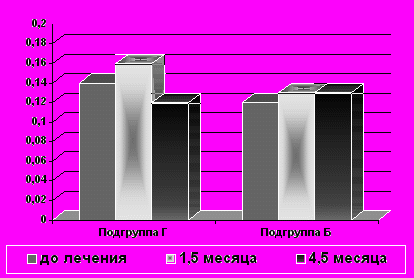 ис. №2 ^ Послеоперационная динамка уровня аутоантител к эластину.
ис. №2 ^ Послеоперационная динамка уровня аутоантител к эластину.*
*- различие достоверно р≤0,01
3. Результаты лечения больных третьей группы.
Больные хроническим простатитом с сопутствующим склерозом шейки мочевого пузыря находились под наблюдением в течении 12 месяцев после оперативного вмешательства.
После выполнения оперативного вмешательства у 14 больных данной группы были получены следующие результаты: стойкое исчезновение признаков инфравезикальной обструкции отмечалось у 12 больных этой группы, у 2 больных в течение 1 года развился рецидив склероза шейки мочевого пузыря, потребовавший повторного оперативного вмешательства.
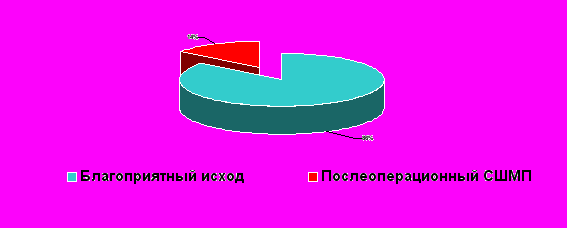
Результаты оперативного лечения больных хроническим простатитом с сопутствующим склерозом шейки мочевого пузыря свидетельствуют, что благоприятные отдаленные результаты, по нашим данным, наблюдаются в 86% случаев.
Таким образом, несмотря на применение современных эндоскопических методов лечения данного заболевания, в 14% случаев возможно возникновение послеоперационного склероза шейки мочевого пузыря, что диктует необходимость разработки методов профилактики и для этой категории больных и представляет интерес для дальнейших исследований.
Рис. №3 ^ Результаты лечения больных третьей группы (n=14).
Результаты морфологического исследования
В ходе анализа морфологической картины тканей предстательной железы и шейки мочевого пузыря было отмечено, что ни распространенное гнойное воспаление предстательной железы, ни локальное продуктивное воспаление, ни конкременты простаты, сами по себе, не приводят к развитию склероза шейки мочевого пузыря. Нами была установлена взаимосвязь морфологических изменений и иммунологических параметров. В ходе исследования было отмечено, что распространение воспаления в подслизистый слой шейки мочевого пузыря сопровождается повышением уровня аутоанител к эластину. Также было выявлено, что сохранение повышенного уровня аутоантител к эластину спустя 4,5 месяца после операции может свидетельствовать о формировании послеоперационного СШМП.
Таким образом, по результатам проведенного исследования, из всех исследованных больных хроническим простатитом с симптомами нарушений мочеиспускания, только у 18% пациентов не было выявлено другого заболевания, ответственного за возникновение вышеуказанных нарушений. В остальных случаях, после тщательного обследования и уточнения диагноза, была выявлена другая патология (СШМП или ДГПЖ), которая и послужила причиной возникновения нарушений мочеиспускания.
ВЫВОДЫ
1.Стандартный диагностический алгоритм у больных хроническим простатитом с нарушением мочеиспускания целесообразно дополнить исследованием иммунного статуса (фенотипированием лимфоцитов, исследованием уровня ЦИК и уровня аутоантител к эластину) для выявления предрасположенности к развитию рубцово-склеротических осложнений.
2.У больных хроническим простатитом с выраженными симптомами нарушений мочеиспускания и склеротическими изменениями тканей предстательной железы определяется повышенный уровень аутоантител к коллагену.
3. Критерием предрасположенности формирования рубцово-склеротических осложнений у больных хроническим простатитом, сочетающимся с доброкачественной гиперплазией предстательной железы, является повышенный уровень аутоантител к эластину.
4.Механизм, приводящий к рубцеванию шейки мочевого пузыря у больных хроническим простатитом, в сочетании с ДГПЖ, реализуется на клеточном уровне и проявляется в угнетении Т-звена иммунной системы, снижении уровня ЦИК 3% и повышении уровня аутоантител к эластину.
5.Степень вовлечения предстательной железы в воспалительный процесс не влияет на возможность возникновения послеоперационных осложнений рубцово-склеротического характера после трансуретральной резекции предстательной железы.
6.Применение 1-адреноблокаторов в лечении хронического простатита с симптомами нарушений мочеиспускания показано больным с ирритативной симптоматикой при нормальном уровне аутоантител к эластину.
7.Применение иммуномодулятора Галавит в комплексной терапии больных хроническим простатитом, подвергающихся оперативному вмешательству на предстательной железе, позволяет уменьшить риск возникновение ранних (инфекционно-воспалительных) и поздних (рубцово-склеротических) послеоперационных осложнений.
^
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1.Повышенный уровень аутоантител к эластину у больных ХП в большинстве случаев указывает на наличие другой патологии, ответственной за возникновение нарушений мочеиспускания, и может служить дополнительным критерием ранней диагностики доброкачественной гиперплазии предстательной железы у больных ХП. Сочетание повышенного уровня аутоантител к эластину и снижение уровня ЦИК3%, может указывать на возможность склероза шейки мочевого пузыря у больных ХП.
2.Предоперационное обследование больных ХП, сочетающимся с ДГПЖ, целесообразно дополнить фенотипированием лимфоцитов и исследованием уровня аутоантител к эластину, для выявления лиц, предрасположенных к развитию послеоперационных осложнений. Ранние послеоперационные осложнения (инфекционно-воспалительные) характерны для больных с угнетением Т-звена иммунной системы, а появление поздних (рубцово-склеротических) - возможно у больных с повышенным уровнем аутоантител к эластину.
3.Перед назначением 1-адреноблокаторов больным ХП с нарушением мочеиспускания необходимо провести комплексное обследование для исключения другой патологии, способной вызвать данные нарушения, особенно у больных с инфравезикальной обструкцией и повышенным уровнем аутоантител к эластину.
4.Для профилактики развития послеоперационных осложнений у больных ХП с ДГПЖ, целесообразно назначение иммуномодулятора Галавит, особенно у лиц с угнетением Т-звена иммунной системы, а также у больных с повышенным уровнем аутоантител к эластину.
5.При двухэтапном лечении больных ХП с ДГПЖ, в случае повышения аутоантител к эластину, ТУРП целесообразно сочетать с эндоскопической коррекцией шейки мочевого пузыря.
6.Послеоперационное обследование больных ХП с ДГПЖ целесообразно дополнить исследованием уровня аутоантител к эластину. Сохранение повышенного уровня аутоантител к эластину, спустя 4,5 месяца после оперативного вмешательства, указывает на возможность развития послеоперационного склероза шейки мочевого пузыря.
^ Список работ, опубликованных по теме диссертации
- Мисник А.В. Этиопатогенез, диагностика и лечение нарушений мочеиспускания у больных хроническим простатитом./ Андрология и генитальная хирургия №2 , 2002, с 6-16.
- Кан Я.Д., Мисник А.В., Вишневский А.Е. Использование иммуномодулятора галавит у больных доброкачественной гиперплазией предстательной железы, сочетающейся с хроническим простатитом./ Материалы X-Российского съезда урологов, Москва 2002, с 118-119.
- Мисник А.В., Кан Я.Д., Кочетов М.М. Использование иммуномодулятора галавит у больных доброкачественной гиперплазией предстательной железы, сочетающейся с хроническим простатитом./ Аллергология и иммунология №2, том 4, 2003, с 145.
- Гришина Т.И., Кан Я.Д., Мисник А.В. Результаты исследования иммунного статуса у больных склерозом шейки мочевого пузыря./ Российский аллергологический журнал. 2007 №3, с 336.
