Лицензированная медсестра, Эрик Ван Вийнгаерден, доктор медицинских наук, Херман Боббаерс, доктор медицинских наук, и Роджер Боуиллон, доктор медицинских наук
| Вид материала | Документы |
- «Дагестанская государственная медицинская академия Федерального агентства по здравоохранению, 546.66kb.
- В. О. Бернацкий доктор философских наук, профессор; > А. А. Головин доктор медицинских, 5903.36kb.
- «Российский научный центр восстановительной медицины и курортологии Росздрава», 372.3kb.
- Лазерная фотодинамическая терапия ожоговых ран (экспериментальное исследование) 14., 295.89kb.
- Демидчик Ю. Е. доктор медицинских наук, член-корр. Нанб, профессор, ректор Белмапо,, 970.61kb.
- Халиф Игорь Львович Доктор медицинских наук, профессор Бредихина Наталия Андреевна, 579.47kb.
- Рохлина Майя Леоновна доктор медицинских наук, профессор Игонин Андрей Леонидович доктор, 564.38kb.
- Рецензенты: доктор медицинских наук А. М. Иваницкий, доктор медицинских наук, 4659.36kb.
- Sante Bureau Regional de l'Europe Всемирная Организация Здравоохранения Европейское, 677.15kb.
- Бахметьев Владимир Иванович Ведущая организация : Государственное общеобразовательное, 587.63kb.
^ ПОКАЗАТЕЛИ РЕЗУЛЬТАТОВ
Первичным показателем результата была смерть в больнице по любой причине. Вторичными, предопределенными показателями результатов были: смерть в отделении интенсивной терапии, смерть в течение 90 дней, количество дней до отучения от искусственной вентиляции легких, количество дней, проведенных в отделении интенсивной терапии и в больнице, начало диализа, новое поражение почек, возникшее в течение интенсивной терапии (либо превышение уровня креатинина в сыворотке крови в два раза по сравнению со значением при поступлении в отделение интенсивной терапии,23 либо максимальный уровень креатинина в сыворотке крови >2,5 мг на децилитр [220 ммоль на литр]), количество дней, в течение которых применялась инотропная или вазопрессорная поддержка, наличие или отсутствие гипервоспаления (уровень С-реактивного белка >150 мг на децилитр), наличие или отсутствие бактериемии, продолжительный (т.е., в течение более чем 10 дней) прием антибиотиков, а также наличие или отсутствие гипербилирубинемии (уровень билирубина >3 мг на децилитр [51 ммоль на литр]). Использование ресурсов интенсивной терапии оценивалось на основании совокупных показателей по шкале TISS-28 (сумма ежедневных показателей), показывающей общее количество случаев терапевтического вмешательства на одного пациента.19 Мы выполнили предопределенный анализ подгруппы для пациентов, проходящих лечение в отделении интенсивной терапии в течение минимум трех дней. Из вторичного исследовательского анализа смертности исключались данные пациентов, прошедших неполный курс интенсивной терапии, или пациентов, которым лечащий врач отменил интенсивную терапию в течение 72 после поступления в отделение, так как данный вид лечения оказался бесполезным.
Для снижения вероятности систематических ошибок при определении продолжительности пребывания в отделении интенсивной терапии, которые могут возникать в связи с задержкой в перевозке пациентов в обычную палату по причине нехватки мест, считалось, что пациенты готовы к выписке из отделения в тот момент, когда больше нет необходимости поддержки функций жизненно важных органов и когда пациенты начинают получать минимум две трети от необходимых калорий энтернальным путем или когда их перемещают в обычную палату. Врачи, наблюдавшие за пациентами, прошедшими курс интенсивной терапии, после их перемещения в обычные палаты, не имели доступа к результатам тестирования уровня глюкозы в крови и не знали о задачах исследования.
| Таблица 1. Характеристики пациентов до начала исследования.* | ||||||
| Параметр | Группа пациентов в соответствии с назначенным лечением | ^ Пациенты, проходившие лечение в ОИТ в течение ≥3 дней | ||||
| | Традиционная терапия (N = 605) | Интенсивная терапия (N = 595) | P-значение | Традиционная терапия (N = 381) | Интенсивная терапия (N = 386) | P-значение† |
| Мужской пол – кол-во (%) Возраст (лет) ИМТ Диагностическая категория – кол-во (%) пациентов в данной категории Заболевания органов дыхания Заболевания желудочно-кишечного тракта или печени Гематологические или онкологические заболевания Другой сепсис Заболевания сердечно-сосудистой системы Неврологические заболевания Заболевания почек Болезни обмена веществ Прочие заболевания Анамнез рака – кол-во (%) Вызванная диализом почечная недостаточность до острого приступа – кол-во (%) Почечная недостаточность при поступлении в отделение интенсивной терапии – кол-во (%)‡ Анамнез диабета – кол-во (%) Лечение инсулином Лечение с использованием пероральных противодиабетических средств, диеты или обоих способов Исходные данные по шкале APACHE II § Средний показатель >40 – кол-во (%) Исходные данные по шкале TISS-28 ¶ Средний показатель >33 – кол-во (%) Уровень глюкозы в крови при поступлении – мг/дл Уровень гликозилированного гемоглобина при поступлении – %‖ Уровень креатинина в плазме крови при поступлении – мг/дл Среднее значение Вероятное отклонение Уровень мочевины в плазме крови при поступлении – мг/дл Среднее значение Вероятное отклонение Уровень аланин-аминотрансферазы в плазме крови при поступлении – IU/литр Среднее значение Вероятное отклонение Уровень С-реактивного белка в плазме крови при поступлении – мг/литр Среднее значение Вероятное отклонение | 382 (63,1) 64±16 24,8±5,1 261 (51,0) 152 (49,7) 51 (52,6) 45 (50,0) 24 (48,0) 31 (50,8) 20 (45,5) 11 (55,0) 10 (50,0) 128 (21,2) 37 (6,1) 120 (19,8) 97 (16,0) 51 (8,4) 46 (7,6) 23±9 18 (3,0) 29±7 125 (20,6) 162±70 6,2±0,9 1,2 0,9–2,1 67 40–110 29 15–64 124 39–226 | 356 (60) 63±16 25,1±5,5 251 (49,0) 154 (50,3) 46 (47,4) 45 (50,0) 26 (52,0) 30 (49,2) 24 (54,5) 9 (45,0) 10 (50,0) 134 (22,5) 37 (6,2) 119 (20,0) 106 (17,8) 65 (10,9) 41 (6,9) 23±10 26 (4,4) 29±7 158 (26,6) 162±71 6,3±0,9 1,2 0,8–2,1 65 36–104 30 16–63 108 36–218 | 0,24 0,61 0,29 0,99 0,57 0,94 0,94 0,41 0,50 0,19 0,45 0,02 0,98 0,12 0,25 0,26 0,50 0,27 | 243 (64) 64±16 24,6±5,1 172 (47,9) 89 (55,6) 37 (48,7) 30 (46,9) 15 (45,5) 14 (50,0) 11 (45,8) 10 (66,7) 3 (37,5) 90 (23,6) 29 (7,6) 92 (24,1) 58 (15,2) 27 (7,0) 31 (8,1) 24±9 11 (2,9) 30±7 96 (25,2) 164±68 6,2±0,9 1,4 0,9–2,4 71 45–115 33 17–77 146 55–236 | 224 (58) 62±16 25,4±5,9 187 (52,1) 71 (44,4) 39 (51,3) 34 (53,1) 18 (54,5) 14 (50,0) 13 (54,2) 5 (33,3) 5 (62,5) 98 (25,4) 31 (8,0) 82 (21,2) 59 (15,3) 41 (10,6) 18 (4,7) 24±10 18 (4,7) 31±7 129 (33,4) 163±67 6,3±0,9 1,3 0,8–2,1 69 37–106 31 17–63 132 48–229 | 0,10 0,20 0,06 0,70 0,57 0,83 0,34 0,98 0,95 0,19 0,46 0,01 0,87 0,21 0,06 0,16 0,55 0,31 |
| * ± значения означает среднее значение ± стандартные отклонения. Для перевода значений для глюкозы в миллимоль на литр необходимо умножить значение на 0,05551. Для перевода значений для мочевины в миллимоль на литр необходимо умножить значение на 0,357. ОИТ означает отделение интенсивной терапии, ИМТ – индекс массы тела (вес в килограммах, разделенный на рост в метрах, возведенный в квадрат), APACHE II – Система физиологических критериев острых и хронических физиологических нарушений, TISS-28 – Система оценки агрессивности терапевтических вмешательств. † P-значения для проведения сравнения между группой традиционной терапии и группой интенсивной терапии были подсчитаны с использованием t-критерия Стьюдента, критерия Манна-Уитни и критерия хи-квадрат, в зависимости от ситуации. ‡ Почечная недостаточность при поступлении в отделение интенсивной терапии определялась как зависимая от диализа или уровень креатинина в сыворотке крови >2,5 мг на децилитр. перевода значений для креатинина в миллимоль на литр необходимо умножить значение на 88,4. § Более высокие значения по шкале APACHE II указывают на более тяжелое заболевание, значение, превышающее 40 указывает на процентиль 90, что означает наиболее тяжелую форму заболеванию. ¶ Согласно шкале TISS-28, каждому терапевтическому вмешательству приписывается ряд очков, при этом более высокие очки соответствуют большему числу терапевтических вмешательств. Сумма очков подсчитывается ежедневно для каждого пациента. Сумма превышающая 33 – верхний лимит вероятных отклонений. ‖ Уровень гликозилированного гемоглобина был определен с помощью иммунотурбодиметрического анализа (Dimension, Dade Behring) (норма – от 4 до 6 процентов). | ||||||
^ СТАТИСТИЧЕСКИЙ АНАЛИЗ
На основании данных нашего предыдущего исследования,5 мы выдвинули гипотезу об абсолютном снижении риска смерти на 7 процентов после минимум трех дней интенсивной инсулинотерапии.
Для проверки данной гипотезы нам потребовалось провести статистическую выборку данных 1200 пациентов на предмет двустороннего альфа-уровня менее 0,05 и бета-уровня 0,2 в целевой группе пациентов, продолжительность пребывания которых в отделении интенсивной терапии составила три дня или более.
Было проведено сравнение параметров до начала исследования и после его окончания с использованием t-критерия Стьюдента, критерия хи-квадрат и критерия Манна-Уитни, в зависимости от ситуации. Эффект терапевтического вмешательства на момент смерти в больнице оценивался с использованием анализа выживаемости Каплан-Мейера и регрессионного анализа пропорциональных рисков. Пациенты, благополучно выписанные из больницы, назывались выжившими. Относительный риск смерти, рассчитанный с использованием регрессионного анализа пропорциональных рисков, был исправлен на широко известные клинически обоснованные исходные факторы риска. Эффект на момент отучения от искусственной вентиляции легких и на момент выписки из отделения интенсивной терапии оценивался с помощью анализа совокупного риска и регрессионного анализа пропорциональных рисков, с исключением случаев ранней смерти.
Представлены средние значения ± стандартные отклонения или срединные значения (с вероятными отклонениями), если нет иных указаний. Анализы группы всех включенных пациентов и группы пациентов, продолжительность пребывания которых в отделении интенсивной терапии составила три дня или более, был проведен отдельно. В целях сравнения с результатами нашего предыдущего исследования в отделении интенсивной хирургии,5 здесь также приведены данные по пациентам, продолжительность пребывания которых в отделении интенсивной терапии составила пять дней или более. Значения P не были откорректированы для множественного значения. Спонсоры исследования не вовлекались в процесс исследования, сбор, анализ или толкование данных или в подготовку настоящего документа.
РЕЗУЛЬТАТЫ
^ ПИТАНИЕ И РЕГУЛИРОВАНИЕ УРОВНЯ ГЛЮКОЗЫ В КРОВИ
В таблице 1 приведены исходные показатели при поступлении в отделение всех 1200 пациентов, включенных в исследование, включая данные 767 пациентов, продолжительность пребывания которых в отделении интенсивной терапии составила минимум три дня. Показатели по питанию и уровню глюкозы в крови приведены на Рисунке 2 (дозы инсулина указаны в Таблице А Дополнительного приложения к полному тексту настоящей статьи, выложенного в Интернете по адресу ссылка скрыта). Гипогликемия чаще возникала в группе интенсивной терапии, чем в группе традиционной терапии. У большинства пациентов наблюдался только один приступ. Тяжесть гипогликемии в обеих группах была схожей (Таблица А Дополнительного приложения). В связи с приступами гипогликемии не отмечалось ухудшения гемодинамики, конвульсий или подобных проявлений. Смертность в отделении интенсивной терапии среди пациентов с гипогликемией составила 66,7 процентов в группе традиционной терапии, по сравнению с 46,4 процентами в группе интенсивной терапии (P = 0,1); смертность в больнице составила 73,3 процента и 61,9 процента, соответственно (P = 0.4). Двое из группы традиционной терапии и трое из группы интенсивной терапии умерли в течение 24 часов после приступа гипогликемии. Независимые факторы риска гипогликемии, помимо интенсивной инсулинотерапии (вероятность успешного исхода, 7,50; доверительный интервал 95 процентов, от 4,50 до 12,50; P<0,001), включали в себя пребывание в отделении интенсивной терапии в течение трех и более дней (вероятность успешного исхода, 3,33; доверительный интервал 95 процентов, от 1,95 до 5,70; P<0,001), почечная недостаточность с необходимостью применения диализа (вероятность успешного исхода, 1,94; доверительный интервал 95 процентов, от 1,19 до 2,84; P = 0,006) и печеночная недостаточность, т.е. уровень аланин-аминотрансферазаы выше 250 единиц на литр (вероятность успешного исхода, 1,62; доверительный интервал 95 процентов, от 1,01 до 2,60; P = 0,04).
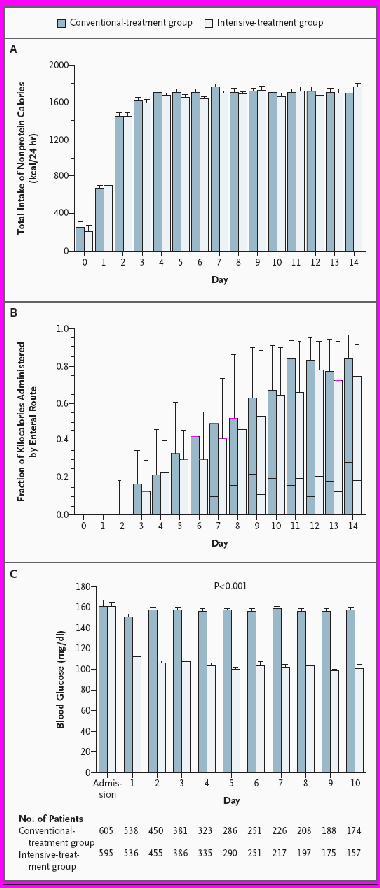 Группа традиционной терапии   Группа интенсивной терапии  День День День Кол-во пациентов: Группа трад. терапии Группа инт. терапии Поступление | Рисунок 2. Питание всех 1200 пациентов в течение первых 14 дней интенсивной терапии и ежедневное измерение уровня глюкозы в крови с утра в течение первых 10 дней интенсивной терапии. В колонке A, питание на отметке 0 означает питание пациентов, принятых в отделение интенсивной терапии после полуночи, между принятием и 7.00, 1 – означает питание в первый день после принятия в отделение, начиная с 7.00. Питание в обеих группах было схожим. Общее число килокалорий дано как среднее значение ± стандартные отклонения. В колонке B, доля питательных веществ, полученных посредством энтерального питания выражена как среднее значение (горизонтальные полосы в столбиках) и вероятные отклонения (процентиль 90 указан в столбике I). В колонке C: у пациентов, пребывание которых в отделении интенсивной терапии составило 3 дня и более, интенсивная инсулинотерапия продолжалась до выписки из отделения (в среднем 12,5 дней, отклонение до 65 дней). P<0,001 для сравнения между двумя группами. Для перевода значений для глюкозы в миллимоль на литр необходимо умножить значение на 0,05551. |
| | |
| |
^ УРОВЕНЬ ЗАБОЛЕВАЕМОСТИ
Пациенты, включенные в исследование
Среди пациентов, включенных в исследование, при приеме других препаратов, кроме инсулина, разница между двумя группами не была статистически значимой. Из 1200 пациентов, включенных в исследование, 9 принимали активированный протеин С для лечения септического шока, 5 из них – в группе традиционной терапии и 4 – в группе интенсивной терапии (P = 0,8). Из 644 пациентов, принимавших кортикостероиды, 327 входили в группу традиционной терапии и 317 – в группу интенсивной терапии (P = 0,8). Лечение кортикостероидами состояло, в основном, в приеме метилпреднизолона, обладающего иммунодепрессивным и антивоспалительным действием (средняя доза 40 мг [вероятное отклонение от 24 до 75] в день, для 233 пациентов в группе традиционной терапии и средняя доза 40 мг [вероятное отклонение от 29 до 65] в день, для 249 пациентов в группе интенсивной терапии; P>0,9). Кортизол назначался в случае предполагаемой надпочечниковой недостаточности, средняя доза 125 мг (вероятное отклонение от 100 до 193) в день, для 129 пациентов в группе традиционной терапии, и средняя доза 135 мг (вероятное отклонение от 100 до 240) в день, для 118 пациентов в группе интенсивной терапии (P = 0,2). Пятеро пациентов, двое в группе традиционной терапии и трое в группе интенсивной терапии, принимали дексаметазон, средняя суточная доза 10 мг (P>0,9).
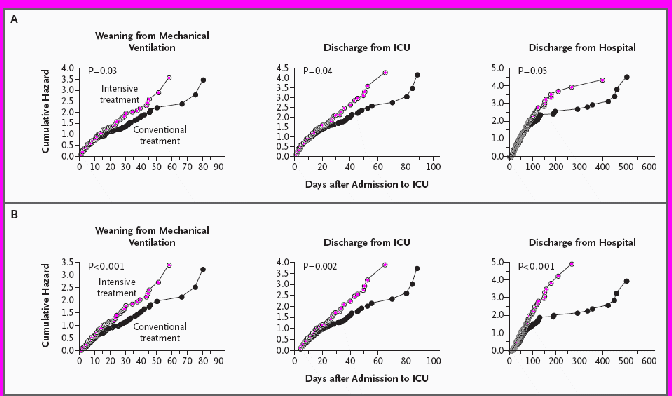
В группе интенсивной терапии уровень заболеваемости был снижен за счет сокращения количества случаев вновь приобретенной почечной недостаточности (с 8,9 до 5,9 процентов, P = 0,04) и более раннего отучения от искусственной вентиляции легких, по сравнению с группой традиционной терапии (относительный риск 1,21; доверительный интервал 95 процентов, от 1,02 до 1,44; P = 0,03), а также более ранняя выписка из отделения интенсивной терапии (относительный риск 1,15; доверительный интервал 95 процентов, от 1,01 до 1.32; P = 0,04) и из больницы (относительный риск 1,16; доверительный интервал 95 процентов, от 1,00 до 1,35; P = 0,05) (Рисунок 3). Не наблюдалось статистически значимого влияния на бактериемию (снижение, от 7 до 8 процентов; P = 0,5), необходимость продолжительного приема антибактериальных препаратов (снижение, от 24 до 21 процентов; P = 0,2), гипербилирубинемия (снижение, от 27 до 25 процентов; P = 0,4), гипервоспаление
(снижение, от 61 до 56 процентов; P = 0,1), или совокупные показатели по шкале TISS-28 (снижение, от 308±16 до 272±13; P = 0,08). Коэффициенты повторного поступления в отделение интенсивной терапии близки по значению в обеих группах (6,3 процента).
^ Продолжительность пребывания в отделении интенсивной терапии в течение более чем трех дней
Среди 767 пациентов, продолжительность пребывания которых в отделении интенсивной терапии составила более трех дней, при приеме других препаратов, кроме инсулина, разница между двумя группами не была статистически значимой. У 386 пациентов, включенных в группу интенсивной терапии, интенсивная терапия в течение минимум трех дней привела к более раннему отучению от искусственной вентиляции легких, по сравнению с традиционной терапией (относительный риск 1,43; доверительный интервал 95 процентов, от 1,16 до 1,75; P<0,001), более ранней выписке из отделения интенсивной терапии (относительный риск 1,34; доверительный интервал 95 процентов, от 1,12 до 1,61; P = 0,002) и выписке из больницы (относительный риск 1,58; доверительный интервал 95 процентов, от 1,28 до 1,95; P<0,001) (Рисунок 3).
В группе традиционной терапии, 28,6 процентам пациентов назначался лечебный диализ, по сравнению с 27,2 процентами пациентов группы интенсивной терапии (P = 0,7). Снижение случаев применения диализа у пациентов, которым не требовался диализ до поступления в отделения интенсивной терапии, не было статистически значимым (22,7 процентов в группе традиционной терапии и 20,8 процентов в группе интенсивной терапии, P = 0,5). Однако было снижено количество случаев вновь приобретенного поражения почек после рандомизации, которое определяется как превышение уровня креатинина в сыворотке крови в два раза по сравнению со значением при поступлении в отделение интенсивной терапии (12,6 процентов в группе традиционной терапии и 8,3 процентов в группе интенсивной терапии, P = 0,05), а у части пациентов – как достижение максимального уровня креатинина в сыворотке крови, превышающего 2,5 мг на децилитр (39,4 и 32,5 процентов, соответственно; P = 0,04). Гипербилирубинемия наблюдалась у 55,2 процентов пациентов группы традиционной терапии и 47,3 процентов пациентов группы интенсивной терапии (P = 0,04). Уровни аланин-аминотрансферазы и аспартат-аминотрансферазы в обеих группах были близки по значению.
Снижение количественного соотношения пациентов с бактериемией (11,3 процентов) или вторичной бактериемией (7,3 процентов) или пациентов, принимающих антибактериальные препараты в течение продолжительного периода, (37,6 процентов в группе традиционной терапии и 31,9 процентов в группе интенсивной терапии, P = 0,09) не было статистически значимым. Однако интенсивная инсулинотерапия привела к снижению частоты возникновения гипервоспаления с 74 процентов в группе традиционной терапии до 67 процентов в группе интенсивной терапии (P = 0,03).
Интенсивная инсулинотерапия привела к снижению совокупных показателей по шкале TISS-28 у пациентов отделения интенсивной терапии на 20 процентов (454±22 в группе традиционной терапии по сравнению с 388±17 в группе интенсивной терапии, P = 0,02), что приводит к сокращению стоимости интенсивной терапии.19,20 Среди пациентов, подвергнутых рандомизации, чье пребывание в отделении интенсивной терапии составило менее трех дней, разница между предельными значениями уровня заболеваемости в двух группах не была статистически значимой. Изучение случаев продолжительности интенсивной инсулинотерапии в течение более пяти дней также показало улучшение предельных значений уровня заболеваемости, однако эффект среди пациентов, проходивших лечение в течение менее пяти дней не был выявлен.
^ Отучение от искусственной вентиляции легких
Отучение от искусственной вентиляции легких
Выписка из отделения интенсивной терапии
Выписка из отделения интенсивной терапии
^ Выписка из больницы
Выписка из больницы
Дней после поступления в отделение интенсивной терапии
Дней после поступления в отделение интенсивной терапии
| Рисунок 3. Влияние интенсивной инсулинотерапии на смертность. Влияние интенсивной инсулинотерапии на момент отучения от искусственной вентиляции легких, на момент выписки из отделения интенсивной терапии и на момент выписки из больницы показан для всех пациентов (анализ всех включенных пациентов, Колонка A) и для подгруппы, состоящей из 767 пациентов, продолжительность пребывания которых в отделении интенсивной терапии составила три или более дней (Колонка B). P-значения для сравнения групп подсчитывались с помощью регрессионного анализа пропорциональных рисков, с исключением случаев ранних смертей. Пациенты обозначены кружками. |
