Р. Н. Аляутдина 2-е издание, исправленное Рекомендовано умо по медицинскому Допущено Министерством образования и фармацевтическому образованию вузов Российской Федерации в качестве России в качестве учебник
| Вид материала | Учебник |
- С. Н. Федоров Н. С. Ярцева А. О. Исманкулов Глазные болезни Рекомендовано умо по медицинскому, 11325.47kb.
- С. В. Дьякова стоматология детского возраста издание пятое, переработанное и дополненное, 7200.9kb.
- Г. В. Плеханова И. Н. Смирнов, В. Ф. Титов философия издание 2-е, исправленное и дополненное, 4810.28kb.
- Н. С. Елманова История международных отношений и внешней политики России 1648-2000, 4874.79kb.
- В. И. Королева Москва Магистр 2007 Допущено Министерством образования Российской Федерации, 4142.55kb.
- Ю. А. Бабаева Допущено Министерством образования Российской Федерации в качестве учебник, 7583.21kb.
- Отечественная история, 1627.22kb.
- К. Э. Фабри Основы зоопсихологии 3-е издание Рекомендовано Министерством общего и профессионального, 5154.41kb.
- Т. В. Корнилова экспериментальная психология теория и методы допущено Министерством, 5682.25kb.
- Т. В. Корнилова экспериментальная психология теория и методы допущено Министерством, 5682.25kb.
| Механизм действия | Антибиотики | Преимущественный характер антимикробного действия |
| Нарушение синтеза клеточной стенки | β-лактамиды Гликопептидные антибиотики Циклосерин Бацитрацин | Бактерицидный « « |
| Нарушение проницаемости цитоплазматической мембраны | Полимиксины Полиеновые антибиотики | Бактерицидный « |
| Нарушение внутриклеточного синтеза белка | Макролиды Тетрациклины Линкозамиды Левомицетин Аминогликозиды | Бактериостатический « « « Бактерицидный |
| Нарушение синтеза РНК | Рифампицин | Бактерицидный |
узкого спектра действия. Вторую группу в свою очередь можно разделить на антибиотики, действующие преимущественно на грамположительную микрофлору (биосинтетические пенициллины, макролиды) и антибиотики, действующие преимущественно на грамотрицательную микрофлору (полимиксины). Кроме того, различают противогрибковые и противоопухолевые антибиотики.
По клиническому применению выделяют основные антибиотики, с которых начинают лечение до определения чувствительности к ним микроорганизмов, вызвавших заболевание, и резервные, которые применяют при устойчивости микроорганизмов к основным антибиотикам или при непереносимости последних.
В процессе применения антибиотиков к ним может развиться устойчивость (резистентность) микроорганизмов, т.е. способность микроорганизмов размножаться в присутствии терапевтической дозы антибиотика. Резистентность микроорганизмов к антибиотикам может быть природной и приобретенной.
Природная устойчивость связана с отсутствием у микроорганизмов «мишени» для действия антибиотика или недоступности «мишени» вследствие низкой проницаемости клеточной стенки, а также ферментативной инактивации антибиотика. При наличии у бактерий природной устойчивости антибиотики клинически неэффективны.
Под приобретенной устойчивостью понимают свойство отдельных штаммов бактерий сохранять жизнеспособность при тех концентрациях антибиотиков, которые подавляют основную часть микробной популяции. Приобретенная устойчивость является либо результатом спонтанных мутаций в генотипе бактериальной клетки, либо связана с передачей плазмид от естественно-устойчивых бактерий к чувствительным видам.
Известны следующие биохимические механизмы устойчивости бактерий к антибиотикам:
- ферментативная инактивация препаратов;
- модификация «мишени» действия антибиотиков;
- активное выведение антибактериальных препаратов из микробной клетки;
- снижение проницаемости клеточной стенки бактерий;
- формирование метаболического «шунта».
Устойчивость микроорганизмов к антибиотикам может иметь групповую специфичность, т.е. не только к применяемому препарату, но и к другим препаратам из той же химической группы. Такая устойчивость называется «перекрестной».
Соблюдение принципов применения химиотерапевтических средств позволяет уменьшить вероятность возникновения устойчивости.
Несмотря на то, что антибиотики характеризуются высокой избирательностью действия, тем не менее они оказывают целый ряд побочных эффектов аллергической и неаллергической природы.
БЕТА-ЛАКТАМНЫЕ АНТИБИОТИКИ
Бета-лактамные антибиотики - это лекарственные средства, имеющие в составе молекулы р-лактамный цикл: пенициллины, цефалоспорины, карбапенемы и монобактамы.
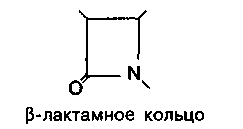
(β-лактамный цикл необходим для проявления противомикробной активности этих соединений. При расщеплении (β-лактамного цикла бактериальными ферментами (р-лактамазами) антибиотики утрачивают антибактериальное действие.
Все бета-лактамные антибиотики обладают бактерицидным эффектом, в основе которого лежит угнетение ими синтеза клеточной стенки бактерий. Антибиотики этой группы нарушают синтез пептидогликана-биополимера, являющегося основным компонентом клеточной стенки бактерий. Пептидогликан состоит из полисахаридов и полипептидов.
В состав полисахаридов входят аминосахара-ацетилглюкозамин и N-аце-тилмурамовая кислота. С аминосахарами связаны короткие пептидные цепи. Окончательную жесткость клеточной стенке придают поперечные пептидные цепочки, состоящие из 5 остатков глицина (пентаглициновые мостики). Синтез пептидогликана протекает в 3 стадии: 1) в цитоплазме синтезируются предшественники пептидогликана (ацетилмурамилпентапептид и ацетилглюкозамин), которые переносятся через цитоплазматическую мембрану с участием липидно-го транспортера, ингибируемого бацитрацином; 2) включение этих предшественников в растущую полимерную цепь; 3) образование поперечных связей между двумя соседними цепями в результате реакции транспептидирования, катализируемой ферментом-транспептидазой пептидогликана.
Процесс расщепления пептидогликана катализирует фермент-муреингидро-лаза, активность которого в нормальных условиях сдерживается эндогенным ингибитором.
Бета-лактамные антибиотики ингибируют:
а) транспептидазу пептидогликана, что приводит к нарушению образования
пептидогликана;
б) эндогенный ингибитор, что приводит к активации муреингидролазы, рас
щепляющей пептидогликан.
Бета-лактамные антибиотики малотоксичны для макроорганизма, так как мембраны клеток человека не содержат пептидогликана. Антибиотики этой группы эффективны преимущественно в отношении делящихся, а не «покоя-
щихся» клеток, поскольку в клетках, находящихся в стадии активного роста, синтез пептидогликана происходит наиболее интенсивно.
ПЕНИЦИЛЛИНЫ
В основе строения пенициллинов лежит 6-аминопенициллановая кислота (6-АПК), которая представляет собой гетероциклическую систему, состоящую из 2 конденсированных колец: четырехчленного-(β-лактамного (А) и пятичленного-тиазолидинового (В).
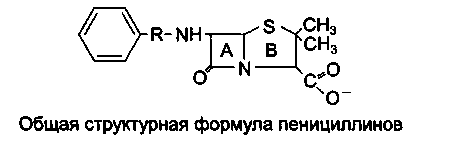
Пенициллины отличаются друг от друга строением ацильного остатка у аминогруппы 6-АПК.
Все пенициллины по способу получения можно разделить на природные (биосинтетические) и полусинтетические.
Природные пенициллины
-Природные пенициллины продуцируются различными видами плесневого гриба Penicillium.
Спектр действия природных пенициллинов включает преимущественно грам-положительные микроорганизмы: грамположительные кокки (стрептококки, пневмококки; стафилококки, не продуцирующие пенициллиназу), грамотрица-тельные кокки (менингококки и гонококки), грамположительные палочки (возбудители дифтерии, сибирской язвы; листерии), спирохеты (бледная трепонема, лептоспиры, боррелии), анаэробы (клостридии), актиномицеты.
Природные пенициллины применяют при тонзиллофарингите (ангине), скарлатине, роже, бактериальном эндокардите, пневмонии, дифтерии, менингите, гнойных инфекциях, газовой гангрене и актиномикозе. Препараты этой группы являются средствами выбора при лечении сифилиса и для профилактики обострений ревматических заболеваний.
Все природные пенициллины разрушаются (β-лактамазами, поэтому их нельзя использовать для лечения стафилококковых инфекций, так как в большинстве случаев стафилококки вырабатывают такие ферменты.
Препараты природных пенициллинов классифицируют на:
1. Препараты для парентерального введения (кислотонеустойчивые)
- Короткого действия Бензилпенициллина натриевая и калиевая соли.
- Длительного действия
Бензилпенициллин прокаин (Бензилпенициллина новокаиновая соль), Бен-затин бензилпенициллин (Бициллин-1), Бициллин-5.
2. Препараты для энтерального введения (кислотоустойчивые)
Феноксиметил пенициллин.
Бензилпенициллина натриевая и калиевая соли являются хорошо растворимыми препаратами бензилпенициллина. Быстро всасываются в системный кровоток и создают высокие концентрации в плазме крови, что позволяет их применять при острых, тяжелопротекающих инфекционных процес-
сах. При внутримышечном введении препараты накапливаются в крови в максимальных количествах через 30—60 мин и практически полностью выводятся из организма через 3-4 ч, поэтому внутримышечные инъекции препаратов необходимо производить через каждые 3—4 ч. При тяжелых септических состояниях растворы препаратов вводят внутривенно. Бензилпенициллина натриевую соль вводят также под оболочки мозга (эндолюмбально) при менингитах и в полости тела - плевральную, брюшную, суставную (при плевритах, перитонитах и артритах). Подкожно применяют препараты для обкалывания инфильтратов. Бензилпенициллина калиевую соль нельзя вводить эндолюмбально и внутривенно, так как освобождающиеся из препарата ионы калия могут вызывать судороги и угнетение сердечной деятельности.
Необходимость частых инъекций натриевой и калиевой солей бензилпенициллина послужила поводом для создания длительно действующих препаратов бензилпенициллина (депо-пенициллинов). Вследствие плохой растворимости в воде эти препараты образуют с водой суспензии и вводятся только внутримышечно. Депо-пенициллины медленно всасываются с места введения и не создают высоких концентраций в плазме крови, поэтому они применяются при хронических инфекциях легкой и средней тяжести.
К пролонгированным пенициллинам относятся бензилпенициллин про каин , или новокаиновая соль бензилпенициллина, которая действует 12— 18 ч, бензатин бензилпенициллин (бициллин-1), действующий 7-10 дней, и бициллин-5, оказывающий противомикробное действие в течение 1 mqq.
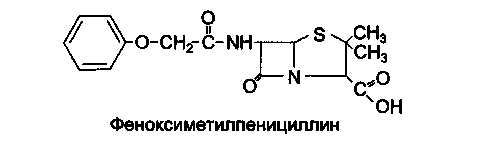
Феноксиметилпенициллин по химическому строению отличается от
бензилпенициллина наличием в молекуле феноксиметильной группы вместо бен-
зильной, что придает ему устойчивость в кислой среде желудка и делает его при
годным для применения внутрь.
Природные пенициллины имеют ряд недостатков, главными из которых являются следующие: разрушение пенициллиназой, неустойчивость в кислой среде желудка (кроме феноксиметилпенициллина) и относительно узкий спектр действия.
Полусинтетические пенициллины
В процессе поиска более совершенных антибиотиков группы пенициллина на основе 6-АПК были получены полусинтетические препараты. Химические модификации 6-АПК проводились за счет присоединения различных радикалов к аминогруппе. Основные отличия полусинтетических пенициллинов от природных касаются кислотоустойчивости, устойчивости к пенициллиназе и спектра действия.
1. Препараты узкого спектра действия, устойчивые к действию пенициллиназы
• Изоксазолиловые пенициллины
Оксациллин, Диклоксациллин.
2. Препараты широкого спектра действия, не устойчивые к действию пени
циллиназы
• Аминопенициллины
Ампициллин, Амоксициллин.
• Карбоксипенициллины
Карбенициллин, Карфециллин, Тикарциллин.
• Уреидопенициллины
Азлоциллин, Пиперациллин, Мезлоциллин. Полусинтетические пенициллины, устойчивые к действию пенициллиназы, отличаются от препаратов бензилпенициллина тем, что они эффективны при инфекциях, вызываемых пенициллиназообразующими стафилококками, поэтому препараты этой группы получили название «антистафилококковые» пенициллины. В остальном спектр действия соответствует спектру природных пеницил-линов, но активность значительно ниже.
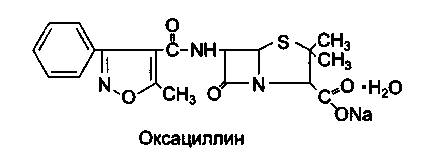
Оксациллин устойчив в кислой среде желудка, но всасывается из желудочно-кишечного тракта всего на 20—30%. Значительная часть связывается с белками крови. Через ГЭБ не проникает.
Препарат применяется внутрь, внутримышечно и внутривенно.
Диклоксациллин отличается от оксациллина высокой степенью абсорбции из желудочно-кишечного тракта (40—45%).
Аминопенициллины отличаются от препаратов бензилпенициллина более широким спектром действия, а также кислотоустойчивостью.
Спектр действия аминопенициллинов включает как грамположительные микроорганизмы, так и грамотрицательные (сальмонеллы, шигеллы, кишечную палочку, некоторые штаммы протея, гемофильную палочку). Препараты этой группы не действуют на синегнойную палочку и пенициллиназообразующие стафилококки.
Аминопенициллины применяют при острых бактериальных инфекциях верхних дыхательных путей, бактериальном менингите, кишечных инфекциях, инфекциях желче- и мочевыводящих путей, а также для эрадикации Helicobacter pylori при язвенной болезни желудка.
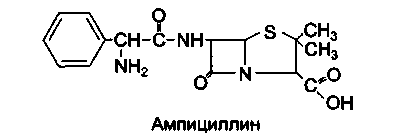
Ампициллин из желудочно-кишечного тракта всасывается неполно (30-40%). В плазме крови незначительно (до 15—20%) связывается с белками. Плохо проникает через ГЭБ. Из организма выводится с мочой и желчью, где создаются высокие концентрации препарата. Препарат вводят внутрь и внутривенно.
Амоксициллин является производным ампициллина со значительно улучшенной фармакокинетикой при приеме внутрь. Хорошо всасывается из желудочно-кишечного тракта (биодоступность 90-95%) и создает более высокие концентрации в плазме крови. Применяется только внутрь.
В медицинской практике используют комбинированные препараты, содержащие разные соли ампициллина и оксациллина. К числу таких препаратов относятся ампиокс (смесь ампициллина тригидрата и натриевой соли оксациллина в соотношении 1:1) и ампиокс-натрий (смесь натриевых солей ампициллина и ок-
сациллина в соотношении 2:1). Эти препараты сочетают широкий спектр действия и устойчивость к пенициллиназе. В связи с этим ампиокс и ампиокс-на-трий применяют при тяжело протекающих инфекционных процессах (сепсис, эндокардит, послеродовая инфекция и др.); при неустановленной антибиотиког-рамме и невыделенном возбудителе; при смешанной инфекции, вызванной грам-положительными и грамотрицательными микроорганизмами. Ампиокс применяется внутрь, а ампиокс-натрий вводится внутримышечно и внутривенно.
Главным достоинством карбокси- и уреидопенициллинов является активность в отношении синегнойной палочки (Pseudomonas aeruginosa), в связи с чем эти пенициллины называются «антисинегнойными». Основным показанием для препаратов этой группы являются инфекции, вызванные синегнойной палочкой, протеем, кишечной палочкой (сепсис, раневые инфекции, пневмонии и др.).
Карбенициллин разрушается в желудочно-кишечном тракте, поэтому вводится внутримышечно и внутривенно. Через ГЭБ не проникает. Около 50% препарата связываются с белками плазмы крови. Выводится преимущественно почками.
Карфециллин, в отличие от карбенициллина, кислотоустойчив и применяется внутрь. Тикарциллин активнее карбенициллина, особенно по влиянию на синегнойную палочку.
Уреидопенициллины в 4—8 раз превосходят карбоксипенициллины по активности в отношении синегнойной палочки. Вводятся парентерально.
Все полусинтетические пенициллины широкого спектра действия разрушаются бактериальными Р-лактамазами (пенициллиназами), что значительно снижает их клиническую эффективность. Исходя из этого, были получены соединения, инак-тивирующие Р-лактамазы бактерий. К ним относятся клавулановая кислота, судь-бактам и тазобактам. Они входят в состав комбинированных препаратов, содержащих полусинтетический пенициллин и один из ингибиторов Р-лактамаз. Такие препараты получили название «ингибиторзащищенных пенициллинов». В отличие от монопрепаратов, ингибиторзащищенные пенициллины действуют на пе-нициллиназообразующие штаммы стафилококков, обладают высокой активностью в отношении грамотрицательных бактерий, продуцирующих Р-лактамазы, а также эффективны в отношении бактероидов.
Фармацевтической промышленностью выпускаются следующие комбинированные препараты: амоксициллин/клавулановая кислота (Амоксиклав, Аугмен-тин), ампициллин/сульбактам (Уназин), пиперациллин/тазобактам (Тазоцин).
Препараты группы пенициллина малотоксичны и обладают большой широтой терапевтического действия. Однако они относительно часто вызывают аллергические реакции, которые могут проявляться в виде крапивницы, кожной сыпи, отека Квинке, бронхоспазма и анафилактического шока. Аллергические реакции могут возникать при любом пути введения препарата, но наиболее часто наблюдаются при парентеральном введении. Лечение аллергических реакций заключается в отмене препаратов пенициллина, а также во введении антигистамин-ных средств и глюкокортикостероидов. При анафилактическом шоке внутривенно вводят адреналин и глкжокортикостероиды.
Кроме того, пенициллины вызывают некоторые побочные эффекты неаллергической природы. К ним относится раздражающее действие. При приеме внутрь они могут вызывать тошноту, воспаление слизистой оболочки языка и ротовой полости. При внутримышечном введении могут быть болезненность и развитие инфильтратов, а при внутривенном — флебиты и тромбофлебиты.
ЦЕФАЛОСПОРИНЫ
К цефалоспоринам относится группа природных и полусинтетических антибиотиков, имеющих в своей основе 7-аминоцефалоспорановую кислоту (7-АЦК).
По химическому строению основа этих антибиотиков (7-АЦК) имеет сходство с 6-АПК. Однако имеются и существенные различия: структура пенициллинов включает тиазолидиновое кольцо, а цефалоспоринов — дигидротиазиновое.
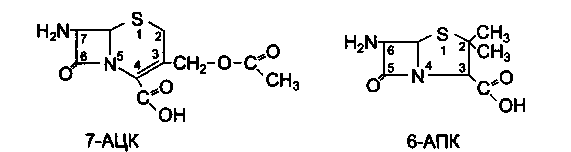
Имеющиеся черты структурного сходства цефалоспоринов с пенициллинами предопределяют одинаковый механизм и тип антибактериального действия, высокую активность и эффективность, низкую токсичность для макроорганизма, а также перекрестные аллергические реакции с пенициллинами. Важными отличительными особенностями цефалоспоринов являются их устойчивость к пени-циллиназе и широкий спектр антимикробного действия.
Цефалоспорины принято классифицировать по поколениям, внутри которых выделяют препараты для парентерального и энтерального введения (табл. 37.2).
Таблица 37.2. Классификация цефалоспоринов
| Путь введения | Поколения цефалоспоринов | |||
| I | II | III | IV | |
| Парентеральный (внутривенно, внутримышечно) | Цефазолин | Цефуроксим | Цефотаксим Цефтриаксон Цефтазидим Цефоперазон | Цефепим Цефпиром |
| Пероральный | Цефалексин Цефадроксил | Цефуроксим- аксетил Цефаклор | Цефиксим | |
Цефалоспорины I поколения
Цефалоспорины I поколения обладают широким спектром действия с преимущественным влиянием на грамположительную флору и сопоставимы по спектру и силе действия с аминопенициллинами. Основной особенностью препаратов этого поколения является их высокая антистафилококковая активность, в том числе против р-лактамазообразующих штаммов. Цефалоспорины I поколения действуют на некоторые грамотрицательные бактерии (кишечную палочку и клеб-сиелл), но разрушаются р-лактамазами грамотрицательных микроорганизмов. К препаратам I поколения первично резистентны синегнойная палочка, протей, энтерококки и бактероиды.
Цефалоспорины I поколения применяются при тонзиллофарингите, инфекциях кожи и мягких тканей, а также для профилактики послеоперационных осложнений.
Цефазолин (Кефзол) при парентеральном введении хорошо проникает в различные органы и ткани, но плохо - через ГЭБ. Создает высокие концентрации в плазме крови. Выделяется почками в неизмененном виде.
Цефалексин (Кефлекс) по спектру активности близок к цефазолину, но хуже действует на грамотрицательные бактерии. Хорошо всасывается из желудочно-кишечного тракта, но высоких концентраций в крови и большинстве органов и тканей не создает. Терапевтическая концентрация в крови после однократного введения сохраняется в течение 4—6 ч.
